高岭石/APTES插层复合物的表征及其脱嵌反应动力学
刘钦甫 纪 阳 杜妍娜 李晓光 梁 鹏
(中国矿业大学(北京)地球科学与测绘工程学院,北京100083)
高岭石/APTES插层复合物的表征及其脱嵌反应动力学
刘钦甫*纪 阳 杜妍娜 李晓光 梁 鹏
(中国矿业大学(北京)地球科学与测绘工程学院,北京100083)
以高岭石/甲醇(K/M)复合物为前驱体,利用置换法制备出了高岭石/γ-氨丙基三乙氧基硅烷插层复合物(K/APTES),并应用XRD、FTIR、TEM、TG-DSC分析等表征手段对复合物进行了分析。结果表明:APTES分子的氨基与前驱体K/M的四面体硅氧烷基、嫁接在铝氧八面体表面上的甲氧基均发生键合作用形成氢键,APTES分子为两层倾斜排列于高岭石层间,倾角大小与温度有关。插层剂APTES破坏了高岭石层间的氢键,加剧了高岭石自身结构中硅氧四面体片层与铝氧八面体片层之间存在的错位,使得K/APTES插层复合物的部分片层卷曲变形。还针对复合物的插层剂APTES的脱嵌反应,采用Satava积分法和Achar-Brindley-Sharp-Wendworth微分法相结合的动力学方法计算得到了完整的动力学三因子:活化能E=197.8 kJ·mol-1,指前因子的对数lg(A/s-1)=14.60,最概然机理函数为:f(α)=[-ln(1-α)]-1,G(α)=α+(1-α)ln(1-α)。
高岭石;γ-氨丙基三乙氧基硅烷;插层;动力学
硅烷偶联剂是一类在分子中同时含有两种不同化学性质基团的有机硅化合物[1],可以增进无机材料与有机材料界面之间的粘结,提高复合材料的性能。近年来硅烷偶联剂在层状粘土矿物插层应用中的研究日趋活跃[2]。
高岭石是一种1∶1型二八面体层状硅酸盐,结构单元层之间以较强的氢键连接,且层间不存在可交换的阳离子,仅有诸如醋酸钾[3-5]、尿素[6-7]、二甲基亚砜[8-10]、水合肼[11-12]和甲酰胺[13]等少数种类的小分子物质可直接对其插层。高岭石无法与硅烷偶联剂直接进行插层反应,须先对其进行插层预处理。目前已有不少学者对高岭石内表面羟基嫁接γ-氨丙基三乙氧基硅烷(APTES)做了一系列研究。2007年,Tonle等[14]以二甲基亚砜插层高岭石复合物为前驱体在高温下完成了γ-氨丙基三乙氧基硅烷在高岭石内表面的嫁接,使高岭石负载了更多反应基团。由于反应温度、气氛、溶剂的不同,硅烷分子以不同方式在层间排列,此方法制备的硅烷嫁接高岭石复合物可测得1.00~2.00 nm不等的层间距。2011年Guerra[15]制备了γ-氨丙基三乙氧基硅烷嫁接高岭石,并用以吸附汞离子。2012年杨淑勤等[2]采用γ-氨丙基三乙氧基硅烷对不同有序度高岭石的层间表面羟基进行嫁接反应,并阐述了嫁接反应机理。
目前,前人均是以高岭石/二甲基亚砜复合物为前驱体,在一定高温下(100~220℃)完成APTES与高岭石层间羟基的嫁接。故这种方法制备的插层复合物,APTES分子为单层排列,层间距不是很大(一般都小于2 nm)。还有,对APTES分子与高岭石层间表面的成键、层间排列方式及片层形貌变化这些方面的研究也不多。本文以高岭石/甲醇复合物为前驱体,在常温下制备出了层间距较大(2.69 nm)的高岭石/γ-氨丙基三乙氧基硅烷插层复合物,对其插层机理和形貌变化进行了深入分析,并探究了温度对复合物的影响。本文还以制备出的复合物为基础,研究了其脱嵌反应的过程,采用Satava积分法和Achar-Brindley-Sharp-Wendworth微分法相结合的动力学方法确定了其最概然机理函数,计算得到了较为精确的活化能和指前因子,从而得到了完整的动力学三因子。
1 实验部分
1.1 实验材料
原料:河北张家口高岭土(K),亨克利结晶度指数为1.31,高岭石含量为95%,其主要化学组成(质量百分比):SiO244.64%;Al2O338.05%;Fe2O30.22%;TiO21.13%。试剂:二甲基亚砜(DMSO,化学式(CH3)2SO),醋酸钾(KAc,化学式CH3COOK),均为分析纯,西陇化工股份有限公司。甲醇(MeOH,化学式CH3OH),纯度99.5%,北京化工厂。γ-氨丙基三乙氧基硅烷(APTES,化学式H2NCH2CH2CH2Si(OC2H5)3),纯度98%,国药集团化学试剂有限公司。
1.2 实验过程
张家口高岭土(K)50 g,加入质量百分比浓度为90%的DMSO水溶液中,在60℃恒温搅拌12 h后离心分离,获得高岭石/二甲基亚砜插层复合物(K/ D),将此固体产物于60℃恒温干燥24 h,取5 g K/D加入120 mL甲醇,室温条件下磁力搅拌24 h,重复甲醇漂洗10次,获得高岭石/甲醇插层复合物(K/ M)。
取1 g湿润状态下的高岭石/甲醇插层复合物(K/M)加入40 mL液态APTES,磁力搅拌24 h,离心分离得高岭石/γ-氨丙基三乙氧基硅烷插层复合物(K/APTES)。
1.3 表征
X射线衍射分析。采用日本RIGAKU公司的D/ max-2500/PC X射线衍射仪测定。测定条件:Cu靶;电压,40 kV;电流,100 mA、150 mA;扫描步宽,0.02°;狭缝系统,SS=1°,RS=0.3 mm;扫描速率为4°· min-1、1°·min-1;扫描范围为1°~30°、2.5°~30°。
红外光谱分析。采用美国Thermofisher公司生产的Nicolet6700型Fourier变换红外光谱仪,扫描范围为4000~600 cm-1。
透射电子显微镜分析。照片使用FEI-Tecnai G2 F30 S-TWIN拍摄,电压600 kV。
TG-DSC分析。采用瑞士梅特勒-托利多公司TGA/DSC1/1600HT型同步热分析仪,升温速率为10℃·min-1,测量范围25~1 000℃。
Materials Studio软件分析。APTES分子的几何构型优化采用Materials Studio软件中Forcite模的Geometry Optimization计算任务,使其能量最小化且表面电荷呈中性。其中,Algorithm采用Smart;Quality采用Medium;Energy值为0.004 kJ·mol-1;Force值为2.1 kJ·mol-1。Method采用Metropolis方法。力场选用PCFF INTERFACE。静电相互作用和范德华相互作用的计算分别采用Ewald和Atom based方法处理。其中非键截断距离设置为1.25nm,同时Spline width和Buffer width分别设为0.1 nm和0.05 nm。
2 结果与讨论
2.1 X射线衍射分析
由图1可知,原矿高岭石(K)的d(001)衍射峰和d(002)衍射峰均比较尖锐。高岭石(K)经二甲基亚砜插层之后,d(001)衍射峰从0.715 nm增大至1.14 nm(K/ D),说明二甲基亚砜分子已成功进入高岭石层间,使其层间距增大了0.425 nm。然后将K/D加入到甲醇溶液中反应,使甲醇取代层间的DMSO分子,并与高岭石内表面羟基发生脱水反应形成甲氧基[16],层间距变为0.88 nm(K/M)。

图1 高岭石及其插层复合物的XRD图Fig.1 XRD patterns of kaolinite and kaolinite intercalation compounds
常温条件下将K/M直接加入液态APTES中,分离出糊状插层复合物K/APTES。由XRD图可知,前驱体K/M经APTES插层之后,d(001)衍射峰从0.88 nm增大至2.69 nm(K/APTES),说明APTES分子已成功进入高岭石层间。K/APTES插层复合物的d(001)衍射峰比较尖锐,而d(002)面衍射峰则比较宽缓低矮。
层间距的变化只能定性地分析APTES分子是否进入了高岭石层间,而插层率(intercalation ratio,IR)则可以定量计算APTES分子进入高岭石层间的量,其公式如下:IR=I(001)(c)/[I(001)(c)+I(001)(k)]。式中:I(001)(c)和I(001)(k)分别表示插层复合物新生的d(001)衍射峰和纯高岭石d(001)衍射峰的相对强度。由上式计算K/APTES插层复合物的插层率为97.1%。
K/APTES的d(001)衍射峰从0.88 nm增大至2.69 nm,层间距扩大了1.81 nm,利用Material studio优化了APTES分子结构并测量其长轴长链长度约为1.03 nm。观察K/APTES层间距的扩大值1.81 nm和 APTES分子链长度1.03 nm两个数值可发现,K/ APTES层间距的扩大值1.81 nm明显大于APTES的分子链长度1.03 nm,但小于APTES的两倍分子链长度2.06 nm。说明APTES分子为两层倾斜排列于高岭石层间,经计算,倾角约为61.5°。下面再分析APTES分子在高岭石层间的成键取向。
观察APTES的结构(图2),其两端官能团为氨基(NH2)和三乙氧基硅基(Si-(OC2H5)3)。为了验证三乙氧基硅基是否与高岭石层间表面发生了键合,选取同样具有三乙氧基硅基但没有氨基官能团的硅烷偶联剂乙烯基三乙氧基硅烷(CH2=CHSi(OC2H5)3)和γ-巯丙基三乙氧基硅烷(HS(CH2)3Si(OC2H5)3),取以上1种硅烷40 mL,各加入1 g湿润状态下的K/M,于室温磁力搅拌24 h离心分离得糊状物,分别标记为a,b。XRD图如图3。

图2 APTES分子结构示意图Fig.2 Structure schematic representation of APTES molecule

图3 高岭石/甲醇插层复合物与其他硅烷的反应产物的XRD图Fig.3 XRD patterns of reaction products of K/M react with other silane coupler
由图3可见,两者的XRD图与其前驱体K/M相差无几,并未出现新的峰,即2种硅烷均不能插入到高岭石层间,这充分证明三乙氧基硅基不能与高岭石层间表面发生键合。由此可知,是APTES分子的氨基与高岭石层间表面发生了键合才使得APTES插入到了高岭石层间。分析K/APTES的前驱体K/M内部结构,结合上文分析所指出的APTES分子为两层倾斜排列于高岭石层间,可推知氨基给出质子和四面体硅氧烷基形成了氢键。至于APTES与铝氧八面体的键合,既可能是接受质子与铝氧八面体的表面羟基形成氢键,也可能是与嫁接在铝氧八面体上的甲氧基形成氢键。为探究这个问题,做了如下对比实验。
取1 g湿润状态下的高岭石/醋酸钾插层复合物(K/KAc)加入40 mL液态APTES,于室温磁力搅拌24小时,离心分离得糊状物,标记为K/KAc/APTES, XRD图谱如图4所示。可见,K/KAc/APTES的XRD图与其前驱体K/KAc相差无几,并未出现新的峰,说明APTES不能插入到K/KAc层间。而APTES可以插入到K/M层间,分析K/M和K/KAc内部结构可知,两者区别只在于和高岭石铝氧八面体表面羟基形成氢键的基团不一样,K/KAc为C=O…HO-Al,而K/M为与高岭石内表面羟基发生脱水反应形成甲氧基(Al-O-CH3)。由此推知,APTES的氨基是与嫁接在铝氧八面体上的甲氧基发生键合作用形成氢键。

图4 高岭石/醋酸钾插层复合物及其与γ-氨丙基三乙氧基硅烷的反应产物的XRD图Fig.4 XRD patterns of K/KAc and K/KAc/APTES intercalation compounds
本文还探究了温度对APTES插层K/M的影响。图5a,b分别为常温及60℃条件下APTES插层K/M所得复合物的XRD图。由图5可见,相较于常温条件,温度提高至60℃后复合物的层间距明显减小,层间距相较于前驱体K/M增大了1.15 nm,层间距的扩大值介于APTES分子的1倍分子链长度1.03 nm与2倍分子链长度2.06 nm之间,说明60℃条件下APTES分子也是两层倾斜排列于高岭石层间,但倾角相较于常温明显减小。经计算,60℃条件下APTES分子的倾角约为33.9°。

图5 常温(a)及60℃(b)条件下反应所得高岭石/γ-氨丙基三乙氧基硅烷插层复合物的XRD图Fig.5 XRD patterns of K/APTES intercalation compound being reacted under the condition of room temperature(a)and 60℃(b)
经上文分析总结,APTES分子的氨基与前驱体K/M的四面体硅氧烷基、嫁接在铝氧八面体表面上的甲氧基均发生键合作用形成氢键,APTES分子为两层倾斜排列于高岭石层间,倾角与温度有关。结构模型如图6所示。

图6 高岭石/γ-氨丙基三乙氧基硅烷插层复合物结构模型Fig.6 Structure model of K/APTES intercalation compound
2.2 红外分析
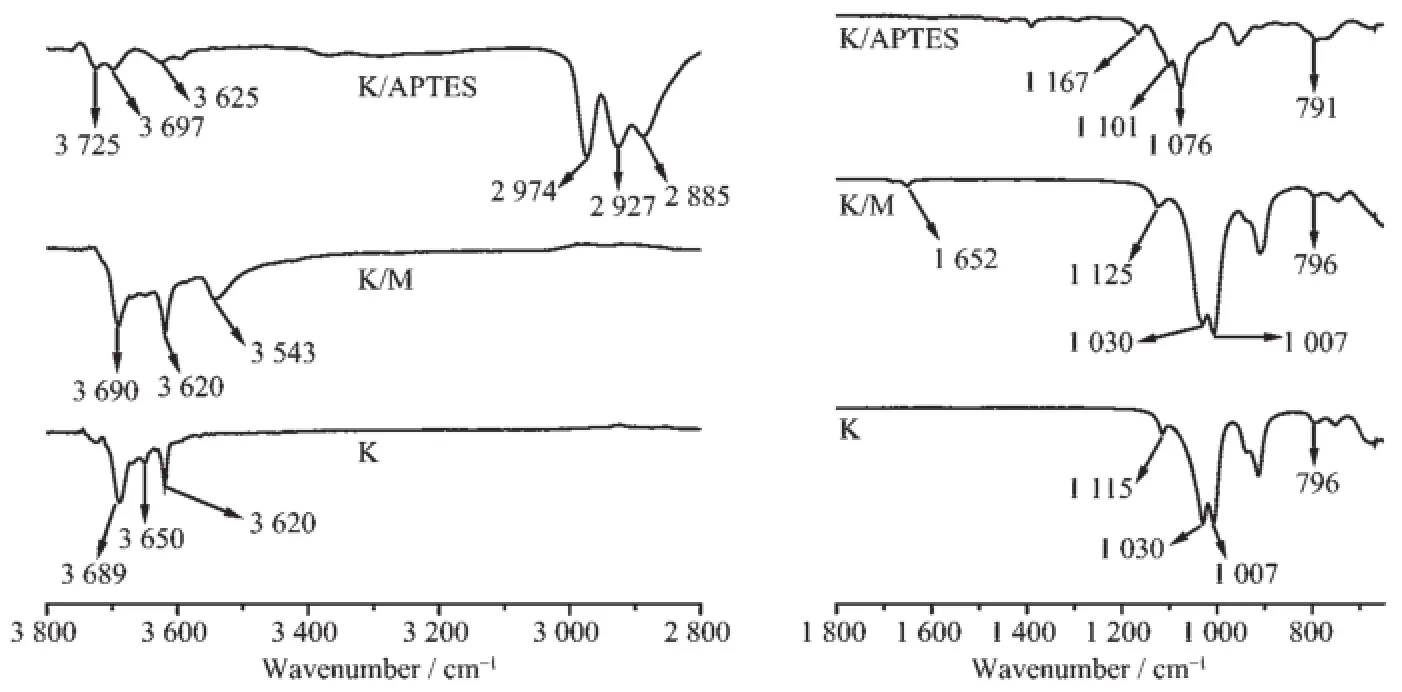
图7 高岭石及其插层复合物的IR图谱Fig.7 IR spectra of kaolinite and kaolinite intercalation compounds
在高岭石晶体中,位于高岭石层间的表面羟基,称为内表面羟基,位于硅氧四面体与铝氧八面体之间的羟基,称为内羟基[17]。图7中K是高岭石原矿的红外光谱图,3 689和3 650 cm-1吸收峰为内表面羟基的伸缩振动峰,3 620 cm-1吸收峰属于内羟基的伸缩振动峰[18]。经甲氧基嫁接之后(K/M),内表面羟基吸收峰有所减弱,且位置发生些许移动,而3 620 cm-1处内羟基的伸缩振动峰并未发生明显变化,表明甲氧基的嫁接只发生于内表面羟基处,并未对内羟基产生影响。Si-O键的对称伸缩振动峰由1 115 cm-1移至1 125 cm-1,Si-O键的反对称伸缩振动峰及羟基转换振动峰位置未发生变化。K/M还在1 652、3 543 cm-1处出现了吸收峰,此为吸附水分子及甲醇分子产生的。
前驱体K/M经APTES插层之后,内表面羟基吸收峰因受插入的APTES分子的扰动而进一步减弱,且位置发生移动,由3 690 cm-11个吸收峰分化为3 725、3 697 cm-12个吸收峰。由于APTES的插层导致高岭石片层出现卷曲变形(详情见2.3形貌分析),内羟基吸收峰受此影响,由3 620 cm-1移至3 625 cm-1。此外,羟基转换振动峰也由796 cm-1移至791 cm-1。Si-O键的振动吸收峰也发生了明显变化。其中,Si-O键的对称伸缩振动峰由1 125 cm-1移至1 167 cm-1,Si-O键的反对称伸缩振动峰1 030、1 007 cm-1分别移至1 101、1 076 cm-1,且强度均也发生明显变化。还有,2 974、2 927、2 885 cm-1位置处也产生了新的振动峰,此为一系列甲基、亚甲基、次甲基的反对称和对称伸缩振动峰,这充分说明APTES分子已经插层进入了高岭石层间。
2.3 形貌分析
实验所用高岭石原矿取自河北张家口,高岭石原矿Hinckley结晶度指数为1.31。在透射电子显微镜下,高岭石颗粒较自形,可见良好的假六方片状晶形,直径约为0.5~3 μm,边缘平直,表面光滑(图8,K)经APTES插层后,高岭石总体仍呈现出六方片状的晶形,但部分片层产生了一定程度的翘起、剥离及卷曲变形,还出现了少量的纳米卷(图8,K/APTES)。这为进一步深加工制备纳米级高岭土打下了良好基础。
APTES分子插入高岭石层间,并和四面体硅氧烷基、铝氧八面体表面羟基均发生键合作用,使得铝羟基和硅氧基之间的氢键断裂,这减弱了高岭石层与层之间的作用力。而高岭石自身结构中硅氧四面体片层与铝氧八面体片层之间存在错位,氢键的断裂加剧了这种错位,于是高岭石片层出现了一定程度的卷曲来抵消上述错位。此外,经APTES插层后,高岭石层间距变大,为片层的卷曲提供了空间。

图8 高岭石及高岭石/γ-氨丙基三乙氧基硅烷插层复合物的TEM图Fig.8 TEM imagines of kaolinite and K/APTES intercalation compound
2.4 TG和DSC分析
图9 K是纯高岭石在升温速率为10℃·min-1的TG和DSC曲线。从图中可以看到,纯高岭石于514.1℃有一个失重台阶,为高岭石脱羟基水转变为偏高岭石所致,失重率为12.7%,与高岭石的理论含水量接近。这证明插层实验所用高岭土基本不含杂质,质量较高。另外,DSC曲线在996.8℃出现一个尖锐的放热峰,该放热峰是由于高岭石重结晶形成莫来石而产生的。高岭石脱羟基和重结晶形成莫来石的反应方程式分别如下:

前驱体高岭石/甲醇插层复合物在升温速率为10℃·min-1的TG和DSC曲线如图9 K/M所示,其热分解过程分2步进行。第一步是K/M插层复合物层间甲氧基的脱嵌分解,失重率为2.03%;第二步为高岭石脱羟基的过程,失重率为11.27%。与高岭石原矿相比,K/M插层复合物脱羟基温度由514.1℃降低至509.8℃,这是由于甲氧基的嫁接破坏了高岭石层间的部分氢键,使内表面羟基键合作用力减弱,更容易脱去。
K/APTES的TG和DSC曲线(图9 K/APTES)表明其热分解过程分3步进行。第一步是K/APTES插层复合物表面水的蒸发及层间甲氧基(甲氧基由甲醇分子与高岭石内表面羟基发生脱水反应而形成,是APTES插层高岭石所用前驱体K/M的结构基团)的脱嵌分解,失重率为7.4%。第二步为插层剂APTES于433.9℃左右发生脱嵌反应,失重率为8.7%;第三步为高岭石脱羟基的过程,失重率为11.3%,占纯高岭石失重的13.0%,这与纯高岭石的失重率和热效应相比非常接近,因此可认为插入高岭石层间的APTES已完全脱嵌。此外,由于APTES的插入破坏了前驱体K/M层间的氢键,使其内表面羟基键合作用力减弱,K/APTES插层复合物脱羟基温度相较于前驱体K/M进一步降低,由509.8℃降低至500.4℃。
2.5 脱嵌反应动力学研究
通过对K/APTES插层复合物加热脱嵌反应过程的研究,可以推测APTES插层高岭石过程,进而推测其插层机理,并为插层过程的控制提供帮助.因此对K/APTES插层复合物的脱嵌反应进行热动力学研究具有十分重要的意义。
对于常见的固相反应来说,其反应方程可以表示为:A(s)→B(s)+C(g)。其反应速率方程的微分和积分形式分别为:

上式中,α表示t时物质A已反应的分数,即转化率;k为反应速率常数(s-1);f(α)为反应机理函数的微分形式。其中,k与反应温度T(绝对温度)之间的关系可用著名的Arrhenius方程(公式2)表示,式中,A为表观指前因子(s-1),E表示表观活化能(J·mol-1),R为通用气体常数(J·mol-1·K-1)。在恒定升温速率条件下,可得公式(3),式中,T0表示DSC曲线偏离基线的始点温度(K),β表示加热速率(K·min-1)。

联立公式(1)、(2)、(3),再经一系列推导可得Satava积分法(公式4)和Achar-Brindley-Sharp-Wendworth微分法[19](公式5)。


由Satava积分法公式知,lg[G(α)]是1/T的线性函数,对K/APTES插层复合物所测得的数据进行线性拟合,并可由斜率算得活化能E,由截距计算出指前因子A。经过计算,线性拟合的拟合优度在99%以上且E和A值在材料热分解反应动力学参数值的正常范围内(活化能E值在80~250 kJ·mol-1之间,指前因子的对数lg(A/s-1)值在7~30之间)的机理函数有如下几个(表1)。
如表1所示,上述5个机理函数的拟合优度均高于99%,且计算出的活化能E值和指前因子A值均在材料热分解反应动力学参数值的正常范围内,如果只是简单的选拟合优度最高的一个机理函数作为K/APTES插层复合物脱嵌反应的最概然机理函数,则很有可能会发生选择错误。这就需要我们用另一种方法(本文选用Achar-Brindley-Sharp-Wendworth微分法)对上述5个机理函数进行检验,能较好的同时符合Satava积分法和Achar-Brindley-Sharp-Wendworth微分法的机理函数便确定为KAPTES插层复合物脱嵌反应的最概然机理函数。用Achar-Brindley-Sharp-Wendworth微分法对上述5个机理函数计算结果(表2)如下。
由表2可知,线性拟合的拟合优度较好的有2个,分别是2号机理函数和9号机理函数。对比易知,2号机理函数的拟合优度较高,达到了99.71%,计算出的E值、A值和Satava积分法计算出的结果也更加接近,且其E值和A值均在材料热分解反应动力学参数值的正常范围内。对2号机理函数分别运用Satava积分法(图10,a)和Achar-Brindley-Sharp-Wendworth微分法(图10,b)进行线性拟合的曲线如下所示,充分表现了2号机理函数对K/ APTES插层复合物脱嵌反应的高度拟合。

表1 Satava积分法计算结果Table1 Results of experimental data by Satava integral method

表2 Achar-Brindley-Sharp-Wendworth微分法计算结果Table2 Results of experimental data by Achar-Brindley-Sharp-Wendworth differential method

图102 号机理函数运用Satava积分法(a)和Achar-Brindley-Sharp-Wendworth微分法(b)的线性拟合曲线Fig.1 0Linear fitting curves of No.2 function by Satava integral method(a)and Achar-Brindley-Sharp-Wendworth differential method(b)
3 结论
(1)以高岭石/甲醇复合物为前驱体,利用置换法制备出了较大层间距(2.69 nm)、高插层率(97.1%)的K/APTES插层复合物。APTES分子的氨基与前驱体K/M的四面体硅氧烷基、嫁接在铝氧八面体表面上的甲氧基均发生键合作用形成氢键,APTES分子为两层倾斜排列于高岭石层间,倾角与温度有关。
(2)插层剂APTES破坏了高岭石层间的氢键,加剧了高岭石自身结构中硅氧四面体片层与铝氧八面体片层之间的错位,使得K/APTES插层复合物的部分片层卷曲变形。
(3)K/APTES插层复合物的热分解过程分3步进行。第一步是K/APTES插层复合物表面水的蒸发及层间甲氧基的脱嵌分解,第二步为插层剂APTES于433.9℃左右发生脱嵌反应,失重率为8.7%;第三步为高岭石脱羟基的过程.
(4)采用Satava积分法和Achar-Brindley-Sharp-Wendworth微分法相结合的动力学方法,求得K/ APTES插层复合物加热脱嵌反应过程遵循Valensi方程,其最概然机理为二维扩散,圆柱形对称,2D,减速形α-t曲线,其机理函数为:f(α)=[-ln(1-α)]-1,G(α)= α+(1-α)ln(1-α)。活化能E和指前因子A均取Satava积分法和Achar-Brindley-Sharp-Wendworth微分法计算结果的平均值,即E=197.8 kJ·mol-1,lg(A/s-1)= 14.60。
[1]CHEN Shi-Rong(陈世容),QU Wan-Xing(瞿晚星),XU Ka-Qiu(徐卡秋).Silicone Material(有机硅材料),2003,17(5): 28-31
[2]YANG Shu-Qin(杨淑勤),YUAN Peng(袁鹏),HE Hong-Ping (何宏平),et al.Acta Mineralogica Sinica(矿物学报),2012, 32(4):10-16
[3]Ledoux R L,White J L.J.Colloid Interface Sci.,1966,21(2): 127-152
[4]Frost R L,Locos O,Kristof J,et al.Vib.Spectrosc.,2001,26 (1):33-42
[5]Frost R L,Kristof J,Kloprogge J T.Spectrochim Acta:Part A,2001,57:603-609
[6]Mako,Kristof J,Horvath E,et al.J.Colloid Interface Sci., 2009,330(2):367-373
[7]Tsunematsu K,Tateyama H.J.Am.Ceram.Soc.,1999,82(6): 1589-1591
[8]ZHANG Yin-Min(张印民),LIU Qin-Fu(刘钦甫),WU Ze-Guang(伍泽广),et al.J.Chinese Ceram.Soc.(硅酸盐学报), 2011,39(10):113-119
[9]Frost R L,Kristof J,Horvath E,et al.Thermachim Acta, 1999,327(1/2):155-166
[10]Gardolinski J E,Carrera L C M,Cantao M P,et al.J.Mater. Sci.,2000,35(12):3113-3119
[11]Cruz M D R,Franco F.Clays Clay Miner.,2000,48(1):63-67 [12]CHEN Zu-Xiong(陈祖熊),YAN Wei(颜卫),WANG Jian(王坚),et al.J.Build.Mater.(建筑材料学报),2000,3(2):151-155
[13]Frost R L,Kristof J,Horvath E,et al.Spectrochim Acta, 2000,56(9):1711-1729
[14]Tonlé I K,Diaco T,Ngameni E,et al.Chem.Mater.,2007, 19(26):6629-6636
[15]Guerra D L,Oliveira S P,Silva R A S,et al.Ceram.Int., 2011,38(2):1687-1696
[16]Komori Y,Enoto H,Takenawa R,et al.Langmuir,2000,16 (12):5506-5508
[17]FENG Li(冯莉),LIN Zhe(林喆),LIU Jiong-Tian(刘炯天), et al.J.Chinese Ceram.Soc.(硅酸盐学报),2006,34(10): 1226-1231
[18]DU Xiao-Man(杜小满),LIU Qin-Fu(刘钦甫),CHENG Hong -Fei(程宏飞),et al.China Non-Metallic Min.Ind.(中国非金属矿工业导刊),2009(6):12-16
[19]HU Rong-Zu(胡荣祖),SHI Qi-Zhen(史启祯).Thermal Analysis Kinetics(热分析动力学).Beijing:Science Press, 2001.
Characterization and Deintercalation Kinetics of
Kaolinite/γ-Aminopropyltriethoxysilane Intercalation Complex
LIU Qin-Fu*JI YangDU Yan-NaLI Xiao-GuangLIANG Peng
(College of Geoscience and Surveying Engineering,China University of Mining&Technology,Beijing 100083,China)
The kaolinite/γ-aminopropyltriethoxysilane(K/APTES)was prepared with a direct displacement intercalation method by using kaolinite/methanol intercalation complex as an intermediate.The samples were characterized by using X-ray diffraction,Fourier transform infrared spectroscopy,thermogravimetric analysis,and TEM analysis.Analysis suggested that the amidogen of APTES forms hydrogen bonds with tetrahedron siloxane and interlayer methoxy group of the kaolinite/methanol intercalation complex.The APTES molecules are arranged in double layer aslant between the kaolinite layers,and the inclination angle is related to the temperature. Because of hydrogen bonds are broken by APTES,the K/APTES intercalation compound appears clear scroll and exfoliation.The kinetic triplet of APTES′deintercalation from K/APTES intercalation complex was calculated by Satava integral method and Achar-Brindley-Sharp-Wendworth differential method.The activation energy E is 197.8 kJ·mol-1,the logarithm of pre-exponential factor lg(A/s-1)is 14.60.The mechanism function is G(α)=α+(1-α)ln(1-α)and f(α)=[-ln(1-α)]-1.
kaolinite;γ-aminopropyltriethoxysilane;intercalation;kinetic
P578.964;TQ324.4
A
1001-4861(2015)03-0501-08
10.11862/CJIC.2015.096
2014-09-18。收修改稿日期:2014-12-13。
国家自然科学基金重点项目(No.51034006)资助。
*通讯联系人。E-mail:lqf@cumtb.edu.cn

