7例骨髓坏死患者的实验室检查结果及临床分析
黄亮,区敏怡
(肇庆市第二人民医院检验科,广东 肇庆526060)
骨髓坏死(bone marrow necrosis,BMN)是继发于骨髓转移性肿瘤、急性白血病、感染和其他原因引起的DIC,也有原因不明,导致骨髓细胞严重变性和坏死(溶解),临床上常以发热、骨痛、贫血和血小板减少为特征的综合征[1]。现将本院1999年至2014年诊治的7例BMN患者的原发病、发病机理、实验室检查特点及临床特征总结分析报道如下。
1 资料与方法
1.1 临床资料 收集了1999年1月-2014年5月我院诊治的7例骨髓坏死患者,其中男性4例、女性3例,发病年龄为18岁到83岁,平均年龄47岁。患者因贫血、出血、不明原因发热、骨痛查因或肝、脾、淋巴结肿大就诊,7例患者均进行骨髓穿刺检查,骨髓细胞学检查呈典型坏死改变。
1.2 方法 对7例BMN患者原发病、发病机理、实验室检查特点及临床特征作回顾性分析。骨髓细胞学涂片采用瑞氏-姬姆萨染色,骨髓病理活检标本采用苏木素和伊红(H&E)染色。BMN分级:参照Maisel分为三级[2]:I级(轻度坏死):可见有核细胞溶解小于20%;II级 (中度坏死):坏死范围 20%~50%,易见有核细胞溶解;III级(重度坏死):骨髓片见有核细胞溶解大于50%以上。
2 结果
2.1 原发病 7例患者原发病均为恶性肿瘤。其中骨髓转移癌2例(胃癌1例、卵巢癌1例)、急性淋巴细胞白血病2例、弥漫大B淋巴瘤1例、急性早幼粒细胞白血病1例、浆细胞骨髓瘤1例。以急性白血病和骨髓转移癌为多见。
2.2 临床表现 7例患者均有不同程度的骨骼疼痛、发热和进行性贫血。其中2例出现全身难以忍受的剧烈骨痛,腰背部疼痛1例,髋部疼痛1例,胸骨疼痛2例,双下肢疼痛1例;持续性高热4例、中度发热2例、低热1例;重度贫血5例、中度贫血2例 ;6例出现出血症状,其中阴道流血1例、消化道出血2例、皮肤及口腔黏膜出血3例;肝肿大5例、脾肿大4例;淋巴结肿大6例,其中纵隔淋巴结肿大2例、全身浅表淋巴结肿大3例、腹腔淋巴结肿大1例;皮肤瘀斑2例。7例BMN患者临床表现及原发病见表1。

表1 7例BMN患者的原发病及主要临床表现
2.3 主要实验室检查结果
2.3.1 骨髓穿刺细胞学检查 7例患者均进行2~3个部位骨髓穿刺,同时进行骨髓活检。所取骨髓液外观呈暗灰色、黄褐色、果酱色或烂桃样,1例伴有恶臭味。骨髓涂片经瑞氏-姬姆萨染色镜检示:有核细胞均呈不同程度核溶解、核固缩和核碎裂,胞核嗜碱性强,细胞轮廓不清,胞浆无法辨认,细胞间充满无定性嗜酸性物质(见图1),坏死骨髓中形态完整者为成熟红细胞、幼红细胞、中性杆状核及中性分叶粒细胞;骨髓转移癌患者涂片尾部可见转移癌细胞团(见图2);骨髓重度坏死5例、中度坏死1例、轻度坏死1例。3例发生多部位骨髓坏死,4例单部位发生骨髓坏死。3例骨髓活检均示正常造血组织和基质结构破坏,染成均一的嗜酸性物质,以缺乏胞核和胞质微细结构的嗜酸细胞空影为特征。

图1 骨髓坏死骨髓涂片细胞学检查示有核细胞溶解,可辨认的特征消失,细胞间充满无定性嗜酸性物质(瑞氏-姬姆萨染液染色,×1000)

图2 骨髓转移癌BMN骨髓象中可见转移癌细胞呈巢状、簇状分布(瑞氏-姬姆萨染液染色×1000)
2.3.2 外周血象 外周血血红蛋白、白细胞及血小板三系均减少者3例,二系减少者4例,其中7例血红蛋白均为减低(17~89g/L),其中5例17-60 g/L、2例61~89 g/L;4例白细胞计数计数减低(1.36~2.98×1012/L);2 例增高 (19.8~98.6×1012/L),1 例计数正常(4.36×1012/L);血小板计数 9~57×109/L 者 5例,60~100×109/L者2例;外周血细胞形态分析3例可见幼稚粒细胞、2例可见幼稚淋巴细胞,6例可见有核红细胞,6例成熟红细胞可见大小不一、不规则形、棘形、泪滴形和破碎红细胞等形态异常。
2.3.3 其它检查 7例血清乳酸脱氢酶(333~4122U/L)、碱性磷酸酶均显著升高(219~1178U/L),7例凝血功能结果均出现异常,分别是APTT(59.2~109s)、PT(19.2~48.9s)、TT(22.3~40.9s)、Fg(0.62~1.56g/L)、D-二聚体 (20.87~98.2μg/ml),2例骨髓转移癌患者肿瘤标志物CA199、CA242显著升高,心肌酶组异常增高1例,肝功能异常2例、肾功能异常2例,X线检查发现骨质破坏3例,胸部CT示双肺下叶感染,双侧少量胸腔积液1例,右侧附件区囊性包块、腹-盆腔积液1例,B超示宫颈管积液及子宫直肠窝积液1例,腹水1例。7例患者部分实验室检 查结果见表2。
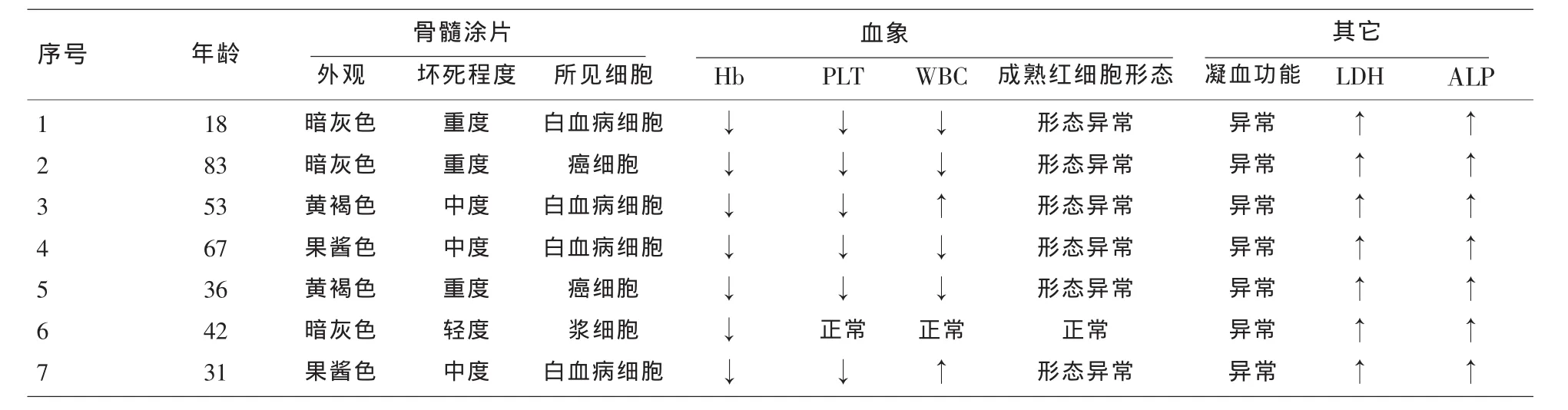
表2 7例BMN患者部分实验室检查结果
2.3.4 治疗及转归 7例患者自确诊到死亡最短生存时间为5d,最长为182d。其中1例(胃癌骨髓转移合并BMN)放弃治疗于离院后21d死亡,1例(卵巢癌骨髓转移)于入院后29d因DIC、多器官功能障碍综合征死亡。3例(原发病为急性白血病2例、淋巴瘤1例)针对原发病积极化疗及予输血、止血、抗感染及镇痛,应用糖皮质激素、维生素D3等对症支持治疗,但因病情较重、治疗效果差,出现DIC、多器官功能障碍、感染性休克,最后因多器官功能障碍综合征或出血死亡,存活时间分别为5d、36d、61d、90d;1例(原发病为浆细胞骨髓瘤)经过化疗并加以改善骨髓微循环及促进造血等治疗,BMN及原发病均获得缓解,发热、骨痛症状消失,贫血有所改善,按期巩固强化治疗,4个月后复发并严重肺部感染入院,再次化疗疗效不佳,外周血象呈进行性快速下降,最后因出血、感染、全身多器官功能障碍死亡,从确诊到死亡整个病程为182天。1例(原发病为急性早幼粒细胞白血病)予亚砷酸+ATRA+柔红霉素诱导化疗过程中出现诱导分化综合症,出现重度BMN,立即停止化疗并用糖皮质激素、维生素D3、促进造血等对症处理,患者病情严重11d后并发DIC死亡。
3 讨论
BMN为一种临床综合征而非独立的疾病,指骨髓中造血细胞和骨髓基质发生面积不等的坏死[4]。BMN是肿瘤侵犯骨髓的常见并发症,常见于白血病、非霍奇金淋巴瘤、转移性肿瘤、放疗及化疗后等,最常见为转移性癌症和急性白血病[1]。非肿瘤原因为一些较少见的疾病如镰状细胞贫血、重症感染(包括结核感染)、弥漫性血管内溶血、急性再障、系统性红斑狼疮、溶血性贫血伴血小板减少(Evans综合症)、获得性免疫缺陷综合征、伤寒等[3]另外,骨髓坏死还可引起非肿瘤性疾病,如感染、中毒、DIC及骨髓增殖性疾病等疾病[5]。本组病例均为恶性肿瘤合并BMN,可见恶性肿瘤为引起BMN的最常见原因。BMN大多发生在原发病进展过程,因此一旦发现BMN应高度警惕当中是否隐藏恶性肿瘤,同时,诊断恶性肿瘤的患者也应警惕是否也有BMN的存在。
目前普遍认为BNM的发病机理可能和以下因素有关[6]:(1)恶性肿瘤细胞在局部压迫、浸润或白血病细胞阻塞、破坏骨髓微血管而导致骨髓坏死。(2)化疗药物、干扰素等应用引起引起骨髓血管损伤。(3)细菌毒素作用导致骨髓毛细血管损伤。(4)白血病细胞大量增殖或恶性肿瘤栓子栓塞骨髓毛细胞血管及血窦导致微循环障碍。此外,有报道[7]BMN还与肿瘤坏死因子密切相关。本组7例患者可能是上述综合因素作用结果导致BMN。
临床上BMN以骨痛、发热及进行性贫血为主要症状,其临床表现、血液学改变及实验室检查结果无明显特异性,不同恶性肿瘤所致BMN有其不同的症状与体征,其实验室检查结果也因原发病不同而异。本组所有患者均有贫血、发热、骨痛和出血,血清碱性磷酸酶、乳酸脱氢酶、凝血功能均异常升高。贫血均呈进行性加重,外周血多数为三系或二系减少,血片分析可见幼红幼粒细胞,这是由于髓外造血、癌细胞侵犯骨髓排挤幼红幼粒细胞、大量癌细胞破坏骨髓屏障导致幼红幼粒细胞进入外周血等因素造成的[8];发热多为高热,推测发热原因主要是感染、坏死细胞或组织释放致热原所致。骨痛通常是多部位、全身性、持续性剧痛,发生在腰背部、胸骨、双下肢等部位多见。7例患者凝血象检查均发现异常,说明BMN患者血液普遍处于高凝状态,存在不同程度DIC,DIC的发生可能与BMN物质通过释放或激活凝血因子导致广泛的微血栓形成而引起。7例血清碱性磷酸酶(ALP)和乳酸脱氢酶(LDH)结果均异常升高,这可能与骨髓细胞和骨质破坏、肿瘤细胞的大量恶性增殖有关,肿瘤组织中的LDH溢出、肿瘤细胞的破溃或坏死致使LDH进入到血液中[9]。当骨髓坏死导致干抽或不能找到肿瘤细胞侵犯骨髓的细胞学证据时,肿瘤标志物对引起BMN原发病的溯源起到重要的辅助诊断价值[10],本组1例胃癌骨髓转移患者血清CA199水平明显升高,1例卵巢癌骨髓转移患者CA125明显升高。
BMN诊断的证据是骨髓细胞的坏死[1]。本组病例骨髓象分析均呈典型坏死特征,表现为有核细胞均呈不同程度核溶解、核固缩和核碎裂,胞核嗜碱性强,细胞轮廓不清,胞浆外溢,每个细胞可辨认的特征消失,无法确定细胞属性,细胞间充满无定性嗜酸性物质。由于骨髓中恶性肿瘤细胞常出现在结构未受损的骨髓[7],而且BMN常会出现在多个部位,与正常骨髓相互交错,有的部位发生BMN,有的部位则是原发病的骨髓象改变[11],也有文献[12]认为BMN程度与坏死范围相关,故多部位穿刺直至发现结构未受损的骨髓对诊断BMN及引起BMN原发病有重要意义。
骨髓是许多恶性肿瘤侵袭转移的好发部位,某些肿瘤的发现可能最早在骨髓中找到了转移癌细胞,一个典型的细胞学改变可使原发病的诊断难题迎刃而解[3]。另外,非侵入性检查磁共振成像(MRI)联合Tc-骨髓扫描,虽然不能作为诊断指标,但可显示BMN受累范围及预后情况,从而区别于其他骨痛,并可指导骨髓穿刺位置,为临床诊断与治疗提供依据[13]。本组7例患者均经2~3个部位穿刺证实BMN,其中4例首次骨髓穿刺即发现典型骨髓坏死改变,2例出现干抽,经多部位穿刺及结合骨髓活检证实,1例首次穿刺后结合核磁共振骨髓扫描指导穿刺位置证实。
BMN需与化疗后骨髓造血功能修复过程的组织学改变作鉴别诊断,后者以不出现凝固性坏死或“细胞空影”的细胞耗竭为特征[14]。BMN的骨髓象也应注意与人为因素所造成的细胞破坏相鉴别[6,8,15],如穿刺针、抽取骨髓液的注射器、涂片用的推玻片和玻片不干燥或染色过程中水滴混进都会引起有核细胞特别是粒系细胞引起核溶解、破裂及变形,成熟红细胞则引起溶血,在红细胞周围有一圈红色状物,染色偏酸,而BMN时成熟红细胞形态一般较为完整;此外,也应注意BMN和涂片不佳相鉴别[8],涂片不佳时骨髓液外观正常,有骨髓小粒,少部分细胞呈毛刺状但胞核清楚可见,无细胞间杂物填充。
BMN病情危重、死亡率高、预后不良,往往在短时间内死于感染、出血或各种栓塞,多数学者认为BMN是可逆转的,取决于原发病及BMN诊治是否及时。故当疑及本病时应及时进行多部位骨髓穿刺检查,结合病理活检及相关实验室检查结果可提高BMN及引起BMN原发病的诊断率。
[1]卢兴国.骨髓细胞学和病理学[M].北京:科学出版社,2008:1004-1005,545.
[2]吴晓芝.血液病诊断与鉴别诊断图谱[M].北京:人民卫生出版社,2009:289-290.
[3]周旭,李响,李郑.10例骨髓坏死临床分析[J].重庆医学,2014,43(18):2342-2344.
[4]王淑娟,王建中,吴振茹.现代血细胞图谱[M].北京:人民卫生出版社,2001:250-252.
[5]宋燕萍,万斌,戴辉,等.骨髓坏死四例临床分析[J].现代实用医学,2007,19(11):878-879.
[6]梁崇,李燕妮.11例骨髓坏死患者的骨髓象分析[J].世界最新医学信息文摘,2013,13(6):134.
[7]何争春,曾云,杨绵本.骨髓坏死[J].昆明医学院学报,2000,21(3):84-88.
[8]刘双.骨髓坏死15例临床分析[J].泰山医学院学报,2010,31(7):534-535.
[9]石沁,宋建新.31例骨髓坏死患者的临床及实验分析[J].医学信息,2013,26(3):86.
[10]赵国军,李俊梅,栗占学,等.骨髓坏死实验室检查及临床分析[J].河北医学,2010,16(12):1525-1527.
[11]钟辉秀.7例骨髓坏死患者临床及实验室检查分析[J].中外健康文摘,2012,9(1):149-150.
[12]孔黛,张菌,马保根,等.恶性血液疾病合并骨髓坏死11例临床分析[J].白血病·淋巴瘤,2012,21(5):305-307.
[13]郭笑如,林芳,傅吉春,等.骨髓坏死患者的实验室检查及临床分析[J].实验与检验医学,2011,29(3):299-300.
[14]浦权,杨梅如.血液病骨髓诊断病理学[M].北京:科学出版社,2002:413-415.
[15]陈新瑶,虞永知.九例骨髓坏死患者的实验室检查结果分析[J].海南医学,2013,24(12):1784-1785.

