反应精馏合成丙酸丙酯模拟与动力学
徐 红, 魏 巍, 虞 昊, 叶 青
(常州大学 石油化工学院, 江苏 常州 213164)
反应精馏合成丙酸丙酯模拟与动力学
徐 红, 魏 巍, 虞 昊, 叶 青
(常州大学 石油化工学院, 江苏 常州 213164)
采用反应动力学研究装置,以强酸性离子交换树脂Amberlyst46TM为催化剂,研究正丙醇和丙酸合成丙酸丙酯的反应动力学。在消除了内外扩散的情况下,考察了催化剂用量、醇/酸摩尔比、反应温度和搅拌转速对丙酸转化率的影响。在催化剂用量15 g、醇/酸摩尔比1.2、反应温度80℃、搅拌转速400 r/min的较优操作条件下,确定了反应动力学参数,获得动力学数据反应活化能Ea=40.35 kJ/mol,指前因子k0=2.16×103L/(mol·min),并运用于稳态模拟中,考察了进料温度以及各段塔板数对产物纯度的影响。优化后的操作条件为进料温度70℃、精馏段塔板数2、反应段板数21、提馏段塔板数11,此时丙酸丙酯产品的摩尔分数达到99.88%以上。
反应精馏; 丙酸丙酯; 反应动力学; 离子交换树脂
丙酸丙酯(ProPro)是一种用途广泛的精细化学品。在油墨、涂料、清洁剂和食品工业调料等行业,它是一种优良溶剂,能与乙醇和乙醚互溶,微溶于水;作为一种无毒、无害的化合物取代了一些能引起空气污染的芳香烃化合物溶剂,例如苯。现有的丙酸丙酯合成方法存在反应时间长、后序处理复杂等问题[1-2],因此研究丙酸丙酯的合成引起更多的关注[3-4]。
近年来,反应精馏[5-7]技术不断成熟,取代了许多常规的工艺流程[8-9]。反应精馏是将化学反应和精馏分离两个步骤集于一塔内操作,能够不断从反应混合物中分离产品,促使化学平衡向产品方向移动,在可逆化学反应中,具有提高转化率、增加选择性、降低能耗、减少投资成本等优势。反应精馏已被用于可逆酯化反应体系中,以解决化学平衡限制的问题[10]。
目前,尚少见关于使用离子交换树脂作催化剂的合成丙酸丙酯反应动力学的研究报道。笔者采用离子交换树脂Amberlyst46TM作为催化剂,运用Aspen Plus模拟反应精馏合成丙酸丙酯的工艺。考察了催化剂用量、醇/酸摩尔比、反应温度和搅拌转速对丙酸转化率的影响,然后采用拟均相模型描述化学反应速率,确定了活化能和指前因子;最终将动力学参数代入反应精馏合成丙酸丙酯的模拟中,探讨了进料温度、各段塔板数等设计参数对产物纯度的影响。
1 实验部分
1.1 原料和催化剂
丙酸(ProAc),化学纯,上海凌峰化学试剂有限公司产品;正丙醇(ProOH),化学纯,江苏强盛功能化学股份有限公司产品;强酸性离子交换树脂(Amberlyst46TM),江苏色可赛思树脂有限公司产品。
1.2 丙酸和正丙醇酯化反应
1.2.1 反应过程
将丙酸置于三口烧瓶中,经恒温水浴预热至反应温度,然后将已预热到反应温度的正丙醇倾入三口烧瓶中,并且加入催化剂Amberlyst46TM。打开搅拌装置,在一定转速下使反应物和Amberlyst46TM充分接触,开始反应并计时。每间隔20 min取样,采用气相色谱法分析样品组成。待反应混合液的组成不再变化,视为反应达到平衡,结束实验。改变操作条件,包括催化剂用量、醇/酸摩尔比、反应温度、搅拌转速,考察它们对该酯化反应的影响。
1.2.2 气相色谱法测定产物组成
采用上海海欣色谱仪器有限公司GC-950气相色谱仪测定酯化反应产物组成。仪器配有FID检测器和固定相为5%SE-30的弹性石英毛细管色谱柱(30 m×0.32 mm×0.4 μm)。柱温130℃,气化温度170℃,检测室温度170℃;载气N2,柱前压0.25 MPa。采用N2000色谱工作站处理数据。
1.3 反应精馏工艺流程
采用离子交换树脂Amberlyst46TM作催化剂,正丙醇和丙酸反应精馏合成丙酸丙酯的工艺流程如图1所示。
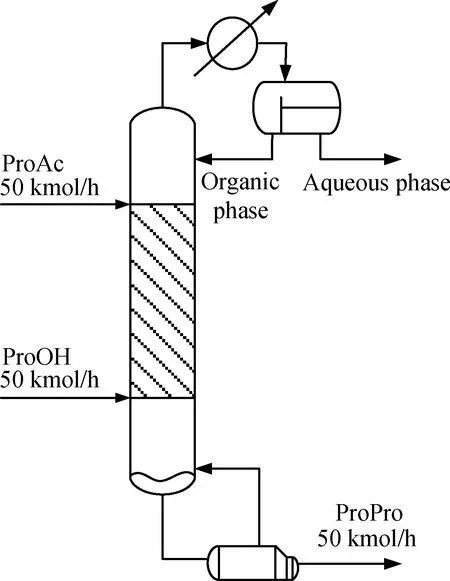
图1 正丙醇(ProOH)和丙酸(ProAc)反应精馏(RD)合成丙酸丙酯(ProPro)流程
由图1可知,丙酸从反应段上部进料,丙醇从反应段下部进料,两者在反应段充分接触并反应。该反应体系比较复杂,能够形成多种共沸物,构成了高度非理想体系。丙醇/水(共沸点87.6℃)以及丙酸/水(共沸点99.9℃)形成2个二元均相共沸物,丙酸丙酯/水(共沸点90.0℃)和水/丙醇/丙酸丙酯(共沸点86.2℃)形成2个非均相共沸物。其中,水/丙醇/丙酸丙酯三元体系形成的非均相共沸物从塔顶蒸出,经冷凝后,于分层器中分层,水相被采出,油相回流至反应段继续反应,产物丙酸丙酯从塔底采出。采用Aspen Plus软件对该反应分离过程进行稳态模拟,Aspen Plus的单元操作模块能够模拟反应精馏装置的物料和热量平衡。
笔者应用UNIQUAC活度系数模型描述该酯化反应中液体的非理想性,由于存在缔合作用,因此采用Hayden-O'Connell状态方程描述其气体的热力学性质。
2 结果与讨论
2.1 操作条件对正丙醇和丙酸合成丙酸丙酯反应的影响
2.1.1 催化剂用量的影响
采用强酸性离子交换树脂Amberlyst46TM催化剂,在反应温度80℃、醇/酸摩尔比1.2、搅拌转速400 r/min的条件下,考察催化剂用量对丙酸转化率的影响,结果示于图2。
由图2可以看出,增大催化剂用量,反应速率明显加快。反应时间相同时,催化剂用量越多,丙酸转化率也越高。当催化剂用量在5~10 g范围,丙酸转化率随反应时间延长而增加的幅度较大;催化剂用量在10~20 g范围,丙酸转化率随反应时间延长而增加的幅度明显降低。本实验选择催化剂用量为15 g。
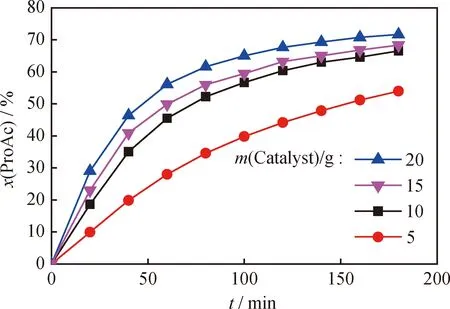
图2 不同催化剂用量下合成丙酸丙酯(ProPro)反应丙酸转化率(x(ProAc))随反应时间(t)的变化
2.1.2n(ProOH)/n(ProAc)的影响
正丙醇和丙酸合成丙酸丙酯的反应是一个可逆反应。为了提高反应物转化率,通常采用某一反应物过量的方式,使化学平衡向产品方向移动。本实验中采用丙醇过量的形式,在温度80℃、催化剂用量15 g、搅拌转速400 r/min的条件下,考察n(ProOH)/n(ProAc)对丙酸转化率的影响,结果示于图3。

图3 不同n(ProOH)/n(ProAc)下合成丙酸丙酯(ProPro)反应丙酸转化率(x(ProAc))随反应时间(t)的变化
由图3可以看出,随着n(ProOH)/n(ProAc)的增大,丙酸转化率也随之增大,但增加幅度较小。在实际生产过程中,正丙醇的使用量不能过多。正丙醇使用量的增加不仅会使馏出液中丙酸丙酯的浓度降低,也会使后处理步骤愈发复杂,增加正丙醇的回收费用,使得该工艺的成本迅速增加。因此选n(ProOH)/n(ProAc)=1.2作为本实验条件。
2.1.3 反应温度的影响
在n(ProOH)/n(ProAc)=1.2、催化剂用量15 g、搅拌转速为400 r/min的条件下,考察反应温度对丙酸转化率的影响,结果示于图4。
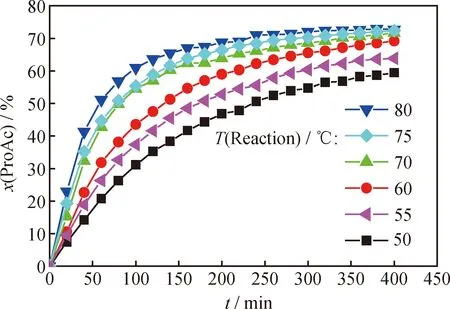
图4 不同温度下合成丙酸丙酯(ProPro)反应丙酸转化率(x(ProAc))随反应时间(t)的变化
由图4可以看出,当温度从50℃升到70℃,反应转化率增加幅度较大;当温度在70~80℃之间,反应400 min时平衡转化率相差很小。在80℃下进行丙酸丙酯合成反应能较快得到一个比较高的丙酸转化率,所以选择80℃为本实验反应温度。
2.1.4 搅拌转速的影响
合成反应中采用搅拌可使反应物与催化剂充分接触,以此来消除外扩散对反应转化率的影响。在n(ProOH)/n(ProAc)=1.2、反应温度80℃、催化剂用量15 g的条件下,考察搅拌转速对丙酸转化率的影响,结果示于图5。

图5 不同搅拌转速下合成丙酸丙酯(ProPro)反应丙酸转化率(x(ProAc))随反应时间(t)的变化
由图5可以看出,当搅拌转速达到300 r/min时,反应的转化率随转速增加的变化已经非常小,外扩散对于反应的影响基本可以忽略不计。为了进一步消除外扩散的影响,所以选400 r/min为本实验搅拌转速。
2.1.5 催化剂粒径的影响
当催化剂用量固定时,反应内扩散的有效因子只是催化剂粒径的函数。为了消除内扩散的影响,本实验使用的离子催化剂粒径小于0.5 mm。在上述反应条件下,考察了催化剂的粒径对丙酸转化率的影响,结果示于图6。
由图6可见,当催化剂粒径小于0.5 mm,内扩散对反应的影响已可消除,因此选用粒径小于0.5 mm的催化剂。
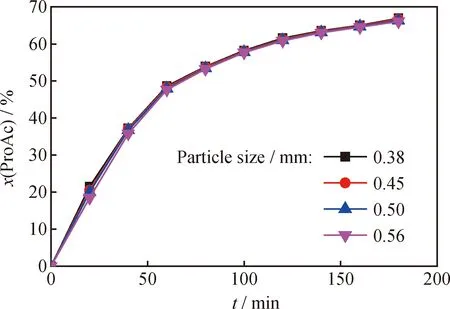
图6 不同催化剂粒径下合成丙酸丙酯(ProPro)反应丙酸转化率(x(ProAc))随反应时间(t)的变化
2.2 正丙醇和丙酸合成丙酸丙酯反应动力学模型的建立
采用拟均相反应模型对正丙醇和丙酸合成丙酸丙酯反应的实验数据进行拟合。假设此反应为二级可逆反应,则反应动力学方程如式(1)所示。
(1)
式(1)中,r为反应速率,r=dcC/dt,mol/(L·min);cA、cB、cC、cD分别为丙酸、正丙醇、产物中丙酸丙酯和水的摩尔浓度,mol/L;K为化学反应平衡常数,K=k+/k-,k+和k-分别为正反应和逆反应速率常数,L/(mol·min)。
当n(ProOH)/n(ProAc)=1.2时,式(1)变为式(2)。
(2)
式(2)中,cA0为丙酸的初始摩尔浓度,mol/L。 由于t=0 时,cC=0,因此积分得到式(3)。
(3)
k+t=Y
(4)
假如该反应为二级反应,式(4)所显示的曲线应为一条直线,直线的斜率等于正反应速率常数k+。由此,可以根据拟均相二级反应模型对实验数据进行一次线性回归,得到正反应速率常数k+,再通过正反应速率常数和温度数据对阿累尼乌斯方程进行一次线性回归,得到宏观动力学方程。
由时间和浓度数据计算出Y值,Y和t之间的线性关系如图6所示。
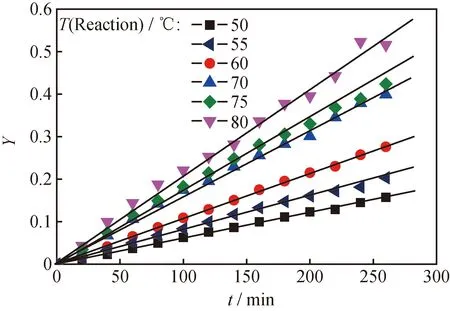
图6 不同温度(T(Reaction))下合成丙酸丙酯(ProPro)反应的Y值与反应时间(t)的线性关系
由图6可以看出,在不同反应温度下,Y对t的线性关系均为通过原点的直线,因此所假设的反应动力学模型能够比较准确地描述该反应过程,并可计算得到不同反应温度下的正反应速率常数k+。阿累尼乌斯方程变形后如式(5)所示。
lnk+=-Ea/RT+lnk0
(5)
将lnk+对1/T作图,得到图7。由图7可以看出,lnk+与1/T呈线性关系,该直线斜率为-Ea/R,截距为lnk+。经拟合得到反应活化能Ea=40.35 kJ/mol,k0=2.16×103L/(mol·min)。

图7 合成丙酸丙酯的正反应速率常数(k+)和反应温度(T(Reaction))的关系
由此得到在该反应温度范围内的正丙醇和丙酸合成丙酸丙酯的反应动力学模型,如式(6)所示。
(6)
2.3 正丙醇和丙酸反应精馏合成丙酸丙酯的模拟
将根据上述反应动力学数据建立的动力学模型应用到反应精馏合成丙酸丙酯的模拟中。在正丙醇和丙酸进料流量分别为50 kmol/h、反应精馏塔操作压力1.01×105Pa、板间距0.6 m、塔径0.9 m的条件下,考察了进料温度、各段塔板数等因素对产物纯度的影响。
2.3.1 进料温度对产物纯度的影响
在精馏段塔板数2、反应段板数21、提馏段塔板数11的条件下,考察了进料温度对正丙醇和丙酸反应精馏产物丙酸丙酯摩尔分数的影响,结果示于图8。
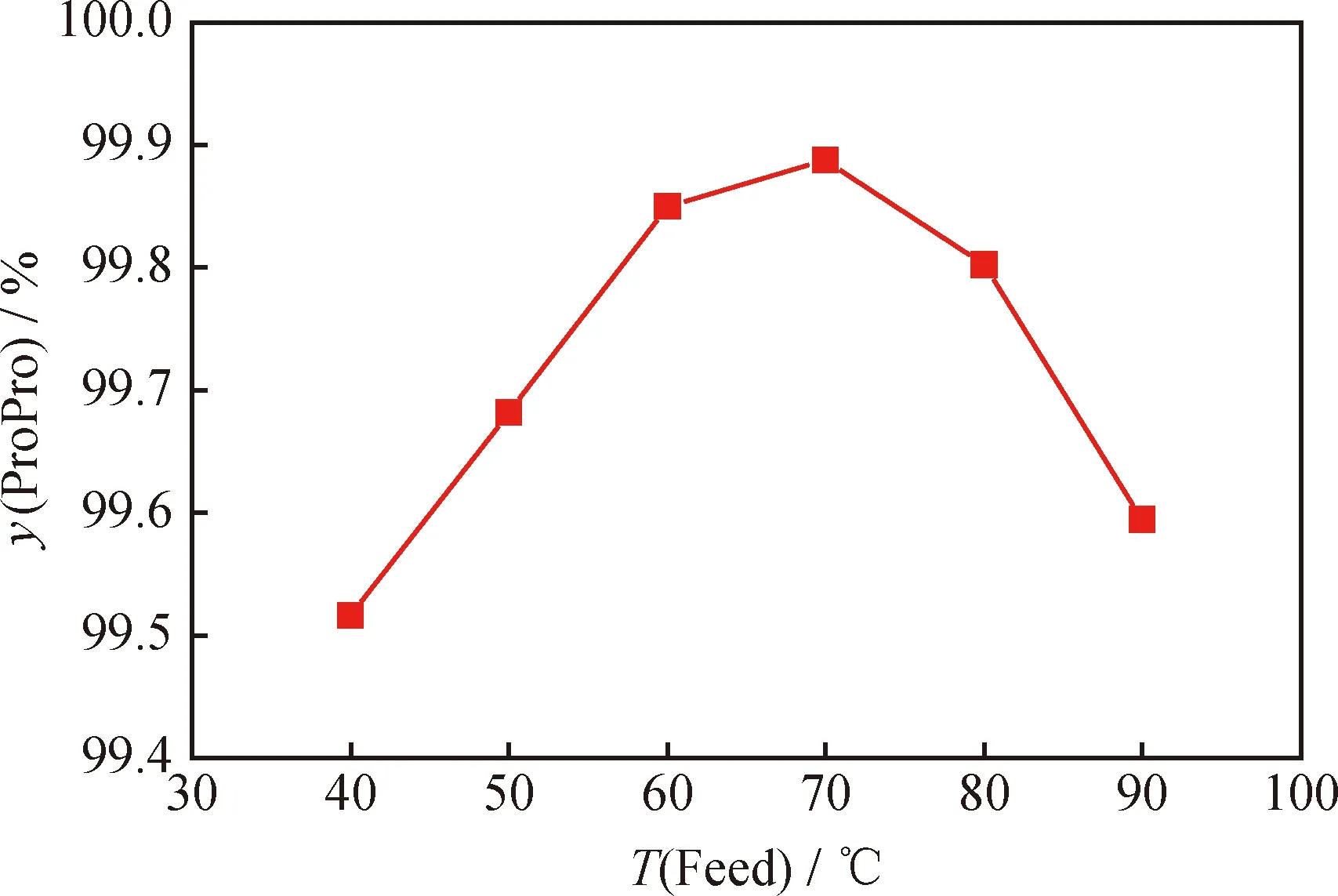
图8 进料温度(T(Feed))对反应精馏合成丙酸丙酯产物中丙酸丙酯摩尔分数(y(ProPro))的影响
由图8看出,正丙醇和丙酸反应精馏产物中,丙酸丙酯的摩尔分数随进料温度的升高先增加后降低;当进料温度为70℃时,丙酸丙酯的摩尔分数最高。因此选择70℃为本反应精馏体系的进料温度,此时丙酸丙酯的摩尔分数达到99.88%。
2.3.2 精馏段塔板数对产物纯度的影响
在进料温度70℃、反应段塔板数21、提馏段塔板数11的条件下,考察了精馏段塔板数对正丙醇和丙酸反应精馏产物中丙酸丙酯摩尔分数的影响,结果示于图9。
从图9可以看出正丙醇和丙酸反应精馏产物中丙酸丙酯的摩尔分数随精馏段塔板数的增加而增加。因为精馏段塔板数增加,分离丙酸的效率提升,使得产品中丙酸含量降低。总体上,精馏段塔板数对产物纯度的影响很小,从经济角度出发,当塔板数为2时,产物中丙酸丙酯的摩尔分数已达到99.88%以上,因此选择2块精馏段塔板。
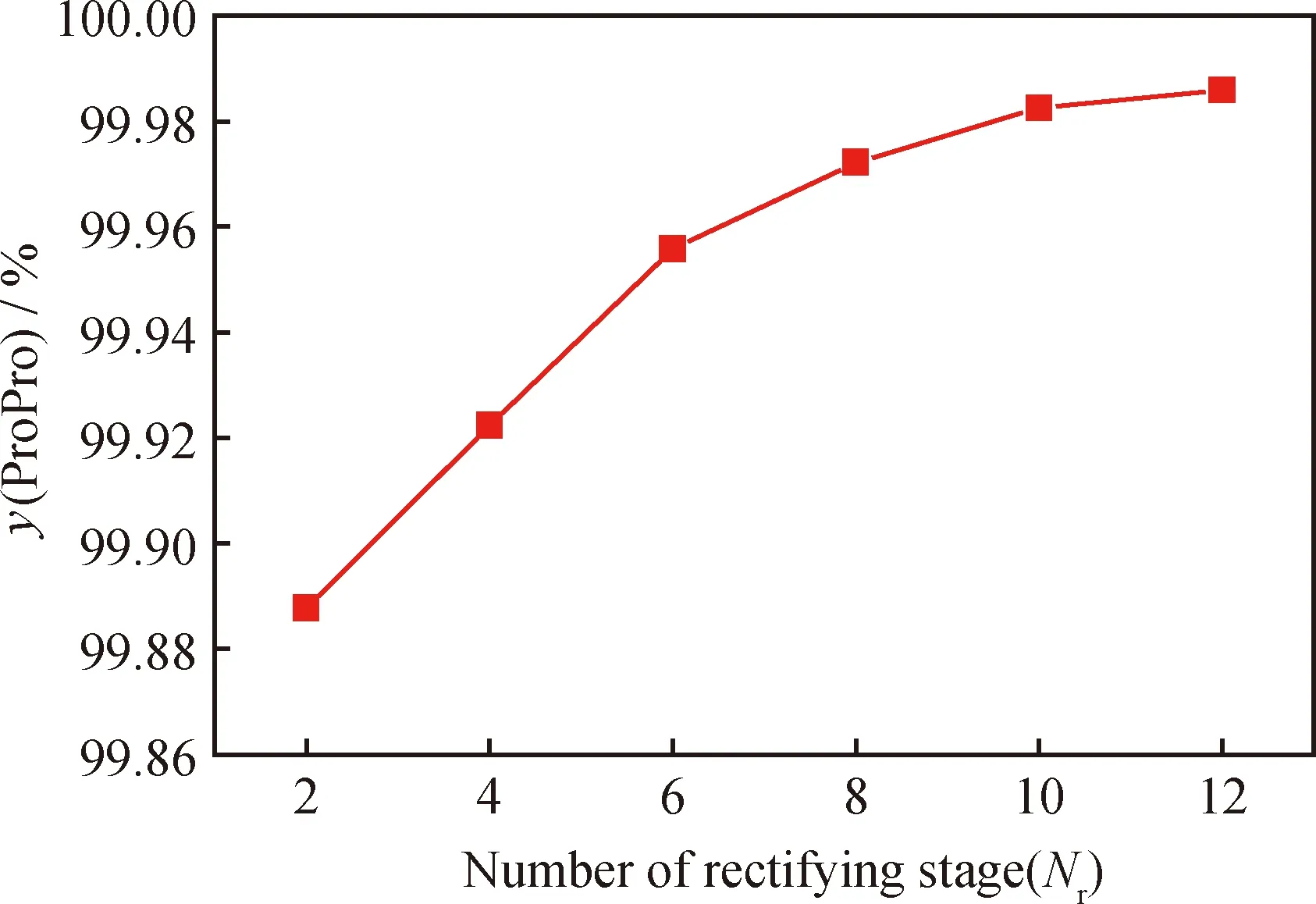
图9 精馏段塔板数(Nr)对反应精馏合成丙酸丙酯产物中丙酸丙酯摩尔分数(y(ProPro))的影响
2.3.3 反应段塔板数对产物纯度的影响
在进料温度70℃、精馏段塔板数2、提馏段塔板数11的条件下,考察了反应段塔板数对产物中丙酸丙酯摩尔分数的影响,结果如图10所示。

图10 反应段塔板数(Nrxn)对反应精馏合成丙酸丙酯产物中丙酸丙酯摩尔分数(y(ProPro))的影响
由图10看出,正丙醇和丙酸反应精馏产物中丙酸丙酯摩尔分数随反应段塔板数的增加而增加。因为增加反应段塔板数相当于延长反应时间,使得原料充分反应,从而提高了丙酸的转化率。塔板数在6~20时,产物中丙酸丙酯的摩尔分数增加幅度比较大,当反应段塔板数超过21,产物中丙酸丙酯的摩尔分数基本不变,因此反应段塔板数为21时较合适,丙酸丙酯的摩尔分数达到99.88%。
2.3.4 提馏段塔板数对产物纯度的影响
提馏段主要将未反应的原料与反应产物分离,从而得到较高纯度的丙酸丙酯。在进料温度70℃、精馏段塔板数2、反应段塔板数21的条件下,考察了提馏段塔板数对丙酸丙酯摩尔分数的影响,结果示于图11。
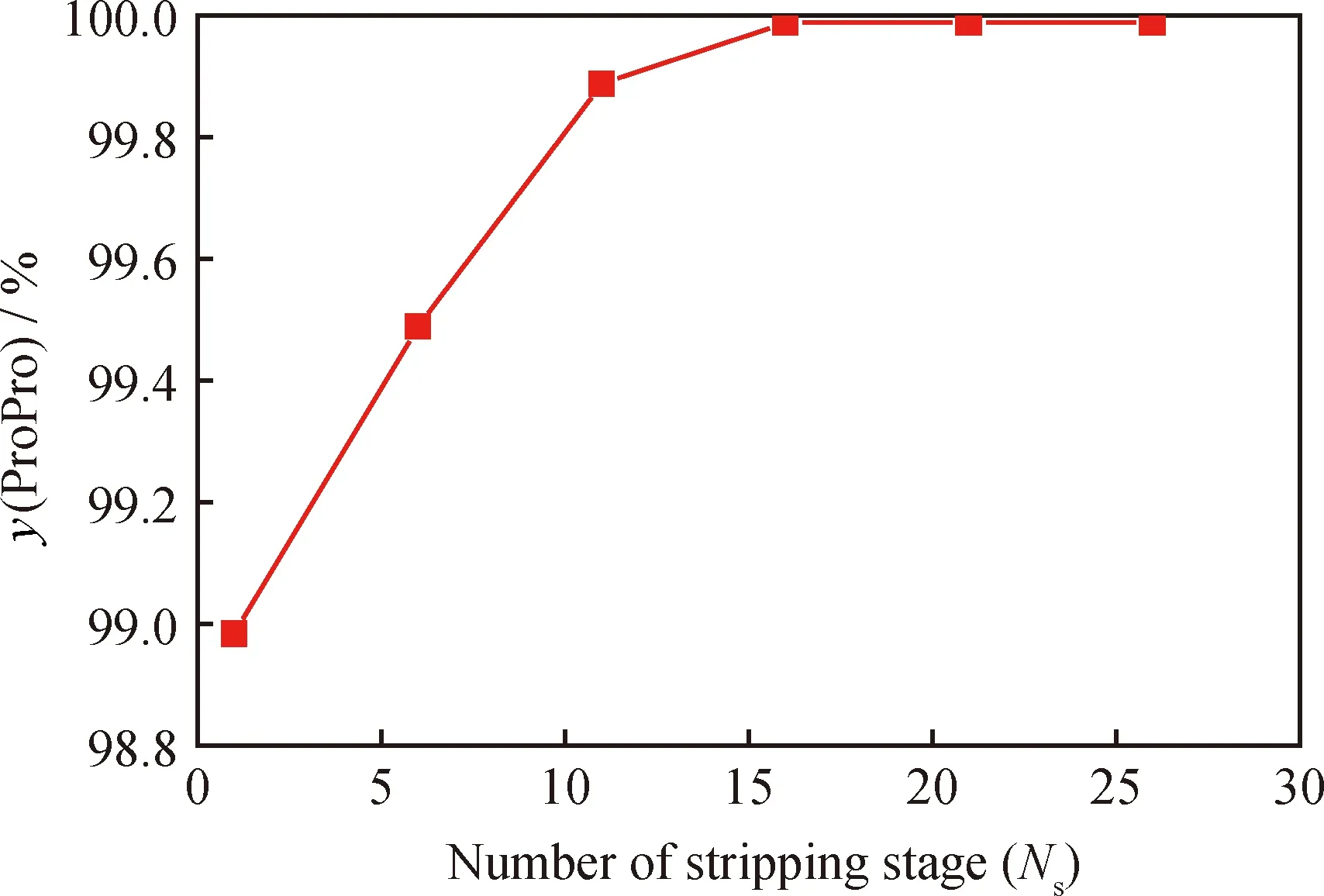
图11 提馏段塔板数(Ns)对反应精馏合成丙酸丙酯产物中丙酸丙酯摩尔分数(y(ProPro))的影响
由图11可以看出,正丙醇和丙酸反应精馏产物中丙酸丙酯的摩尔分数随提馏段塔板数的增加而增加。塔板数在1~11之间,丙酸丙酯的摩尔分数增加较快;塔板数超过11块之后,增加趋势变慢;塔板数在15以上时,产物中丙酸丙酯的摩尔分数基本不再随塔板数的增加而变化。从经济和产品纯度两方面综合考虑,提馏段塔板数为11较合适,此时产物中丙酸丙酯的摩尔分数达到99.88%。
2.3.5 反应精馏塔液相组成分布
从反应精馏合成丙酸丙酯的过程模拟中得到反应精馏塔内各组成分布数据,结果示于图12。
由图12看出,反应段内正丙醇和丙酸发生酯化反应生成了丙酸丙酯和水,少量丙酸丙酯与水和未反应的正丙醇形成三元共沸物进入精馏段,其中丙酸丙酯是其主要组分;大部分丙酸丙酯、水和未反应的正丙醇和丙酸在提馏段得到分离,从而得到摩尔分数高达99.88%以上的丙酸丙酯产品。
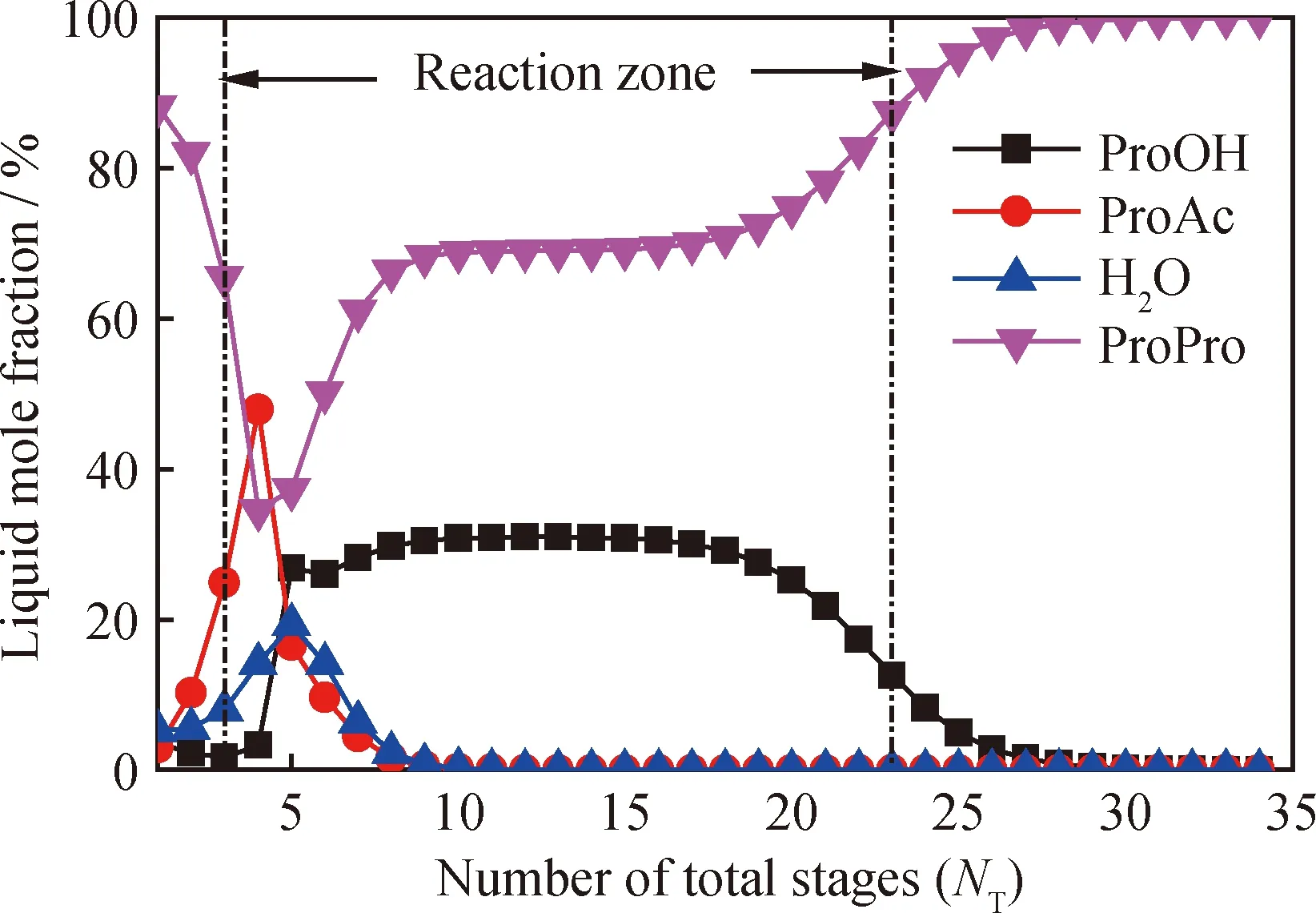
图12 正丙醇和丙酸反应精馏体系内液相组成随总塔板数(NT)的分布
3 结 论
(1) 为了对反应精馏合成丙酸丙酯进行模拟,采用动力学装置考察了催化剂用量、醇/酸摩尔比、反应温度和搅拌转速对丙酸转化率的影响,以获得模拟所需的动力学参数。最佳操作条件为催化剂用量为15 g、醇/酸摩尔比1.2、反应温度80℃、搅拌转速400 r/min。
(2) 建立了正丙醇和丙酸合成丙酸丙酯反应动力学方程
(3) 将反应动力学数据运用到模拟反应精馏合成丙酸丙酯过程中,讨论了进料温度、各段塔板数对产物纯度的影响。最佳反应精馏合成丙酸丙酯的条件为进料温度70℃、精馏段塔板数2、反应段板数21、提馏段塔板数11,此时丙酸丙酯产品的纯度(摩尔分数)达到99.88%以上。
[1] 郑来昌, 索继栓. 丙醇铝催化丙醛一步合成丙酸丙酯[J].精细石油化工进展,2001,2(7):5-7.(ZHENG Laichang, SUO Jishuan. Synthesis of propyl propionate from propanal by catalysis of aluminum propoxide[J].Advances in Fine Petrochemicals, 2001, 2(7): 5-7.)
[2] 谭志斗, 刘菊英, 李国祥.硫酸钛催化合成丙酸丙酯[J].湖北民族学院学报:自然科学版,2005,21(3):43-45.(TAN Zhidou, LIU Juying, LI Guoxiang. Catalytic synthesis of propyl propionate by Ti(SO4)2·4H2O[J]. Journal of Hubei Institute for Nationalities(Natural Science Edition), 2005, 21(3): 43-45.)
[3] ALTMAN E, KREIS P, VAN GERVEN T, et al. Pilot plant synthesis ofn-propyl propionate via reactive distillation with decanter separator for reactant recovery.Experimental model validation and simulation studies[J]. Chemical Engineering and Processing: Process Intensification, 2010, 49(9): 965-972.
[4] KELLER T, MUENDGES J, JANTHARASUK A, et al. Experimental model validation forn-propyl propionate synthesis in a reactive distillation column coupled with a liquid-liquid phase separator[J]. Chemical Engineering Science, 2011, 66(20): 4889-4900.
[5] WILLIAM L L, YU C C. Reactive Distillation Design and Control[M]. New York: John Wiley & Sons, 2009.
[6] MALONE M F, DOHERTY M F. Reactive distillation[J]. Industrial & Engineering Chemistry Research, 2000, 39(11): 3953-3957.
[7] BLAGOV S, BESSLING B, SCHOENMAKERS H, et al. Feasibility and multiplicity in reaction-distillation processes for systems with competing irreversible reactions[J]. Chemical Engineering Science, 2000, 55(22): 5421-5436.
[8] 徐红, 秦继伟, 李旭峰,等.反应精馏制备醋酸异辛酯新工艺的模拟研究[J].现代化工,2013,33(12):126-129.(XU Hong, QIN Jiwei, LI Xufeng, et al. Simulation study of new process for acetic acid isooctyl ester by reactive distillation[J]. Modern Chemical Industry, 2013, 33(12): 126-129.)
[9] WILLIAM L L, PSZALGOWSKI K M, SCHAEFER M R, et al. Design and control of conventional and reactive distillation processes for the production of butyl acetate[J]. Industrial & Engineering Chemistry Research, 2004, 43(25): 8014-8025.
[10] LIN Y D, CHEN J H, HUANG H P, et al. Process alternative for methyl acetate conversion using reactive distillation: Transesterification versus hydrolysis[C]//Proceedings of the AIChE Annual Meeting, San Francisco (CA), 2006.
Simulation and Reaction Kinetics of Synthesis of Propyl Propionate by Reactive Distillation
XU Hong, WEI Wei, YU Hao, YE Qing
(InstituteofPetrochemicalTechnology,ChangzhouUniversity,Changzhou213164,China)
The reaction kinetics ofn-propyl propionate synthesis fromn-propyl alcohol (ProOH) and propionic acid (ProAc) was studied by using strongly acidic ion-exchange resin Amberlyst46TMas catalyst in the reaction kinetics apparatus. The influences of the catalyst dosage, the mole ratio of ProOH to ProAc, the reaction temperature, the stirrer speed on the conversion of ProAc were discussed under the condition of eliminating both internal and external mass transfer resistances. The catalyst dosage of 15 g, the ProOH to ProAc mole ratio of 1.2, the reaction temperature of 80℃ and the stirrer speed of 400 r/min were the optimum operating conditions, under which the parameters of reaction kinetics, i.e, reaction activation energyEa=40.35 kJ/mol and pre-exponential factork0=2.16×103L/(mol·min), were obtained. The influences of the feed temperature and the stage number of each section on the purity of product were discussed as the parameters obtained were applied in steady-state simulation. The feed temperature of 70℃, 2 trays in rectifying section, 21 trays in reaction section and 11 trays in stripping section were the optimized operating conditions, under which the productn-propyl propionate of above 99.88% of molar fraction was obtained.
reaction distillation;n-propyl propionate; reaction kinetics; ion-exchange resin
2014-07-07
中国石油化工股份有限公司基金项目(411024)资助
徐红,女,硕士研究生,从事传质与新型分离技术方面的研究
叶青,女,教授,博士,从事化工分离过程方面的研究;Tel:0519-86330355;E-mail: yeqing@cczu.edu.cn
1001-8719(2015)06-1363-07
TQ 225.2
A
10.3969/j.issn.1001-8719.2015.06.016

