手性双烯配体的合成介绍
宋瑞娟
(西安文理学院化学工程学院,陕西西安 710065)
手性双烯配体的合成介绍
宋瑞娟
(西安文理学院化学工程学院,陕西西安710065)
手性双烯配体是近年来用于不对称催化反应中的一种新型配体,该类型配体的出现为过渡金属催化的不对称反应研究开辟了新的领域, 成为近年来研究的热点,一系列不同骨架的结构的手性双烯配体被相继报道。本文综述了手性双烯配体的合成研究现状,重点介绍了其合成方法:不对称催化合成法、手性源合成法和外消旋体拆分法,并总结了各种合成方法的优缺点。
手性双烯合成综述
手性双烯配体是Hayashi课题组在2003年首先发现的一种结构特殊的新型手性配体。该类型配体的出现为过渡金属催化的不对称反应研究开辟了新的领域,成为近年来研究的热点,一系列不同骨架的结构的手性双烯配体被相继报道。本文主要就手性双烯配体配体的制备方法做一简要介绍。
目前使用的手性双烯配体主要通过以下三种途径获得:不对称催化合成法、手性源合成法和外消旋体拆分法。
1 不对称催化合成法
最早Hayashi等采用的手性双烯配体就是用不对称催化反应制备得到(图1)[1]。降冰片二烯(二环庚二烯,缩写NBD)1在Pd/(R)-MeO-mop的存在下经不对称氢硅烷化反应得到99%ee光学纯的二醇2[2]。经Swern氧化后,其中一个羰基转化为缩醛保护起来,得到3.在LDA和PyNTf2的作用下,3转化为三氟甲磺酸烯酯化合物,接下来以PdCl2(dppf)为催化剂,与BnMgBr经交叉偶联反应得到4。水解缩醛,对另一个羰基重复同样的反应,得到(1R,4R)-2,5-二苄基二环[2.2.1]庚-2,5-二烯5(用类似的方法也得到了配体6)。
2 手性源合成法
Carreira课题组合成了一种手性二环[2.2.2]辛二烯(图2)[3]。以廉价的萜烯(-)-香芹酮(7)作为原料,经NBS溴代,在tBuOK和tBuOH作用下,形成8和它的一个非对映异构体,色谱法分离。进而8转化为三氟甲磺基烯酯化合物,再通过偶联反应引入芳基,从而得到9和10)。这种方法简单有效,可以大量制备高度光学纯的手性双烯配体。
3 外消旋体拆分法
用于制备手性双烯的拆分法主要包括以下三种:化学拆分法、手性HPLC拆分法和有机金属配合物拆分法。
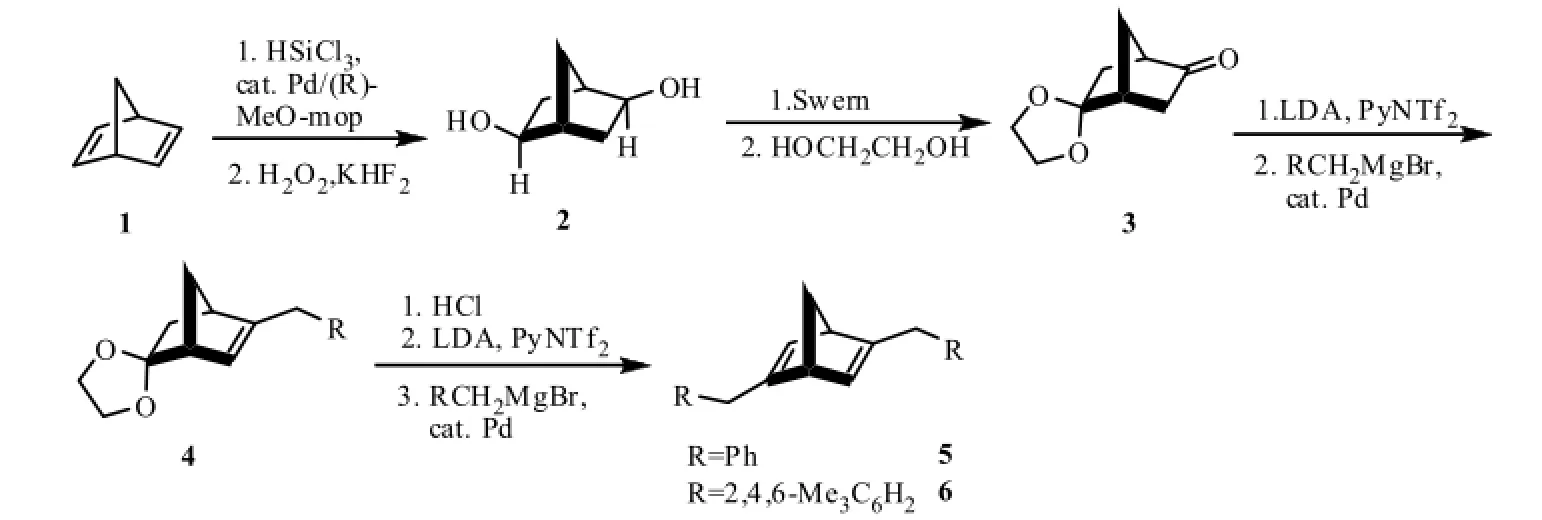
图1 手性二环[2.2.1]庚二烯 5 和 6的合成Fig.1 Synthesis of the chiral bicyclo[2.2.1]heptadienes 5 and 6

图2 手性二环[2.2.2]辛二烯9和10的合成Fig. 2 Synthesis of the chiral bicyclo[2.2.2]octadienes 9 and 10
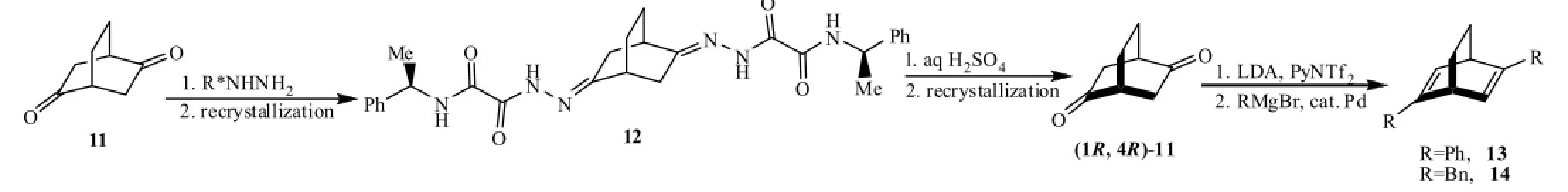
图3 手性二环[2.2.2]辛二烯27和28的合成Fig. 3 Synthesis of the chiral bicyclo[2.2.2]octadienes 27 and 28

图4 手性二环[3.3.1]壬二烯35和手性二环[3.3.2]癸二烯21的合成Fig.4 Synthesis of the chiral bicyclo[3.3.1]nonadienes 21 and bicyclo[3.3.2]decadienes 22
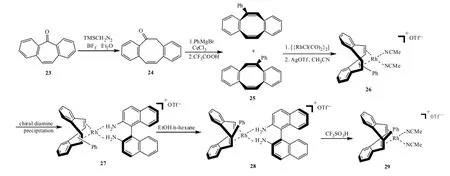
图5 取代的二苯基环辛二烯的拆分Fig. 5 Resolution of a substituted dibenzocyclooctatetraene
3.1化学拆分法
具有二环[2.2.2]辛二烯骨架的配体13和14可用化学拆分法获得(图3)[4]。利用外消旋的二酮11与(R)-5-(1-苯乙基)氨基草酰肼形成的腙可分步结晶的特点将其拆分,光学纯的(1R,4R)-二环[2.2. 2]辛-2,5-二酮(11)先转化为二(三氟甲磺酸烯酯),然后与BnMgBr或PhMgBr发生交叉偶联反应得到2,5-二取代二环辛二烯13和14。该方法产率低,主要是因为由拆分法得到关键中间体(1R,4R)-11的产率仅有0.5%。
3.2手性HPLC拆分法
具有二环[3.3.1]和二环[3.3.2]骨架结构的手性二烯配体即采用手性HPLC拆分法获得(图4)[5,6]。外消旋的二酮15与苯基铈试剂作用得到17。二醇17脱水后得到2,6-二苯基二环[3.3.1]壬-2,6-二烯19。通过制备高效液相色谱用手性固定相进行拆分,可获得光学纯度的21。22可依同样方法获得。
3.3有机金属配合物拆分法
Grützmacher课题组开发了有机金属配合物拆分法,即对映体通过外消旋的二烯络合物的形式与金属形成非对映异构体,接下来加入手性二胺,结晶分离(图5)[7]。
4 结语
在前面介绍的手性双烯配体的合成方法中,手性源合成法相对比较廉价,但可适合采用的手性源非常有限,而且配体的结构会受到采用的手性源的限制;拆分法也是目前获得手性双烯的主要方法之一,化学拆分法常常会受到各种底物的限制,且使用拆分试剂价格昂贵,拆分产率不高,限制了该方法的应用,而手性制备柱亦是非常昂贵,不适宜配体的大量制备;尽管目前已有一系列手性双烯配体被合成,并相继用于多种不对称催化反应,但开发高效、价廉的手性双烯配体依然是未来的一个重大挑战。不对称催化合成是最理想的合成方法,它仅用少量手性催化剂即可将大量潜手性底物对映选择性地转化为手性产物。从理论上讲,通过这种方法可以合成人们需要的任何手性物质。因此,设计合理的路线,通过不对称催化的方法获得手性双烯配体是未来的一大挑战。
[1]Hayashi T,Ueyama K,Tokunaga N,et al.A chiral chelating diene as a new type of chiral ligand for transition metal catalysts:Its preparation and use for the rhodium-catalyzed asymmetric1,4-addition[J].J.Am.Chem.Soc.2003,125(38):11508-11509.
[2]Uozumi Y,Lee S Y,Hayashi T.Asymmetric functionalization of bicycloalkenes by catalytic enantioposition-selective hydrosilylation[J].Tetrahedron Lett.1992,33(47):7185-7188.
[3]Fischer C,Defieber C,Suzuki T,et al.Carreira.Readily available [2.2.2]-bicyclooctadienes as new chiral ligands for Ir(I):catalytic,kinetic resolution of allyl carbonates[J].J.Am. Chem. Soc.2004,126(6):1628-1629.
[4]Tokunaga N,Otomaru Y,Okamoto K,et al.C2-Symmetric bicyclo[2.2.2]octadienes as chiral ligands:Their high performance in Rhodium-catalyzed asymmetric arylation of N-tosylarylimines[J].J.Am.Chem.Soc.2004,126(42):13584-13585.
[5]Otomaru Y,Tokunaga N,Shintani R,et al.C2-Symmetric bicyclo[3.3.1]nonadiene as a chiral ligand for Rhodium-catalyzed asymmetric arylation of N-(4-nitrobenzenesulfonyl)arylimines[J].Org.Lett.2005,7(2),307-310.
[6]Otomaru Y,Kina A,Shintani R, et al.C2-Symmetric bicyclo[3. 3.1]nona-2,6-diene and bicyclo[3.3.2]deca-2,6-diene:new chiral diene ligands based on the 1,5-cyclooctadiene framework[J]. Tetrahedron:Asymmetry,2005,16(9),1673-1679.
[7]La¨ng F,Breher F,Stein D,et al.Chiral olefins as steering ligands:syntheses of C1-symmetric dibenzo[a,e]cyclooctenes(Rdbcot)[J].Organometallics,2005,24(12),2997-3007.
陕西省教育厅科学研究计划及基地项目(14JK2132),西安市科技计划项目(CXY1352WL06)
宋瑞娟(1980—),女,山西临汾,讲师,研究方向为小分子有机合成。

