果胶改性及应用研究进展
孙绪兵,廖立敏,付孝锦(内江师范学院化学化工学院,“果类废弃物资源化”四川省高等学校重点实验室,四川内江641100)
果胶改性及应用研究进展
孙绪兵,廖立敏,付孝锦
(内江师范学院化学化工学院,“果类废弃物资源化”四川省高等学校重点实验室,四川内江641100)
果胶是一种天然高分子化合物,主链由带负电荷的半乳糖醛酸组成的同型聚糖,具有无毒、易降解及生物相容性等特点,广泛用于食品、医药和日化等行业,但存在抗水差、机械性能差和加工困难等缺点,常采用物理、化学和生物方法对其改性,不同的改性方法制备的改性果胶性质不同,主要有吸附、抗癌、抗菌和载药等。本文介绍了近二十年来对果胶改性及应用的研究进展,主要涉及烷基化、酰胺化、磺化、季铵化、巯基化、氧化、乙烯化、接枝以及共混等途径改性,并对果胶改性及应用进行展望。
果胶,改性,衍生物,应用
果胶是植物中的一种酸性多糖物质,主要存在于植物的细胞壁和细胞内层,主链是由D-半乳糖醛酸以α-(1→4)键相连而成,在半乳糖醛酸C6上羧基有许多以甲酯形式存在,未酯化的羧基以游离酸形式或钠盐等形式存在,其结构如图1所示。按其酯化度可分为高酯果胶(酯化度>50%或甲氧基含量7.0%~16.3%)和低酯果胶(酯化度≤50%或甲氧基含量≤7.0%),高酯果胶只能在可溶性固形物高于55%和pH在2~3.5之间才能凝胶,低酯果胶在钙离子或其他二价阳离子存在下有糖或无糖均能形成凝胶[1]。果胶能溶于水,不溶于乙醇和其他有机溶剂,无毒、易降解、不污染环境和生物相容性,具有良好的凝胶性、吸附性、增稠性、稳定性和成膜性,广泛用于食品、医药和日化等行业。但因其抗水和机械性能差以及加工困难等缺点,限制了其应用。基于果胶分子中存在羧基、羟基和甲氧基等特征基团,可通过物理、化学和生物方法对其进行改性。魏子淏等[2]从柑橘果胶结构和特点、化学改性(酸法脱酯改性、碱性脱酯改性和酰胺化脱酯改性)、生物改性(酶法脱酯)、物理改性(高温高压和冷冻处理)以及改性果胶生理功能特性进行综述,而对其他化学改性果胶方法及应用提及较少。本文对近二十年来通过烷基化、酰胺化、磺化、季铵化、巯基化、氧化、乙烯化、接枝以及共混等途径对果胶改性及应用进行了综述,并对果胶改性及应用进行展望。
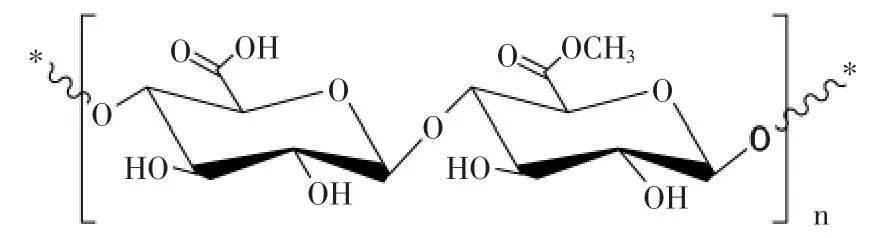
图1 果胶结构示意图Fig.1 Structure sheme of pectin
1 烷基化改性
果胶可与酸酐或卤代烃反应进行烷基化改性,常用的酸是十六烷酸、十八烯酸、(Z,Z)-9,12-十八烷二烯酸,卤代烃是溴代烷。制备的烷基化果胶改变了凝胶性、水溶性、乳化性能、抗菌性以及热稳定性等。
1.1与酸酐反应
果胶与酸酐反应首先是将酸制备成酸酐,以碳酸钾作催化剂对果胶进行酯化改性,反应如图2所示。Monfregola等[3-4]在高温无溶剂、Kamnev等[5]和Calce等[6-7]以微波辅助使用以上三种酸酐对果胶改性。改性后保留原果胶结构,降解方式与未改性果胶相似,吸水率具有双重吸附行为,随取代度增加而降低。十六烷酸改性具有疏水性,而(Z,Z)-9,12-十八烷二烯酸、十八烯酸改性仅在高浓度下才具有疏水性。十八烯酸和(Z,Z)-9,12-十八烷二烯酸改性果胶不仅能够抑制金黄色葡糖球菌和大肠杆菌生长,而且胶涂覆到聚乙烯薄膜上能够降低氧气的渗透,可用在食品包装材料中。Renard等[8-9]使用乙酸酐对果胶改性。乙酰化果胶流体力学体积变化不大,能溶于乙醇和丙酮,能抑制酶水解,在钙离子、锌离子和铅离子存在下不能形成凝胶,相比于未乙酰化果胶因引入更多比例的非水溶性基团使得乙酰化果胶具有优异的乳化性能[10]。Almeida等[11]制备了酯化度为24%的无定形马来酸酐改性果胶。改性后引入更多酯基和存在有序区域使热稳定提高,外观形态发生明显变化,表面负电荷增加,能够有效抑制结肠癌细胞的成长,对非洲绿猴肾细胞没有任何毒素影响,可用于抗肿瘤生物相容性材料。
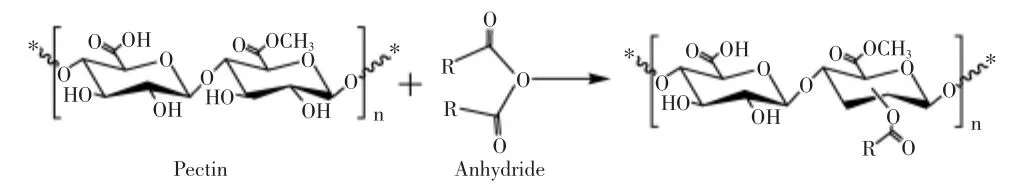
图2 酸酐烷基化果胶反应示意图[6,8]Fig.2 Reaction scheme for the alkylation of pectin with anhydride[6,8]
1.2与卤代烃反应
果胶与卤代烃反应具有两种历程,一是在碱性溶液中,果胶中羟基氢被烷基取代成醚,将长链烷基引入果胶[12]。另一种是以二甲基亚砜(DMSO)为溶剂,烷基铵盐(TBAI)为催化剂,果胶羧基与卤代烷中烷基生成酯[13]。改性后果胶水溶性随烷基碳数目改变,碳数目越多,疏水性越强。反应如图3所示。Morris等[14]将低甲氧基果胶和去酯果胶使用以上两种反应历程分别与对溴甲基苯甲酸和苄基溴反应。去酯果胶引入少量对甲基苯甲酸醚对流体力学性质无影响,而低甲氧基果胶因发生β消除反应使果胶链裂解使得分子量降低,尤其与苄基溴反应更加明显。余杰等[15]使用两种方法将溴代烷(溴代十二烷和溴代辛烷)对果胶进行疏水改性,制备了改性果胶/壳聚糖水凝胶。两种改性果胶水溶性均低于未改性果胶,羟基烷基化果胶不能与壳聚糖形成很好的水凝胶;酯化果胶与壳聚糖水凝胶成胶良好,水凝胶饱和溶胀度大大降低,对硝苯地平具有缓释作用。

图3 卤代烃烷基果胶反应示意图[14]Fig.3 Reaction scheme for the alkylation of pectin with halogenated hydrocarbons[14]
2 酰胺化改性
酰胺化改性果胶指果胶上的甲氧基被胺基取代或使用1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(EDC)活化羧基与胺基进行酰胺化反应,反应如图4所示。Sinitsya等[16]在甲醇溶液中,使用13种伯胺与高甲氧基果胶进行氨基取代甲氧基得到部分酰胺果胶,产率因伯胺结构和反应条件不同在6%~70%之间变化。改性果胶的物理化学性质和应用与引入胺的结构有关。脂肪胺和芳香胺改性果胶的水溶性比未改性果胶水溶性差,含极性或带电基团胺仍保持良好水溶性,含阳离子基团胺具有两亲性,含碳碳双键或芳环胺可进行加成或取代反应,含氯、环氧乙烷或其他氨基酸胺可以分子间交联。酰胺果胶的亲水亲油性还与取代度有关,如胆汁酸、脂肪酸和胆固醇,吸附性能随取代度增加而提高[17-18]。Kurita等[19]为了解决果胶在食品行业应用中溶解过程容易结块的问题,增加果胶水溶性,使用甘氨酸、甘氨酸甲酯和双甘氨肽在极性有机溶剂中对果胶进行改性,甘氨酸和双甘氨肽改性果胶水溶性明显提高。Munarin等[20]制备了可用于细胞组织工程输送且具有较高的细胞相容性和可调节生物降解性精氨酰-甘氨酰-天冬氨酸(RGD肽)改性果胶。Fajardo等[21]在碱性条件下,通过EDC活化羧基,得乙二胺改性果胶。在酸性条件下,酰胺果胶氨基硫酸软骨素磺酸基通过静电作用形成表面粗糙、孔分布不规则的紧凑聚电解质复合物,可用于细胞生长的生物材料。通过酰胺化反应,可使具有生物活性的氨基酸、肽、酶等固定到果胶分子上。此外,Mishra等[22]使用戊二醛交联乙醇胺酰胺果胶制备了水凝胶膜。该薄膜结晶度提高,拉伸强度降低,溶胀性能和释药性能随胺基的增多而加快,具有较好的保水性能和B-16黑色素瘤细胞和人血兼容等生物相容性,可作为伤口敷料。

图4 果胶酰胺化反应示意图[16,21]Fig.4 Reaction scheme for the amidation of pectin[16,21]
3 磺化改性
磺化改性是指果胶分子结构单元C2和C3结构单元中部分羟基与含磺酸基团的物质如氯磺酸、3-氯-2-羟基丙磺酸、三氧化硫等反应,常用的溶剂有甲酰胺、吡啶和二甲基亚砜等,反应如图5所示。Cipriani等[23]和Maas等[24]制备的磺化果胶可通过抑制α凝血酶和凝血酶原激酶形成而具有抗凝血和抗血栓活性。Bae等[25]制备的磺化果胶黏度降低,絮凝能力、抗芽孢杆菌和费希尔弧菌能力提高。
4 季铵化改性
同磺化改性一样,果胶上的羟基可以与氯化铵盐进行季铵化改性得到季铵化阳离子果胶。常用的铵盐是3-氯-2-羟丙基三甲基氯化铵(CHPTMAC)[26-28],反应如图5所示。得到的季铵盐改性果胶吸潮率和保湿率随季铵化度增加而增加,对葡萄球菌菌株、大肠埃希氏菌和枯草芽胞杆菌具有明显的抑制效果,能够与质粒DNA形成复合物,可用于制药、包装、防腐和化妆等领域。Yang等[29]利用微波辅助制备的季铵盐改性柑橘果胶絮凝剂,在模拟废水中对色拉油和六价铬的去除率分别为79%和77%。通过优化合成吸附条件以及添加硫酸锌和聚氯化铝,可使去除率分别达到95%和98.4%。王春香等[30]也进行了类似研究。

图5 果胶磺化(季铵化)反应示意图[27-29]Fig.5 Reaction scheme for the sulfation(quaternization)of pectin[27-29]
5 巯基化改性
巯基化改性是指将巯基(氨基)酸通过酰胺化反应或酯化反应将巯基引入果胶,反应如图6所示,巯基改性保留了果胶凝胶性,极大提高了黏附性能(氧化巯基生成二硫键)。Majzoob等[31]使用巯基丙氨酸通过酰胺反应改性果胶,并制备了巯基丙氨酸果胶锌珠。巯基改性果胶保留了原果胶的生物相容性、降解性、低毒性和凝胶性,提高了溶胀比,渗透性提高了1.61倍,黏附性能整整提高5倍。巯基丙氨酸果胶锌珠通过氧化形成二硫键显著提高了巯基果胶在模拟胃肠道的稳定性,释放胰岛素曲线和未改性果胶锌珠具有相同趋势,其结论与Sharma等[32-33]制备的巯基乙酸改性果胶凝胶相同,可用于黏膜系统给药。Perera等[34-35]通过喷雾干燥法将结肠药物甲硝唑与对氨基硫酚改性果胶制备成颗粒,研究表明巯基的引入提高崩解特性,6 h内释放的甲硝唑是未改性果胶的1/34.4,缓释的甲硝唑可以通过加入果胶酶或还原剂加速释放,但是巯基改性果胶对细胞存活率没有显著影响,可作为结肠定位载药使用。Hauptstein等[36]为了提高巯基聚合物的pH使用范围和反应活性,用L-半胱氨酸改性果胶,加入2-巯基-3-吡啶甲酸得到二聚体,通过交换反应得到含二硫键的改性果胶。结果表明,巯基改性使得崩解时间延长2倍,黏附性能提高5倍,释放时间可持续36 h,降低了pH依赖性,对压成的药片硬度无影响,因此含二硫键的改性果胶可以用在黏膜黏附药物释放,特别是难溶性药物的吸收利用。

图6 果胶巯基化反应示意图[32-35]Fig.6 Reaction scheme for thiolation of pectin[32-35]
6 乙烯化改性
果胶可与含乙烯官能团的化合物进行反应,向果胶中引入乙烯基,常用的乙烯基官能团化合物是甲基丙烯酸缩甘油酯,反应如图7所示。已见报道的多糖与甲基丙烯酸缩甘油酯进行反应存在两种途径[37],酯交换或者开环反应,具体采用何种方式取决于反应溶剂。当使用极性非质子溶剂如二甲基亚砜,则为快速可逆的酯交换机制;当使用酸性水溶液介质,则属于缓慢不可逆的开环反应机制。制备的乙烯果胶进一步聚合得到具有pH和时间响应的材料。Maior等[38]用过硫酸钠引发开环反应制备的甲基丙烯酸缩甘油酯果胶,通过溶液浇铸制备了具有pH和时间响应以及可降解性薄膜,该膜可作为药物涂层防止药物提前释放,使药物能够准确有效的释放。Guilherme等[39]用N,N’-亚甲基双丙烯酰胺(MBA)交联甲基丙烯酸缩甘油酯果胶制备得到具有pH响应水凝胶,其溶胀率随pH增加和乙烯化果胶含量增加而增加,当pH超过6溶胀速率常数明显降低,凝胶吸水接近平衡,溶胀过程变慢,凝胶吸水降低。Silva等[40]利用甲基丙烯酸缩甘油酯分别与果胶和二氧化钛在pH3.5盐酸溶液中进行乙烯化改性,以聚乙烯醇为乳化剂,加入四氧化三铁,过硫酸钠为引发剂,超声反应制备了四氧化三铁/二氧化钛/果胶纳米微球。微球中微粒之间通过无机物与果胶之间物理和化学作用连接,释放抗生素阿莫西林的速率比纯果胶微球慢,在酸性介质通过大分子松弛持续释放。在远程磁场的作用下,通过打断纳米微球的松弛和扭曲效应来阻止释放药物,防止药物提前释放,使药物载送到指定位置。此外,细胞毒性研究表明,果胶中引入四氧化三铁和二氧化钛毒性水平在可接受范围之内,因此该纳米微球在生物材料中具有应用潜能。

图7 果胶乙烯化反应示意图[38,40]Fig.7 Reaction scheme for vinylation of pectin[38,40]
7 氧化改性
果胶是一组聚半乳糖醛酸,重复半乳糖醛酸单元C2和C3邻羟基能够被高碘酸或高碘酸盐氧化断裂,形成开链二醛衍生物,反应如图8所示。Gupta等[41-42]报道了反应条件对高碘酸氧化果胶产物产率影响以及反应条件对高碘酸氧化果胶与明胶原位交联反应的交联度影响。Takei等[43]将抗肿瘤药物阿霉素通过亚胺键连接到氧化果胶,乙二酸二酰肼交联得到水凝胶,其释放阿霉素的速率可以通过调节乙二酸二酰肼与氧化果胶的比例控制,释放的阿霉素仍然具有抗癌活性,释放的氧化果胶同未改性果胶相比能够有效阻止同型癌细胞聚集,因此能够抑制体内癌细胞转移。Munarin等[44]为了调整细胞粘附和提高果胶的生物降解性,将果胶使用高碘酸钠进行氧化改性,改性后可能因为β糖苷键旋转自由度大,导致水解使特性粘度和分子量降低,具有良好微球成型、生物相容性、低毒性、速降解性和机械性能,可作为细胞输送材料使用。

图8 果胶氧化反应示意图[41,44]Fig.8 Reaction scheme for oxidation of pectin with periodate[41,44]
8 接枝改性
果胶可以通过自由基聚合进行接枝改性,接枝单体包括丙烯酰胺(AM)、丙烯酸(AA)、甲基丙烯酸(MAA)、N-异丙基丙烯酰胺(NIPAM),2-丙烯酰氨基-2-甲基丙烷(AMPS)等水溶性单体,常用的引发剂有过硫酸盐、硫酸铈铵以及过硫酸盐-亚硫酸氢盐等氧化还原体系等,反应如图9所示。此外还常加入交联剂MBA,改性后增大了果胶分子量,改善了果胶的物理化学性质,可用于废水处理和药物释放等领域。果胶在食品加工过程中由于受到剪切而不稳定,为了提高其剪切稳定性,Mishra等[45]将AM接枝到果胶。Chauhan等[46]将制备的AM接枝果胶用于水处理中阻止硫酸钙垢的形成。Geethanjali等[47]研究了AA(钠)或AM接枝果胶在3.5%NaCl溶液中碳钢的缓释性能。结果表明这两种果胶接枝共聚物缓蚀率大约为85%,AM接枝果胶缓蚀性能略高于AA接枝果胶。Sutar等[48]使用戊二醛交联AM接枝果胶得到凝胶膜,该薄膜的成膜性能和凝胶性能优于未接枝果胶,并且具有生物相容性,对水杨酸释放具有pH响应,因此该薄膜能够用于药物释放和生物植入材料使用。此外Chauhan等[49]将AM、NIPAM、AMPS分别与果胶进行接枝改性,并制备了水凝胶,研究水凝胶吸附废水中金属离子和生物降解性能。结果表明制备的水凝胶具有温度和pH响应,水凝胶对废水中金属离子吸附具有选择性,AMPS接枝果胶水凝胶具有高吸水率和降解性能。

图9 果胶接枝反应示意图[45,49]Fig.9 Reaction scheme for grafting of pectin[45,49]
9 共混改性
果胶因其抗水性差和强度低限制其应用,为了拓宽应用范围和使用条件,一种方法是通过与其他聚合物共混,另外一种就是加入无机填料。常用的聚合物是壳聚糖、直链淀粉、海藻酸钠等,常用的无机纳米材料是氧化铁、氧化锌、硫化镉,共混物可以作为药物载体、食用薄膜、染料和金属离子吸附剂等。
9.1与天然高分子化合物共混
将果胶与聚合物共混不仅不影响其优异性能,而且能够得到单独使用时没有的性能,更加重要的是开发了制备果胶基新材料的途径,通过共混可以提高果胶的力学性能、扩大应用范围。在碱性条件下,果胶和直链淀粉可使用三偏磷酸钠进行交联改性。交联改性提高了果胶的杨氏模量、临界应力、应变回复率,降低了透湿性;热稳定性随着果胶含量增加而增加;载药凝胶流变性随果胶含量的增加而变差;凝胶强度随直链淀粉比例的增加而增大。在模拟结肠消化液中改性果胶抗酶降解能力提高,但吸水率未得到显著改善,可以用作结肠药物包覆使用[50-52]。Patel等[53]制备了包覆美沙拉嗪、吲哚美辛的果胶/壳聚糖共混薄膜,壳聚糖的引入降低了包覆层厚度,且能保护药物提前释放,其结论与Fernández-Hervás等[54]相同。Kaur等[55]制备果胶/壳聚糖共混物,载送盐酸卡维地洛的利用率比直接口服高2.14倍。宋燕等[56]采用离子移变胶凝法,以三聚磷酸钠、氯化钙为固化剂,制备载胰岛素的壳聚糖/果胶微球。微球中果胶与壳聚糖以物理作用连接,外观圆整,粒径大小分布均匀,体外释药具有明显的缓释作用,但是包封率有待提高。Galus等[57]采用溶液浇铸方法制备了海藻酸钠/低甲氧基果胶薄膜,得到的薄膜连续均匀透明,外观不受复合膜组成变化影响,厚度随果胶的增加而增加,机械性能取决于共混膜的组成配比和相容性。Cataldo等[58]报道了海藻酸钠/果胶钙凝胶球吸附二价铬和铜离子,吸附机理主要为离子交换,吸附量随着凝胶中果胶比例增加而升高。Giosafatto等[59]使用柑橘果胶和菜豆蛋白质为原料,转谷氨酰胺酶为交联剂,制备了可食用性薄膜。该薄膜机械性能,阻二氧化碳、氧气和水蒸气渗透性能与化学合成塑料具有相同特点,可在4℃或-20℃低温下使用;在模拟胃液和十二指肠液中,因含转谷氨酰胺酶更加容易被消化,可作为食品包装材料使用。此外,果胶还可以与壳寡糖[60]、溶菌酶[61]等进行共混改性。
9.2与合成聚合物共混
为了提高果胶薄膜的热稳定性和机械性能,Mishra等[62]以戊二醛交联果胶和聚乙烯吡咯烷酮共混物制备了水凝胶薄膜,共混使玻璃化转变温度升高,拉伸强度随聚乙烯吡咯烷酮含量的增加而增大,该薄膜能溶胀,药物释放具有pH响应,与B16黑色素瘤细胞具有生物相容性。Liu等[63]制备了果胶/聚丙交酯-乙交酯复合材料,其力学性能远远优于纯果胶,与聚丙交酯-乙交酯相当,保水性和与蛋白质反应活性与果胶相当,与细胞的黏附性能得到提高,复合物材料的侧链还可以进一步化学改性,可用于组织再生和活性物质的载送。黄曹[64-66]、姚女兆等[67]以果胶和聚乙烯醇通过分子间氢键或互穿交联形成水凝胶。该水凝胶具有一定结晶度,存在两种结晶区,具有多孔结构,软而韧、蠕变特性好,缓冲载荷能力较强,渗透性好和溶胀性能好等特点;是一种比较好的粘弹性材料,细胞毒性为0~1级,生物相容性良好,可用于替代病变椎间盘髓核组织。
9.3与无机纳米材料共混
有机无机纳米复合材料因其协同效应倍受重视,兼具无机有机组分的优点,并且在力学、电磁学、生物学等方面赋予材料许多优异的性能,正成为材料科学研究的热点之一。果胶具有无毒、易降解、及生物相容性等特点,因此以果胶为有机组成的复合纳米材料相继被报道。Shi等[68]在室温水溶液中将纳米氧化锌掺入果胶中,得到颗粒大小为150 nm,平均直径为70 nm的无机有机复合纳米材料氧化锌/果胶。该纳米材料在肠胃中易被吸收,可用于食品行业。Gupta等[69]采用共沉淀法制备了果胶/硫化镉纳米复合材料,研究其光降解亚甲基蓝染料。结果表明:光照6 h后,可见光照射降解亚甲基蓝为95.5%,钠灯照射降解为89.9%,同时该材料具有优异的抗菌活性。Gong等[70]采用直接包裹共沉淀法合成了球形果胶/氧化铁纳米磁性材料。该纳米材料能够吸附铜离子,吸附机制为离子交换和静电吸附,最大的吸附量为48.99 mg/g,吸附后能用乙二胺四乙酸再生循环使用,循环一次为93.7%,循环五次为58.66%。Sahu等[71]用氯化钙交联超顺磁性氧化铁纳米材料和果胶溶液制备了球形纳米材料,在模拟肠液中是稳定的,可作为药物载体、磁流体热疗等应用。Rakhshaee等[72-73]通过超声制备了戊二醛或己二酸交联果胶/氧化铁纳米微粒,其吸附亚甲基蓝的能力为:己二酸交联果胶/四氧化三铁>戊二醛交联果胶/四氧化三铁>果胶/四氧化三铁纳米材料。Dai等[74]先用十一烯酸和十八烯酸对氧化铁进行改性,超声振荡下制备了具有带负电荷的氧化铁/钙离子/果胶的两相界面纳米材料,具有高饱和磁化度、超顺磁性、高生物相容性和生物降解性,可作为药物的优异的载体通过磁体快速高效的到达指定位置释放,减少副反应的发生。
此外,科研工作者还将果胶与天然高分子和合成聚合物或无机材料制备成三元共混物来改性。Tsai等[75]制备了壳聚糖/果胶/阿拉伯胶三元共混薄膜,其载送的胰岛素能在6 h完全释放。Tripathi等[76]制备的壳聚糖/聚乙烯醇/果胶三元共混膜能结晶,表面粗糙不均匀,对大肠杆菌、金黄色葡糖球、芽孢杆菌、假单胞菌和白色念珠菌具有抗菌活性,可用于食品包装材料。Ghaffari等[77]以果胶、壳聚糖、和丙烯酸树脂为原料制备了系列共混膜。结果表明:制备的共混膜都是不混溶无定型的,果胶和壳聚糖复合物成膜的pH在这两种聚合物酸度系数(PKa)之间。果胶/壳聚糖薄膜是水溶性的,溶胀过程具有pH响应,在pH7.4磷酸盐缓冲溶液中溶胀比是pH6的磷酸缓冲溶液的2.5倍,因其高溶胀比使果胶/壳聚糖薄膜在模拟小肠中会提前溶胀而使药物释放,因此需要添加非水溶性聚合物丙烯酸树脂降低溶胀比。由壳聚糖/果胶/丙烯酸树脂薄膜释放茶碱曲线具有S特征,在pH6的磷酸盐缓冲溶液具有一个突然释放过程,初始阶段缓慢释放,改变pH立刻变为突然释放,其原因可能是由于改变了膜的孔隙大小。而果胶/丙烯酸树脂,丙烯酸树脂薄膜药物释放具有线性特征。果胶酶加入不能明显影响膜药物释放。Dutta等[78]制备了新型球状100~150 nm的果胶/壳聚糖铁磁性纳米材料,相比于果胶钙纳米材料对药物双氯芬酸钠包封率60.6%,该纳米材料因壳聚糖的协同效应可使包封率达到99.5%。体外药物释放具有缓释和pH响应特性,在pH7.4的磷酸盐缓冲溶液中药物释放曲线遵从Korsemeyer-Peppas模型溶胀控制机理。该纳米材料具有饱和磁化强度、超顺磁性和药物缓释性质,可以用于磁性靶向药物释放。
10 结论与展望
果胶作为天然生物高分子,具有无毒、易降解及生物相容性等性能,随着人们对果胶质量和用量要求越来越高,单一的结构很难满足社会发展的需要,物理、化学和生物改性的研究将赋予果胶新的性质,其改性发展趋势为:引入新的活性功能基团物质开发新的合成路线制备新型材料,使产品多样化,功能明确化;不断深入研究果胶及衍生物结构,更加注重果胶改性机理研究;探索改性果胶在人体内的功能特征以及代谢机理,以期待改性果胶材料在医疗中取得更加广泛应用;加快改性果胶生产产业化程度。果胶作为FAO/WHO推荐的不限定每日摄取量食品添加剂,相信改性果胶在食品和医药领域具有广阔的发展前景。
[1]张学杰,郭科,苏艳玲.果胶研究新进展[J].中国食品学报,2010,10(1):167-174.
[2]魏子淏,杨伟,刘夫国,等.改性柑橘果胶研究进展[J].中国食品添加剂,2014,25(3):194-200.
[3]Monfregola L,Leone M,Vittoria V,et al.Chemical modification of pectin:environmental friendly process for new potential material development[J].Polymer Chemistry,2011,2(4):800-804.
[4]Monfregola L,Bugatti V,Amodeo P,et al.Physical and water sorptionpropertiesofchemicallymodifiedpectinwithan environmentally friendly process[J].Biomacromolecules,2011,12:2311-2318.
[5]Kamnev A A,Calce E,Tarantilis P A,et al.Pectin functionalised by fatty acids:Diffuse reflectance infrared Fourier transform(DRIFT)spectroscopic characterisation[J].Journal of Molecular Structure,2015,1079:74-77.
[6]Calce E,Bugatti V,Vittoria V,et al.Solvent-Free Synthesis of Modified Pectin Compounds Promoted by Microwave Irradiation[J].Molecules,2012,17(10):12234-12242.
[7]Calcea E,Mignognab E,Bugattic V,et al.Pectin functionalized with natural fatty acids as antimicrobial agent[J].International Journal of Biological Macromolecules,2014,68:28-32.
[8]Renard C M G C,Jarvis M C.Acetylation and methylation ofhomogalacturonans1:optimisationofthereactionand characterisation of the products[J].Carbohydrate Polymers,1999,39(3):201-207.
[9]Renard C M G C,Jarvis M C.Acetylation and methylation of homogalacturonans 2:effect on ion-binding properties and conformations[J].Carbohydrate Polymers,1999,39(3):209-216.
[10]Leroux J,Langendorff V,Schick G,et al.Emulsion stabilizing properties of pectin[J].Food Hydrocolloids,2003,17(4):455-462.
[11]Almeida E A M S,Facchi S P,Martins A F,et al.Synthesis and characterization of pectin derivative with antitumorproperty against Caco-2 colon cancer cells[J].Carbohydrate Polymers,2015,115(22):139-145.
[12]郑学芳,杨华,刘力恒,等.烷基化果胶的合成工艺[J].化学世界,2008,7:419-421.
[13]Pappas C S,Malovikova A,Hromadkova Z,et al.Determination of the degree of esterification of pectinates with decyl and benzyl ester groups by diffuse reflectance infrared Fourier transform spectroscopy(DRIFTS)and curve-fitting deconvolution method[J].Carbohydrate Polymers,2004,56(4):465-469.
[14]Morris G A,Hromádková Z,Ebringerová A,et al.Modification of pectin with UV-absorbing substitutents and its effect on the structural and hydrodynamic properties of the water-soluble derivatives[J].Carbohydrate Polymers,2002,48(4):351-359.
[15]余杰,武文洁.果胶疏水化改性及其应用的探讨[J].天津科技大学学报,2012,27(5):43-46.
[16]Sinitsya A,Cˇopıíková J,Prutyanov V,et al.Amidation of highly methoxylated citrus pectin with primary amines[J].Carbohydrate Polymers,2000,42(4):359-368.
[17]Synytsya A,Cˇopıíková J,Marounek M,et al.N-octadecylpectinamide,ahydrophobicsorbentbasedon modification of highly methoxylated citrus pectin[J].Carbohydrate Polymers,2004,56(2):169-179.
[18]Zouambia Y,Moulai-Mostefa N,Krea M.Structural characterizationandsurfaceactivityofhydrophobically functionalized extracted pectins[J].Carbohydrate Polymers,2009,78(4):841-846.
[19]Kurita O,Miyake Y,Yamazaki E.Chemical modification of citrus pectin to improve its dissolution into water[J].Carbohydrate Polymers,2012,87(2):1720-1727.
[20]Munarin F,Petrini P,Tanzi M C,et al.Biofunctional chemically modified pectin for cell delivery[J].Soft Matter,2012,8:4731-4739.
[21]Fajardo A R,Lopes L C,Pereira A G B,et al.Polyelectrolyte complexes based on pectin-NH2and chondroitin sulfate[J]. Carbohydrate Polymers,2012,87(3):1950-1955.
[22]Mishra R K,Mondal S,Dutt M,et al.Preparation and characterization of amidated pectin based hydrogels for drug delivery system[J].Journal of Materials Science:Materials in Medicine,2008,19(6):2275-2280.
[23]Cipriani T R,Gracher A H P,Souza L M,et al.Influence of molecular weight of chemically sulfated citrus pectin fractions on their antithrombotic and bleeding effects[J].Thrombosis and Haemostasis,2009,101(5):860-866.
[24]Maas N C,Gracher A H P,Sassaki G L,et al.Sulfation pattern of citrus pectin and its carboxy-reduced derivatives:Influenceonanticoagulantandantithromboticeffects[J]. Carbohydrate Polymers,2012,89(4):1081-1087.
[25]Bae Y I,Joe Y N,Rha H J,et al.Effect of sulfation on the physicochemical and biological properties of citrus pectins[J]. Food Hydrocolloids,2009,23(7):1980-1983.
[26]Katav T,Liu L S,Traitel T,et al.Modified pectin-based carrier for gene delivery:Cellular barriers in gene delivery course[J].Journal of Controlled Release,2008,130(2):183-191.
[27]Fan L H,Cao M,Gao S,et al.Preparation and characterization of a quaternary ammonium derivative of pectin[J].Carbohydrate Polymers,2012,88(2):707-712.
[28]Šimkovic I,Mendichi R,Uhliariková I.Modification of polygalacturonic acid hydroxyls with trimethylammoniumand/or sulfonate-2-hydroxypropyl group[J].Carbohydrate Polymers,2008,74(3):611-616.
[29]Yang K,Li Y J,Chen Y C.Removal of Oil and Cr(VI)from Wastewater Using Modified Pectin Flocculants[J].Journal of Environmental Engineering,2014,140(2):1-10.
[30]王春香,杨鲲,李玉静,等.改性果胶絮凝剂对废水中油脂和Cr(Ⅵ)的去除[J].西南师范大学学报:自然科学版,2014,39(1):20-27.
[31]Majzoob S,Atyabi F,Dorkoosh F,et al.Pectin-cysteine conjugate:synthesis and in-vitro evaluation of its potential for drug delivery[J].Journal of Pharmacy and Pharmacology,2006,58:1601-1610.
[32]SharmaR, AhujaM.Thiolatedpectin:Synthesis,characterization and evaluation as a mucoadhesive polymer[J]. Carbohydrate Polymers,2011,85(3):658-663.
[33]Sharma R,Ahuja M,Kaur H.Thiolated pectin nanoparticles:Preparation,characterization and ex vivo corneal permeationstudy[J].Carbohydrate Polymers,2012,87(2):1606-1610.
[34]Perera G,Barthelmes J,Bernkop-Schnürch A.Novel pectin-4-aminothiophenole conjugate microparticles for colon-specific drug delivery[J].Journal of Controlled Release,2010,145(3):240-246.
[35]Perera G,Hombach J,Bernkop Schnürch A.Hydrophobic Thiolation of Pectin with 4-Aminothiophenol:Synthesis and In Vitro Characterization[J].AAPS Pharm Sci Tech,2010,11(1):174-180.
[36]Hauptstein S,Müller C,Dünnhaupt S,et al.Preactivated thiomers:Evaluation of gastroretentive minitablets[J].International Journal of Pharmaceutics,2013,456(2):473-479.
[37]Sutter M,Siepmann J,Hennink W E,et al.Recombinant gelatin hydrogels for the sustained release of proteins[J].Journal of Controlled Release,2007,119(3):301-312.
[38]Maior J F A S,Reis A V,Muniz E C,et al.Reaction of pectin and glycidyl methacrylate and ulterior formation of free films by reticulation[J].International Journal of Pharmaceutics,2008,355(1-2):184-194.
[39]Guilherme M R,Moia T A,Reis A V,et al.Synthesis and waterabsorptiontransportmechanismofapH-sensitive polymer network structured on vinyl-functionalized pectin[J]. Biomacromolecules,2009,10(1):190-196.
[40]Silva E P,Sitta D L A,Fragal V H,et al.Covalent TiO2/ pectin microspheres with Fe3O4nanoparticles formagnetic fieldmodulated drug delivery[J].International Journal of Biological Macromolecules,2014,67:43-52.
[41]GuptaB,TummalapalliM,Deopura B L,et al.Functionalization of pectin by periodate oxidation[J].Carbohydrate Polymers,2013,98(1):1160-1165.
[42]Gupta B,Tummalapalli M,Deopura B L,et al.Preparation and characterization of in-situ crosslinked pectin-gelatin hydrogels[J].Carbohydrate Polymers,2014,106:312-318.
[43]Takei T,Sato M,Ijima H,et al.In situ gellable oxidized citrus pectin for localized delivery of anticancer drugs and preventionofhomotypiccancercellaggregation[J]. Biomacromolecules,2010,11(12):3525-3530.
[44]Munarin F,Petrini P,Tanzi M C,et al.Biofunctional chemically modified pectin for cell delivery[J].Soft Matter,2012,8:4731-4739.
[45]Mishra R K,Sutar P B,Singhal J P,et al.Graft copolymerization of pectin with polyacrylamide[J].Polymer-Plastics Technology and Engineering,2007,46:1079-1085.
[46]Chauhan K,Kumar R,Kumar M,et al.Modified pectinbased polymers as green antiscalants for calcium sulfate scale inhibition[J].Desalination,2012,305(1):31-37.
[47]Geethanjali R,Sabirneeza A A F,Subhashini S.Watersoluble and biodegradable pectin-grafted polyacrylamide and pectin-grafted polyacrylic acid:Electrochemical investigation of corrosion-inhibition behaviour on mild steel in 3.5%NaCl media[J/OL].Indian Journal of Materials Science,2013-11-21[2014-4-7].http://dx.doi.org/10.1155/2014/356075.
[48]Sutar P B,Mishra R K,Pal K,et al.Development of pH sensitive polyacrylamide grafted pectinhydrogel for controlled drug delivery system[J].Journal of Materials Science:Materials in Medicine,2008,19(6):2247-2253.
[49]Chauhan G S,Kumari A,Sharma R.Pectin and acrylamide based hydrogels for environment management technologies:synthesis,characterization,and metal ions sorption[J].Journal of applied Polymer Science,2007,106:2158-2168.
[50]Soares G A,Castro A D,Cury B S F,et al.Blends of crosslinked high amylose starch/pectin loaded with diclofenac[J]. Carbohydrate Polymers,2013,91(1):135-142.
[51]Prezotti F G,Meneguin A B,Evangelista R C,et al. Preparation and characterization of free films of high amylose/ pectin mixtures cross-linked with sodium trimetaphosphate[J]. Drug Development and Industrial Pharmacy,2012,38(11):1354-1359.
[52]Carbinatto F M,Castro A D,Cury B S F,et al.Physical properties of pectin-high amylose starch mixtures cross-linked withsodiumtrimetaphosphate[J].InternationalJournalof Pharmaceutics,2012,423(2):281-288.
[53]Patel N V,Patel J K,Shah S H,et al.Design,development and in vitro evaluation of Mesalamine tablets containing Pectin and Chitosan for colon-specific drug delivery[J].Journal of Applied Polymer Science,2010,1(2):94-102.
[51]Fernández-Hervás M J,Fell J T.Pectin:chitosan mixtures as coatings for colon-specific drug delivery:an in vitro evaluation[J].International Journal of Pharmaceutics,1998,169(1):115-119.
[55]Kaur A,Kaur G.Mucoadhesive buccal patches based on interpolymer complexes of chitosan-pectin for delivery of carvedilol[J].Saudi Pharmaceutical Journal,2012,20(1):21-27.
[56]宋燕,王开裕,温少红,等.载胰岛素壳聚糖-果胶微球的制备及性能研究[J].中南药学,2013,11(6):435-441.
[57]Galus S,Lenart A.Development and characterization of composite edible films based on sodium alginate and pectin[J]. Journal of Food Engineering,2013,115(4):459-465.
[58]Cataldo S,Cavallaro G,Gianguzza A,et al.Kinetic and equilibrium study for cadmium and copper removal from aqueous solutions by sorption onto mixed alginate/pectin gel beads[J]. Journal of Environmental Chemical Engineering,2013,1(4):1252-1260.
[59]Giosafatto C V L,Pierro P D,Gunning P,et al.Characterization of Citrus pectin edible films containing transglutaminasemodified phaseolin[J].Carbohydrate Polymers,2014,106:200-208.
[60]Zhang W,Mahuta K M,Mikulski B A,et al.Novel pectinbased carriers for colonic drug delivery.[J].Pharmaceutical Development&Technology,2014:1-4.
[61]Bayarri M,Oulahal N,Degraeve P,et al.Properties of lysozyme/low methoxyl(LM)pectin complexes for antimicrobial edible food packaging[J].Journal of Food Engineering,2014,131:18-25.
[62]Mishra R K,Datt M,Banthia A K.Synthesis and characterization of pectin/PVP hydrogel membranes for drugdelivery system[J].AAPS Pharm Sci Tech,2008,9(2):395-403.
[63]Liu L S,Won Y J,Cooke P H,et al.Pectin/poly(lactide-coglycolide)composite matrices for biomedical applications[J]. Biomaterials,2004,25(16):3201-3210.
[64]黄曹,瞿东滨,赵卫东,等.果胶/聚乙烯醇复合水凝胶的生物力学评价[J].中国脊柱脊髓杂志,2008,18(1):60-63.
[65]黄曹,金大地,张忠民,等.果胶/聚乙烯醇复合水凝胶的生物相容性评价[J].南方医科大学学报,2008,28(3):453-456.
[66]黄曹,卢玲,瞿东滨,等.新型人工髓核材料—果胶/聚乙烯醇复合水凝胶的制备及其溶胀性能[J].复合材料学报,2008,25(1):69-74.
[67]姚女兆,王文军,金大地.新型人工髓核材料果胶/聚乙烯醇复合水凝胶生物相容性研究[J].中南医学科学杂志,2011,39(4):399-402.
[68]ShiL,GunasekaranS.Preparationofpectin-ZnO nanocomposite[J].Nanoscale Res Lett,2008,3(12):491-495.
[69]Gupta V K,Pathania D,Asif M,et al.Liquid phase synthesis of pectin-cadmiumsulfide nanocomposite and its photocatalytic and antibacterial activity[J].Journal of Molecular Liquids,2014,96:107-112.
[70]Gong J L,Wang X Y,Zeng G M,et al.Copper(II)removal by pectin-iron oxide magnetic nanocomposite adsorbent[J]. Chemical Engineering Journal,2012,185-186:100-107.
[71]Sahu S,Dutta R K.Novel hybrid nanostructured materials of magnetite nanoparticles and pectin[J].Journal of Magnetism and Magnetic Materials,2011,323(7):980-987.
[72]Rakhshaee R,Giahi M,Pourahmad A.Removal of methyl orange from aqueous solution by Azolla filicoloides:Synthesis of Fe3O4nano-particles and its surface modification by the extracted pectin of Azolla[J].Chinese Chemical Letters,2011,22(4):501-504.
[73]Rakhshaee R,Panahandeh M.Stabilization of a magnetic nano-adsorbent by extracted pectin to remove methylene blue from aqueous solution:A comparative studying between two kinds of cross-likened pectin[J].Journal of Hazardous Materials,2011,189(1-2):158-166.
[74]Dai J J,Wu S X,Jiang W,et al.Facile synthesis of pectin coated Fe3O4nanospheres by the sonochemical method[J]. Journal of Magnetism and Magnetic Materials,2013,331:62-66.
[75]Tsai R Y,Chen P W,Kuo Y T,et al.Chitosan/pectin/gum Arabic polyelectrolyte complex:Process-dependent appearance,microstructureanalysisanditsapplication[J].Carbohydrate Polymers,2014,101:752-759.
[76]Tripathi S,Mehrotra G K,Dutta P K.Preparation and physicochemical evaluation of chitosan/poly(vinyl alcohol)/ pectinternaryfilmforfood-packagingapplications[J]. Carbohydrate Polymers,2010,79(3):711-716.
[77]Ghaffari A,Navaee K,Oskoui M,et al.Preparation and characterization of free mixed-film of pectin/chitosan/Eudragit RRS intended for sigmoidal drug delivery[J].European Journal of Pharmaceutics and Biopharmaceutics,2007,67(1):175-186.
[78]Dutta R K,Sahu S.Development of diclofenac sodium loaded magnetic nanocarriers of pectin interacted with chitosan for targeted and sustained drug[J].Colloids and Surfaces B:Biointerfaces,2012,97:19-26.
Research progress of modification and application of pectin
SUN Xu-bing,LIAO Li-min,FU Xiao-jin
(College of Chemistry and Chemical Engineering,Neijiang Normal University,Key Laboratory of Fruit Waste Treatment and Resource Recycling,Neijiang 641100,China)
Pectin was a natural polymer,which was composed of negatively charged D-galacturonic acid,with the features of non-toxic,easy degradation and biological compatibility.It could be widely used in food,pharmaceutical,chemical and cosmetic industries.In order to overcome the disadvantages of poor water resistance,mechanical properties and processing difficulties,and extend the application fields,various techniques including chemical,biological and physical methods have been employed to modify pectin that resluting in different derivatives which have adsorption,antibacterial,anticancer and drug loading properties.In the paper,progress on modification of pectin nearly twenty years was reviewed by introduction of the techniques and related derivatives briefly.The progress was mainly in the modificaiton through alkylation,amidation,sulfation,quaternization,thiolation,oxidation,vinylation,grafting and blending.It also prospects the development and application of pectin in the future.
pectin;modification;derivative;applicaiton
TS201.2
A
1002-0306(2015)20-0384-08
10.13386/j.issn1002-0306.2015.20.070
2015-01-16
孙绪兵(1982-),男,硕士研究生,研究方向:水溶性高分子材料及改性,E-mail:37591174@qq.com。

