六氟磷酸锂概述及制备工艺研究
刘永生
(天津长芦华信化工股份有限公司,天津河东300180)
1 六氟磷酸锂物性
六氟磷酸锂分子式为 LiPF6,相对分子量为:151.91;CAS:21324-40-3;EINECS:244-334-7。
六氟磷酸锂为白色结晶或粉末,相对密度为1.50。潮解性强,易溶于水,还溶于乙醚,低浓度的甲醇、乙醇、丙酮、碳酸酯类等有机溶剂。六氟磷酸锂的稳定较差,加热至60℃即可有少量分解为氟化锂和五氟化磷,加热至175~185℃时可大量分解。
2 六氟磷酸锂的主要用途[1]
六氟磷酸锂做为锂离子电池电解质,主要用于锂离子储能电池及其他日用电池,同时是近中期不可替代的锂离子电池电解质。
3 六氟磷酸锂国内外生产现状[2]
随着科技的发展,高容量、高容量比的锂离子电池有着广阔的应用空间。作为锂离子电池的电解质材料,六氟磷酸锂在应用和环境保护方面有着独特的优势,成为锂离子电池的主要原料。
美国著名氟科学家J H Simmons早在1950年就提出了六氟磷酸锂的合成方法。至今,已经有多种方法制备六氟磷酸锂并将其应用于锂电池的电解质。
由于六氟磷酸锂合成难度较高,整个生产过程涉及高低温、无水无氧操作、高纯精制、强腐蚀,对设备和操作人员要求高,工艺难度极大,我国在六氟磷酸锂产业化方面落后于日本等发达国家。
国内较早进行六氟磷酸锂开发的是天津化工研究设计院,从1996年开始在国内首次开展六氟磷酸锂电解质的研究,并于1999年完成了4 t/a的中试装置。2005年经天津金牛电源材料产业化,建设80 t/a的六氟磷酸锂建设项目,并于2010年实现了500 t/a的产能。2000年西安中富科技(西安核技术研究所提供技术)完成小试试验,但未见产业化报道。2010年底,巨化集团凯圣公司通过技术引进开始六氟磷酸锂的中试,借助其电子级无水氟化氢产品和技术优势,开始进军六氟磷酸锂产品。河南多氟多化工股份有限公司2009年开始20 t/a的中试,计划2011年完成200 t/a的生产能力。
综上所述,除了天津金牛拥有500 t/a的产能并全部自用外,国内其他电解液生产厂家所用的六氟磷酸锂基本采购国外的产品。2010年国内的六氟磷酸锂产能约为1745 t/a左右(包括日本森田化工在张家港公司的产能),根据各公司的项目进展预计2012年产能会达到3100 t/a。
我国六氟磷酸锂仍处于中试或产业化的初级阶段。对所有公开的专利进行的统计显示:多氟多、天津化工研究设计院和中南大学申请的专利居前三位,对专利的类型进行区别,可以看出3/4属于六氟磷酸锂的合成,而另外1/4侧重于装置和工艺,可见国内的研究重点仍以合成为主,而对生产工艺的改进,生产设备和产品的精制等研究相对薄弱。表1列出了国内主要六氟磷酸锂的专利。
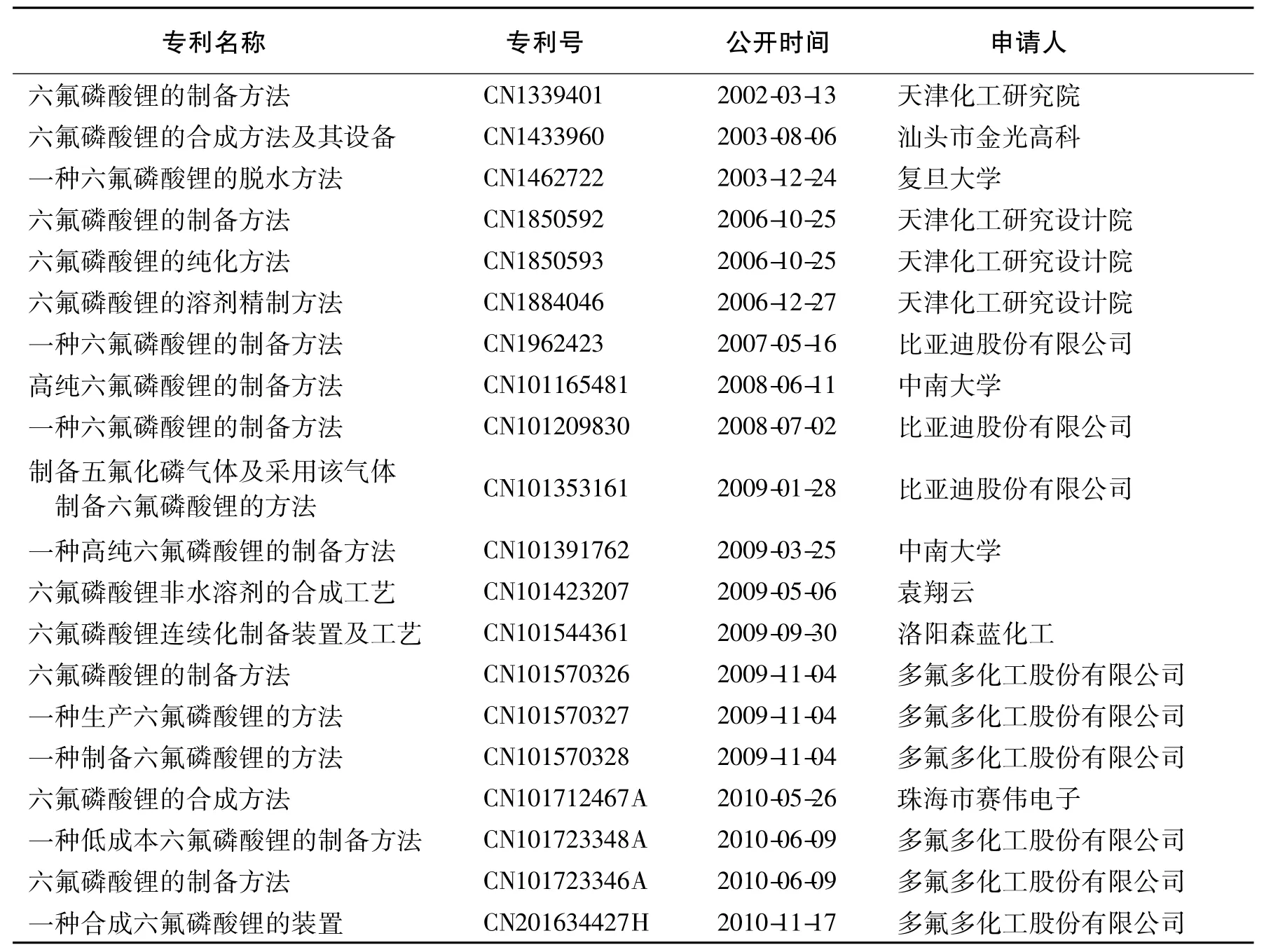
表1 国内六氟磷酸锂专利统计Table 1 Six fluorine lithium phosphate patent statistics of china
目前亚洲已成为六氟磷酸锂的主要生产区域,其中日本是最大的生产国,日本的中央硝子、关东电化和森田化工是世界三大生产商,中央硝子、森田化工已经落户中国或者与国内企业开始合作,并有扩产的计划。
由于技术原因,目前国内产品的品质落后于日本,高品质的六氟磷酸锂几乎完全被日本公司垄断,国内的电解液生产企业也多从国外进口,限制了国内锂电池发展的步伐。
4 六氟磷酸锂的市场前景[3]
随着科学技术的不断进步,尤其是电子信息产业的迅猛发展,手提电脑、移动电话机、电动汽车等用量的增长,对高能量化学电源的需求与日俱增。随之而产生的对污染小、比电容工作高及工作性能好的能源电池的要求也越来越高。
锂离子电池由于其优异的电性能及安全、无环境公害、能量大、工作电压高、长寿命等特点,深受各国重视,展示了广阔的应用前景,使锂离子电池的研究和开发成为世界性的。六氟磷酸锂是制造锂离子电池电解质的主要原料,由于其具有良好的离子导电率和电化学稳定性,是目前最常用的电解质锂盐。
目前六氟磷酸锂在我国未能实现完全国产化。这不仅导致国内使用的六氟磷酸锂仍然依赖进口,而且由于六氟磷酸锂的产业化是其他新型电解质锂盐研发的重要基础,因此这种情况也会阻碍新型电解质锂盐的研发工作。
此外,在我国能源结构调整的大背景下,随着电动自行车的普及和新能源汽车的推广,对六氟磷酸锂的需求量大规模增加,因此国内六氟磷酸锂生产技术研究及产业化问题已迫在眉睫。
5 商业化六氟磷酸锂的质量指标[4]
虽然目前并未见到有关六氟磷酸锂的质量标准,但是从一些厂家的六氟磷酸的质量标准及商业化锂离子电池对六氟磷酸锂的质量要求可以看出,作为一种有竞争力的产品,六氟磷酸锂至少应该具有以下质量指标:
1.纯度 >99.5%;2.水含量 <30 ×10-6;3.氟化氢含量 <150×10-6;4.不溶物含量 <0.5%;5.某些金属如 Fe、Al、Mn、Zn、Cr、Ni、Ti、Cu、K 等离子含量均 <20 ×10-6。
6 六氟磷酸锂主要制备方法[5-7]
根据近20年关于六氟磷酸锂制备方面的文献调研,总结出六氟磷酸锂的制备方法主要有4种:气-固反应法、氟化氢溶剂法、有机溶剂法和离子交换法。
6.1 气-固反应法
气-固反应法是将气态磷的卤化物与LiF直接反应,生成六氟磷酸锂。其反应方程式为:
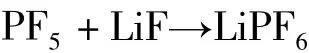
这种方法是将气态PF5通入放有LiF固体的容器中,两者即可反应生成LiPF6。该反应在高温高压下进行,且未使用任何溶剂,生成的LiPF6将LiF完全包覆,形成一层保护膜,阻止反应的进一步进行,所以该方法产率低,产物中有大量未反应的LiF,很难实现大规模生产。
为了提高LiPF6的产率,采用多孔活性LiF为原料,在不使用任何介质的情况下直接反应,可制得LiPF6的高纯品。
具体的制备方法为:将LiF和HF在50~200℃反应,生成LiPF2,再将生成的 LiPF2在60~700℃减压除去HF,生成多孔的LiF使之与PF5反应,生成LiPF6。温度是控制该反应过程的重要因素,影响着反应速率、HF的利用率、空隙率等。该方法的反应式如下:

该方法得到的产品纯度高,但原料成本高,工序过多,连续生产困难。
该方法一次性生成LiPF6的产率约为30%,若采用反复通脱HF,通PF5的方法可以提高LiPF6的产率。据估计,反复通脱HF,通PF515次,产率可达95%。
Ulrich等以PCl5、POCl3作为原料与LiF直接反应,反应后的混合物经有机溶剂萃取分离后获得产品。具体的做法为:将PCl5、POCl3与LiF先在150~300℃反应0.1~5 h,再在60~120℃反应0.1~5 h。
最后反应产物在0~80℃用有机溶剂从固体混合物中分离出来,获得的产品可用乙醚进行纯化,纯化后的纯度一般可>99.0%,但过程中使用了有机试剂,无疑增添了环境污染等问题。
气固反应法制备LiPF6的优点:过程比较简单,而且易于操作。
缺点:产率太低。用多孔LiF制备LiPF6并反复通脱HF,通PF5的方法虽然产率较高,但是反应时间过长,而且要使用有机溶剂对产品进行提纯,产品中难免混有微量的杂质离子。
6.2 HF 溶剂法
HF溶剂法是将LiF溶于HF溶液中,然后通入PF5气体进行反应。该方法是制备LiPF6的经典方法。
具体做法是:在不锈钢容器中,LiF溶于HF溶液,在25℃时向容器中加入PF5,将此反应维持12 h后挥发除去其中的气体物质,获得LiPF6产品,获得的产品中只含有痕量的LiF。
可以用PCl5替代PF5,从而降低生产成本,反应方程式如下:
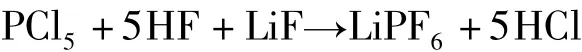
反应过程为:LiF溶于无水HF溶液中,控制一定温度,然后缓慢加入PCl5,反应结束后,加热到-20~100℃,通入惰性气体除去HF气体,析出LiPF6晶体,将晶体在减压下进一步除去HF可得到纯度达到99%以上的LiPF6。罗斗灿等也提出了采用PCl5制备LiPF6,该方法原料易得,产品纯度高,但低温操作困难,反应时间长,流程难以实现连续化,并存在较多的杂质离子。
日本专利对上述方法进行了优化,在-20℃或更低的温度下将PCl5与HF反应生成白色结晶物HPF6,并将该固体从溶液中分离出来,升温到-10~20℃,使其分解为 HF和 PF3,从而制得 PF5气体。将气体以一定的速率通入到LiF的HF溶液中,即可制得LiPF6。通过该方法去除了原料中的杂质离子,制得了更高纯度的LiPF6。
日本专利中还介绍了以更廉价的PCl3为原料制得LiPF6。用 PCl3与 HF反应得到 PF3,再以将PF3与Cl2反应得到PF3Cl2,然后将其与HF反应得到PF5,最后将PF5与LiF反应得到LiPF6,该反应用料经济实惠,反应容易控制。反应方程式如下:
PCl3+3HF→PF3+3HCl(第一次氟化过程)
PF3+Cl2→PF3Cl2(氯化过程)
PF3Cl2+2HF→PF5+2HCl(第二次氟化过程)
PF5+LiF→LiPF6
HF溶剂法制备LiPF6优点:反应速度快、转化率高。
缺点:过程中使用了具有强腐蚀性的HF、PF5。因此,对反应容器的耐腐蚀性要求较高,同时还要注意未转化的LiF混入产品及HF脱除等问题。
6.3 有机溶剂法
LiPF6由于热分解温度较低(30℃)、不稳定,很容易分解为PF5和LiF,难以储备;此外,HF溶剂法中使用的HF有很强的腐蚀性和危险性,不易接受。有机溶剂法采用没有腐蚀性的有机络合剂来替代HF,既避免了上述方法的不足,又稳定了LiPF6。常用的络合剂有乙腈、醚、吡啶等。
利用低毒、无腐蚀性的乙腈为络合剂,使PF5与LiF反应,由于乙腈不能溶解LiF或发生反应,同时也不与上述方法所得的LiPF6中的杂质发生反应或溶解这些杂质,因此较易将生成的Li(CH3CN)4PF6与杂质分离出来。通过-10~0℃减压挥发除去CH3CN可制得纯度高、比表面积大的LiPF6。反应方程式如下:
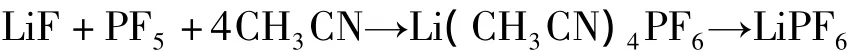
由于乙腈的活性低于LiF,故应该先将LiF与乙腈混合,然后通入PF5,使PF5优先与LiF反应。如果先将乙腈与PF5混合就形成络合物,不利于PF5的反应。
Willmann等以吡啶为有机溶剂制得LiPF6。美国专利中介绍了其他几种有机溶剂:一种为饱和低链烷基醚,另一种是低烷基蜡。
有机溶剂法优点:避免了使用具有强腐蚀性的HF作为溶剂,操作相对安全,同时降低了对设备的防腐要求。
缺点:使用的PF5必须自己制备,仍具有较强的腐蚀性和毒性,对操作人员仍有一定的危害。同时,该法还存在PF5与有机溶剂发生反应以及有机溶剂与LiPF6之间形成复合物,从而导致有机溶剂从最终产品中脱除较困难的问题。
6.4 离子交换法
离子交换法的反应方程式如下:
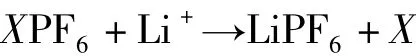
其中,X主要为Na+、K+、NH+4等离子。
离子交换法优点:避免使用PF5作为原料。
缺点:使用的醇基锂或氨等同样会和有机溶剂发生类似有机溶剂中存在的问题。而且这种方法使用的原料价格较贵,使得这种方法只是处于实验室阶段难于实现工业化生产。
7 制备方法选择及制备工艺
综上所述,选择Ulrich等以PCl5与LiF直接反应的方法制备LiPF6[7]。这种方法的优点是原料相对于以上所述的制备方法中涉及到的氟气、三氟氧磷、氟化氢等毒性较低、成本较低,且反应放热不强烈,易于控制、危险性小,适用于工业生产。
该反应的反应原理被认为是两步反应:
(1)5LiF+PCl5→PF5+5LiCl
(2)PF5+LiF→LiPF6
7.1 反应原料及产物的物化性质
反应原料及产物的物化性质见表2。

表2 主要物料性质Table 2 The main material properties
7.2 小实验需要的设备及原料
小实验需要的设备及原料见表3。
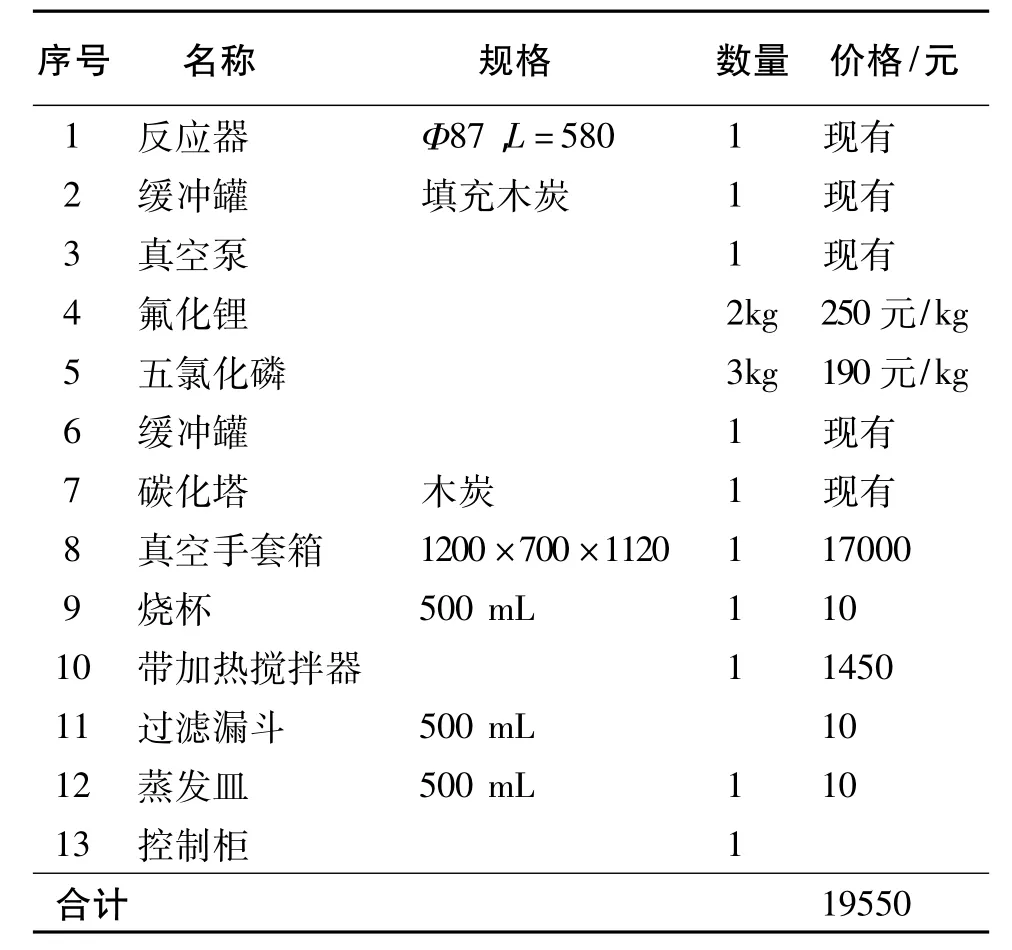
表3 反应设备及原料Table 3 The reaction equipment and raw materials
7.3 工艺流程框图
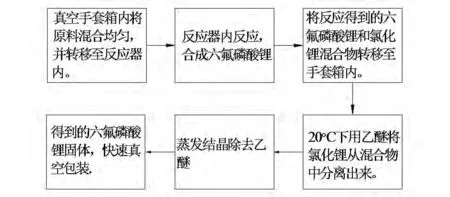
图1 六氟磷酸锂合成及纯化工艺流程框图Fig.1 Six fluorine lithium phosphate synthesis and purification process flow diagram
反应器内合成六氟磷酸锂工艺流程见图2。
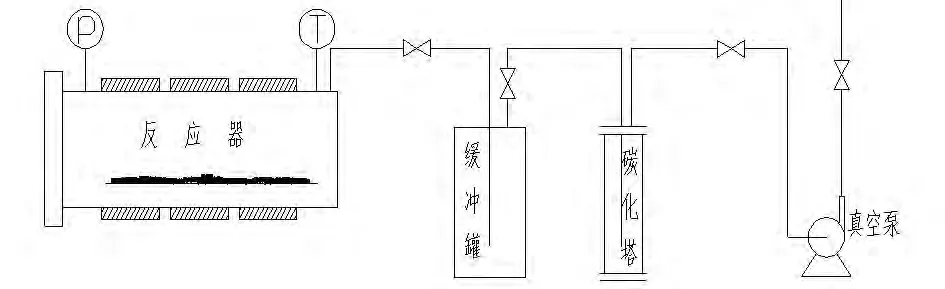
图2 反应器内合成六氟磷酸锂图Fig.1 The reactor for synthesis of six fluorine lithium phosphate
7.4 实验步骤
1.将真空手套箱充满干燥的氮气,将200 g的五氯化磷和300 g的氯化锂混合均匀(摩尔比1∶7.2),作为反应原料。
2.迅速将混合后的反应原料移至反应器内。封闭反应器,抽空至-0.1 MPa,保持30 min,压力不上涨,说明反应器不漏,进行下面操作,否则需要消除漏点。
3.加热反应器并打开抽空阀抽空,至100℃维持0.5 h。关闭抽空阀,关闭真空泵。这个过程用于除去反应原料中的水分。
4.加热反应器,控制反应温度在190~260℃,反应时间为1 h。
5.控制反应温度在80~140℃,时间为2~4 h。
6.冷却反应器,反应器温度降到60℃时,抽空反应器至-0.1 MPa,除去反应器中的PF5。
7.打开反应器,将反应产物迅速转移到真空手套箱内。
8.用烧杯将反应产物溶解到乙醚溶剂中,控制温度在20℃左右,用搅拌器进行搅拌。
9.由于LiPF6溶于乙醚,而LiCl微溶于乙醚,可以采用过滤的方法将LiCl除去。
10.将澄清溶液放到蒸发皿中,对LiPF6与乙醚的溶液进行加热至30℃,并抽空除去乙醚溶剂。
11.真空密封包装得到LiPF6产品。
8 应急与防护
8.1 防护措施
呼吸系统防护:可能接触其蒸气时,应该佩带防毒口罩,必要时佩带防毒面具。眼睛防护:戴化学安全防护眼镜。防护服:穿工作服(防腐材料制作)。手防护:戴橡皮手套。其它:工作现场严禁吸烟。
8.2 急救措施
皮肤接触:立即脱去污染的衣着,用大量流动清水彻底冲洗。眼睛接触:立即提起眼睑,用流动清水冲洗10 min或用2%碳酸氢钠溶液冲洗。吸入:迅速脱离现场至空气新鲜处。注意保暖,保持呼吸道通畅。必要时进行人工呼吸。就医。
灭火方法:干粉、砂土、二氧化碳。禁止用水。
[1]吴克安,任建纲.六氟磷酸锂的发展现状与市场前景[J].浙江化工,2011,42(6):1-2.
[2]宁斌,邹金鑫.六氟磷酸锂制备方法的研究进展[J].贵州化工,2011,36(5):1-2.
[3]庄全超,武山,刘文元,等.六氟磷酸锂生产工艺研究[J].电池工业,2005,10(3):2-3.
[4]张景利.国内外六氟磷酸锂制备进展[J].化学推进剂与高分子材料,2001(4):2-4.
[5]代玉林,白有仙,邹金鑫.六氟磷酸锂制备工艺研究进展[J].天津化工,2010,24(4):2-3.
[6]宋兵魁,王福生,王凤花,等.制备锂离子电解质六氟磷酸锂的工艺探讨[J].天津化工,2004,18(2):2-4.
[7]黄晓霞,张志业,王辛龙.一种六氟磷酸锂的简易合成工艺[J].四川化工,2009,12(2):2-3.

