3-取代吲哚-2-酮类化合物的设计、合成及抗肿瘤活性研究
·论著·
3-取代吲哚-2-酮类化合物的设计、合成及抗肿瘤活性研究
周浩,周峰,周有骏(第二军医大学药学院药物化学教研室,上海 200433)
[摘要]目的设计合成对微管蛋白和血管内皮细胞生长因子受体2(VEGFR-2)激酶具有双重抑制作用的3-取代吲哚-2-酮类化合物,考察其体外抑瘤活性。方法以取代的苯胺为起始原料,经缩合、环合、还原、取代等反应制得系列目标化合物,并考察该系列化合物对微管蛋白和肿瘤细胞的抑制活性。结果共合成了11个新的目标化合物。实验结果显示,化合物j9对微管蛋白和VEGFR-2激酶具有双重抑制活性。所有目标化合物对3种肿瘤细胞株均有中等强度的抑制活性。结论该类化合物是一类具有多靶点作用的抗肿瘤化合物。
[关键词]血管靶向药物;3-取代吲哚-2-酮类化合物;微管蛋白抑制活性;激酶抑制活性
[基金项目]国家自然科学基金(21172260)
[作者简介]周浩,硕士研究生.Tel:15001753465;E-mail:zhouhaoin2008@126.com
[通讯作者]周有骏,教授,博士生导师.研究方向:抗肿瘤药物的设计与合成.Tel:(021)81871231; E-mail:zhouyoujun2005@aliyun.com
[中图分类号]R916.1[文献标志码]A
DOI[]10.3969/j.issn.1006-0111.2015.02.010
[收稿日期]2014-11-03[修回日期]2015-01-20
Design, synthesis and anti-tumor activitiesinvitroof novel 3-substituted indolin-2-one compounds
ZHOU Hao,ZHOU Feng,ZHOU Youjun(Department of Medical Chemistry, School of Pharmacy, Second Military Medical University, Shanghai 200433, China)
Abstract[]ObjectiveTo compose and evaluate anti-tumor activities of 3-substituted indole-2-one compounds which may have dual inhibitory activities against both tubulin protein and VEGFR-2 tyrosine kinase. MethodsTarget compounds were prepared starting from substituted aniline via condensation, cyclization and reduction. Results11 target compounds were synthesized and all the compounds displayed moderate anti-proliferative activities against three tumor cell lines. Compound j9 showed a certain inhibitory activity against both VEGFR-2 kinase and tubulin protein in vitro. ConclusionThis series of indolin-2-one derivatives were found to be a novel kind of multi-target inhibitor.
[Key words]vascular targeting drug; 3-substituted indolin-2-one compounds; tubulin inhibitory activities; kinase inhibitory activities
肿瘤是一种全球性的常见病、多发病,严重威胁人类的生命健康和生活质量。近年来,由于人们不良的生活习惯及生存环境的恶化,使得肿瘤的发病率呈逐年上升趋势。因此,合理的肿瘤治疗手段显得格外重要。
自从1971年Folkman[1]首次提出肿瘤新生血管对肿瘤的生长及扩散起重要作用以来,肿瘤血管靶向治疗受到了高度重视。肿瘤血管靶向治疗与传统的抗肿瘤药物相比,具有选择性高、毒性小,抗瘤谱广等优点,这些优势使得肿瘤血管靶向药物发展十分迅速,并成为一种有效的肿瘤治疗手段[2,3]。
3-取代吲哚-2-酮类化合物是一类通过抑制酪氨酸激酶受体(RTKs)而发挥作用的肿瘤血管靶向药物,如SU5416是由Sugen公司研发的一种靶向血管内皮细胞生长因子受体2(VEGFR-2)酪氨酸激酶抑制剂[4]。SU5416衍生物Sunitinib maleate(商品名:Sutent,由Pfizer开发) 在2006年1月获得FDA批准上市,用于治疗胃肠基质细胞癌和进展期肾细胞癌[5]。
反式-3,5,4′-三甲氧基白藜芦醇(TMS),是由意大利布雷西亚大学生物医学与技术学院等单位研制开发的反式白藜芦醇三甲基化衍生物(图1)。研究表明,TMS可以影响鼠科主动脉血管内皮细胞(MAE)中微管蛋白的聚合作用,干扰其微管聚合中心的形成。1.0 μmol/L浓度的TMS能明显降低MAE细胞中微管蛋白的聚合,从而发挥血管阻断作用[6]。
分析SU5416和TMS的结构,以SU5416和TMS为先导化合物,以各种取代芳环置换SU5416中的吡咯环,设计并合成具有两者相似骨架并对酪氨酸激酶受体和微管蛋白具有双重抑制活性的新型肿瘤血管化合物。
目标化合物以取代苯胺为起始原料,经缩合、环合、还原、取代等四步反应制得。目标化合物结构和合成路线见图2。

图1 SU5416、Sutent和TMS的结构式

图2 目标化合物结构及合成路线 反应条件:(a) 水合三氯乙醛, 十水合硫酸钠,盐酸羟胺,浓盐酸,回流,2 h;(b)浓硫酸,80~90 ℃,20 min; (c)三氟乙酸,三乙基硅烷,室温,4 h;(d)取代苯甲醛,哌啶,乙酸,乙酸乙酯,室温,8~48 h
1实验部分
1.1仪器及材料85-1型磁力搅拌器(上海志威电器有限公司);ZD267型机械搅拌器(北京京伟欣业电器有限公司);KE-20-5型旋转蒸发仪(上海予华仪器设备有限公司);SHB-Ⅲ型循环水式多用真空泵(巩义市英峪华科仪器厂);RY-2熔点仪(天津市分析仪器厂,温度计经校正);Bruker AC-300P型核磁共振氢谱(溶剂为DMSO,300 MHz);Varian-1200L型质谱仪;合成过程中所用原料及试剂均为市售分析纯。
1.2目标化合物的合成
1.2.12-(肟基)-N-苯乙酰胺类化合物(g)的合成向反应瓶中加入水合三氯乙醛(44.5 g,0.27 mol)和水(1 L),搅拌溶解后,分别加入十水合硫酸钠(650 g,2.02 mol)、取代苯胺(0.25 mol)、盐酸羟胺(54.2 g,0.78 mol)和浓盐酸(21 ml)。剧烈搅拌下,加热回流25 min,然后于室温下冷却搅拌2 h,过滤,烘干,得褐色固体(g),收率86.2%~94.6%。
1.2.2二氢吲哚-2,3-二酮类化合物(h)的合成向反应瓶中加入浓硫酸(120 ml),于50℃下保温,分批加入化合物(g)0.20 mol,控制内温80~90℃。加完溶液后保温20 min,倒入冰水(250 ml)中,搅拌1 h,用乙酸乙酯(150 ml×3)提取,合并有机相,无水硫酸钠干燥,浓缩后得褐色粗品。用乙酸(80 ml)重结晶,得棕黄色固体(h),收率71.4%~83.1%。
1.2.3吲哚-2-酮类化合物(i)的合成氮气保护下,向反应瓶中分别加入(h)10 mmol、三氟乙酸10 ml和三乙基硅烷(3.48 g,30 mmol),于25 ℃搅拌4 h。将反应液减压浓缩后,加入乙醚(5 ml),搅拌0.5 h,过滤,洗涤,烘干,得类白色固体(i),收率89.6%~97.3%。
1.2.43-苯亚甲基吲哚-2-酮类化合物(j)的合成向100 ml反应瓶中加入化合物(i)2 mmol、取代苯甲醛(2.4 mmol)、哌啶(0.1 mmol)、乙酸(0.1 mmol)、分子筛(10 g)和乙酸乙酯(50 ml)。室温下搅拌反应8~48 h,硅藻土过滤,得橙黄色至浅棕色清液。减压浓缩后,得粗品,硅胶柱层析,以PE-EA体系洗脱,得系列化合物j1~j11,收率27.3%~84.6%。
1.2.5目标化合物(j9)的单晶培养 将j9溶解于二氯甲烷和乙酸乙酯的混合溶剂中,然后静置慢慢挥发溶剂3~5 d,等至母液中析出橘红色长方形晶体,过滤后干燥。
1.3结果与讨论共合成了11个目标化合物。所有目标化合物均未见文献报道。目标化合物的化学结构、熔点及光谱数据见表1。实验采用单晶X-衍射测定化合物j9的构型。结果显示其为Z构型(图3、图4),与先导化合物的构型相一致。
表1目标化合物的化学结构、熔点及光谱数据

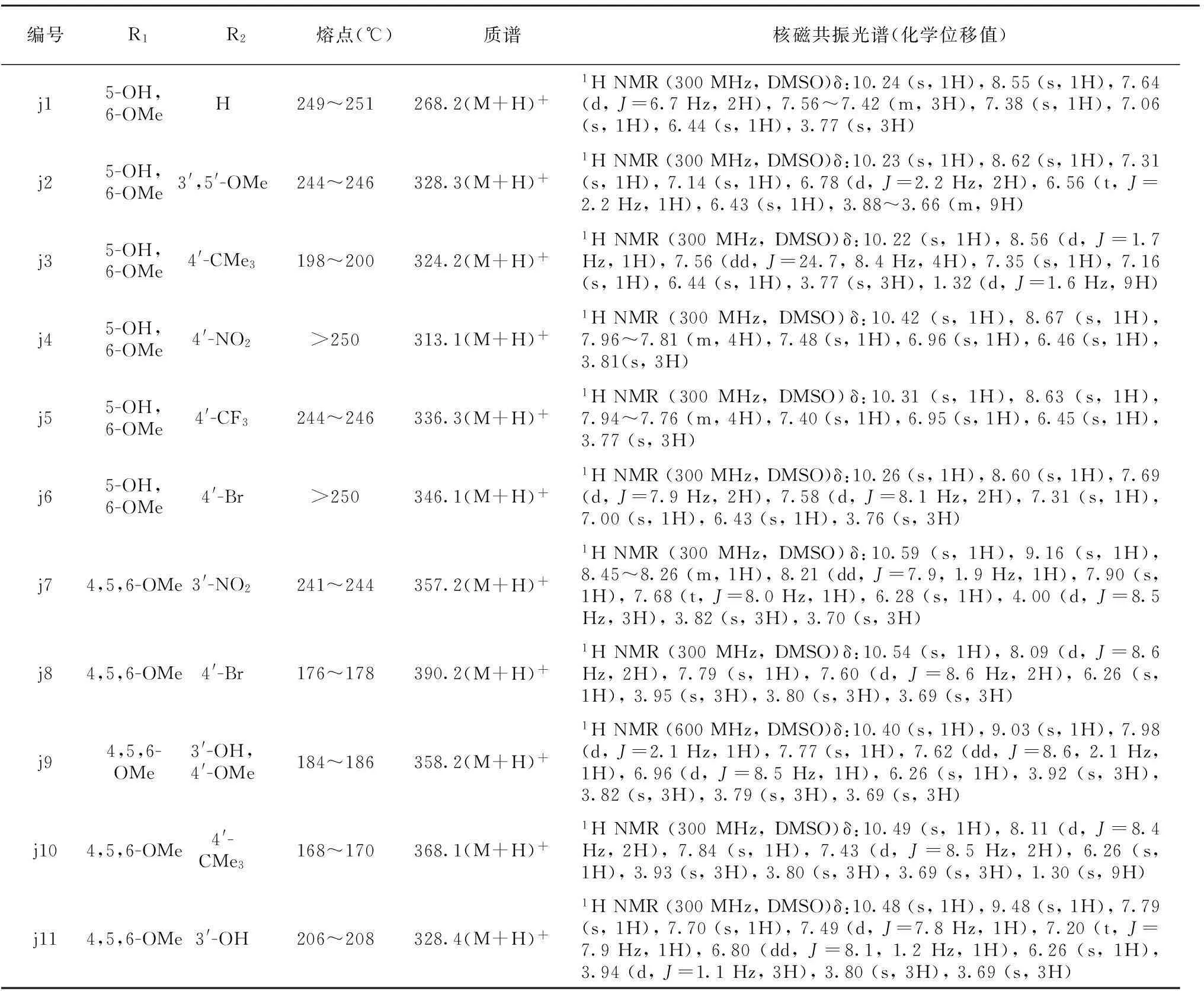
编号R1R2熔点(℃)质谱核磁共振光谱(化学位移值)j15-OH,6-OMeH249~251268.2(M+H)+1HNMR(300MHz,DMSO)δ:10.24(s,1H),8.55(s,1H),7.64(d,J=6.7Hz,2H),7.56~7.42(m,3H),7.38(s,1H),7.06(s,1H),6.44(s,1H),3.77(s,3H)j25-OH,6-OMe3',5'-OMe244~246328.3(M+H)+1HNMR(300MHz,DMSO)δ:10.23(s,1H),8.62(s,1H),7.31(s,1H),7.14(s,1H),6.78(d,J=2.2Hz,2H),6.56(t,J=2.2Hz,1H),6.43(s,1H),3.88~3.66(m,9H)j35-OH,6-OMe4'-CMe3198~200324.2(M+H)+1HNMR(300MHz,DMSO)δ:10.22(s,1H),8.56(d,J=1.7Hz,1H),7.56(dd,J=24.7,8.4Hz,4H),7.35(s,1H),7.16(s,1H),6.44(s,1H),3.77(s,3H),1.32(d,J=1.6Hz,9H)j45-OH,6-OMe4'-NO2>250313.1(M+H)+1HNMR(300MHz,DMSO)δ:10.42(s,1H),8.67(s,1H),7.96~7.81(m,4H),7.48(s,1H),6.96(s,1H),6.46(s,1H),3.81(s,3H)j55-OH,6-OMe4'-CF3244~246336.3(M+H)+1HNMR(300MHz,DMSO)δ:10.31(s,1H),8.63(s,1H),7.94~7.76(m,4H),7.40(s,1H),6.95(s,1H),6.45(s,1H),3.77(s,3H)j65-OH,6-OMe4'-Br>250346.1(M+H)+1HNMR(300MHz,DMSO)δ:10.26(s,1H),8.60(s,1H),7.69(d,J=7.9Hz,2H),7.58(d,J=8.1Hz,2H),7.31(s,1H),7.00(s,1H),6.43(s,1H),3.76(s,3H)j74,5,6-OMe3'-NO2241~244357.2(M+H)+1HNMR(300MHz,DMSO)δ:10.59(s,1H),9.16(s,1H),8.45~8.26(m,1H),8.21(dd,J=7.9,1.9Hz,1H),7.90(s,1H),7.68(t,J=8.0Hz,1H),6.28(s,1H),4.00(d,J=8.5Hz,3H),3.82(s,3H),3.70(s,3H)j84,5,6-OMe4'-Br176~178390.2(M+H)+1HNMR(300MHz,DMSO)δ:10.54(s,1H),8.09(d,J=8.6Hz,2H),7.79(s,1H),7.60(d,J=8.6Hz,2H),6.26(s,1H),3.95(s,3H),3.80(s,3H),3.69(s,3H)j94,5,6-OMe3'-OH,4'-OMe184~186358.2(M+H)+1HNMR(600MHz,DMSO)δ:10.40(s,1H),9.03(s,1H),7.98(d,J=2.1Hz,1H),7.77(s,1H),7.62(dd,J=8.6,2.1Hz,1H),6.96(d,J=8.5Hz,1H),6.26(s,1H),3.92(s,3H),3.82(s,3H),3.79(s,3H),3.69(s,3H)j104,5,6-OMe4'-CMe3168~170368.1(M+H)+1HNMR(300MHz,DMSO)δ:10.49(s,1H),8.11(d,J=8.4Hz,2H),7.84(s,1H),7.43(d,J=8.5Hz,2H),6.26(s,1H),3.93(s,3H),3.80(s,3H),3.69(s,3H),1.30(s,9H)j114,5,6-OMe3'-OH206~208328.4(M+H)+1HNMR(300MHz,DMSO)δ:10.48(s,1H),9.48(s,1H),7.79(s,1H),7.70(s,1H),7.49(d,J=7.8Hz,1H),7.20(t,J=7.9Hz,1H),6.80(dd,J=8.1,1.2Hz,1H),6.26(s,1H),3.94(d,J=1.1Hz,3H),3.80(s,3H),3.69(s,3H)

图3 j9的单晶衍射分子图

图4 j9的晶胞图
2生物活性研究
2.1体外抑瘤活性实验参考四氮唑盐还原法(MTT法)[7,8]测定样品对MDA-MB-435、HCT116、CEM细胞株的作用强度。测试结果见表2。
2.2体外微管蛋白抑制活性实验采用文献[9]方法和微管蛋白试剂盒方法(cyto-dynamix screen 03), 以CA4为对照药品,测定化合物j9对微管蛋白的抑制活性,两者浓度均为10 μmol/L,
j9的抑制
率为47.1%,CA4抑制率为92.4%。
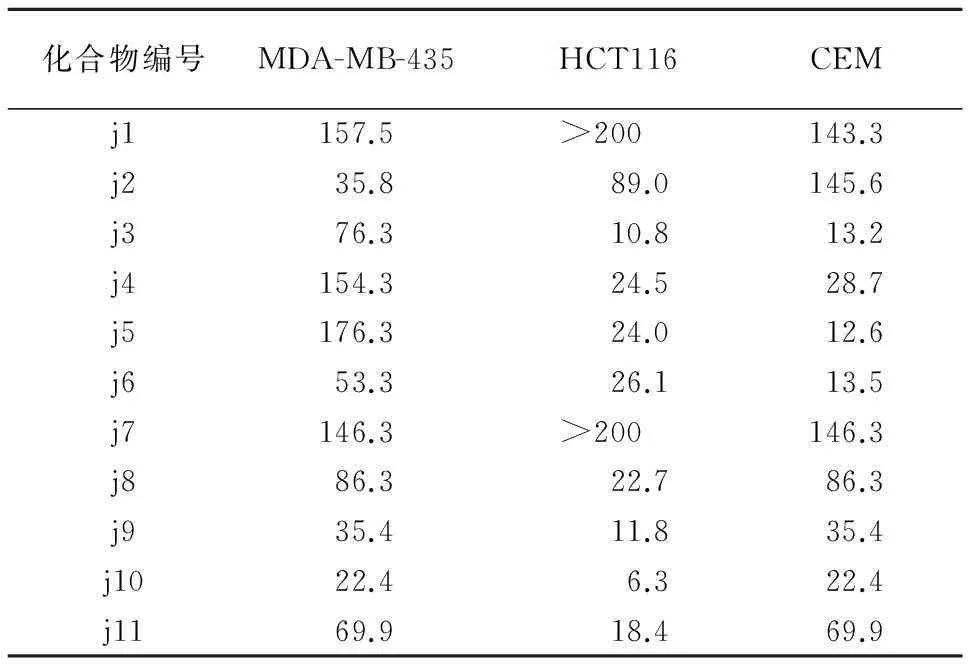
表2 目标化合物的肿瘤抑制活性(IC 50,μmol/L)
2.3体外VEGFR-2激酶抑制活性实验采用酶联免疫吸附法 (enzyme-linked immunesorbent assay, ELISA),以Su11248为对照药品,在490 nm波长下使用酶标仪(molecular devices spectramax 190)测得样品的吸光度A490值。j9与Su11248的浓度均为10 μmol/L,抑制率分别为42.9%和84.9%。
2.4结果与讨论体外抑瘤活性结果显示,所有目标化合物对3种肿瘤细胞均具有中等强度的抑制活性。其中化合物j10对HCT116的抑制活性最强,IC50达6.3 μmol/L。化合物j9的生物活性研究显示,该化合物对微管蛋白和VEGFR-2均具有中等强度的抑制活性。
实验结果表明,本研究设计合成的新型3-取代吲哚-2-酮类化合物是一类对微管蛋白和VEGFR-2激酶具有双重抑制活性的抗肿瘤化合物。本研究为深入开展多靶点作用抗肿瘤化合物的设计打下了一定的研究基础,也为微管蛋白和VEGFR-2激酶双重抑制剂提供了新的结构类型。
【参考文献】
[1]Folkman J. Tumor angiogenesis:therapeutic implications[J]. N Engl J Med,1971,285(21):1182-1186.
[2]Bergers G,Benjamin LE.Tumorigenesis and the angiogenic switch[J]. Nat Rev Cancer,2003,3(6):401-410.
[3]Brem S,Brem H,Folkman J,etal. Prolonged tumor dormancy by prevention of neovascularization in the vitreous[J]. Cancer Res,1976,36(8):2807-2812.
[4]Fong TA,Shawver LK,Sun L,etal. Su5416 is a potent and selective inhibitor of the vascular tyrosine kinase catalysis,tumor vascularization,and growth endothelial growth factor receptor (Flk-1/KDR) that inhibits of multiple tumor types[J]. Cancer Res,1999,59(1):99-106.
[5]吕金玲. 苹果酸舒尼替尼(sunitinib malate)[J]. 中国药物化学杂志,2007,17(3):194-194.
[6]Belleri M,Ribatti D,Nicoli S,etal. Antiangiogenic and vascular-targeting activity of the microtubule-destabilizing trans-resveratrol derivative 3,5,4'-trimethoxystilbene[J]. Mol Pharmacol,2005,67(5):1451-1459.
[7]Gieni RS,Li Y,Hayglass KT. Comparison of [3H] thymidine incorporation with MTT- and MTS-based bioassays for humanand murine IL-2 and IL-4 analysis.tetrazolium assays provide markedly enhanced sensitivity[J]. J Immunol Methods,1995,187(1):85-93.
[8]张帆,王晓欢,马俊杰.4,6-双苯基-2-氨基-3-氰基吡啶类化合物的合成及其抗肿瘤活性研究[J]. 中国药物化学杂志,2011,21(5):352-357.
[9]Hamel E. Evaluation of antimitotic agents by quantitative comparisons of their effects on the polymerization of purified tubulin[J]. Cell Biochem Biophys,2003,38(1):1-22. J. Tumor angiogenesis:therapeutic implications[J]. N Engl J Med,1971,285(21):1182-1186.
[2]Bergers G,Benjamin LE.Tumorigenesis and the angiogenic switch[J]. Nat Rev Cancer,2003,3(6):401-410.
[3]Brem S,Brem H,Folkman J,etal. Prolonged tumor dormancy by prevention of neovascularization in the vitreous[J]. Cancer Res,1976,36(8):2807-2812.
[4]Fong TA,Shawver LK,Sun L,etal. Su5416 is a potent and selective inhibitor of the vascular tyrosine kinase catalysis,tumor vascularization,and growth endothelial growth factor receptor (Flk-1/KDR) that inhibits of multiple tumor types[J]. Cancer Res,1999,59(1):99-106.
[5]吕金玲. 苹果酸舒尼替尼(sunitinib malate)[J]. 中国药物化学杂志,2007,17(3):194-194.
[6]Belleri M,Ribatti D,Nicoli S,etal. Antiangiogenic and vascular-targeting activity of the microtubule-destabilizing trans-resveratrol derivative 3,5,4'-trimethoxystilbene[J]. Mol Pharmacol,2005,67(5):1451-1459.
[7]Gieni RS,Li Y,Hayglass KT. Comparison of [3H] thymidine incorporation with MTT- and MTS-based bioassays for humanand murine IL-2 and IL-4 analysis.tetrazolium assays provide markedly enhanced sensitivity[J]. J Immunol Methods,1995,187(1):85-93.
[8]张帆,王晓欢,马俊杰.4,6-双苯基-2-氨基-3-氰基吡啶类化合物的合成及其抗肿瘤活性研究[J]. 中国药物化学杂志,2011,21(5):352-357.
[9]Hamel E. Evaluation of antimitotic agents by quantitative comparisons of their effects on the polymerization of purified tubulin[J]. Cell Biochem Biophys,2003,38(1):1-22.
[本文编辑]顾文华

