尿嘧啶和5-溴尿嘧啶的低温热容
张晓晔 薛 斌 程 泽 谭志诚 史 全,*
(1沈阳工业大学石油化工学院,辽宁辽阳111003;2中国科学院大连化学物理研究所热化学实验室,辽宁省能源材料热化学重点实验室,洁净能源国家实验室,辽宁大连116023)
尿嘧啶和5-溴尿嘧啶的低温热容
张晓晔1,2薛 斌1,*程 泽1,2谭志诚2史 全2,*
(1沈阳工业大学石油化工学院,辽宁辽阳111003;2中国科学院大连化学物理研究所热化学实验室,辽宁省能源材料热化学重点实验室,洁净能源国家实验室,辽宁大连116023)
采用综合物性测量系统(PPMS)的热容测量模块在1.9-300 K温度区间内对两种药物中间体(尿嘧啶和5-溴尿嘧啶)的低温热容进行了测量与研究.结果表明,在测量温区内两种化合物的低温热容随温度的上升而逐步增加,无任何热异常现象产生;在相同温度下,5-溴尿嘧啶的热容数值始终高于尿嘧啶.利用低温热容理论模型对热容数据进行了拟合,并计算得到了0-300 K温区的摩尔熵变、焓变等热力学函数.此外,通过热容拟合数据计算得到的尿嘧啶和5-溴尿嘧啶在298.15 K的标准摩尔规定熵分别为(132.48±1.32)和(165.39±1.65)J· K-1·mol-1.
尿嘧啶;5-溴尿嘧啶;热容;综合物性测量系统;热力学函数
1 引言
嘧啶类化合物是与生命活动息息相关的一类结构特殊的含氮杂环化合物,广泛存在于人体及生物体内,具有抗菌及促进植物生长的特性,1被广泛应用于医药及农药中间体等领域.如5-氟尿嘧啶化合物是抗肿瘤药物,在临床应用上有很好的疗效;2, 4-二氨基-6-羟基嘧啶可生产抗贫血药叶酸;2嘧啶(硫)醚类化合物是一类效果很好的除草剂.1此外,嘧啶类化合物在调节光电性质方面也具有非常重要的作用,可被用作有机发光二极管(OLED)功能材料、液晶材料、荧光探针等.3
近年来,作为组成RNA中4种碱基之一的尿嘧啶进入了人们的研究视野,4,5它是组成核糖核酸的重要部分,被广泛用于医药及生化研究.尿嘧啶作为医药中间体可合成尿嘧啶替加氟片,对治疗肠癌、胃癌、乳腺癌等多种癌症具有较好的临床效果. 5-溴尿嘧啶作为卤代尿嘧啶的一种,是尿嘧啶上的氢被溴取代的人工碱基相似体,在生物体内可以取代DNA中的胸腺嘧啶,并且兼具抗肿瘤和抗病毒的特性,6-8是合成抗炎药物的主要成分.并且5-溴尿嘧啶对中国对虾、明虾的胚胎初期以及幼体生长发育可起到促进作用.9
©Editorial office ofActa Physico-Chimica Sinica
尿嘧啶及其衍生物因具有上述的独特性质被作为合成抗肿瘤及抗病菌药物的中间体广泛地应用于医药研究领域;而研究该类化合物的热力学性质不仅可以促进相关合成工艺的研究,还可以为药物的反应机理以及分子结构与性质的关联研究提供重要的实验数据和理论依据.10因此,国内外学者对尿嘧啶及其衍生物的热力学性质进行了一系列研究.例如,Zielenkiewicz等11采用流动量热法在水溶液中298.15 K温度下测量尿嘧啶烷基化衍生物的偏摩尔热容,测量结果显示热容与取代的亚甲基—CH2—数目呈线性关系,亚甲基数目越多,则热容越大.Zielenkiewicz等12在前人研究的基础上,利用差示扫描量热法(DSC)在298.15-343.15 K温度范围内研究了甲基取代尿嘧啶衍生物、烷基化尿嘧啶衍生物和卤代尿嘧啶衍生物的热容,同样发现热容与亚甲基数目有关,并且探讨了C—CH3、N—CH3和C—NO2基团以及F、Cl、Br、I卤素原子在298.15 K时满足Chickos的加和理论.此外,对于甲基取代的尿嘧啶衍生物,Zielenkiewicz12和Chickos13等发现Chickos的加和理论不能区分甲基的取代位置,但是可以区分卤素取代和烷基链或环的取代位置.然而,有关尿嘧啶及其衍生物的低温热力学性质,尤其是低温比热性质的研究文献中却鲜有报道;这类热力学性质直接关系到该类化合物的合成、药物作用机理以及分子结构与性质关联等领域的研究.
本文利用综合物性测量系统(PPMS)第一次在1.9-300 K温区测量了尿嘧啶和5-溴尿嘧啶的低温热容,并通过理论模型对实验数据进行了拟合,计算得到了0-300 K温区内的热力学函数.此外,还对两种化合物的热容数据进行了对比,利用晶格振动模式讨论了在整个实验温区内热容的差异.
2 实验部分
2.1 实验样品
本量热实验的样品尿嘧啶和5-溴尿嘧啶纯度均大于99%,分别购自苏州亚科化学试剂股份有限公司和上海迈瑞尔化学技术有限公司.尿嘧啶和5-溴尿嘧啶的CAS号分别为66-22-8和51-20-7,其结构式如图1所示.热容测试的样品制备过程中所用的铜箔购自Alfa Aesar化学有限公司,铜箔厚度为0.025 mm,纯度为0.99999.此外,还采用X射线粉末衍射仪(XRD,PANalytical,40 kV,40 mA;荷兰)对样品进行了测试,由实验结果(图2所示)可知样品的XRD衍射峰与标准峰一致.
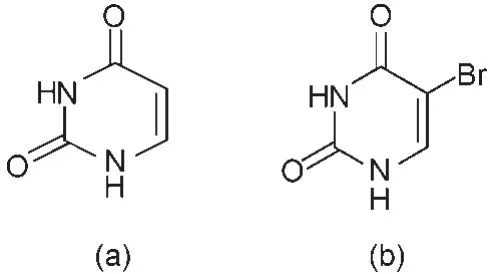
图1 尿嘧啶(a)和5-溴尿嘧啶(b)的分子结构Fig.1 Molecular structures of uracil(a)and 5-bromouracil(b)
2.2 量热装置与实验方法
低温热容测量所使用的量热装置为美国Quantum Design公司生产的综合物性测量系统中的热容测量模块,仪器型号为PPMS-9,测量温区为1.9-400 K,可变磁场为±9 T.本PPMS仪器于2014年7月在中国科学院大连化学物理研究所热化学实验室安装,经测定量热标准物质高纯度铜块的热容确证其测量准确度在20 K以下温区为±2%,20 K以上温区±0.6%.14尿嘧啶和5-溴尿嘧啶的低温热容实验温区为1.9-300 K,磁场设定为零,实验数据采集的温度间隔在100 K以下温区为lgT(T为进行热容测量的温度)、100 K以上温区为10 K.利用PPMS测量固体粉末样品热容一般对导热性差的样品测量误差较大;为了提高样品的导热性,将高纯度的铜片与样品充分混合并一起压制成片,然后再对样品进行热容测量.样品具体制备方法可参看文献.15,16量热实验所使用的样品质量尿嘧啶为13.24 mg、5-溴尿嘧啶为18.68 mg.
3 结果与讨论
3.1 热容测量结果
尿嘧啶与5-溴尿嘧啶两种化合物在1.9-300 K温区的热容测量结果列于表1;热容随温度变化的曲线Cp,m- T如图3所示,其中的小插图为10 K以下温区的实验数据.从图3可以看出,尿嘧啶和5-溴尿嘧啶的热容曲线在测量温度范围内均为一条光滑曲线,且热容数值随温度的升高而稳定的增大,表明在此温度范围内这两种化合物热力学性质稳定、没有相变或其它任何热异常现象发生.通过对比可以看出,在相同温度下5-溴尿嘧啶的摩尔热容值高于尿嘧啶;且随着温度的升高二者的热容差值增大,当温度达到一定值后该差值的增加趋势减缓.
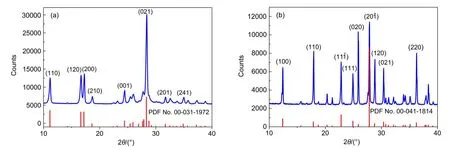
图2 尿嘧啶(a)和5-溴尿嘧啶(b)的X射线衍射(XRD)图谱Fig.2 X-ray diffraction(XRD)spectra of uracil(a)and 5-bromouracil(b)

表1 尿嘧啶和5-溴尿嘧啶摩尔热容(C⊖p,m)实验值Table 1 Experimental molar heat capacities(C⊖p,m)of uracil and 5-bromouracil
3.2 数据拟合和热力学函数计算
热容是物质的一个总体性质,其可以表示为晶格、电子、磁性等不同能量性质贡献的总和.一般温度较高时,热容的晶格贡献较大,可以把其它的贡献掩盖;但是当温度足够低时(一般小于25 K),晶格的贡献会减小到可以与其他贡献相当.这样在低温时就可以通过低温热容理论模型对实验热容数据进行拟合,从而将热容的各个贡献提取出来,为研究物质的相关物理性质提供重要的实验依据.17-20对于尿嘧啶和5-溴尿嘧啶10 K以下的实验数据,我们采用以下模型对数据进行拟合:


图3 尿嘧啶与5-溴尿嘧啶的热容实验值与拟合值Fig.3 Plot of the experimental and fitted heat capacities of uracil and 5-bromoruacil
其中,γT一般表示为电子、晶格缺陷或氧空位的热容贡献;对于此类有机化合物该贡献可能是因为样品在合成过程中出现的一些缺陷引起的.(B3T3+ B5T5+B7T7+B9T9)为比热的晶格贡献.18,21尿嘧啶和5-溴尿嘧啶的热容实验数据与拟合数据的百分比偏差如图4所示,可以看出在该温区内两种样品的拟合偏差均在±3%以内.此外,还计算了尿嘧啶和5-溴尿嘧啶数据拟合的均方根偏差(RMSD)分别为0.91%和0.89%.这就说明了方程(1)能够较准确地表达该温区内的热容实验数据.
对于50 K以上温区我们采用了德拜-爱因斯坦方程(方程(2))对实验数据进行了拟合.22,23该方程中, D(θD)和E(θE)分别代表德拜方程和爱因斯坦理论方程,θD和θE分别为德拜温度和爱因斯坦温度,m、n、a和b为拟合公式的调整系数.值得注意的是,方程(2)在这里仅对实验数据进行拟合,其中的各个拟合参数没有任何物理意义.

在10-50 K温区内,我们采用的多项式对实验数据进行了拟合,24其方程表示如下:
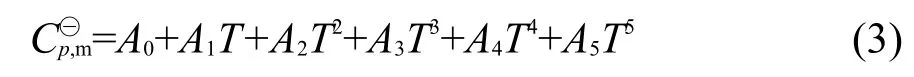
尿嘧啶和5-溴尿嘧啶实验摩尔热容通过方程(1)、(2)和(3)拟合得到的拟合参数及RMSD值列于表2,热容拟合值呈现于图3.根据这些拟合方程和拟合参数以及热力学关系式(4)和(5),计算了这两个化合物在0-300 K温区的摩尔熵变、摩尔焓变等热力学函数,并将这些函数值列于表3.尿嘧啶和5-溴尿嘧啶在温度T=298.15 K时的标准摩尔熵变分别为(132.48±1.32)和(165.39±1.65)J·K-1·mol-1.

图4 尿嘧啶与5-溴尿嘧啶10 K以下温区实验值与拟合值的相对偏差Fig.4 Plot of deviations of the experimental heat capacities from the fitted values against temperatures for uracil and 5-bromoruacil below 10 K

表2 尿嘧啶和5-溴尿嘧啶热容的拟合参数Table 2 Fitting parameters of heat capacities of uracil and 5-bromouracil

表3 尿嘧啶和5-溴尿嘧啶的标准热力学函数Table 3 Standard thermodynamic functions of uracil and 5-bromouracil


continued Table 3
3.3 两种化合物热容对比
由图3可以看出,由于受分子结构中溴取代基的影响,5-溴尿嘧啶的摩尔热容在整个测量温区内始终大于尿嘧啶.为了进一步分析溴取代基的热容贡献,计算了这两种化合物的摩尔热容拟合值的差值,其计算结果如图5所示.从图中可以看出,两种化合物的热容差(即溴取代基对热容的影响)在低温区随温度的升高迅速增大,当达到30 K左右温区时增速明显减慢,之后达到高温区时增速趋于平缓.可以用分子的振动频率来理解这种现象.在温度较低时,分子被紧紧地束缚,热容的贡献主要来自分子中原子之间的振动能量;尿嘧啶环中的C、N、O等原子结合力强,振动频率低,从而表现出的热容值就相对较低;而对于5-溴尿嘧啶,其除了拥有尿嘧啶环的振动外,还有溴取代基的振动,且溴与尿嘧啶环相对环内的原子结合力小,从而溴与其相连的环内C原子之间的振动就相对较大,表现出的热容值就较大.这就可以将两种化合物低温区的热容差值归结于是主要由溴取代基与尿嘧啶环上C原子的振动引起的.当温度较高时,分子的束缚力逐渐减弱,溴取代基的振动对热容的影响逐渐较小,整个分子的振动对热容的贡献增大;当温度高于一定值时,由于这两种化合物具有相似的分子结构,分子的振动成为热容的主要贡献,使得两者的热容差值趋于一定值.
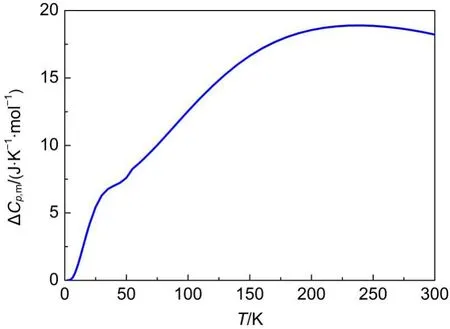
图5 尿嘧啶与5-溴尿嘧啶的比热拟合差值与温度的关系Fig.5 Plot of fitted heat capacity differences between uracil and 5-bromoruacil against temperatures
值得一提的是,Zielenkiewicz等12采用差示扫描量热法(DSC)在298.15-343.15 K温度范围内也对尿嘧啶和5-溴尿嘧啶的热容进行了测量,其测量值在298.15 K分别为131.8和144.7 J·K-1·mol-1,明显高于本文的测量值121.81和140.06 J·K-1·mol-1;此外,他们计算的两种化合物热容的差值(12.9 J·K-1·mol-1)也略低于我们的差值(18.25 J·K-1·mol-1).实际上DSC测量热容的准确度一般为±5%,有甚者可达±20%;这主要是因为该测量方法是动态的测量过程,测量的准确度受仪器的升温速率、样品的填充密度以及测量的气氛等因素影响大,因此该方法一般不用于精确的热容测量.而本文中采用的弛豫方法的准确度在高温时一般在±1%,是目前量热研究中小样品量热容测量普遍采用的方法.15,16,25因此,我们认为本文对尿嘧啶和5-溴尿嘧啶的热容测量更为准确,并且我们采用综合物性测量系统的热容测量模块,实现了温度1.9-300 K范围内热容的测量,比DSC法的测量温度范围更宽.
4 结论
利用综合物性测量系统测量了尿嘧啶和5-溴尿嘧啶在1.9-300 K温区的热容性质,并通过热容理论模型对实验数据进行了拟合;基于拟合数据,计算了这两种化合物在0-300 K温区内的热力学函数,并得到了298.15 K温度下的标准摩尔规定熵分别为(132.48±1.32)和(165.39±1.65)J·K-1·mol-1.通过对两种化合物摩尔热容的比较,利用晶格振动模式讨论了溴取代基与尿嘧啶分子振动对热容的贡献.通过与文献中差示扫描量热的热容测量结果对比,本文中在298.15 K的热容测量值低于文献报道值.鉴于差示扫描量热热容测量误差较大,我们认为本文对这两种化合物的热容测量结果以及热力学函数计算更为准确,并建议今后有关这两种物质的热力学研究中采用本研究工作中得到的热力学数据.
(1)Bai,S.Z.;Lou,X.H.;Yin,G.L.Shan Xi Chem.Indus.2009, 29,16.[白素贞,娄新华,尹桂玲.山西化工,2009,29,16.]
(2)Fang,W.Fine.Spec.Chem.2008,16,15.[方 巍.精细与专用化学品,2008,16,15.]
(3)Mei,Q.B.;Weng,J.N.;Tong,B.H.;Tian,R.Q.;Jiang,Y.Z.; Hua,Q.F.;Huang,W.Acta Phys.-Chim.Sin.2014,30(4),589. [梅群波,翁洁娜,童碧海,田汝强,蒋渊知,华庆芳,黄 维.物理化学学报,2014,30(4),589.]doi:10.3866/PKU. WHXB201402182
(4)Cao,G.J.;Zheng,W.J.Acta Phys.-Chim.Sin.2013,29(10), 2135. [曹国进,郑卫军.物理化学学报,2013,29(10),2135.] doi:10.3866/PKU.WHXB201308011
(5)Palafox,M.A.;Tardajos,G.;Guerrero,A.M.;Rastogi,V.K.; Mishra,S.P.;Ojha,W.Kiefer.Chem.Phys.2007,340,17.
(6)Alcolea,P.M.;Tardajos,G.;Guerrero,M.A.;Vats,J.K.; Hubert,J.;Rastogi,V.K.Spectrochim.Acta A 2010,75,1262.
(7)Miszczak,Z.E.;Wozniak,K.Zeitschrift Fur Naturforschung Section C-A Journal Of Biosciences 1997,52,670.
(8)Coats,E.;Glave,W.R.;Hansch,C.J.Med.Chem.1970,13, 913.doi:10.1021/jm00299a027
(9)Lai,G.Y.;Kong,J.;Wang,Q.Y.;Zhang,T.S.;Luo,K.;Huang, X.Q.J.Fish.Sci.China 2008,15,860.[赖光艳,孔 杰,王清印,张天时,罗 坤,黄雪芹.中国水产科学.2008,15,860.]
(10)Feng,Y.;Rainteau,D.;Chachaty,C.;Yu,Z.W.;Wolf,C.; Quinn,P.J.Biophysical Journal 2004,86(4),2208.doi: 10.1016/S0006-3495(04)74279-4
(11)Zielenkiewicz,A.;Desgranges,G.R.;Roux,A.H.;Grolier,J.P. E.;Wierzchowski,K.L.;Zielenkiewicz,W.J.Sol.Chem.1993, 22,907.doi:10.1007/BF00646602
(12)Zielenkiewicz,W.;Kozbial,M.;Swierzewski,R.;Szterner,P. J.Chem.Eng.2007,52,93.
(13)Chickos,J.S.;Acree,W.E.J.Phys.Chem.Ref.2002,31,537.
(14)Shi,Q.;Snow,C.L.;Boerio-Goates,J.;Woodfield,B.F. J.Chem.Thermodyn.2010,42,1107.doi:10.1016/j. jct.2010.04.008
(15)Shi,Q.;Boerio-Goates,J.;Woodfield,B.F.J.Chem. Thermodyn.2011,43,1263.doi:10.1016/j.jct.2011.03.018
(16)Shi,Q.;Zhang,L.Y.;Schlesinger,M.E.;Boerio-Goates,J.; Woodfield,B.F.J.Chem.Thermodyn.2013,61,51.doi: 10.1016/j.jct.2013.02.001
(17)Gopal,E.S.R.Specific Heats at Low Temperatures;Plenum Press:New York,1966;pp 20-111.
(18)Shi,Q.;Zhang,L.Y.;Schlesinger,M.E.;Boerio-Goates,J.; Woodfield,B.F.J.Chem.Thermodyn.2013,62,86.doi: 10.1016/j.jct.2013.02.023
(19)Shi,Q.;Park,T.J.;Schliesser,J.;Navrotsky,A.;Woodfield,B. F.J.Chem.Thermodyn.2014,72,77.doi:10.1016/j. jct.2014.01.021
(20)Ma,C.C.;Shi,Q.;Brian,F.W.;Navrotsky,A.J.Chem. Thermodyn.2013,60,191.doi:10.1016/j.jct.2013.01.004
(21)Phillips,N.E.;Rev,C.Solid State Sci.1971,2,467.
(22)Woodfield,B.F.;Shapiro,J.L.;Stevens,R.;Boerio-Goates,J.; Putnam,R.L.;Helean,K.B.;Navrotsky,A.J.Chem. Thermodyn.1999,31,1573.doi:10.1006/jcht.1999.0556
(23)Woodfield,B.F.;Boerio-Goates,J.;Shapiro,J.L.;Putnam,R. L.;Navrotsky,A.J.Chem.Thermodyn.1999,31,245.doi: 10.1006/jcht.1998.0447
(24)Ribeiro da Silva,M.A.V.;Ribeiro da Silva,M.D.M.C.;Lobo Ferreira,A.I.M.C.;Shi,Q.;Woodfield,B.F.;Goldberg,R.N. G.J.Chem.Thermodyn.2013,58,22.
(25)Lashley,J.C.;Hundley,M.F.;Migliori,A.;Sarrao,J.L.; Pagliuso,P.G.;Darling,T.W.;Jaime,M.;Cooley,J.C.;Hults, W.L.;Morales,L.;Thoma,D.J.;Smith,J.L.;Boerio-Goates, J.;Woodfield,B.F.;Stewart,G.R.;Fisher,R.A.;Phillips,N.E. Cryogenics 2003,43(6),369.doi:10.1016/S0011-2275(03) 00092-4
Low Temperature Heat Capacities of Uracil and 5-Bromouracil
ZHANG Xiao-Ye1,2XUE Bin1,*CHENG Ze1,2TAN Zhi-Cheng2SHI Quan2,*
(1School of Petrochemical Engineering,Shenyang University of Technology,Liaoyang 111003,Liaoning Province,P.R.China;2Dalian National Laboratory for Clean Energy,Liaoning Province Key Laboratory of Thermochemistry for Energy and Materials,Thermochemistry Laboratory,Dalian Institute of Chemical Physics,Chinese Academy of Sciences, Dalian 116023,Liaoning Province,P.R.China)
The heat capacities of uracil and 5-bromouracil were measured using a quantum design physical property measurement system(PPMS)in the temperature range of 1.9-300 K.The experimental results indicate that the heat capacities of the two compounds increase with increasing temperature,and no thermal anomalies are observed across the whole temperature range studied.The heat capacity values of 5-bromouracil are larger than those of uracil as it has a higher molecular weight but a similar molecular structure.The heat capacities were fitted to theoretical models and the thermodynamic functions were calculated based on the curve fitting. Thestandardmolecularentropiesat298.15Kweredeterminedtobe(132.48±1.32)and(165.39±1.65)J·K-1·mol-1for uracil and 5-bromouracil,respectively.
Uracil;5-Bromouracil;Heat capacity;Physical property measurement system; Thermodynamic function
O641
10.3866/PKU.WHXB201501122www.whxb.pku.edu.cn
Received:November 25,2014;Revised:January 12,2015;Published on Web:January 12,2015.
∗Corresponding authors.SHI Quan,Email:shiquan@dicp.ac.cn;Tel:+86-411-84379213.XUE Bin,Email:xue-b@163.com;Tel:+86-419-5319372

