国产日本当药中獐牙菜苦苷与当药苷的HPLC含量测定及其品质评价
国产日本当药中獐牙菜苦苷与当药苷的HPLC含量测定及其品质评价
余小磊1,卢燕2,黄庆3,陈道峰2
(1.江西中医药大学药学院,江西 南昌 330004;2.复旦大学药学院生药学教研室,上海 201203;
3.日本富基株式会社,日本 神户 6580032)
摘要:目的建立一种可以同时测定日本当药中獐牙菜苦苷与当药苷的方法,对我国引种与日本产的日本当药进行品质评价和比较。方法采用高效液相色谱法,色谱柱为Phenomenex C18(4.6 mm×250 mm,5 μm);流动相为乙腈-水,梯度洗脱,流速为1 mL·min-1,柱温为30 ℃,进样量为10 μL,检测波长分别为238、247 nm。结果獐牙菜苦苷、当药苷分别在0.019~1.234 mg·mL-1(r=1)、0.002~0.232 mg·mL-1(r=0.999 8)内呈良好的线性关系,平均加样回收率分别为99.50%、99.90%,RSD值分别为1.58%、2.10%。我国引种日本当药与日本产样品相比,个别成分相对含量略有差异,其中獐牙菜苦苷含量较高,达到了97.21 mg·g-1,而当药苷含量则较低;不同产地的日本当药均以花中有效成分含量最高。结论我国引种的日本当药中的獐牙菜苦苷含量高,很有开发价值,该文所建方法为我国对国产日本当药的合理开发利用和质量控制提供了依据和技术。
关键词:日本当药;高效液相色谱;獐牙菜苦苷;当药苷;品质评价
基金项目:科技部“重大新药创制”重大科技专项课题(No.2009ZX09301-011)
作者简介:余小磊,女,研究方向:中药分析,E-mail:303628094@qq.com
通讯作者:卢燕,女,博士研究生,副教授,硕士生导师,研究方向:中草药活性成分与质量控制,Tel:021-51980157,E-mail:luyan@fudan.edu.cn
中图分类号:R284文献标识码:A
Determination of swertiamarin and chiratin inSwertiajaponicaby HPLC and its quality evaluation
YUXiao-lei1,LUYan2,HUANGQing3,CHENDao-feng2
(1.SchoolofPharmaceuticalSciences,JiangxiUniversityofTraditionalChineseMedicine,Nanchang
330004,China;2.DepartmentofPharmacognosy,SchoolofPharmacy,FudanUniversity,Shanghai
201203,China;3.JapanTomimotoCo.,Ltd.,Kobe6580032,Japan)
Abstract:ObjectiveTo establish an HPLC method for the determination of swertiamarin and chiratin in Swertia japonica,as well as to evaluate the quality of S.japonica samples from China and Japan.MethodsThe determination method was developed on Phenomenex C18 column,eluting by a mixture of acetonitrile and water in gradient.The detector was set at 238 nm for swertiamarin and 247 nm for chiratin.ResultsThe line ranges of swertianmarin and chiratin were 0.019~1.234 mg·mL-1(r=1) and 0.002~0.232 mg·mL-1(r=0.999 8),respectively.The average recoveries were 99.50% (RSD=1.58%) and 99.90%(RSD=2.10%),respectively.The HPLC chromatograms of S.japonica samples from Japan and China were similar except for the relative height of some peaks.Compared with samples from Japan,S.japonica cultivated in China contained more swertiamarin and less chiratin.Both swertiamarin and chiratin were present with high content in flowers of S.japonica.ConclusionS.japonica was rich with swertiamarin as a potential medicinal resource.The quantitative method can be used in the development and quality control of S.japonica in China.
Key words:Swertiajaponica;HPLC;Swertiamarin;Chiratin;Quality evaluation
日本当药是龙胆科獐牙菜属植物SwertiajaponicaMakino的全草,性寒、味苦,归肝、肾、大肠经,具有消湿热、健胃及抗胆碱的功效[1],主要分布在日本、朝鲜[2]。据文献报道,日本当药的粗提物对于胃损伤及结肠癌有一定的修复及预防作用[2,3],在日本,主要作为苦味健胃剂来使用[2],是一种很有开发价值的药用资源。日本当药中富含环烯醚萜类、三萜类和黄酮类化合物,其中环烯醚萜类成分獐牙菜苦苷及当药苷具有多种生物活性,包括保肝、抗胆碱、镇痛镇静和护肤护发作用等[4~7],但现版日本药局方的Swertiae Herba标准中仅测定獐牙菜苦苷的含量[8]。我国的当药来源于同属植物瘤毛獐牙菜(S.pseudochinensisHara.)的全草,也具有清湿热、健胃的功效,其质量控制方法以獐牙菜苦苷和当药苷作为指标成分[9~12]。目前日本当药已在我国浙江引种,但尚未建立相关的质量标准。为了评价国产日本当药的质量,并比较日本当药与我国传统当药的差异,本研究在文献方法基础上,建立了高效液相色谱(HPLC)法同时测定日本当药中獐牙菜苦苷和当药苷两种活性成分的含量,对日本当药不同批次、不同产地及不同部位的样品进行了分析,并对日本当药与当药进行了比较,以期为日本当药在我国的成功引种及资源开发利用提供科学依据。
1仪器与试药
1.1仪器Agilent HP1200型高效液相色谱仪;AB135-S天平(梅特勒-托利多仪器有限公司);US10300AH超声波清洗器(北京优晟联合科技有限公司);DIY-200C型中药粉碎机(上海比朗仪器有限公司)。
1.2试药当药苷对照品(中国药品生物制品检定所,批号:111742-200501);獐牙菜苦苷(自制,经质谱、氢谱和碳谱确证结构,纯度大于98%);4批日本当药药材中有2批为日本原产样品,2批为中国浙江引种样品,经复旦大学药学院陈道峰教授鉴定均为SwertiajaponicaMakino的全草,标本存放于复旦大学药学院生药学教研室,6批当药样品为市场上不同产地的药材,经陈道峰教授初步鉴定为獐牙菜属植物的全草,具体品种有待进一步鉴定;乙腈(国药集团化学有限公司,色谱纯);水(杭州娃哈哈集团有限公司,去离子水);其他试剂均为分析纯。
2方法与结果
2.1色谱条件色谱柱:Phenomenex C18(4.6 mm× 250 mm,5 μm);流动相:乙腈-水(0~10 min,13%~13%;10~12 min,13%~20%;12~35 min,20%~50%;35~38 min,50%~100%;38~50 min,100%~100%);流速:1 mL·min-1;獐牙菜苦苷检测波长为238 nm,当药苷检测波长为247 nm;柱温:30 ℃。在上述色谱条件下,獐牙菜苦苷和当药苷对应的保留时间分别为7.9 min和11.8 min,分离度良好,色谱图见图1。
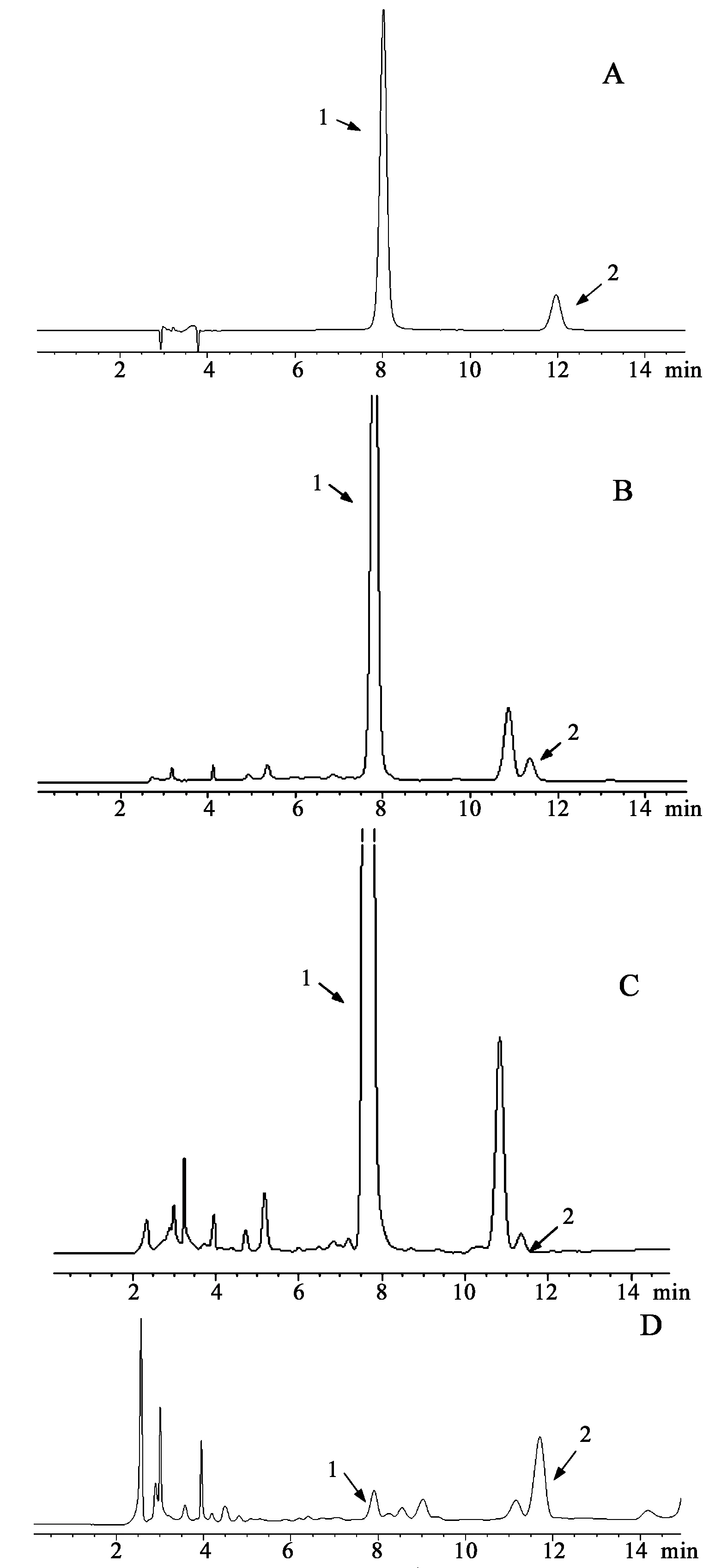
图1 HPLC色谱图(247 nm) A.混合对照品;B.日本产日本当药;C.国产日本当药;D.当药 1.獐牙菜苦苷;2.当药苷
2.2对照品溶液的制备分别精密称定对照品獐牙菜苦苷6.17 mg和当药苷1.16 mg,分别置5 mL容量瓶中,用甲醇稀释至刻度,摇匀,作为对照品储备液(浓度分别为1.234 mg·mL-1和0.232 mg·mL-1)。
2.3供试品溶液的制备取日本当药或当药药材粉末(过3号筛)约0.1 g,精密称定,置三角烧瓶中,用移液管精密移取10 mL甲醇于三角烧瓶中,称重,超声处理(功率200 W,频率40 kHz)40 min,放冷,称重,用甲醇补足所失重量,摇匀,过滤,所得滤液作为供试品溶液。
2.4线性关系考察将獐牙菜苦苷储备液依次稀释至2、4、8、16、32、64倍,精密吸取上述稀释液及储备液各10 μL注入高效液相色谱仪,以峰面积Y对进样浓度X求得回归方程为Y=13 154X-25.541(r=1);将当药苷储备液依次稀释2、4、8、16、32、64、128倍,精密吸取上述稀释液及储备液各10 μL注入高效液相色谱仪,以峰面积Y对进样浓度X求得回归方程为Y=17 183X-3.156 2(r=0.999 8)。结果表明,獐牙菜苦苷在0.019~1.234 mg·mL-1内呈良好的线性关系,当药苷在0.002~0.232 mg·mL-1内呈良好的线性关系。
2.5精密度试验取浓度为0.617 mg·mL-1的獐牙菜苦苷溶液,按上述色谱条件连续进样6次,每次进样10 μL,獐牙菜苦苷峰面积的RSD值为1.13%;取浓度为0.007 mg·mL-1的当药苷溶液,相同方法测定,当药苷峰面积的RSD值为1.90%。结果表明该方法精密度良好。
2.6稳定性试验取批号为74-KY-2012M的日本当药粉末(过3号筛)约0.1 g,精密称定,制备供试品溶液,室温放置,分别于0、3、5、7、9、12 h进样(每次进样10 μL),计算獐牙菜苦苷及当药苷含量,其RSD值分别为0.54%和1.36%,表明供试品溶液在12 h内稳定性良好;另于1、2、3、4、5 d进样(每次进样10 μL),计算獐牙菜苦苷及当药苷含量,其RSD值分别为1.52%和2.57%,表明供试品溶液在5天内稳定性良好。
2.7重复性试验取批号为74-KY-2012M的日本当药粉末(过3号筛)0.1 g,精密称定,平行6份,制备供试品溶液,注入高效液相色谱仪测定,计算得到獐牙菜苦苷及当药苷平均含量分别为59.91 mg·g-1和1.84 mg·g-1,其RSD值分别为1.9%和2.5%,结果表明该方法重复性良好。
2.8加样回收率考察取批号为74-KY-2012M的日本当药粉末(过3号筛)0.05 g,置于三角烧瓶中,精密称定,平行6份,分别精密加入獐牙菜苦苷对照品溶液(2.848 mg·mL-1)1 mL和当药苷对照品溶液(0.144 mg·mL-1)1 mL,再用移液管精密移取8 mL的甲醇,按供试品溶液制备方法进行处理,测定并计算加样回收率,獐牙菜苦苷和当药苷的平均回收率分别为99.5%、99.9%,RSD分别为1.58%、2.10%,结果见表1。
2.9样品测定
2.9.1不同产地日本当药及当药的含量测定取各批次日本当药药材粉末及当药药材粉末(过3号筛)约0.1 g,精密称定,制备供试品溶液,分别测定其中獐牙菜苦苷及当药苷的含量,结果见表2。

表1 獐牙菜苦苷及当药苷的加样回收率( n=6)

表2 日本当药及当药中獐牙菜苦苷和当药苷的含量比较( n=3)
由结果可知,浙江引种的日本当药与日本产样品相比,两者HPLC色谱图中成分种类基本一致,但个别成分相对含量不同,其中獐牙菜苦苷的含量以浙江产样品较高,而当药苷含量以日本产样品较高。日本当药与当药成分差异显著,尤其是獐牙菜苦苷的含量远远高于6批当药商品中獐牙菜苦苷的含量,当药苷的含量差异也比较明显。
2.9.2日本当药不同部位的含量测定从批号为74-KY-2012M及浙江-1 2批日本当药药材中挑拣出根、茎、叶和花4个部位,粉碎,精密称取各个部位药材粉末(过3号筛)约0.1 g,制备供试品溶液,分别测定其中獐牙菜苦苷及当药苷的含量,结果见表3。

表3 日本当药不同部位中獐牙菜苦苷和当药苷的含量( n=3)
由上述表中结果可知,无论是日本产还是浙江引种的日本当药中,獐牙菜苦苷及当药苷在花中的含量都是最高的,而且远远高于其他部位,提示花期为日本当药的最佳采收期。
3讨论
獐牙菜苦苷及当药苷是日本当药和当药的主要活性成分,本研究发现,无论是日本原产还是我国引种的日本当药都富含獐牙菜苦苷,其含量不仅远远高于日本药局方中日本当药中的獐牙菜苦苷的含量标准(20 mg·g-1)[8],也高于《中国药典》2010年版中当药中獐牙菜苦苷的含量标准(35 mg·g-1)[12]。而与《中国药典》2010年版当药的当药苷含量标准(0.7 mg·g-1)[12]相对照,日本原产日本当药含量明显高于标准,引种的日本当药含量略低于标准。因此,很有必要加强对国产日本当药的开发利用,同时深入比较日本当药与当药的药效差异。
我国獐牙菜属植物有79种,市场上当药品种混乱,质量参差不齐[9]。本研究从市场上收集到的6批当药药材质量差异明显,其中当药苷的含量基本符合现行《中国药典》标准,但獐牙菜苦苷的含量都远低于药典标准,为不合格药材,推测可能都是伪品或混淆品,其具体植物来源还有待鉴定,也说明现行当药质量标准急需完善,以提高其真伪鉴别的专属性。今后研究中,将收集足够批次的正品当药与日本当药样品,进行两种当药的比较与质量标准完善研究。
参考文献:
[1] Kimura Y,Sumiyoshi M.Effects of Sweitia japonica extract and its main compound swertiamarin on gastric emptying and gastrointestinal motility in mice[J].Fitoterapia,2011,82 (6):827-833.
[2] Yamahara J,Kobayashi M,Matsuda H,et al.Anticholinergic action of Swertia japonica and an active constituent[J].J Ethnopharmacol,1991,33 (1-2):31-35.
[3] Yamahara J,Konoshima T,Sawada T,et al.Biologically active principles of crude drugs:pharmacologica actions of Swertua japonica extracts,swertainmarin and gentianine[J].Yakugaku Zasshi,1978,98 (11):1446-1451.
[4] 马丽娜,田成旺,张铁军,等.獐牙菜属植物中环烯醚萜类成分及其药理作用研究进展[J].中草药,2008,39 (5):790-795.
[5] 胡若琪,饶娴宜,冯毓正,等.獐牙菜甙对实验大鼠肝病理形态学的影响[J].云南中医学院学报,1991,14 (1):35-38.
[6] 姜燕.獐牙菜属植物化学成分的研究概况[J].国外医药(植物药分册),1990,5 (3):99-103.
[7] 李冬梅,肖怀,刘光明.獐牙菜属植物研究进展[J].大理学院学报,2007,6 (2):77-80.
[8] 日本药局方委员会.日本药局方(第十六版)[S].东京:日本厚生劳动省,2012:1764.
[9] 李建晨,贾玉捷,杨晓靖,等.市售当药的质量考察与资源状况分析[J].中药材,2012,35 (5):696-698.
[10] 段吉平,牛小莲,袁浩,等.HPLC测定当药中当药苷的含量[J].中国药师,2012,15 (9):1274-1276.
[11] 黄文哲,许春晖,周大成,等.RP-HPLC测定当药中环烯醚萜和三萜类成分含量[J].中国中药杂志,2007,32 (32):2494-2496.
[12] 国家药典委员会.中华人民共和国药典2010年版(一部)[S].北京:中国医药科技出版社,2010.

