反丁烯二酸酯类物质结构与抑菌性能关系
邱松山,姜翠翠,周如金,刘杰凤
(广东石油化工学院果蔬加工与贮藏工程中心,广东 茂名 525000)
反丁烯二酸酯类物质结构与抑菌性能关系
邱松山,姜翠翠,周如金,刘杰凤
(广东石油化工学院果蔬加工与贮藏工程中心,广东 茂名 525000)
摘要:采用密度泛函理论(DFT)考察反丁烯二酸酯类化合物结构与抑菌活性之间的定量构效关系(QSAR)。在B3LYP/6-311++ G(d)基组下对13种反丁烯二酸酯类化合物进行几何构型优化和频率计算,选取最高占据轨道能量EHOMO、最低空轨道能量ELUMO及两者的绝对差值∆E、偶极矩(μ)、零点能、平均分子极化率(p)等量化参数作为量子化学描述符,通过多元逐步回归分析筛选影响抑菌活性的主要因素并建立化合物量化参数和抑菌活性之间的QSAR模型方程,并用留一法交叉验证模型的稳定性及预测能力。结果表明反丁烯二酸酯类化合物抑制枯草芽孢杆菌性能与其结构参数∆E、μ、ZPE之间存在着较高的线性关系,∆E和μ越大,抑菌活性越大,相关系数R=0.957,此类化合物抑制枯草芽孢杆菌活性的理论值与实验值的相关性良好,表明该模型能较好的预测此类具有α,β-不饱和羰基母体结构的反丁烯二酸酯类化合物的抑菌活性。
关键词:反丁烯二酸酯类化合物;构效关系;抗菌活性;计算机模拟;构型优化;外部预测
反丁烯二酸酯类防腐剂是目前使用非常广泛的一类抑菌剂,具有使用方便、无残毒、生产成本低、价格便宜等特点,是目前饲料、谷物较为理想的防霉抑菌剂。具有α,β-不饱和羰基母体结构的反丁烯二酸单甲酯(MMF)、反丁烯二酸二甲酯(DMF)、反丁烯二酸单乙酯(MEF)、反丁烯二酸单丁酯(MBF)、反丁烯二酸单辛酯(MOF)等抑菌作用突出[1]。食品防腐剂分子结构与活性之间关系的研究一直是一个受关注的课题,研究表明通过对不同浓度的MMF、MEF、MBF的抑菌效果的比较,5种反丁烯二酸单酯对11种常见霉菌都有一定的抑菌作用,其中对青霉的抑菌效果较好,对木霉、曲霉、根霉也有较好的抗菌效果[2]。周常义等[3]研究表明,离子型反丁烯二酸单甲酯对金黄色葡萄球菌、枯草芽孢杆菌的最小抑菌浓度为 0.06g/L,现有的研究均表明非对称反丁烯二酸酯类是一类具有良好防霉抗菌性能的化合物,对霉菌、酵母菌具有较好的抗菌效果。
防腐剂的抑菌性能本质上取决于化合物的量子生物化学特性,探讨反丁烯二酸酯类防腐剂的量子化学与抑菌活性之间的关系及其抑菌机制有着重要的理论意义和实践意义[4-5]。定量结构-活性关系(quantitative structure-activity relationship,QSAR)的发展非常迅速,结合实验数据通过数学模型定量描述化合物的分子结构、理化性质和活性之间的关系,从而能够建立化合物结构与活性-性质之间的数学模型[6]。邱松山等[7]分析了具有抗菌活性的11种对羟基苯甲酸酯类化合物的定量构效关系,结果表明化合物的最低空轨道能量、偶极距和极化率是影响对羟基苯甲酸酯类化合物抗菌活性的主要因素。郭新竹等[8]对丁烯二酸酯类分子的偶极矩、能量等量子生物化学特性进行计算,并对17种含α,β-不饱和羰基结构的分子连接性指数与抗菌活性进行回归分析,结果表明抑菌效果与抑菌剂的分子前线轨道能量的绝对值成反比,抑菌能力与抑菌剂的最高占有轨道能量呈显著的直线回归关系,且不饱和结构及其杂原子在发挥抗菌功能中起着重要的作用。周如金等[9]对目标化合物分子的量子化学参数进行优化筛选,结果表明含α,β-不饱和羰基结构的化合物周边的分子碎片对抗菌活性影响较大。ZHU等[10]和TRESADERN等[11]分别通过对含α,β-不饱和羰基结构的防腐剂分子的拓扑参数和量子化学参数进行线性回归,获得此类化合物的定量结构与抑菌活性之间的QSAR关系模型,该模型表明此类防腐剂持久的抑菌性能主要取决于防腐剂容纳电子的能力,因此探讨反丁烯二酸酯类化合物结构与生物活性的QSAR模型可大大增加对其分子抑菌活性机制的解释,从而为更高效的抑菌剂开发奠定基础。本文采用Gaussian 09软件对13种反丁烯二酸酯类化合物的分子构型进行结构优化与频率分析,在6-311++G(d)基组的水平下对其分子和相应的基团进行计算,用密度泛函理论(DFT)建立反丁烯二酸酯类化合物量化参数和抑菌活性之间的QSAR模型,在稳定构型下得到反丁烯二酸酯类化合物抗大肠杆菌活性间的构效关系,为研究新型高效反丁烯二酸酯类抑菌物奠定基础。
1 材料与方法
1.1 主要仪器及试剂
756PC分光光度计,上海菁华科技仪器有限公司,SW-CJ-2FD超净工作台,苏州安泰空气技术有限公司,LS-50HD数显压力蒸汽灭菌器,江阴滨江医疗设备有限公司;NRY-1102C立式恒温摇床,上海南荣实验室设备有限公司,FE20K酸度计,梅特勒-托利多国际贸易(上海)有限公司。
葡萄糖、盐酸、氢氧化钠、二甲基亚砜等为分析纯试剂,牛肉膏、蛋白胨、琼脂粉等为生化试剂;所用水为去离子水,灭菌后使用。
1.2 最低抑菌浓度(MIC)分析
供试菌种:枯草芽孢杆菌(B. subtilis ATCC 6633):由广东石油化工学院生物实验室提供,接种至营养肉汤培养基,菌种使用前在固体培养基上活化一次。
营养肉汤培养基(NB):牛肉膏0.3%、蛋白胨1%、葡萄糖1%、氯化钠0.5%,pH=7.0~7.2。细菌固体营养肉汤培养基则添加2%的琼脂,培养基在使用之前121℃灭菌20min,待用。
供试的15种反丁烯二酸酯类化合物如表1所示,使用前配成1.00mg/mL溶液。
菌悬液的制备:枯草芽孢杆菌(B. subtilis)在30℃培养24h,之后稀释至0.5麦氏比浊度(OD625nm= 1.1~1.3),用培养基将菌悬液以1∶50稀释至最终浓度104CFU/mL。
最低抑菌浓度(MIC)测定:参考文献[12]的方法进行,将反丁烯二酸酯类样品溶于DMSO中,倍比稀释,然后加入菌悬液中,使之最终浓度为1.00mg/mL,37℃恒温培养48h,DMSO在培养基中的最终浓度不超过2%,强光清澈透明、无可见微生物生长,化合物最低浓度即为MIC,试验重复3次。
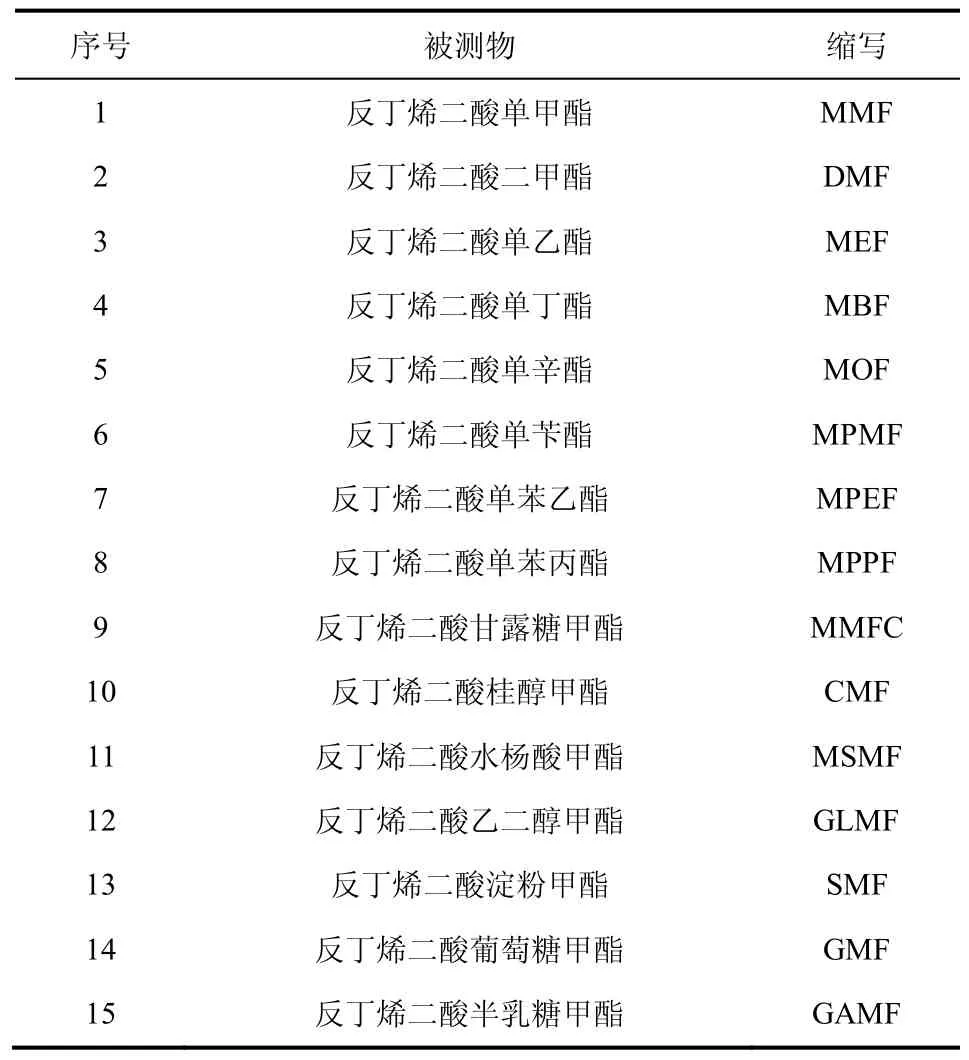
表1 反丁烯二酸酯类化合物一览表
1.3 量化方法和量化参数
采用Gaussian 09量子化学程序包[13]中的密度杂化泛函B3LYP方法,在6-311++ G(d)基组下优化13种反丁烯二酸酯类化合物的几何构型和频率计算,选取主要反映分子特征结构的最高占据轨道能量EHOMO、最低空轨道能量ELUMO及两者的绝对差值∆E作为表征分子间相互作用的参数,选取衡量分子极性的偶极矩(μ)、零点能(zero-point energy,ZPE)、平均分子极化率(p)等6个量化参数研究反丁烯二酸酯类化合物结构与抑菌活性之间的关系,几何构型优化均收敛,经频率分析表明无虚频。反丁烯二酸酯类化合物的抗菌最低抑菌浓度lg(1/MIC)及量子化学参数值见表2。
2 结果与分析
2.1 量化参数选择
选取13种反丁烯二酸酯类化合物的lg(1/MIC)作为活性参数,应用SPSS软件分析相关化合物的抑菌活性lg(1/MIC)与量化计算所得的参数之间的相关性,结果如表3所示。
由表3可知,反丁烯二酸酯类化合物抑菌活性lg(1/MIC)与∆E、µ、p、ZPE等的相关系数较大,与ZPE成负相关,与∆E、µ成正相关。
2.2 定量构效关系(QSAR)
QSAR研究主要从化合物结构出发,结合生物活性实验数据建立二维或多维函数关系,揭示分子结构与其活性间的构效关系,从而为新分子的设计及评价提供理论依据[14],本文在95%置信区间内应用SPSS软件对抑菌活性和量化参数进行逐步回归分析,获得抑菌活性lg(1/MIC)和各量化参数之间的最佳模型方程。
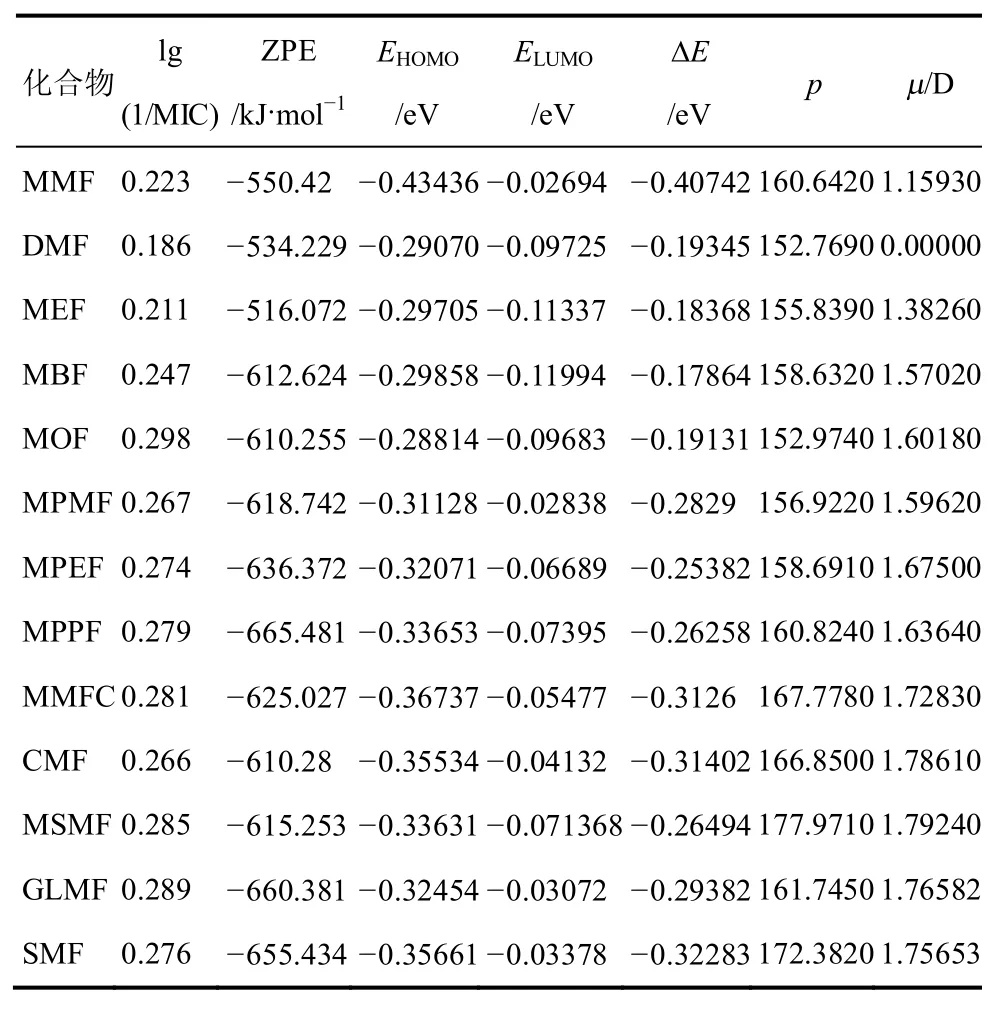
表2 B3LYP/6-311++G(d)基组下反丁烯二酸酯类化合物的抑菌活性及量化参数
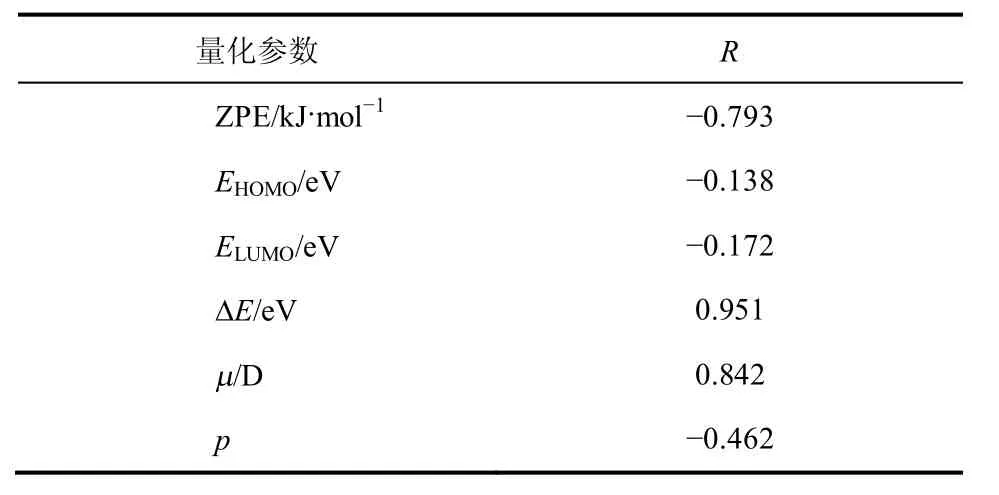
表3 反丁烯二酸酯类化合物的抑菌活性与量化指数的相关系数
lg(1/MIC) = 30.578×∆E+0.014×μ−0.019×ZPE
R=0.957,R2=0.916,R2aj=0.929,F=32.099,n=13,Sig.<0.000
由该QSAR方程可知,所研究的反丁烯二酸酯类化合物的抑菌活性lg(1/MIC)与其结构参数∆E、µ、ZPE之间存在着较高的线性关系。∆E和µ越大,抑菌活性越大,相关系数R=0.957,表明该模型能较好地预测此类具有α,β-不饱和羰基母体结构的反丁烯二酸酯类化合物的抑菌活性。
2.3 分子结构对抑菌活性的影响
研究表明反丁烯二酸酯类防腐剂抑菌作用依赖于化合物基团的空间立体特性,只有化合物抑菌活性中心与微生物生命分子的活性功能域发生有效接触,反丁烯二酸酯类化合物才能发挥抗菌作用。在分子间的自由碰撞过程中,化合物反应活性中心周围空间位阻愈小,抑菌活性中心原子发生有效碰撞的概率就愈大,其抗菌活性相对愈强[8,15]。宁正祥等[15]研究表明,反丁烯二酸酯类化合物结构中含有α,β-不饱和羰基结构,具有电子中继系统且羰基电子与相邻烯键电子间形成共轭效应,具有强的电子缓冲能力;此外,反丁烯二酸酯类的抑菌活性比相应的顺式构型的丁烯二酸酯类高几倍,表明影响抑菌剂抑菌效果发挥的首要因素是空间位阻效应,并决定了抑菌剂分子中的反应活性中心直接与菌体中的受体部位发生有效碰撞的频率占抗菌剂分子与受体总碰撞频率的比例[16]有关。能量最高的占据轨道HOMO和能量最低的空轨道LOMO统称为前线分子轨道,不同化合物分子参与反应的HOMO与LUMO的能量越接近,相互作用越强,体系就越稳定;HOMO和LUMO重叠越大,分子间形成的键就越牢固,化合物表现出的生物活性就越大[11,17]。反丁烯二酸酯类化合物分子中电子得失和转移能力主要取决于HOMO和LUMO能量,不同分子的抑菌活性受能量差∆E的影响较大,此类化合物中羧基酯化后亲脂性比母体分子增强,其抑菌性能与化合物的分子结构有较大关联,抑菌性能本质上取决于防腐剂与微生物作用时的电子行为,由所建立的QSAR方程可知,反丁烯二酸酯类化合物的抑菌活性与分子的∆E和µ呈正相关性,在反丁烯二酸类物质的骨架引入极性供电子基对分子发挥抑菌作用是有利的,这为更具抑菌活性的反丁烯二酸酯类化合物的设计奠定了基础。
2.4 QSAR模型验证
反丁烯二酸酯类化合物抑菌活性lg(1/MIC)实验值与理论值的相关性及残差如图1和图2所示。由图1、图2可知,化合物抑菌活性lg(1/MIC)理论值与实验值的相关性良好,且其残差值以0为中心符合正态分布。
采用方差膨胀因子(VIF)[7]评价所建立的QSAR模型中各自变量的共线性,结构参数∆E、µ、ZPE的平均VIF为2.976,表明样本对回归模型结果的稳定性和可靠性影响较小,相关参数的选取可靠。
2.5 QSAR模型的外部预测
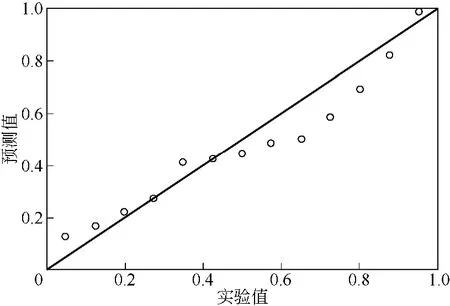
图1 lg(1/MIC)理论值与实验值的相关性

图2 13种反丁烯二酸酯类化合物lg(1/MIC)残差分布
选取所测13种以外的2种反丁烯二酸酯类化合物GMF和GAMF对所建立的QSAR模型进行外部预测,GMF和GAMF抑菌活性lg(1/MIC)采用1.2节的方法进行,分析计算值和实验测定值的残差结果如表4所示,计算值与测定值基本符合。
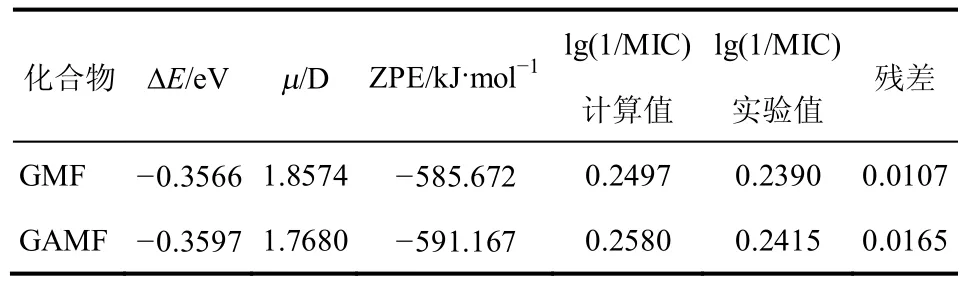
表4 根据模型计算所得数据和残差表
3 结 论
在B3LYP/6-311++G(d)水平上对具有抑菌活性的13种反丁烯二酸酯类化合物进行构型优化和频率计算,逐步回归分析筛选影响抗大肠杆菌活性的主要参数,建立反丁烯二酸酯类化合物抑制枯草芽孢杆菌的QSAR方程:
lg(1/MIC) = 30.578×∆E+0.014×μ-0.019×ZPER2=0.916,R2aj=0.929
反丁烯二酸酯类化合物抑制枯草芽孢杆菌活性lg(1/MIC)与其结构参数∆E、μ、ZPE之间存在着较高的线性关系,∆E和μ越大,化合物抑菌活性越大,所建立的模型验证表明反丁烯二酸酯类化合物抑制枯草芽孢杆菌活性lg(1/MIC)的理论值与实验值的相关性良好,该模型能较好地预测此类具有α,β-不饱和羰基母体结构的反丁烯二酸酯类化合物的抑菌活性。
参 考 文 献
[1] 闫澍. 富马酸酯类防腐剂的合成与抑菌性能研究[D]. 大连:大连理工大学,2006.
[2] 黄斌,蒋立建,丁军. 几种富马酸单酯的抑菌效果研究[J]. 食品科技,2005,5:36-38.
[3] 周常义,欧光南,苏国成,等. 离子型反丁烯二酸单甲酯的合成及抑菌活性研究[J]. 食品科学,2009,30(2):142-145.
[4] 宁正祥,高建华. 食品防腐剂的抗菌机理及构效关系[J]. 广州食品工业科技,1997,13(3):1-4.
[5] 张桂芝. 食品防腐剂的分子结构和抗菌活性的关系[J]. 新疆农业科学,2004,41:42-44.
[6] YANG C,SHAO Y,ZHI X,et al. Semisynthesis and quantitative structure-activity relationship(QSAR) study of some cholesterolbased hydrazone derivatives as insecticidal agents[J]. Bioorganic & Medicinal Chemistry Letters,2013,23(17):4806-4812.
[7] 邱松山,姜翠翠,周如金,等. 对羟基苯甲酸酯类化合物抗菌活性的定量构效关系探讨[J]. 现代食品科技,2014,30(6):98-102.
[8] 郭新竹,宁正祥,黄志良. 含α,β-不饱和羰基结构抗菌剂的定量结构-活性关系研究[J]. 广东药学院学报,2001,17(3):178-179.
[9] 周如金,曾霞,黄敏,等. 含α,β-不饱和羰基结构化合物的定量结构-活性关系研究[J]. 食品科学,2008,29(8):128-132.
[10] ZHU H,GUO W,SHEN Z,et al. QSAR models for degradation of organic pollutants in ozonation process under acidic condition[J]. Chemosphere,2015,119:65-71.
[11] TRESADERN G,CID J M,TRABANCO A A. QSAR design of triazolopyridine mGlu2 receptor positive allosteric modulators[J]. Molecular Graphics and Modeling,2014,53:82-91.
[12] MA Y L,ZHOU R J, ZENG X Y,et al. Synthesis,DFT and antimicrobial activity assays in vitro for novel cis/trans-but-2-enedioic acid esters[J]. Journal of Molecular Structure,2014,1063:226-234.
[13] FRISCH M J,TRUCKS G W,SCHLEGEL H B,et al.Gaussian09,Revision B.01[M]. Wallingford C T:Gaussian,Inc.,2009:9096580.
[14] 夏树伟,毛雅嫔,薛倩倩,等. 取代喹啉类化合物抗菌活性的定量构效关系及分子设计[J]. 高等学校化学学报,2011,32(10):2415-2420.
[15] 宁正祥,谭龙飞,张德聪,等. α,β-不饱和羰基化合物的分子结构特性与抗菌活性间的关系[J]. 应用化学,1996,13(1):38-42.
[16] SAMET M,RAHMI K,TUBA İ,et al. Synthesis,structure-activity relationships,and in vitro antibacterial and antifungal activity evaluations of novel pyrazole carboxylic and dicarboxylic acid derivatives[J]. European Journal of Medicinal Chemistry,2014,78 (5):86-96.
[17] IMAMURA Y,SUZUKI K,IIZUKA T,et al. Linearity condition for orbital energies in density functional theory (Ⅴ):extension to excited state calculations[J]. Chemical Physics Letters,2015,618:30-42.
研究开发
Relationship between antibacterial activity and structure of fumaric acid esters
QIU Songshan,JIANG Cuicui,ZHOU Rujin,LIU Jiefeng
(Development Centre of Technology for Fruit & Vegetables Storage and Processing Engineering,Guangdong University of Petrochemical Technology,Maoming 525000,Guangdong,China)
Abstract:The quantitative structure-activity relationship (QSAR) between molecular structures and antibacterial activity of fumaric acid esters was studied using the density functional theory (DFT) at the B3LYP functional at the level of 6-311++G(d) basis set. The energy of the highest occupied molecular orbital EHOMO,the energy of the lowest unoccupied molecular orbital ELUMO,the difference of energy ∆E,the dipole moment μ,the zero-point energy (ZPE) and the average molecular polarizability (p) were selected as the structural descriptors. The geometries and the QSAR model of the samples were optimized and the stable complexes were obtained. The stability and predictive ability of the model were examined by the “leave-one-out” cross-validation method.The results suggest that the dipole moment μ,∆E and zero-point energy are the predominant factors affecting the antibacterial activity against B. subtilis. The antifungal activity increases with the increase of ∆E and μ. The obtained QSAR model has a good stability and predictive ability for such inhibitors.
Key words:fumaric acid esters; structure-activity relationship; antibacterial activity; computer simulation;structure optimization; outer prediction
收稿日期:2015-06-17;修改稿日期:2015-09-01。基金项目:广东省部产学研结合项目(2013B090600032)、茂名市科技计划(2014007)及果蔬加工与贮藏工程中心开放基金(2015A005)项目。第一作者:邱松山(1978—),男,博士,副教授。联系人:周如金,博士,教授。E-mail tustqss@163.com。
DOI:10.16085/j.issn.1000-6613.2016.03.035
中图分类号:TS 201.2
文献标志码:A
文章编号:1000–6613(2016)03–0879–05

