全球肉毒毒素市场发展趋势
骆叶,张建民,刘迪,孙毅,孙燚,李建华,胡兴越,冯莺吴慧玲,王莉,蔡华英,陈寅,姜方震,张旭东,朱全超
(邵逸夫医院肉毒毒素中心,更美App消费者中心)
全球肉毒毒素市场发展趋势
骆叶,张建民,刘迪,孙毅,孙燚,李建华,胡兴越,冯莺吴慧玲,王莉,蔡华英,陈寅,姜方震,张旭东,朱全超
(邵逸夫医院肉毒毒素中心,更美App消费者中心)
自1989年肉毒毒素首次被FDA批准治疗斜视之后,在全球肉毒毒素共被超过88个国家批准了29个适应症。近20年来其稳定的治疗效果和安全性已经逐步得到了广泛的认可,从最初的用来治疗眼睑痉挛、面肌痉挛、痉挛性斜颈、斜视等到后来的逐步批准应用于美容领域。目前全球肉毒毒素品牌共有10多个,本文就全球肉毒毒素市场发展趋势作简要分析阐述。
肉毒毒素;市场份额;适应症;FDA;KFDA;CFDA;CMA
1 概 述
肉毒毒素注射具有操作方便,无须手术,痛苦小,副作用少,见效快等特点。近20年来其稳定的治疗效果和安全性已经逐步得到了广泛的认可,从最初临床用于治疗斜视、痉挛性斜颈、眼睑痉挛、面肌痉挛等到后来逐步批准应用于美容领域。2016年1月22日FDA批准了美国艾尔建公司(Allergan)的保妥适(Botox,Onabotulinumtoxin A)用于治疗成人下肢痉挛。至此,肉毒毒素在全球共被超过88个国家批准了29个适应症。据统计[1],目前仅保妥适就拥有超过2800份公开广泛的研究文献,在全球已有超过4200万人次的临床治疗应用。全球接受肉毒毒素治疗患者的比例越来越高,肉毒毒素注射的技术也日新月异。
国际美容整形外科学会(ISAPS)统计显示:2015年全球肉毒毒素注射到达462.78万人次。目前保妥适(Botox)在治疗领域的增长速度远高于美容领域,虽然保妥适仍是全球肉毒毒素市场份额第一的产品,但是随着越来越多的同类产品出现,其市场份额已从2005年的最高点86%已跌至2015年的74%(见图1)。2005-2013年全球肉毒毒素市场复合增长率(CAGR)13.20%,期间保妥适市场年复合增长率(CAGR)11.5%。预计到2019年全球肉毒毒素市场份额前三位分别为:美国Allergan的Botox(约68%),法国Galderma的Dysport和Azzalure(约12%),德国Merz的Xeomin(约5%)。目前全球已上市及在研发肉毒毒素产品共有10多个。

图1 :1998-2015年全球肉毒毒素产品VS 保妥适市场销售状况
2.肉毒毒素的临床应用进展
自1978年Alan Scott博士第一次将肉毒毒素应用于临床治疗斜视,至今已有30年的历史。目前已发展为治疗各种局限性张力障碍性疾病,其疗效稳定而可靠。起初医生将肉毒毒素用于治疗面部痉挛和其他肌肉运动紊乱症,用它来放松肌肉神经,以此达到停止肌肉痉挛的目的。治疗过程中医生们发现,肉毒毒素在消除皱纹方面具有更加显著的功效,于是肉毒毒素美容注射术应运而生,并迅速风靡全球。
皱纹产生来自于肌肉的运动,肌肉的运动是由神经递质乙酰胆碱进行支配和调节的。由于肉毒毒素的治疗原理是阻断Snare蛋白通过胞吐作用释放神经递质乙酰胆碱(见图2),从而达到放松肌肉的作用,从根本上预防并且消除动态性皱纹。随着肉毒毒素基础研究得进展,我们发现肉毒毒素不仅阻断了乙酰胆碱的释放,同时还有可能阻断P物质等炎性介质,因此其临床用途逐渐发展为以下四类:
2.1 肌肉功能亢进的临床用途
A肌张力障碍(主要包括颈部肌张力障碍、眼睑痉挛、口下颌肌张力障碍、痉挛性构音障碍、作家职业性痉挛、足肌张力障碍、音乐家痉挛、面肌痉挛、Meige综合征、抽动障碍和口吃)。
B高功能性面部皱纹;
C偏侧面肌痉挛;
D斜视;
E 眼球震颤;
F 卒中和脑瘫后肢体痉挛;
G震颤:四肢、颈部、声带;
H肌阵挛;
I其他喉部疾病:童音症、声带突肉芽肿。2.2 自主神经系统的应用
A多汗症:腋下、手掌、足底和面部;
B良性前列腺增生;
C流涎/涎腺囊肿/多涎;
D鼻炎;
E食管上括约肌/食管下括约肌失迟缓症;
F神经性膀胱功能亢进;
G味觉性出汗综合征;
H肛裂;
I阴道痉挛/肛门痉挛。
2.3 感觉神经系统/疼痛综合征/抗炎性反应方面的应用
A紧张性头痛;
B慢性偏头痛;
C颞下颌关节紊乱/磨牙症;
D肌筋膜疼痛;
E带状疱疹后遗神经痛;
F关节炎;
G三叉神经痛;
H腰痛。
2.4 腺体、内分泌细胞调节的应用
生长激素/肢端肥大症。
肉毒毒素为一些罕见的神经系统疾病增加了一种治疗选择,随着临床研究的进展,对这些罕见的疾病会有更深刻的认识。表1列举了一部分保妥适在不同地区和国家批准的适应症。

表1 不同地区和国家批准的适应症

图2 肉毒毒素的作用机制[2]
3 肉毒毒素的分类与差异
肉毒毒素是一种生物制剂产品,其生产工艺过程决定了产品的特性,因此不同品牌的肉毒毒素不具有等量换算的特点,可以说没有两个肉毒毒素产品是完全一样的。肉毒毒素注射已经成为了当今世界的主流治疗手段,明确各种肉毒毒素产品的特点和差异是至关重要的,这有助于更精准地使用注射产品并减少不必要的并法症发生概率。
肉毒毒素是肉毒梭菌生长繁殖过程中产生的一种细菌外毒素,根据其抗原性的不同分为A-G七个亚型,其中A,B,E,F型是引发人肉毒中毒的型别,C,D型是动物禽类肉毒中毒的型别,G型尚无引起中毒的正式报道。其中A、B型属于注射型肉毒毒素,目前应用最广泛的当属A型肉毒毒素,效力也是最强的。B型肉毒毒素主要可以用于对A型肉毒毒素产生抗体的患者。
从治疗方式来分类,A型肉毒毒素又分为注射用肉毒毒素和外用肉毒毒素。所谓的外用肉毒毒素,是指将A型肉毒毒素通过皮肤转运,外用肉毒毒素给一些难以注射的解剖位置或者不希望通过注射的方法来获得治疗的患者提供选择。
FDA特别指出,不同品牌的肉毒毒素之间是不可以进行等量换算的。除了维持时间基本上都在120天左右之外,不同品牌的肉毒毒素在效力,弥散度、分子量、赋型剂,纯化方法上都是不同的。
4 全球肉毒毒素品牌产品及正在开发产品简介
4.1 目前全球肉毒毒素产品大致有以下10多种:
4.1.1 Onabotulinumtoxin A,Botox, Allergan, Inc.(US)
Onabotulinumtoxin A是世界上应用最广泛,迄今为止全球销量排第一的产品,也是美国艾尔建公司的拳头产品。在中国商品名是保妥适,在其他国家是Botox(美国加拿大)、Vistabel(法国)、Botox Vista(日本)、Vistabex(意大利)。它的特点是其分子量是单一恒定的900KD,规格有50U、100U、200U三种,运用的赋形剂是可追溯的人血白蛋白,用真空干燥法进行干燥,2-8度冷藏有效期为36个月。产品特点是作用精准,纯度高,安全性好,不容易产生过敏和耐药。目前保妥适在全球超过88个国家上市,获批29个适应症。
Abobotulinumtoxin A由英国Ipsen公司生产,最早于1999年通过CE认证,于2009年通过FDA认证,商品名为丽舒妥(中国)、Dysport、Azzalure(国外)、Reloxin(目前已废除使用该名称)。Dysport和Azzalure只是每瓶的剂量不同, 规 格 有125U(Azzalure)、300U、500U两种,其余特异性与生物活性均相同。它的分子量是300KD、500KD、900KD不等,运用的赋形剂是可追溯的人血白蛋白,用冻干法进行干燥,有效期为15个月。目前丽舒妥在全球75个国家上市。
IncobotulinumtoxinA由德国Merz公司生产,最早于2005年通过CE认证,于2010年通过FDA认证,商品名为希尔敏(中国)、Xeomin(美国)、Bocouture(英国),规格有50U、100U,2016年2月9日Xeomin在美国新上市了针对成人上肢痉挛适应症(2015年12月23日FDA已批准)[3]的 200U的新剂型。它的分子量为单一的150KD,不含络合蛋白,因此可以降低过敏和抗体形成的风险。Xeomin无需冷藏,常温就可以保存,有效期为36个月,赋性剂是人血白蛋白,用真空干燥法进行干燥。目前希尔敏在全球超过20个国家上市。

4.1.2 Abobotulinumtoxin A,Dysport,IpsenBiopharm, Ltd.(UK)

4.1.3 Incobotulinumtoxin A,Xeomin,Merz Pharma Gmbh& Co.(Germany)

4.1.4 RimabotulinumtoxinB,Myobloc, WorldMeds(US)
RimabotulinumtoxinB由 美 国SolsticeNeurosciences公司生产(该公司已被WorldMeds公司收购),于2000年首次通过FDA批准上市,商品名为麦保克(中国)、Myobloc(美国)、NeuroBloc(日本)。麦保克是以液态形式保存的,注射前无须配置,性状较稳定。常温下可以保存约9个月,2-8度冷藏保存36个月。它的规格有2500U5000U、10000U三种,分子量约为700KD,产品特点是起效更快,维持时间较A型肉毒毒素短,副作用发生率较A型肉毒毒素高,注射疼痛感较A型肉毒毒素强烈[4]。
4.1.5 Neuronox、Innotox、Coretox,Medytox Solutions, Inc. (KR)

Neuronox于2006年在韩国首先获批通过,至今以Botulift、Siax、Cunox、Medytoxin等商品名在印度、香港、泰国、哥伦比亚、菲律宾等全球27个国家获批,目前市场份额全球第四。纽诺适的配方与保妥适相近,分子量为单一的900KD,赋形剂为人血白蛋白。不同的是,纽诺适用冻干法进行干燥,在2-8度冷藏的保质期为24个月,其规格有50U、100U、150U、200U四种。
2013年12月11日,Medytox公司在韩国推出了新一代肉毒毒素Innotox,它的规格是液态25U[5]、50U(50U是2015年5月26日获KFDA批准上市[6])两种,获得的是中重度20-65岁成人皱眉纹的适应症。2014年Medytox将Innotox的海外经销权出售给Allergan,目前Innotox正在进行皱眉纹适应症的临床实验[7]。
2015年8月Medytox投资了556亿韩元宣布开始研发Incobotulinumtoxin A(Xeomin)的仿制肉毒毒素Coretox,宣布以“Innotox+Coretox”的扩大肉毒毒素产业为策略,预计2019年Coretox在韩国上市。
4.1.6 Botulax,Hugel Pharma (KR)
Botulax的产地是韩国,由Hugel Pharma出品,于2009年在日本获批,2010年在韩国获批,此后逐渐出口泰国,哥伦比亚,智利等国家。Botulax的分子量为单一的900KD,赋形剂为人血白蛋白,保质期是36个月,其规格有25U、50U、100U、200U四种,商品名有Regenox,Zentox,Reage、Juvenlife等。目前在韩国排名第二,Hugel公司与CROMA-PHARMA签订了长达10年的战略合作协议,将Botulax推向欧洲市场[8]。
4.1.7 Nabota,DaewoongPharma Philippines, Inc.(KR)
Nabota (DWP450)的产地是韩国[9],由韩国本土著名的大熊制药DaewoongPharma Philippines, Inc.出品,Nabota的分子量为单一的900KD,赋形剂为人血白蛋白,保质期是36个月[10]。2013年12月,大雄与Pharmavital签订了价值约十亿韩元的销售合同,计划2014-2016年在拉丁美洲的15个国家(除阿根廷之外)销售A型肉毒毒素,包括墨西哥,哥伦比亚,委内瑞拉和巴西等[11]。
2014年4月大熊制药公司宣布将扩大Nabota的海外市场,目标是进军90个海外国家,此后Nabota依次在泰国、巴拿马上市,并且在玻利维亚、危地马拉开始了临床实验。其中最重要的是,2014年9月11日 FDA接受了美国进口商Evolus的新药Evosyal (EV001)进行临床试验(Nabota在美国的商品名为EVOSYAL)的申请,2015年1月22日ALPHAEON公司宣布FDA批准了EVOSYAL™治疗眉间纹的III期临床研究(ALPHAEON收购了美国EVOSYAL的独家经销权)[12],2015年12月30日 Evolus完成了EV-002(NCT02334436)与EV-001(NCT02334423)在眉间纹的III期临床研究试验,以及更新了眉间纹(NCT02184988)的II期临床试验[13]。EVOSYAL™计划于2017年在美国上市,这将会是第一个在美国上市的亚洲品牌的肉毒毒素。
Nabota的规格是50U(2015年1月8日获批, 代 码 8806416059302)、100U( 2013年11月29日获批,代码8806416056301)。2015年6月,Nabota完成了中风后上肢肌痉挛适应症的III期临床试验,推出了200U规格(代码 8806416061008)[14]。
4.1.8 BTX-A、Hengli,LanzhouInstitute(China)
BTX-A产地为中国,由兰州生物制品研究所有限责任公司生产,商品名有衡力、Lantox、Lanzox、Prosigne、Redux、Liftox,于1993年在中国首次获批通过,目前衡力在韩国等20多个国家均有销售。其分子量为300-900KD不等,赋形剂是猪明胶,通过冻干法进行干燥,保质期为36个月,规格是50U、100U,需要在2-8度冷藏。
4.1.9 Relatoks,Microgen NPO(RU)
Relatoks是俄罗斯非政府组织Microgen公司生产制造的注射用A型肉毒毒素,于2013年通过俄罗斯卫生部的认证(批号LP-001 593 19.03.2012),2014年初获批上市[15]。目前规格有50U、100U,使用冻干法进行干燥,在2-8度冷藏的条件下,保质期为36个月,赋形剂是明胶与蔗糖[16]。
4.1.10 BOTOGenie™,Bio-Med Pvt. Ltd.(India)
BOTOGenie是印度Bio Med公司在本地生产的A型肉毒毒素,于2007年1月在印度问世。目前规格有50U、100U,使用冻干法进行干燥,在2-8度冷藏的条件下,保质期为24个月,赋形剂是乳糖[17]。

4.1.11 PurTox,Johnson& Johnson (US)
PurTox是150K的纯A型肉毒毒素神经毒素分子, 由Mentor公 司 (Mentor Worldwide LLC, Santa Barbara, California)进行研发,它已经完成了FDA批准的III期临床试验。PurTox类似于Xeomin(不含络合蛋白),并旨在提高眉间皱纹和前额皱纹的外观。然而,在Mentor被强生公司用1.1亿美元收购之后,2014年4月PurTox被宣布停止临床实验[18]。
4.1.12 Masport®, Masoondarou Biopharmaceutical Co.(Iran)
Masport是 MASOONDAROU公 司 生 产,2015年由伊朗卫生部(MOH)和食品与药物组织(FDO)的认证的A型肉毒毒素(产品代码2112149267750001[19]),维持时间在4到6个月,每瓶500U,使用冻干法进行干燥,在2-8度冷藏的条件下,赋形剂是人血白蛋白和乳糖。在伊朗适应症包括:皱眉纹、额纹、鱼尾纹、吸烟者纹和原发性腋窝多汗症5项。
4.1.13 BTXA,IntasBiopharmaceuticals(India)
BTXA是印度IntasBiopharmaceuticals公司生产,规格为100U,在印度适应症为眼睑痉挛[20]。
各个品牌的肉毒毒素差异详见表5。
4.2 正在开发的肉毒毒素产品
4.2.1 RT001、RT002(Daxibotulinum toxin A),Revance Therapeutics,Inc(US)
RT001(Daxibotulinum toxin A Topical Gel)是外抹型肉毒毒素凝胶,它是目前局部应用的肉毒毒素替代品中临床前景较好的,由美国Revance公司进行研发。RT001是150 KD的纯神经毒素,它通过离子键与以细胞穿透肽CPP为基础的肽配对来形成经皮渗透(见图3)[21]。目前RT001正在进行中重度鱼尾纹III期临床实验,并且自2015年9月开始了对局部多汗症的II期临床实验。RT001在中重度鱼尾纹的志愿者治疗30分钟后即出现了明显的疗效,目前在新加坡也开始了RT001用于偏头痛和其他慢性头痛的研究。

RT002(Daxibotulinum toxin Afor Injection )是Revance公司的另外一个正在研发的产品,RT002是A型肉毒毒素的一种新型的注射剂型,其研究设计比现有的肉毒毒素更精准持久。目前RT002已经开始了眉间纹、宫颈肌张力障碍的II期临床实验,见表2[22]。
4.2.2 ANT-1207、AI-09,Allergan, Inc(US)
ANT-1207是美国Anterios正在研发的局部外用乳液型肉毒毒素,用高度纯化的肉毒杆菌发酵而成,通过按摩皮肤的方式吸收,目前处于腋窝多汗症,面部痤疮,和外眦线(鱼尾纹皱纹)的II期临床实验(见表3)。Anterios公司是一家拥有NDS技术(通过外抹的方式,向皮肤靶向递送肉毒毒素和其它大分子,而不是通过注射其或其他侵入性治疗的技术)的生物制药公司。 NDS技术当然也可以使大分子作为现成使用液体注射产品的配方。2016年1月7日,Allergan公司宣布成功收购Anterios公司[23]。
AI-09是该公司正在研发的A型肉毒毒素的一种新颖的可注射制剂,注射用的AI-09与局部外用的肉毒候选产品ANT-1207一起使用,将为肉毒毒素不方便精准注射的部位提供新的治疗选择方案。同样AI-09采用了NDS技术,即不需要干燥也不需要赋形剂人血白蛋白,并且将直接预存在注射器中,更方便了医生的使用。AI-09是目前处于皱眉纹的临床前研究阶段。
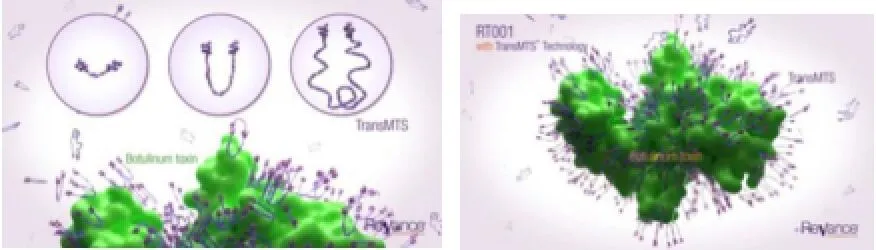
图3 RT001的作用机制
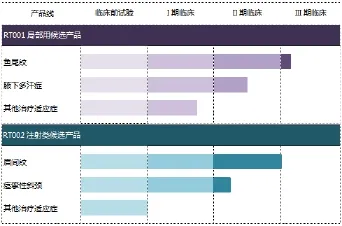
表2 RT001/RT002临床试验进展
5.全球肉毒毒素市场发展趋势
5.1 国外肉毒毒素市场发展趋势
国际美容整形外科学会(ISAPS)2015年报告的预测,全球肉毒毒素市场将从2013年的1.3亿美元增长到2020年的2.7亿美元[24]。2015年全球肉毒毒素市场美国艾尔建公司的保妥适(Botox)仍占有73.8%的份额,据第一位(见图4)。英国Ipsen公司生产的Dysport,德国Merz公司生产的Xeomin,韩国Medytox公司生产的Neuronox和中国兰州生物制品研究所有限责任公司生产的BTX-A分别占有15%,7%,2%和1.5%的市场份额。随着越来越多的不同品牌的肉毒毒素上市保妥适的市场份额一直在下降,但驱动保妥适增长的原因主要还是来自于不断获批的临床应用新适应症,尤其是保妥适在治疗领域的不断扩大应用(见图5)。疾病的治疗是硬性需求,肉毒毒素在治疗领域的适应症数量远远超过了美容领域(见图6、图7)。1989-2016年FDA批准在美国上市的肉毒毒素品牌及适应症见表4。2009-2015年美国艾尔建公司(Allergan)和英国艾普森公司(Ipsen)肉毒毒素销售状况见图8。
5.2 国内肉毒毒素市场发展趋势
目前我国CFDA批准的肉毒毒素只有两个。一个是美国艾尔建公司的保妥适(Botox),另一个是中国兰州生物制品研究所有限责任公司生产的衡力(BTX-A)。IMS统计数据显示:2015年国内的肉毒毒素的销量已经达到了1.13亿人民币,其中保妥适、衡力分别为5943.21万人民币及5376.47万人民币,分别占52.50%及47.50%(见图9)。2015年保妥适和衡力在我国销售的情况见图10。

表3 ANT-1207/AT-09临床试验进展

图4 2015年全球肉毒毒素市场份额[25]
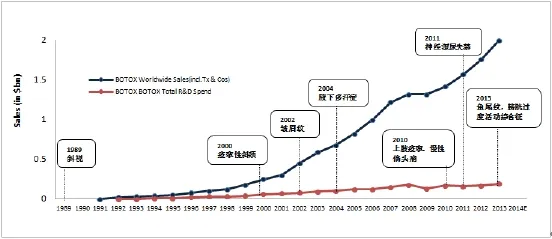
图5 保妥适(Botox)临床应用开发及适应症与销量关系一览[26]

图6 2018-2028全球保妥适治疗美容市场预测(单位:百万美元)
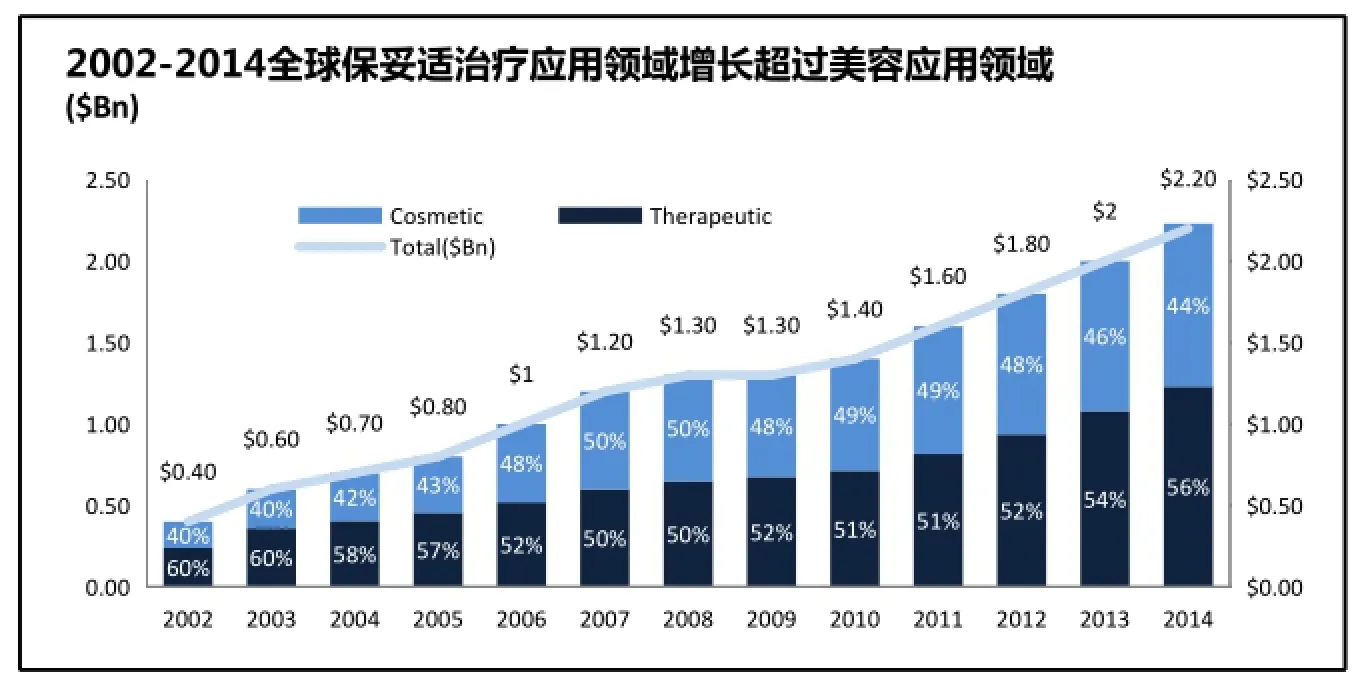
图7 2002-2014全球BOTOX治疗领域增长速度超越美容领域(单位:10亿美金)

图8 2009-2015年美国艾尔建公司和英国艾普森公司肉毒毒素销售状况[22,23]
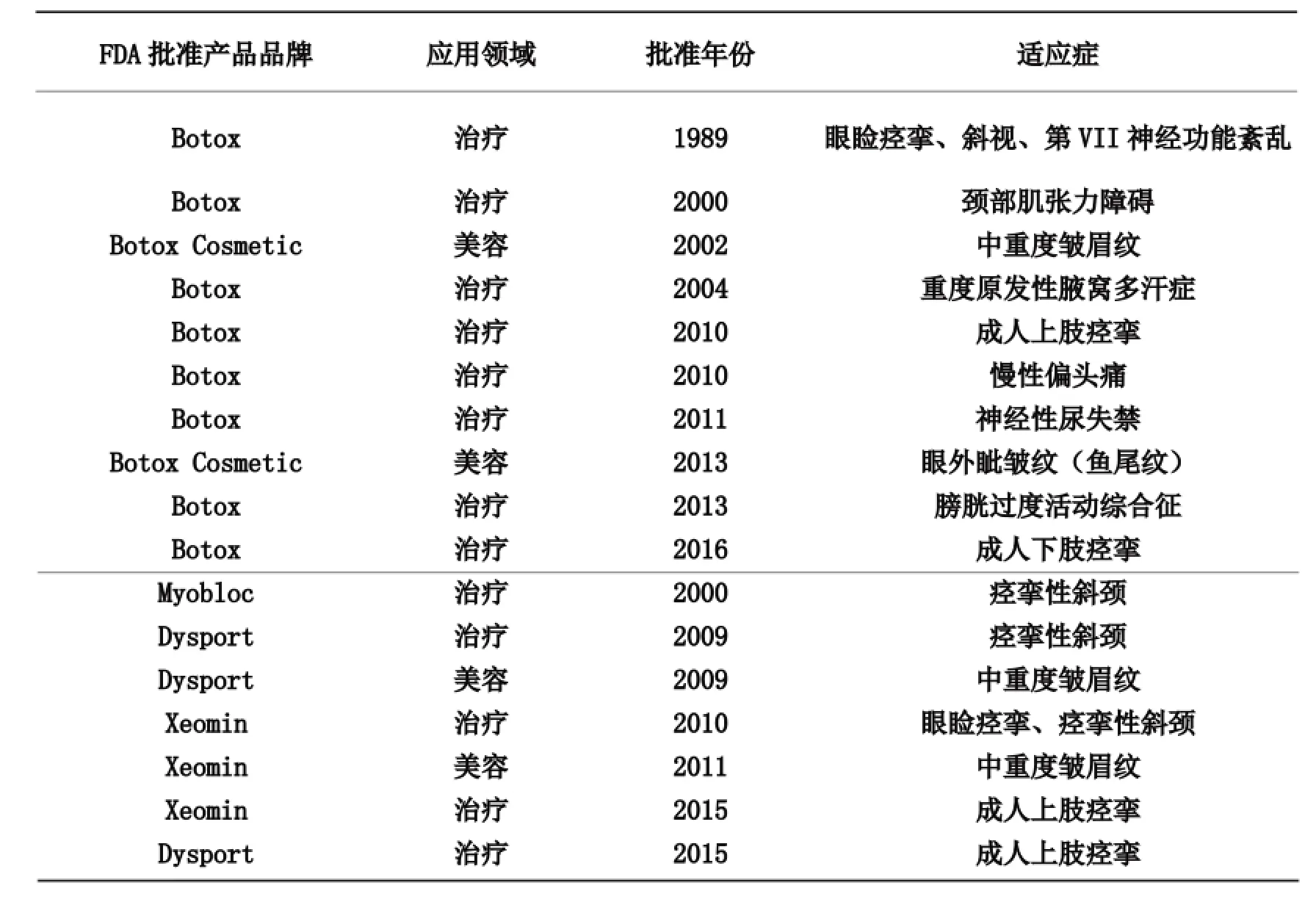
表4 1989-2016年FDA批准在美国上市的肉毒毒素品牌及适应症
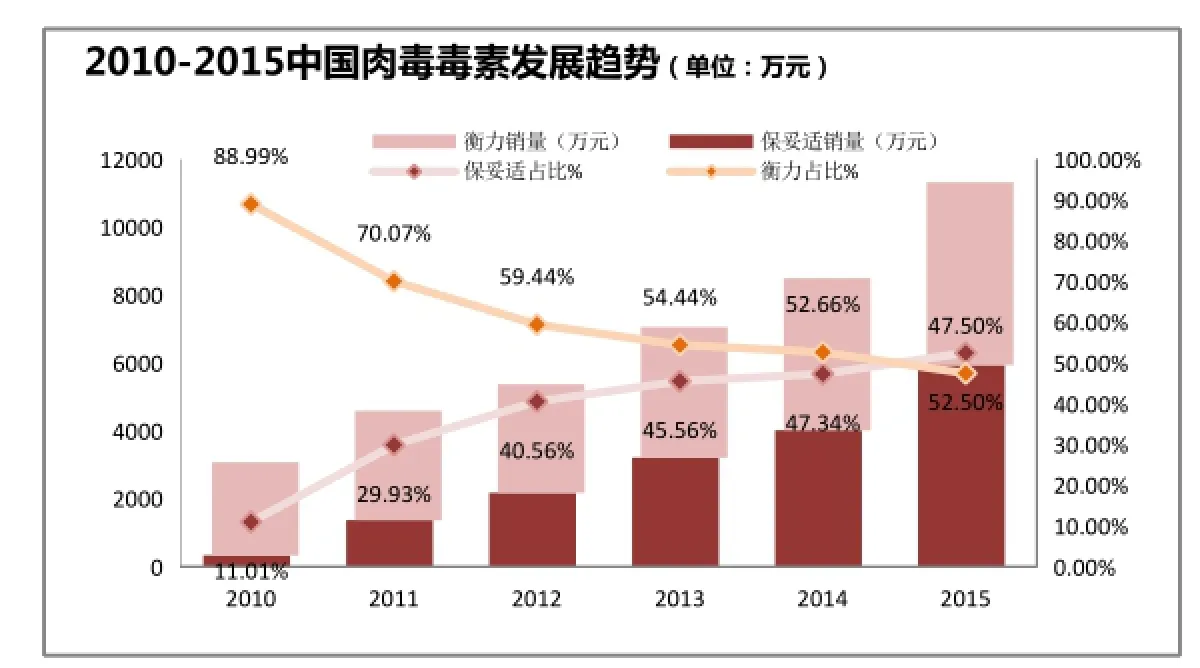
图9 2010-2015年中国肉毒毒素发展趋势
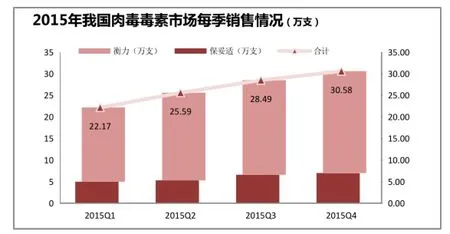
图10 2015年我国肉毒毒素市场每季销售情况
6.肉毒毒素的未来
肉毒毒素注射不论是在治疗功能、治疗效果及治疗成本方面都显示出其巨大的发展潜力及优势,唤发着人们对美的现实渴求及美容消费冲动,这种合力推动了市场需求的不断扩大,而数据告诉了我们过去却预示着未来市场的需求趋势。
6.1 新适应症审批
肉毒毒素治疗的临床应用不断发掘和新适应症审批,新的肉毒毒素制剂不断开发,趋于更有效,更安全微创,更便利和更经济。(见表6表7)
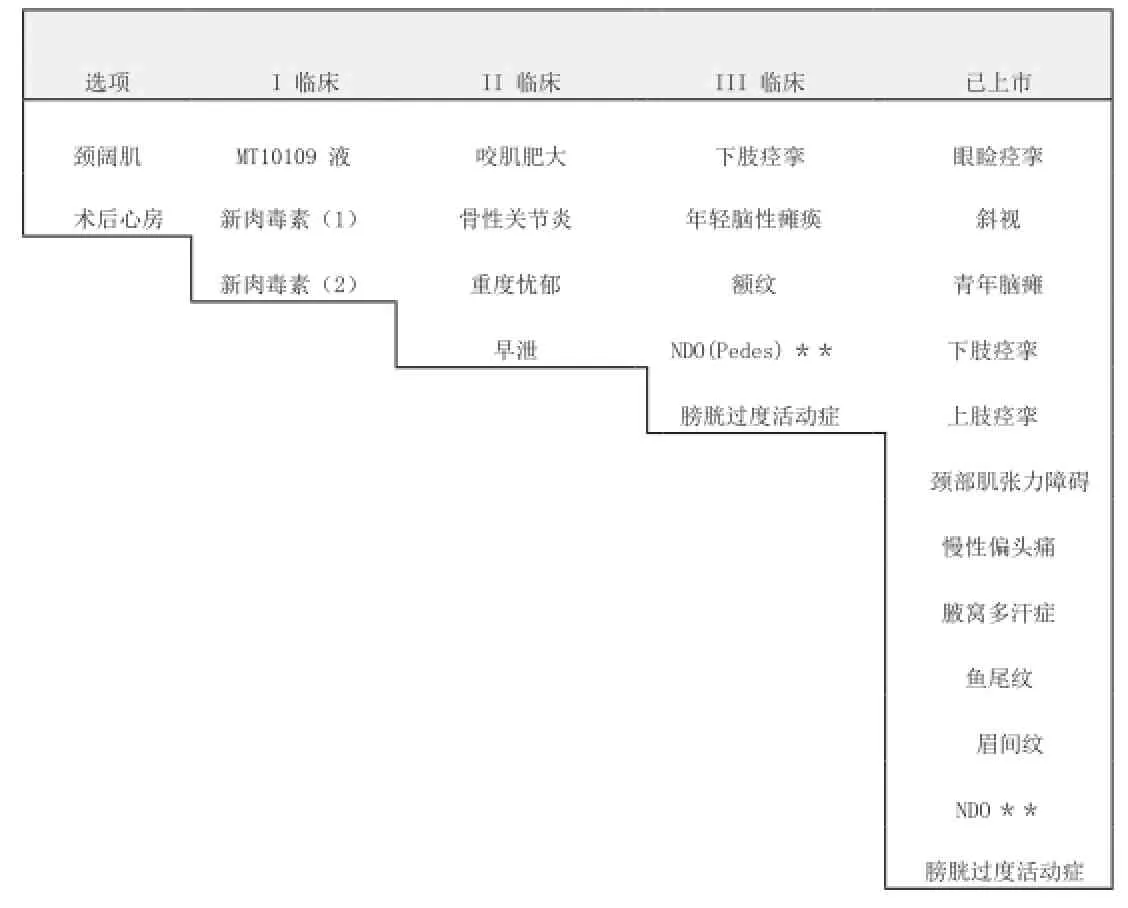
表6 BOTOX未来适应症上市计划[26]
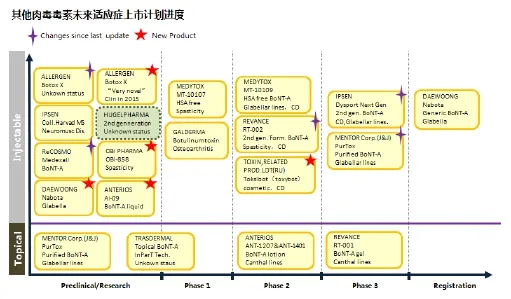
表7 :其他肉毒毒素未来适应症上市计划[26]
6.2 肉毒毒素注射与精准医疗
由于注射肉毒毒素后的不良反应包括面神经分支麻痹、咀嚼无力、口腔干燥、偶发头痛等。这些症状可能是药物弥散出肌肉组织至相应部位所导致,并随着药物的代谢逐渐缓解。在注射过程中,医生要充分了解肌肉及周围组织的解剖结构,准确把握注入药物的部位和剂量;避免药物过度稀释、注射溶液过多而导致非预期的弥散作用,因此精准医疗是肉毒毒素未来注射技术得以提高的有利武器。
首先是疾病诊断的精准,相关疾病的基因检测。确定肌张力异常的特定肌肉是肉毒毒素注射治疗的前提。其次是临床评估的精准,3D影像学评估系统补充或代替不同的量表系统,更形象,更易测量和记录,更具临床指导意义,可自动报告导致功能异常的靶肌肉,易于随访和教学。此外肉毒毒素靶组织的精准定位,在传统目测和手摸基础上采用影像和电生理定位。不同的病种,不同人种,不同肉毒毒素制剂合适的剂量有助于大数据分析。
6.3 互联网+肉毒毒素治疗与大数据分析
建立肉毒毒素治疗信息数据库移动化,搭建医患沟通和科研合作的大数据平台,丰富肉毒毒素患者管理以及科研课题合作的大数据来源。目前国内第一款肉毒毒素App(BTXA)已经上线(见图11),智能客户端的使用为医生的临床工作提供了便捷可靠的工具,通过App可以实现如下功能:为医生建立影像资料的数据库,方便医生对患者进行远程随访,实现在线肉毒毒素网络大讲堂等教育模块,指导初级注射医生学习,指导肉毒毒素注射后的患者护理,以及方便资深注射医生间进行学术交流。最后,App为患者提供了寻医问药的平台,让患者在远程可以得到专业人员的指导,患者间相互交流。
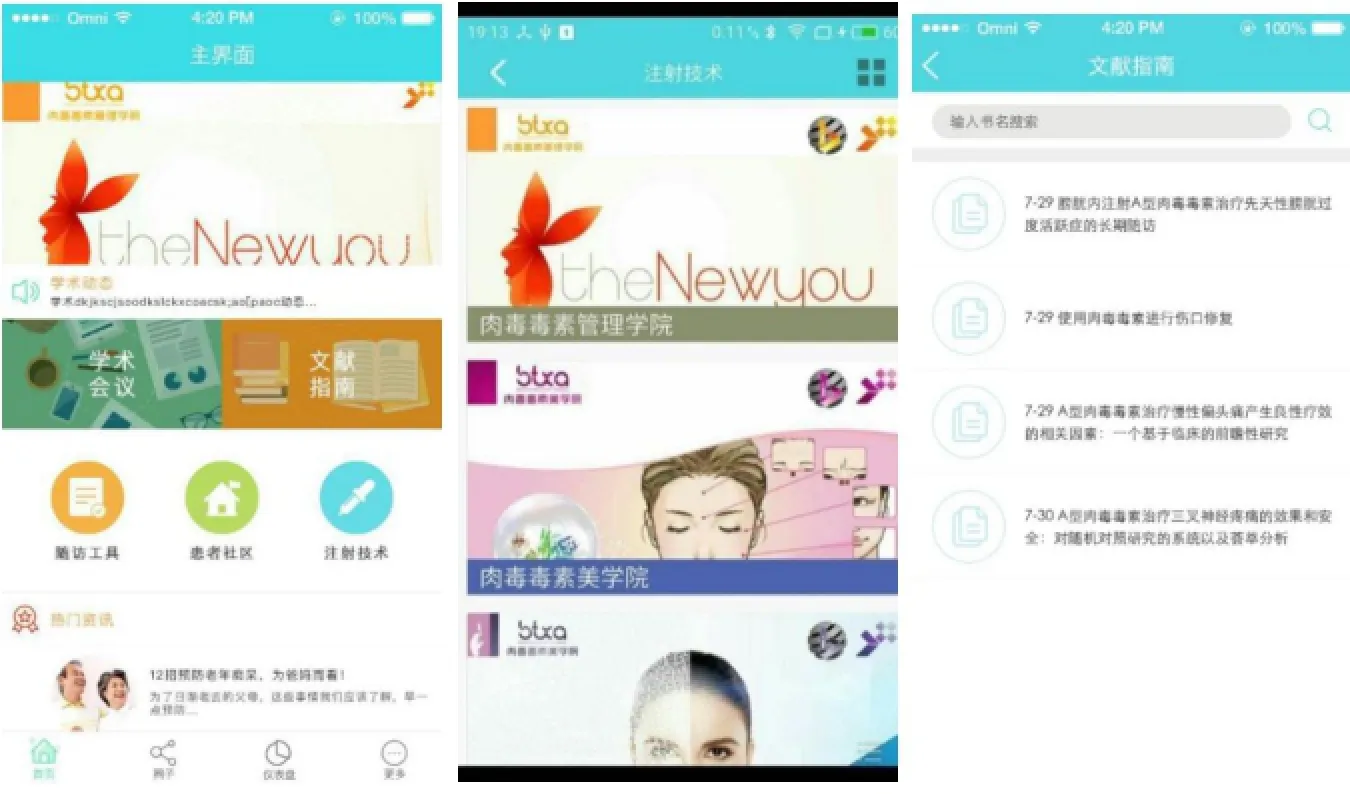
图11 BTXA的界面

表5 全球肉毒毒素品牌对比
参 考 文 献
[1].http://www.prnewswire.com/news-releases/us-fdaapproves-botox-onabotulinumtoxina-for-the-treatmentof-lower-limb-spasticity-in-adults-300208358.html
[2]MedytoxAnnual Report 21 Jan 2016,Ipsen Annual Report 2015,Merz Annual Report 2015
[3]http://www.merzusa.com/wp-content/uploads/Merz-North-America-Announces-Xeomin-Adult-ULS-FDA-Approval-FINAL_v2.pdf
[4]Botulinum toxin for glabellar lines: a review of the efficacy and safety of currently available products. Am J ClinDermatol 2011; 12:377–388. 8.
[5]Hyun-Mi Oh 1, Joo Hyun Park 1, DaeHeon Song 2,and MyungEun Chung 2 ,Efficacy and Safety of a New Botulinum Toxin Type AFree of Complexing Proteins,Toxins 2016, 8, 4; doi:10.3390/toxins8010004
[6]http://www.medy-tox.co.kr/k_new/html/infor_4_01_view.ph p?data=aWR4PTQxNjEmcGFnZWNudD0wJmxldHRlcl9ubz05OSZvZm ZzZXQ9MTAmc2VhcmNoPSZzZWFyY2hzdHJpbmc9JnByZXNlbnRfbnV tPTk0||&boardIndex=3&tn=1&sn=1
[7]http://www.g-enews.com/ko-kr/view. php?ud=201512232128438073044_1
[8] http://www.croma.at/en/news-2/?id=133
[9]http://www.g-enews.com/ko-kr/view. php?ud=201512232128438073044_1
[10]https://www.daewoong.co.kr/daewoongkr/product/product_goods_view.web?srno=481&sCate=3#none;
[11]http://adisinsight.springer.com/downloads/ mediarelease/1832/809158496.html
[12]http://www.prnewswire.com/news-releases/alphaeonbegins-phase-iii-study-for-its-neurotoxinevosyal-300024220.html
[13]www.hysec.com/f/tsnr/[D2016]/2016.../RR_3003309051.pdf
[14]http://www.drugd.co.kr/
[15]http://relatoxfh.ru/press.php?id=1
[16]http://relatoxfh.ru/relatox.php
[17]Http://www.biomedindia.in/botogenie-vaccine.htm
[18]http://www.reuters.com/article/us-johnsonandjohnsonwrinkles-idUSBREA3A1YC20140411
[19]Https://translate.googleusercontent.com/translate_ c?depth=1&hl=zh-CN&prev=search&rurl=translate. google.co.jp&sl=fa&u=http://irancode.ir/Search/ ProductECatalogue%3FID_NationalCode%3D5352108&usg=ALk JrhiUgm6i5JGTesKxrYCiVd23Yirung
[20]http://www.intaspharma.com/index.php?option=com_djcata log2&view=item&id=159:btxa&cid=1:pharma&Itemid=76
[21]www.revance.com
[22]http://www.revance.com/product-pipeline/
[23] http://anteriosinc.com/products/
[24]GBI Research, KDB Daewoo Securities Research
[25] GBI Research, KDB Daewoo Securities Research
[26]Allergan R&D Open-Day Presentation November 2015
[27]Walker TJ, Dayan SH. Comparison and overview of currently available neurotoxins. J ClinAesthetDermatol. 2014;7:31–39.
Since FDA’s first approved of Botox in the treatment of strabismus in 1989, botulinum toxin is registered in more than 88 countries worldwide, with a number of 29 indications. For the past 20 years , its stable therapeutic effect and safety has gradually been widely recognized, from treating blepharospasm , hemifacial spasm , spasmodic torticollis , strabismustothe medical aestheticarea. There are more than 10 brands of botulinum toxin currently, this paper tends to analyztheglobal botulinum toxin market trends and its impact on China.
Botulinum Toxin, Marketing Share,Indication,FDA,KFDA,CFDA,CMA
— 多适应症药物准入评估方法比较研究

