60℃加热1小时灭活病毒方法对常规临床检测指标的影响研究
李晓东,廖 昊,刘 妍,李 乐,陈容娟,李 奇,陈 丽,黄鹏宇,王学晶,徐东平
60℃加热1小时灭活病毒方法对常规临床检测指标的影响研究
李晓东,廖昊,刘妍,李乐,陈容娟,李奇,陈丽,黄鹏宇,王学晶,徐东平
[摘要]目的 基于60 ℃加热1 h可有效灭活埃博拉病毒的观点,探讨用该条件加热处理对常规临床检测指标的影响。方法 对40例受检者用枸橼酸钠抗凝管和EDTA-K2抗凝管分别采集静脉血,标本分为2份,检测未进行加热灭活处理(灭活前)和进行了加热灭活处理(灭活后)样本的生物化学、免疫、凝血和血常规指标,比较热灭活前后各指标的差异。结果 与灭活前相比,灭活后样本的生物化学和免疫项目中总蛋白、总胆红素、肌酐、总胆固醇、甘油三酯、钠、钾、氯、C-反应蛋白、尿素氮、葡萄糖、HBsAb水平差异无统计学意义(P均>0.05);白蛋白、球蛋白、前白蛋白、丙氨酸氨基转移酶、天冬氨酸氨基转移酶和乳酸脱氢酶有较显著降低,但下降幅度不到80%且灭活前、后数据存在相关性(r>0.80,P<0.01),用回归方程校正后检测数据仍具有参考价值;碱性磷酸酶、γ-谷氨酰基转移酶、胆碱酯酶和肌酸激酶的测定值下降非常明显(P均<0.01),且灭活前后2组数据无显著相关性。凝血检测项目中,D-二聚体在2组间的差异无统计学意义(P>0.05);其余项目均受到热灭活严重影响。血常规项目中,血红蛋白、白细胞和血小板计数在2组间的差异无统计学意义(P>0.05),但样本须要事先稀释。结论 60 ℃加热1 h灭活处理对部分生物化学、免疫和血常规项目无明显影响,部分项目检测值明显降低,但其中有6项指标经校正后仍具参考价值。
[关键词]埃博拉病毒属;临床试验;检疫
埃博拉病毒主要通过接触患者或感染动物的血液、体液、分泌物和排泄物等而引起感染,临床表现主要为突起发热、出血和多脏器损害[1]。埃博拉病毒对化学药品敏感,乙醚、去氧胆酸钠、β-丙内酯、福尔马林、次氯酸钠等消毒剂可以完全灭活病毒;钴60照射、γ射线也可使之灭活。该病毒在常温下较稳定,在4 ℃存放1个月,感染性无明显变化,但对加热比较敏感,我国《埃博拉出血热防控方案》中明确60 ℃加热1 h或100℃加热5 min即可灭活[2]。
埃博拉病毒的传染性强,接触患者和患者样本须要高度防护[3]。对患者样本检测须在移动生物安全防护三级(P3)实验室中进行,但受限于空间狭小,不适宜在内开展临床常规实验指标的检测。由于无临床实验室检测指标,使患者的治疗以及相关科研工作受到极大影响。如果对患者血液标本在P3实验室中进行简单地离心和加热灭活处理,再对灭活后的血液或血清标本在常规实验室进行相关临床实验指标的检测,既可解决P3实验室条件限制,又可消除实验室工作人员在检测中的感染风险。本研究通过对样品加热60 ℃ 1 h以模拟灭活埃博拉病毒的条件,分析灭活前和灭活后临床实验指标的差异,为今后在没有P3实验室条件下通过热灭活病毒开展临床实验检测提供参考。
1 对象与方法
1.1 对象 共40例受检对象,其中20例为解放军第三○二医院收治的慢性HBV感染者,20例为健康志愿者。
1.2 仪器 生物化学项目由日立生物化学分析仪
(日本)完成检测,免疫项目由罗氏化学发光免疫分析仪(日本)完成检测,血凝项目由希斯美康血凝分析仪(日本)完成检测,血红蛋白由希斯美康血细胞分析仪(日本)完成检测,血小板和白细胞由2人分别计数各3次,取平均值。加热灭活采用恒温水浴箱(中国上海)中60 ℃放置1 h。
1.3 血液样品处理方法 对每例受试对象分别用枸橼酸钠抗凝管和EDTA-K2抗凝管抽取2管外周静脉血。其中枸橼酸钠抗凝管血液样品进行离心后,将血浆平均分成2份,取其中1份样本进行加热处理,随后对2份样本同时进行生物化学项目、免疫项目和血凝项目检测。将EDTA-K2抗凝管样品平均分为3组共6份:其中2份用0.9%氯化钠稀释5倍以防止加热过程中血液凝固,取其中1份样本进行加热处理,随后对2份样本同时进行血红蛋白检测;另外2份用1%草酸铵稀释20倍破坏血液中的红细胞和白细胞,取其中1份样本进行加热处理,随后对2份样本同时进行血小板计数;另外2份用3%冰醋酸稀释20倍溶解血液中的红细胞,取其中1份样本进行加热处理,随后对2份样本同时进行白细胞计数。
1.4 结果评价 对灭活前和灭活后的样本检测数值进行比较,差异无统计学意义,表明加热处理对该检测指标无显著影响。加热后检测值变化幅度<5倍,且统计分析热灭活前、后两组的检测值有显著相关性时,建立回归方程校正检测结果。加热后检测值变化幅度5倍以上时,提示该指标不适于加热后检测。
1.5 统计学处理 采用SPSS 16 .0软件进行统计分析。计量资料呈符合正态分布,用±s表示,各指标热灭活前后水平差异比较用自身配对t检验。对部分指标热灭活前后水平进行直线回归分析。检验水准a=0.05。
2 结 果
2.1 生物化学和免疫检测项目 灭活前组与灭活后组相比,总蛋白、总胆红素、肌酐、总胆固醇、甘油三酯、钠、钾、氯、C-反应蛋白、尿素氮、葡萄糖和HBsAb水平差异无统计学意义(P均>0.05);白蛋白、球蛋白、前白蛋白、丙氨酸氨基转移酶、天冬氨酸氨基转移酶和乳酸脱氢酶水平差异有统计学意义(P均<0.01),但2组数据存在相关性(r>0.80,P<0.01);碱性磷酸酶、γ-谷氨酰基转移酶、胆碱酯酶和肌酸激酶的差异有统计学意义(P均<0.01),2组数据无相关性(P>0.05)。见表1。
2.2 血常规和凝血检测项目 灭活前组与灭活后组相比,血常规项目血红蛋白、白细胞和血小板计数差异无统计学意义(P均>0.05);凝血检测项目D-二聚体差异无统计学意义(P>0.05),其余项目如凝血酶原活动度、凝血酶原时间、纤维蛋白原等均受到热灭活严重影响,无法得到具体数值。见表2。
2.3 检测项目结果校正 为了对热灭活后检测数值下降5倍以内的项目进行校正,即用灭活后的检测值反推灭活前的检测值(真实值),对灭活前后的指标数值进行直线相关和回归分析,得到的回归方程和相关系数,如表3和图1所示。
3 讨 论
2014年3月非洲暴发的埃博拉疫情严重威胁世界公共卫生安全[4]。埃博拉病毒易于在人群中传播,感染后病死率较高,国家卫生和计划生育委员会将其归属于第一类、四级生物危害等级的病原微生物[5]。培养埃博拉病毒必须在生物安全四级实验室,常规实验室检测须在P3实验室内进行[6]。目前我国和非洲均缺乏P3实验室,而且很多临床检测项目在P3实验室中无法进行。对埃博拉病毒感染患者治疗须要监测肝、肾、心功能等生物化学和免疫指标。如果不作任何处理即对血液进行相关临床项目检测,极易因职业暴露增加医护工作者感染风险[7]。在检测之前先进行病毒灭活处理,可消除检测人员的职业暴露危险。
埃博拉出血热防控方案明确了60 ℃加热1 h可彻底灭活埃博拉病毒[2]。在本研究中我们对血液样本进行了同样的处理,发现灭活处理对总蛋白、总胆红素、总胆固醇、甘油三酯、钠、钾、氯、C-反应蛋白、肌酐、尿素氮、葡萄糖、 HBsAb、血红蛋白、白细胞、血小板计数和D-二聚体这些指标无显著影响,此前国外的研究结果也得到了类似的结论[8-10]。白蛋白、球蛋白、前白蛋白、丙氨酸氨基转移酶、天冬氨酸氨基转移酶和乳酸脱氢酶等指标热灭活前后数值差异有统计学意义,可以通过线性回归方程校正灭活后的结果,使其仍具有临床参考价值。碱性磷酸酶、 γ-谷氨酰基转移酶、胆碱酯酶、肌酸激酶等指标受加热灭活的影响显著,无法通过校正得到有意义的检测结果。此外,热灭活后凝血功能相关的蛋白活性明显下降,无具体的检测结果,不建议热灭活后检测。因此本研究结果提示,对于热灭活后数值降低在5倍以内的指标,可以通过标准品进行校正。即已知浓度的标准品与检测样品采取相同的处理措施,然后用标准品的检测值建立回归方程,将待测样品灭活后的检测值代入方程即可得到灭活前的校正检测数值。

表1 生物化学和免疫检测项目热灭活前后结果Table 1 Biochemical and immunological indicators before and after heating inactivation

表2 白细胞、血小板和血红蛋白热灭活前后检测结果Table 2 WBC, PLT and HGB levels before and after heat inactivation

表3 热灭活后部分检测项目结果的校正方程Table 3 Regression equation of some laboratory indicators after heating inactivation
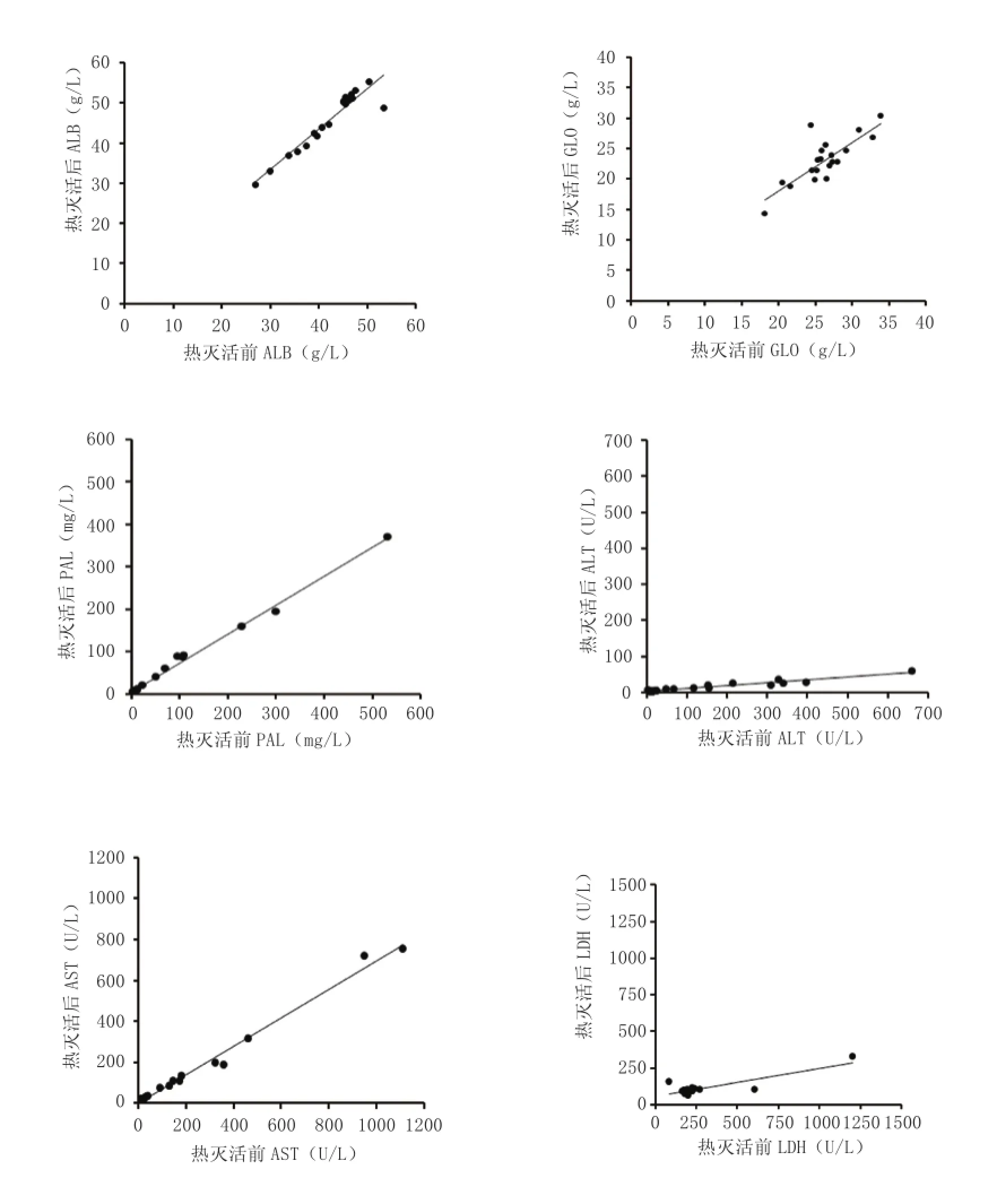
图1 部分检测指标热灭活前后水平散点图注:ALB.白蛋白; GLO.球蛋白; PAL.前白蛋白; ALT.丙氨酸氨基转移酶; AST.天冬氨酸氨基转移酶; LDH.乳酸脱氢酶Figure 1 Scatter plot of some laboratory indicators before and after heating inactivation
本研究涵盖了大多数常规实验室检测项目,一般情况须要应用3种采集管:真空干燥管用于生物化学及免疫项目的检测,枸橼酸钠抗凝管用于凝血项目的检测,EDTA-K2抗凝管用于血常规的检测。本研究直接应用血浆进行生物化学项目检测,减少了对受试者血液采集量,简化了操作步骤,可提高P3实验室的检测效率。
本研究的结果显示加热灭活处理对大部分生物化学和免疫项目并无影响或影响较小,部分检测项目可通过校正消除影响。60 ℃1 h加热灭活埃博拉病毒不需昂贵的仪器设备,简单易行,对多数临床检测项目结果不会造成影响,且部分可以校正,可考虑作为一种临床实验室工作人员防止医源性感染切实可行的标本处理方法。
【参考文献】
[1] World Health Organization. Ebola virus diseases[EB/OL]. [2015-08-16]. http://www. who.int/mediacentre/factsheets/ fs103/zh/.
[2] 中华人民共和国国家卫生和计划生育委员会.埃博拉出血热防控方案(第2版)[J]. 全科医学临床与教育, 2014(5): 483-486.
[3] World Health Organization. Hand hygiene in health care in the context of Filovirus disease outbreak response[EB/OL]. [2015-08-16]. http://www.who.int/csr/resources/publications/ ebola/ hand-hygiene/en/.
[4] 张云辉, 王姝, 陈玉琪, 等. 埃博拉出血热研究现状及2014年疫情进展[J]. 传染病信息, 2014, 27(4):3-8.
[5] 中华人民共和国国家卫生和计划生育委员会.卫生部关于印发《人间传染的病原微生物名录》的通知[EB/OL]. [2015-08-16]. http://www.nhfpc.gov.cn/zhuzhan/wsbmgz/201304/ 64601962954745c1929e814462d0746c.shtml.
[6] 郑江花, 胡绿荫, 李海聪, 等. 埃博拉病毒感染性标本在生物安全三级实验室的临床检验与生物安全防护[J]. 传染病信息,2014, 27(5):257-259.
[7] Kreuels B, Wichmann D, Emmerich P, et al. A case of severe Ebola virus infection complicated by gram-negative septicemia[J]. N Engl J Med, 2014, 371(25):2394-2401.
[8] Chong YK, Ng WY, Chen SP, et al. Effects of a plasma heating procedure for inactivating Ebola virus on common chemical pathology tests[J]. Hong Kong Med J, 2015, 21(3):201-207.
[9] Mitchell SW, Mccormick JB. Physicochemical inactivation of Lassa, Ebola, and Marburg viruses and effect on clinical laboratory analyses[J]. J Clin Microbiol, 1984, 20(3):486-489.
[10] Schlenke P. Pathogen inactivation technologies for cellular blood components: an update[J]. Transfus Med Hemother, 2014,41(4):309-325.
(2015-11-27 收稿 2016-01-20 修回)
(责任编委 曲 芬 本文编辑 张云辉)
[文献标志码][中国图书资料分类号] R512.62 A
[文章编号]1007-8134(2016)03-0160-05
DOI:10.3969/j.issn.1007-8134.2016.03.009
*Corresponding author. WANG Xue-jing, E-mail: wangxuejing@263.net; XU Dong-ping, E-mail: xudongping302@sina.com
[基金项目]北京市科委科技计划项目(D131100005313016),全军医学科技“十二五”科研项目重点课题(BWS11J048),新发突发传染病研究北京市重点实验室资助项目(2014XFTF04)
[作者单位]100039 北京,解放军第三〇二医院临床研究管理中心(李晓东、廖昊、刘妍、李乐、陈容娟、李奇、陈丽、黄鹏宇、徐东平);100123 北京,民航总医院检验科(王学晶)
[通讯作者 ]王学晶,wangxuejing@263.net; 徐东平,E-mail∶xudongping302@sina.com
Effects of sample processing by heating at 60 ℃for one hour on routine clinical laboratory indicators
LI Xiao-dong, LIAO Hao, LIU Yan, LI Le, CHEN Rong-juan, LI Qi, CHEN Li, HUANG Peng-yu, WANG Xue-jing*, XU Dong-ping*
Research Center for Clinical and Translational Medicine, 302 Military Hospital of China, Beijing 100039, China
[Abstract]Objective To evaluate the influence of the heating procedure on clinical laboratory indicators based on the understanding that heating at 60 ℃ for 1 hour is an effective assay for inactivation of Ebola virus. Methods Blood samples of 40 subjects involved in this study were collected in sodium citrate anticoagulation tubes and EDTA-K2 anticoagulation tubes respectively, and divided into two equal aliquots. One aliquot was analyzed for biochemical, immunological, coagulation and blood routine examination parameters without preheating (prior-inactivation group), and the other was analyzed for these parameters after heating at 60 ℃ for 1 hour (post-inactivation group). The differences in these parameters between prior-inactivation group and post-inactivation group were compared. Results In terms of biochemical and immunological tests, as compared with prior-inactivation group, total protein, TBIL, CRE, TC, TG, NA, K, CL, CRP, BUN, GLU and HBsAb in post-inactivation group were not significantly different (P>0.05); ALB, GLO, PAL, ALT, AST and LDH decreased significantly, but the decreased variations were less than 80% and there was a correlation between the levels of the two groups (r>0.80, P<0.01), thus the data were still interpretable after calibration with regression equation; ALP, GGT, CHE and CK had a significant decrease (P<0.01) and no correlation was observed between the two groups. In terms of coagulation tests, D-dimer showed no significant difference between the two groups (P>0.05); the other coagulation indicators were significantly different between the two groups. In terms of blood routine tests, HGB, WBC and PLT had no significant differences between the two groups (P>0.05), provided that samples were diluted beforehand. Conclusions Heat inactivation at 60 ℃ for 1 hour has no significant influence on some biochemical, immunological and blood routine tests, but significantly affects some other tests, among which 6 items are still interpretable after calibration.
[Key words]Ebolavirus; clinical trial; quarantine

