铁缺乏与左室射血分数保留性心力衰竭的关系
黄南清,郑学鸥
·论著·
铁缺乏与左室射血分数保留性心力衰竭的关系
黄南清1,郑学鸥1
目的 探讨铁缺乏与左室射血分数保留性心力衰竭(HFpEF)的相关性。方法 入选179 例HFpEF患者作为研究对象,检测患者的铁蛋白、转铁蛋白饱和度及可溶性转铁蛋白受体指数及心功能。根据血清铁蛋白或者转铁蛋白饱和度水平,将179例HFpEF患者分为铁缺乏组(n=61)和非铁缺乏组(n=118),探讨铁缺乏与HFpEF之间的相关性。结果 缺铁组与非缺铁组两组相比心脏超声检查中左心房内径(LAD)[(48.76±9.67)mm vs. (42.89±8.55)mm],二尖瓣早期血流速度/舒张晚期血流速度比值(E/A)[(1.14±0.35 vs.(0.93±0.29)],氨基末端脑钠肽前体(NT-proBNP)[(1903.14± 123.27)pg/ml vs. (1601.23±115.93)pg/ml]、6分钟步行试验(6MWT)[(351.71±74.27)m vs. (389.96 ±79.31)m]、NYHA心功能分级差异均有统计学意义(P<0.05)。铁蛋白、转铁蛋白饱和度及转铁蛋白受体指数与LAD、E/A、NT-proBNP、6MWT结果均存在相关性;铁蛋白及转铁蛋白饱和度、转铁蛋白受体指数在不同心功能分级之间有显著性差异(P<0.05) ,且随着NYHA心功能分级的增加,铁蛋白及转铁蛋白饱和度降低,转铁蛋白受体指数增加(P<0.05)。结论 铁缺乏与HFpEF存在相关性,有必要对心力衰竭患者早期进行铁缺乏的筛查。
左室射血分数保留性心力衰竭;铁缺乏;相关性
心力衰竭是各种临床心血管疾病发展至终末阶段的常见综合征之一,因其高发生率、高病死率而受到广泛关注[1]。既往临床上更多关注的是由心室收缩功能障碍引起的心力衰竭(HFrEF),而对左室射血分数保留的心力衰竭(HfpEF);左室射血分数(LVEF)在45%~50% 或50%以上所知较少,对其病理生理机制与诊疗策略均未得到一致性结论。国外研究报道HFpEF约占心力衰竭总人群的56%,已经成为心血管临床医生面临的常见难题之一[2]。HFpEF患者往往同时伴有舒张功能障碍、血管硬化及其它并发症,如常见的缺铁甚至贫血[3],其病死率与射血分数降低性心力衰竭患者相当,大大降低患者的生存质量。慢性心衰诊断和治疗指南[4]指出对于所有慢性心力衰竭(CHF)患者均建议检测、评价是否存在铁缺乏,但目前少有补铁、预防贫血等相关措施,大多仅在患者出现贫血症状时检查铁蛋白及血清铁水平,血红蛋白降低不明显的铁缺乏症早期患者大多被忽视。本研究旨在了解HFpEF患者的血清铁蛋白、转铁蛋白饱和度与心力衰竭症状、心功能NYHA分级、氨基末端脑钠肽前体(NT-proBNP)、心脏彩超指标之间的关系,为补充铁剂纠正铁缺乏提供理论依据。
1 资料与方法
1.1研究对象 入选南方医科大学附属小榄医院心内科2013年12月至2015年5月收治179例HFpEF作为研究对象,所有患者均符合《欧洲心脏协会》HFpEF的诊断标准[5]。其中男性103例,女性76例;NYHA功能分级:心功能Ⅱ级76例,心功能Ⅲ级75例,心功能Ⅳ级28例。纳入标准:①符合HFpEF的诊断标准,具有典型的有心力衰竭症状及体征;②LVEF≥50%;③近3个月内NYHA分级Ⅱ~Ⅳ;④NT-proBNP≥1500 pg/ml;⑤健康状态适合随访;⑥签署患者知情同意书。排除标准:①LVEF<50%;②血红蛋白(Hb)<60 g/L;③肺源性心脏病、大量心包积液、严重心律失常、心脏起搏器植入术后,限制性心肌病、肥厚性心肌病,严重的心脏瓣膜病和先天性心脏病患者;④严重肝肾功能不全及恶性肿瘤患者。
1.2方法 对所有患者进行临床病史、体格检查、12导联心电图、心脏超声多普勒、6分钟步行实验(6MWT)、静脉血铁代谢及NT-BNP等检测。所有患者均接受除铁剂外的常规心力衰竭药物治疗。根据血清铁蛋白或者转铁蛋白饱和度水平,将179例HFpEF患者分为铁缺乏组(n=61)和非铁缺乏组(n=118)。铁缺乏的标准定义如下[6],血清铁蛋白<100 μg/L,或者铁蛋白介于100~299 μg/L之间且转铁蛋白饱和度(TSAT)<20%。
铁代谢指标:静脉血清铁蛋白、转铁蛋白饱和度(TAST)=血清铁离子浓度(μg/dl)/[血清转铁蛋白浓度(mg/dl)×1.25]、转铁蛋白受体指数:转铁蛋白受体指数=血清转铁蛋白受体/log10血清转铁蛋白。心力衰竭检测指标:客观指标:心脏超声多普勒左心房内径(LAD)、二尖瓣早期血流速度/舒张晚期血流速度比值(E/A)、左心室舒张末期内径(LVEDD)、静脉血NT-proBN、6MWT;主观指标:NYHA心功能分级。
1.3统计学处理 采用统计学软件SPSS 21.0进行数据分析。计量资料以(±s)表示,两组间比较采用两样本独立t检验,多组间的比较采用单因素方差分析,多组间两两比较采用SNK法。等级资料采用两样本的秩和检验。两组连续变量之间的相关性采用Pearson相关分析。P<0.05认为差异有统计学意义。
2 结果
2.1缺铁与非缺铁患者的心力衰竭常规指标比较 两组患者心脏超声检查中LAD、E/A差异具有统计学意义(P<0.05)。两组间NT-proBNP、6MWT水平差异也均有统计学意义(P<0.05)(表1)。
2.2铁缺乏指标与心衰指标的相关性分析 铁蛋白与E/A、NT-proBNP、6MWT均存在相关性;转铁蛋白饱和度与LAD、E/A、NT-proBNP、6MWT均存在相关性;转铁蛋白受体指数与LAD、E/A、NT-proBNP、6MWT均存在相关性(P均<0.05)(表2)。
2.3不同心功能分级间铁缺乏指标比较 不同心功能分级间铁蛋白、转铁蛋白饱和度、转铁蛋白受体指数的差异均有统计学意义(P<0.05),组间两两比较显示随着心功能分级的增加,铁蛋白及转铁蛋白饱和度降低,转铁蛋白受体指数增加(P<0.05)(表3)。
3 讨论
表1 两组间心功能指标比较(±s)
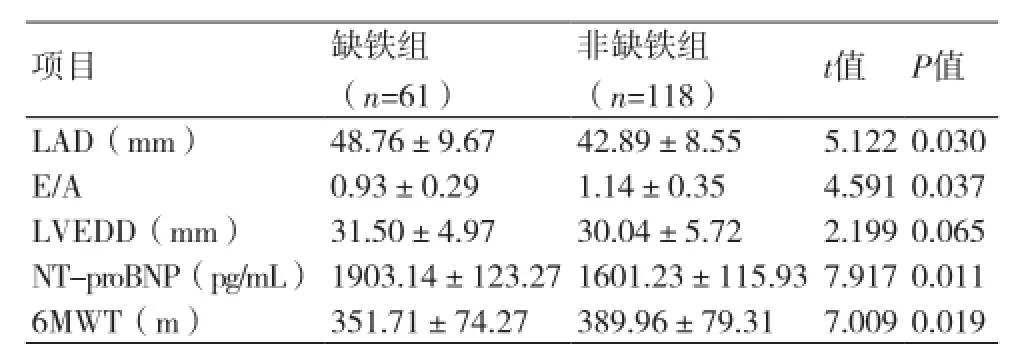
表1 两组间心功能指标比较(±s)
注:LAD:左心房内径;E/A :二尖瓣早期血流速度/舒张晚期血流速度比值;LVEDD:左心室舒张末期内径;NT-proBNP:氨基端脑钠肽前体;6MWT:6分钟步行试验
项目 缺铁组(n=61)非缺铁组(n=118)t值P值LAD(mm)48.76±9.6742.89±8.555.122 0.030 E/A0.93±0.291.14±0.354.591 0.037 LVEDD(mm)31.50±4.9730.04±5.722.199 0.065 NT-proBNP(pg/mL)1903.14±123.27 1601.23±115.93 7.917 0.011 6MWT(m)351.71±74.27 389.96±79.317.009 0.019
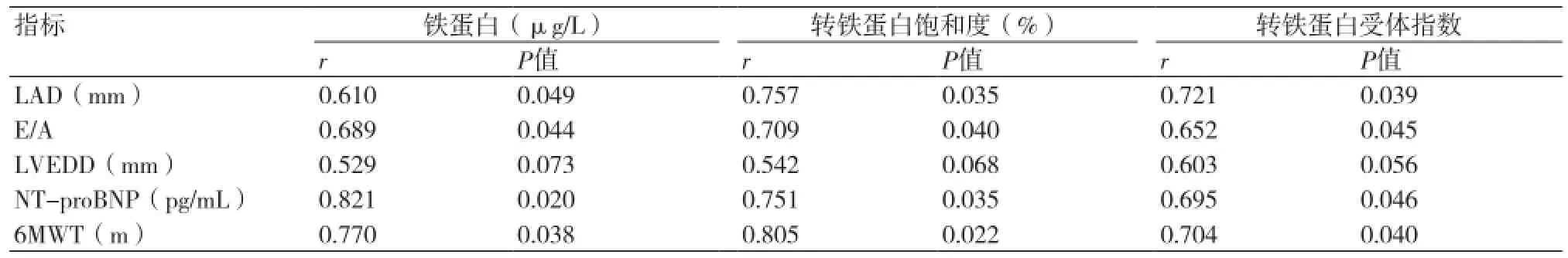
表2 铁缺乏与各心功能的相关性分析(n=179)
研究表明HFpEF发病率一直呈上升趋势[7]。心力衰竭患者均存在明显的胃肠道功能紊乱及广泛的慢性炎症,使铁的吸收、储存和代谢出现障碍,不能被靶器官摄取和利用[8]。铁作为人体维持自稳态的关键元素,参与人体细胞生长及红细胞形成、氧的运输及储存、骨骼肌和心肌的氧化代谢等多项生理过程,机体铁不足将影响血液携氧能力及机体对氧的利用,降低患者的有氧运动能力,并通过分子信号传导通路,刺激左心室肥厚、扩张、心肌纤维化。从病理生理血角度分析,在心动周期的舒张时相,心室的舒张依赖于充足的细胞氧化代谢过程提供能量,而铁离子的代谢就是细胞氧化代谢过程中的重要环节。因此,铁缺乏被认为是左室舒张功能受限,心功能和患者运功耐力减低的重要原因。
目前铁缺乏对HFpEF患者的影响尚缺乏研究,本研究通过对HFpEF患者的缺铁状况进行调查分析,发现伴缺铁患者的心脏超声指标、NT-proBNP、6MWT均差于正常铁水平的患者;铁缺乏程度越重,患者心功能状态越差,因此有必要在心力衰竭常规检查同时进行铁缺乏筛查。对于此类患者及时给予补铁治疗对于改善患者运动耐力、NYHA心功能分级及生活质量及预后可能具有积极意义。研究已经证明铁剂治疗可显著促进HFrEF的治疗效果和改善预后[9],但目前未见针对HFpEF患者的缺铁性治疗研究,是可进一步研究的方向。
在铁利用障碍的机制研究中,已有报道在HFrEF患者中会出现铁转运的异常,因为心肌转铁蛋白受体出现下调[10],但是否HFpEF患者也存在相同的铁代谢异常仍待验证,也是值得进一步探讨的话题。
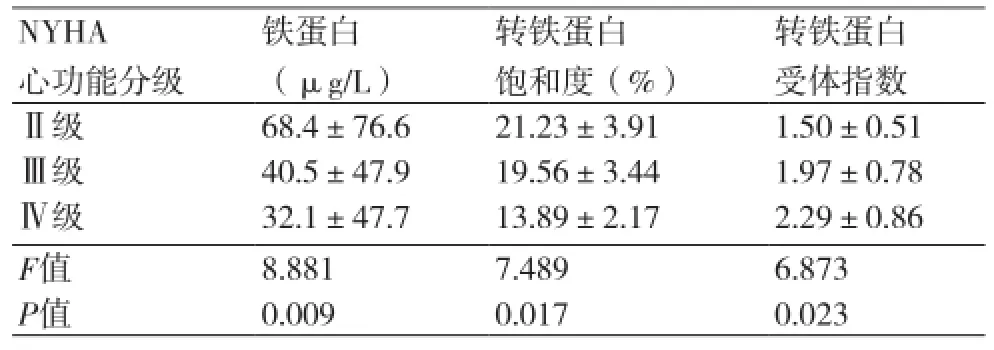
表3 不同心功能分级间铁缺乏指标比较
[1] Stewart S,MacIntyre K,Capewell S,et al. Heart failure and the aging population: an increasing burden in the 21st century? [J]. Heart,2003,89(1):49-53.
[2] Hogg K,Swedberg K,McMurray J. Heart failure with preserved left ventricular systolic function; epidemiology, clinical characteristics and prognosis[J]. J Am Coll Cardiol,2004,43(3):317-27.
[3] Anand, I.S., Anemia and chronic heart failure implications and treatment options. J Am Coll Cardiol,2008,52(7):501-11.
[4] Van Craenenbroeck EM,Pelle AJ,Beckers PJ,et al. Red cell distribution width as a marker of impaired exercise tolerance in patients with chronic heart failure[J]. Eur J Heart Fail,2012,14(1):54-60.
[5] Dickstein K,Cohen-Solal A,Filippatos G,et al. ESC guidelines for the diagnosis and treatment of acute and chronic heart failure 2008. Eur J Heart Fail,2008,10(10):933-89.
[6] Comin Colet J,Enjuanes C,González G,et al. Iron deficiency is a key determinant of health-related quality of life in patients with chronic heart failure regardless of anaemia status. Eur J Heart Fail,2013,15 (10):1164-72.
[7] Fitzgibbons TP,Meyer TE,Aurigemma GP,et al. Mortality in Diastolic Heart Failure. Cardiology in Review,2009,17(2):51-5.
[8] 周京敏,崔洁. 铁缺乏症是慢性心力衰竭治疗的新目标[J]. 岭南心血管病杂志,2015,21(1):7-11.
[9] Ponikowski P,Van Veldhuisen DJ,Comin-Colet J,et al. Beneficial effects of long-term intravenous iron therapy with ferric carboxymaltose in patients with symptomatic heart failure and iron deficiency[J]. Eur Heart J,2015,14,36(11):657-68.
[10] Hentze MW,Muckenthaler MU,Andrews NC. Balancing acts: molecular control of mammalian iron metabolism[J]. Cell,2004,117(3):285-97.
本文编辑:张灵
The correlation between iron deficiency and heart failure with preserved left ventricular ejection fraction
HUANG Nan-qing*, ZHENG Xue-ou.*XiaoLan Hospital of Southern Medical University, Zhongshan, 528415, China.
ZHENG Xue-ou; E-mail: zxo-175@163.com
Objective To study the correlation between iron deficiency and heart failure with preserved left ventricular ejection fraction (HFpEF). Methods 179 HFpEF patients were enrolled. Ferritin, transferrin saturation, soluble transferrin receptor index and cardiac function index were tested. Participants were divided into iron deficiency group (n=61) and non-iron-deficiency group (n=118) based on the level of ferritin or transferrin saturation. The correlation between iron deficiency and HFpEF were studied. Results The difference of left atrium diameter (LAD) [(48.76±9.67)mm vs. (42.89±8.55)mm], ratio of early peak (E) to late peak (A) of mitral flow velocities (E/A) in cardiac ultrasound test [(1.14±0.35 vs.(0.93±0.29)], N-terminal pro brain natriuretic peptide [NT-proBNP,(1903.14±123.27)pg/ml vs. (1601.23±115.93)pg/ml], 6-min-walk-test [6MWT,(351.71±74.27)m vs. (389.96±79.31)m], and NYHA heart function classification between two groups were statistically significant (P<0.05). There was a correlation between level of ferritin, transferrin saturation and soluble transferrin receptor index with LAD, E/A, NT-proBNP and 6MWT. The level of ferritin, transferrin saturation and soluble transferrin receptor index among different cardiac function classification were significantly different (P<0.05). Along with cardiac function classification increasing, level of ferritin and transferrin saturation was decreased, while soluble transferrin receptor index increased. Conclusion There is correlation between iron deficiency and HFpEF,it is necessary to screening iron deficiency in heart failure patients.
Heart failure with preserved left ventricular ejection fraction; Iron deficiency; Correlation
R541.61
A
1674-4055(2016)06-0746-03
1528415 中山,南方医科大学附属小榄医院心血管内科
郑学鸥,E-mail:zxo-175@163.com
10.3969/j.issn.1674-4055.2016.06.31

