甲磺酸沙喹那韦三甲基壳聚糖微球的制备*
沈依蕾,徐蓓华,胡晓渝
(浙江医药高等专科学校,浙江 宁波 315100)
甲磺酸沙喹那韦三甲基壳聚糖微球的制备*
沈依蕾,徐蓓华,胡晓渝
(浙江医药高等专科学校,浙江宁波315100)
为了提高甲磺酸沙喹那韦的生物利用度,制备了甲磺酸沙喹那韦三甲基壳聚糖微球并考察其体外溶出度。用喷雾干燥法制备甲磺酸沙喹那韦三甲基壳聚糖微球,用红外光谱进行鉴定,采用PBS7.4缓冲液和0.1 mol/L盐酸溶液考察微球的体外药物释放速率,用HPLC法检测药物浓度。结果显示,制备得到的甲磺酸沙喹那韦三甲基壳聚糖微球在体外近中性及酸性条件下能够持续释放,无突释现象。甲磺酸沙喹那韦三甲基壳聚糖微球有利于口服给药后,药物的持续释放。
甲磺酸沙喹那韦;三甲基壳聚糖;微球
沙喹那韦是FDA批准上市的第一个治疗艾滋病(HIV)的蛋白酶抑制剂,对HIV-1和HIV-2蛋白酶有强大的抑制作用,对急慢性感染细胞都有抗病毒活性。它具有低毒,高效、高选择性的特点[1],是目前国内获准生产的九种抗艾滋病药物之一,销售情况良好[2],与其它抗HIV药物配合使用,可以显著降低患者体内的病毒数量,亦可降低与艾滋病有关的感染几率。但是沙喹那韦在水中不溶,临床使用甲磺酸沙喹那韦(MSQU)制成口服剂型,通常情况下其生物利用度仅为4%[3],两大主要影响因素是:①水溶性差,严重影响了溶出及吸收;②广泛的首过效应。
三甲基壳聚糖(TMCS)是壳聚糖三甲基化季铵衍生物,具有与壳聚糖相似的优点,如有很好的生物相容性和生物可降解性,对皮肤和黏膜无刺激,并且能促进药物在胃肠道吸收,能与小肠表皮细胞作用,介导暂时开放细胞紧密连接,增强蛋白在黏膜表面的吸收,促进细胞旁路转运。但是比壳聚糖更为优越的是,它不管在酸性还是在中性、碱性环境中都携正电荷,具有良好的溶解性,因此在肠道中,也能够促进药物吸收;另外具有对肠道黏膜的粘附性,能增加药物与肠道的接触时间。壳聚糖在肠道中不能溶解,则严重影响了它的促吸收功能。
为了提高甲磺酸沙喹那韦在胃肠道的吸收能力,进而提高其生物利用度,本实验通过喷雾干燥法制备了甲磺酸沙喹那韦三甲基壳聚糖微球,并考察了其体外药物释放速率。
1 试剂与仪器
1.1试剂
甲磺酸沙喹那韦,上海佰世凯化学科技有限公司(批号:120805);三甲基壳聚糖(TMCS,分子量600 kDa,分子量100 kDa,季铵化取代率为28%),自制;乙腈、磷酸二氢钾、氢氧化钠,购自中国国药上海化学试剂公司;其余试剂均为市售分析纯。
1.2仪器
Avance 500 型核磁共振波谱仪;Tensor 27型傅里叶变换红外光谱仪(KBr压片),德国Bruker公司;TU-1810紫外可见分光光度计,北京普析通用仪器有限责任公司;U3000高效液相色谱仪,SPD-10A 型紫外检测器,美国戴安公司 ;BS110S 系列电子天平,北京赛多利斯天平有限公司;Winner 2000Z智能全自动台式激光粒度分析仪,济南微纳仪器有限公司;SHA-B 恒温振荡器,国华企业。
2 实验方法
2.1标准曲线的线性关系考察[4-5]
色谱条件:色谱柱:ODS C18柱(250 mm×4.6 mm,5 μm);流动相:乙腈-0.02 mol/L磷酸缓冲液(取磷酸二氢钾2.7262 g,加水溶解,氢氧化钠调节pH至6.7,定容至1000 mL)(60:40);流速:1.0 mL/min;检测波长:300 nm;柱温:25℃;进样量:20 μL。
标准曲线的绘制:精密称取甲磺酸沙喹那韦,以甲醇为溶剂配制成质量浓度为0.01,0.025,0.05,0.1,0.15,0.2 mg/mL 的甲磺酸沙喹那韦溶液,进样,记录色谱图。
2.2甲磺酸沙喹那韦三甲基壳聚糖微球制备
精确称取适量三甲基壳聚糖(分子量600 kDa/TMCS60,或分子量100 kDa/TMCS10)溶于200 mL蒸馏水中,搅拌至完全溶解,配成TMCS水溶液,待用。精确称取440 mg甲磺酸沙喹那韦,投入200 mL蒸馏水中,稍加热使溶解,配制成浓度为2.2 mg/mL的饱和溶液。将上述配制的200 mL TMCS水溶液和200 mL甲磺酸沙喹那韦饱和溶液混合,用喷雾干燥法干燥,选择喷雾干燥器的进口温度为120℃,进料速度为3 mL/min,空气流量为400 L/h。收集干燥颗粒,得到甲磺酸沙喹那韦三甲基壳聚糖微球[6]。
2.3载药量及包封率测定[6]
得到的甲磺酸沙喹那韦三甲基壳聚糖微球,通过高效液相法在300 nm的波长来测定吸收度。根据标准曲线计算甲磺酸沙喹那韦的浓度。
载药量=(微球中含药量/微球的总质量)×100%
包封率=(微球中包封的药物量/药物投料量)×100%
2.4溶出速度测定
制备得到的甲磺酸沙喹那韦三甲基壳聚糖微球,分别测定其溶出度。精密称取40 mg甲磺酸沙喹那韦三甲基壳聚糖微球,投入透析袋中,加入10 mL介质,两端扎紧,再投入90 mL介质(0.1 mol/L HCl溶液或者pH=7.4的PBS磷酸溶液)中,磁力搅拌,温度为37℃。在0.25 h、0.5 h、1 h、2 h、4 h、6 h、8 h、10 h时取出介质0.5 mL,并补充同体积释放介质。通过高效液相法在300 nm的波长来测定吸收度,然后根据标准曲线计算甲磺酸沙喹那韦的浓度。
3 结果与讨论
3.1标准曲线测定
以峰面积A为纵坐标,甲磺酸沙喹那韦质量浓度C(mg/mL)为横坐标,进行线性回归,得甲磺酸沙喹那韦回归方程:A=137.48C-0.0076(r=0.999)。
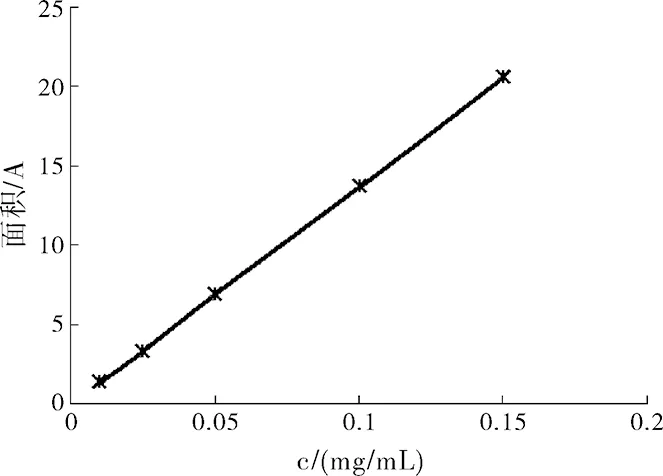
图1 甲磺酸沙喹那韦的标准曲线
3.2甲磺酸沙喹那韦三甲基壳聚糖微球的制备
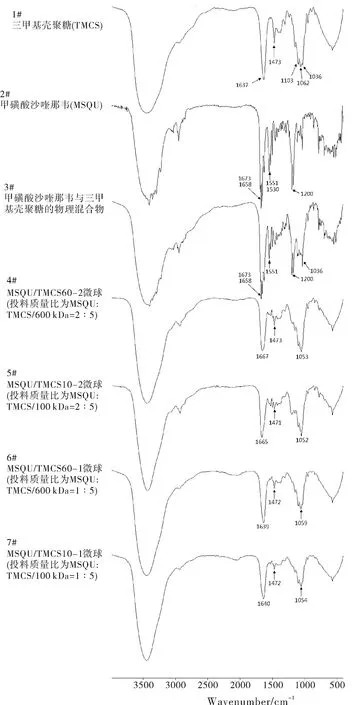
图2 红外图谱
根据图2,甲磺酸沙喹那韦三甲基壳聚糖微球的红外图谱(图2中4#~7#)与甲磺酸沙喹那韦与三甲基壳聚糖的物理混合物(图2中3#)比较:甲磺酸沙喹那韦与三甲基壳聚糖的物理混合物(图2中3#)在2000~1200区段的特征峰是1673 cm-1,1658 cm-1,1551 cm-1,1530 cm-1,1200 cm-1,1036 cm-1,兼具有甲磺酸沙喹那韦和三甲基壳聚糖的特征峰,与微球有明显差异;MSQU/TMCS60-2微球在2000~1200区段的特征峰是:1667 cm-1,1473 cm-1,1053 cm-1(见图2中4#);MSQU/TMCS10-2微球在2000~1200区段的特征峰是:1665 cm-1,1471 cm-1,1052 cm-1(见图2中5#);MSQU/ TMCS60-1微球在2000~1200区段的特征峰是:1639 cm-1,1472 cm-1,1059 cm-1(见图2中6#);MSQU/TMCS10-1微球在2000~1200区段的特征峰是:1640 cm-1,1472 cm-1,1054 cm-1(见图2中7#),均与混合物有明显不同。其中MSQU/TMCS60-2微球和MSQU/TMCS10-2微球由于载药量较高,与原料三甲基壳聚糖的红外图谱差异较大,具体表现在微球中出现了新的峰位1667 cm-1或1665 cm-1,而无三甲基壳聚糖的特征峰1637 cm-1。MSQU/ TMCS60-1微球和MSQU/TMCS10-1微球由于载药量较低,与三甲基壳聚糖的红外特征相似。
3.3载药量及包封率测定
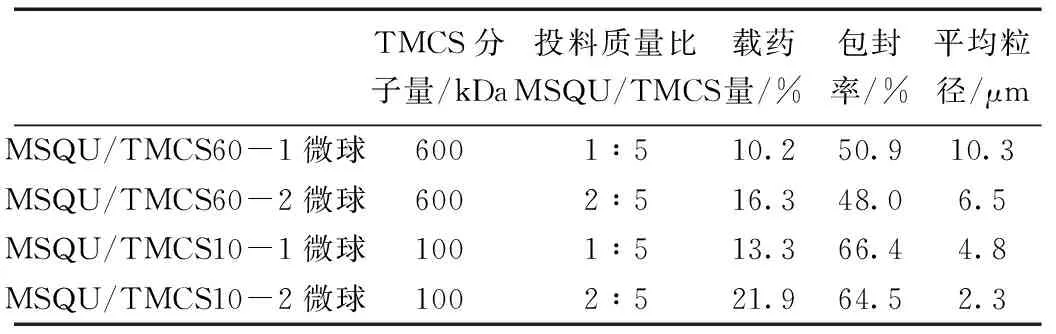
表1 甲磺酸沙喹那韦三甲基壳聚糖微球的含药量、包封率和粒径结果
从表1中可看出,TMCS的分子量大小影响了载药量和微球粒径,分子量增大载药量有所下降,可能与材料形成微球的效率有关:TMCS分子量越小越容易成微球;同时,TMCS分子量越小,形成微球后的粒径也越小。从投料质量比看,MSQU/TMCS的比值越高,载药量越大,粒径也减小。
3.4溶出速度测定
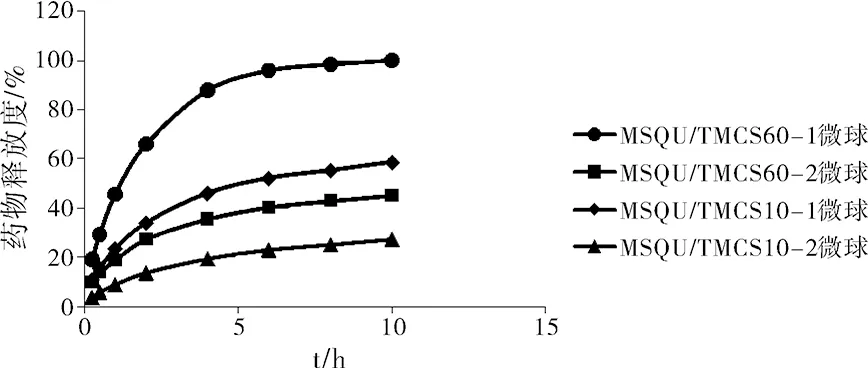
图3 在0.1 mol/L HCl溶液中微球的溶出度
如图3所示,制备的甲磺酸沙喹那韦三甲基壳聚糖微球在0.1 mol/L HCl溶液中早期无突释现象,呈现良好的缓释效应。在酸性介质中,由于三甲基壳聚糖易于溶解,使得三甲基壳聚糖含量高的微球更快速地释放药物。MSQU/TMCS60-1微球,4 h 释放度达到了88%,8 h达到了98%,比MSQU/TMCS60-2微球的释放速度快很多,后者在8 h的释放度是43%。MSQU/TMCS10-1微球,4 h释放度达到46%,8 h达到55%,也比MSQU/TMCS10-2微球的释放速度快,后者在8 h的释放度仅为25%。
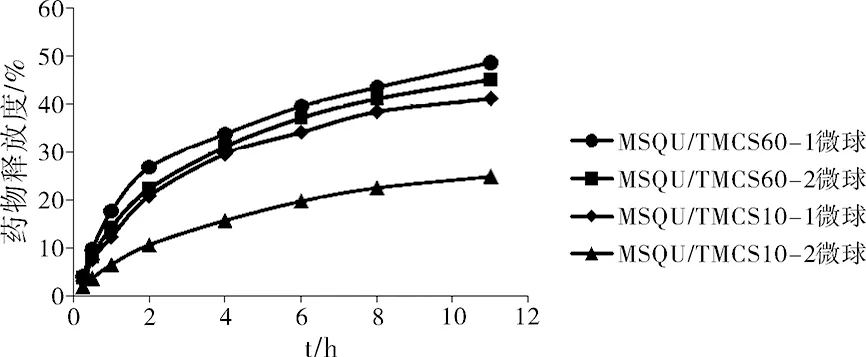
图4 在pH 7.4的PBS缓冲液中微球的溶出度
如图4所示,本实验制备的甲磺酸沙喹那韦三甲基壳聚糖微球在pH7.4的PBS缓冲液中早期也无突释现象,呈现良好的缓释效应。在近中性介质中,MSQU/TMCS60-1微球的释放速度大大放缓,8 h的释放度是44%;而MSQU/TMCS60-2微球的释放速度则几乎不受介质影响,8 h的释放度是45%,可见三甲基壳聚糖的高含量对药物在酸性介质中释放的影响较大。同样可以看到MSQU/TMCS10-1微球在近中性介质中的释放度有所下降,8 h的释放度是38%,而MSQU/TMCS10-2微球的释放速度也几乎不受介质影响,在中性介质中8 h的释放度是23%。
4 结 论
所制备的四个甲磺酸沙喹那韦三甲基壳聚糖微球同时具备了在酸性及近中性条件下的缓慢释放能力,有利于口服给药后药物的持续释放。其中MSQU/TMCS60-1微球在酸性条件下释放最快,释放速度适中的微球是MSQU/TMCS60-2微球和MSQU/TMCS10-1微球,其溶出度受酸碱环境影响较小,微球体内药物释放和吸收情况在进一步考察中。
[1]charies Fournier,Michie Hamon,Martiai Hamon,et al.Preparation and preciinicai evaiuation of bioresorbabie hydroxyethyistarch microspheres for transient arteriai emboiization[J].International Journal of Pharmaceutics,1994,106:41-49.
[2]陈英,王春丽,任雪莲.抗艾滋病药国内市场分析[A].第六届沈阳科学学术年会文集(B)[C].沈阳,2009:85-88.
[3]关屹,闫冬.沙奎那韦琥珀酸半酯盐及其制剂:中国,201110152919.9[P].2011-11-30.
[4]罗金文,朱海霖,李会林.HPLC测定沙奎那韦的含量及其有关物质[J].中国药学杂志,2006,41(1):67-69.
[5]高素英,陈龙珠.高效液相色谱法测定甲磺酸沙喹那韦胶囊主药及有关物质含量[J].医药导报,2009,28(2):233-234.
[6]蔡鑫君,程巧鸳,赵宁,等.喷雾干燥法制备川芎嗪壳聚糖微球的研究[J].中草药,2008,39(5):679-682.
Preparation of Saquinavir Mesylate Loaded N-trimethyl Chitosan Microspheres*
SHEN Yi-lei,XU Bei-hua,HU Xiao-yu
(Zhejiang Pharmaceutical College,Zhejiang Ningbo 315100,China)
In order to improve the bioavailability of saquinavir mesylate,saquinavir mesylate loaded N-trimethyl chitosan microspheres was prepared and their vitro dissolution was studied.Saquinavir mesylate loaded N-trimethyl chitosan microspheres was prepared by spray drying.The formation of microspheres were confirmed by infrared spectroscopy(IR).The drug release rate of microspheres was studied in PBS7.4 buffer or 0.1 mol/L hydrochloric acid solution in vitro,and drug concentrations were detected by HPLC.Results showed that saquinavir mesylate loaded N-trimethyl chitosan microspheres was prepared,which released saquinavir mesylate in neutral and acidic conditions continuously in vitro,without any sudden release.Microspheres were suitable for gastrointestinal drug delivery.
saquinavir mesylate; N-trimethyl chitosan; microspheres
浙江省大学生科技创新项目(2013R433005);宁波市科技局社会发展项目(2010C50035)。
沈依蕾(1993-),女。
徐蓓华(1977-),女,副教授。
R914
A
1001-9677(2016)06-0055-03

