卡莫氟分散片制备工艺研究
窦建华 侯喜媛(天方药业有限公司 驻马店 463000)
卡莫氟分散片制备工艺研究
窦建华侯喜媛(天方药业有限公司驻马店463000)
目的:研究卡莫氟分散片制备工艺。方法:以崩解时限、溶出度、硬度、脆碎度为考察指标,采用正交实验,对卡莫氟分散片制备工艺进行研究。结果:按制备工艺制得的卡莫氟分散片,可在3min内完全崩解。结论:优选制备工艺制得的卡莫氟分散片,分散均匀度符合现行版《中国药典》要求,溶出度明显优于普通片剂。
分散片 高效液相色谱法 溶出度 生物利用度 分散均匀度 稳定性
卡莫氟是新一代氟尿嘧啶类药物,主要用于治疗消化道和乳腺恶性肿瘤,因其水溶性差,几乎不溶于水,普通片剂溶出度较低。笔者利用正交试验对制剂工艺进行研究,研制了分散度高、溶出速度快、吸收快、生物利用度高的卡莫氟分散片,并对其分散均匀度与溶出度进行了考察,详情如下:
1 材料与设备
1.1药品与试剂:卡莫氟片(南通制药);卡莫氟分散片(自制);MCC、十二烷基磺酸钠、Glucose、CMS-Na、PVPk30、蛋白糖、SiO2、MS、乙醇均为国产药用级;盐酸、甲醇、醋酸均为国产分析纯。
1.2设备与仪器:FL-15B沸腾干燥制粒机(重庆英格),FZB-150型粉碎整粒机(温州市嘉南),SYH-50三维运动混合机(常州市豪龙),GZPL16型全自动高速旋转压片机(北京国药龙立),AE200电子分析天平(上海梅特勒-托利多仪器公司)、YD-1片剂硬度测试仪(天津市国铭医药设备)、CJY-300B片剂脆碎度测试仪(上海黄海药检仪器厂)、ZBS-6G智能崩解试验仪、ZRS-8G智能溶出仪(天津大学无线电厂),L7420高效液相色谱仪(日本日立)。
2 方法
2.1卡莫氟分散片的制备:按卡莫氟片《中国药典》2010年版二部的处方量,称取卡莫氟、MCC、CMS-Na、Glucose、蛋白糖后过100目筛,加入FL-15B沸腾干燥制粒机,用适量2%PVPk30溶液(溶有十二烷基磺酸钠的70%乙醇)作粘合剂沸腾制粒,喷浆结束干燥至50℃,加入SiO2、MS,用FZB-150型粉碎整粒机整粒,用SBH-50三维运动混合机混合均匀,GZPL16型全自动高速压片机压片。
2.2生产工艺筛选:本次试验对制备工艺影响较大的四个因素MCC、十二烷基磺酸钠、CMS-Na、Glucose进行正交实验[1],拟定了三个水平,采用L9(34)正交表进行实验,把制得的分散片的崩解时限、溶出度、硬度、脆碎度作为测定指标,确定最佳制备工艺。
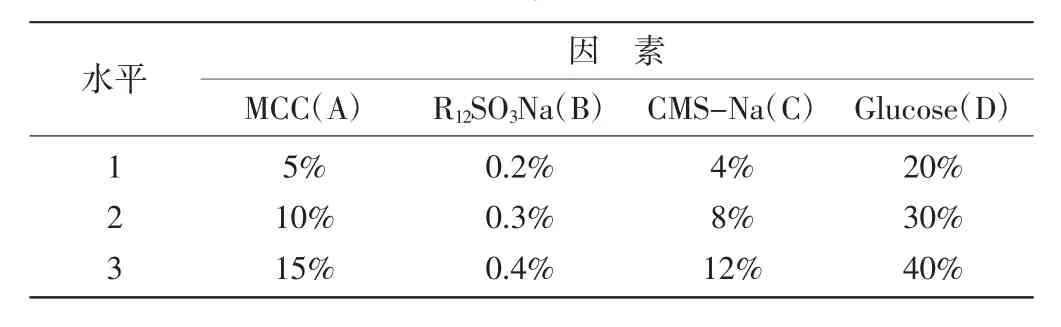
表1 因素水平表
2.3分散均匀性检查[2]:按《中国药典》2015年版四部制剂通则0101片剂分散均匀性检查法项下检查。
3 结 果
3.1正交实验结果
3.1.1结果见表2。
3.1.2从极差分析:R3B>R3A>R3C>R3D表明片芯溶出度的最大影响因素是B;R4B>R4C>R4D>R4A表明片芯崩解的最大影响因素是B。
3.1.3从指标随因素变化图来分析:从指标随因素变化图纵向和横向同时进行对比分析:片芯溶出度宜高,崩解宜短,硬度应适当,脆碎度宜小。因此:选定处方最优水平组合为A3B2C1D2。
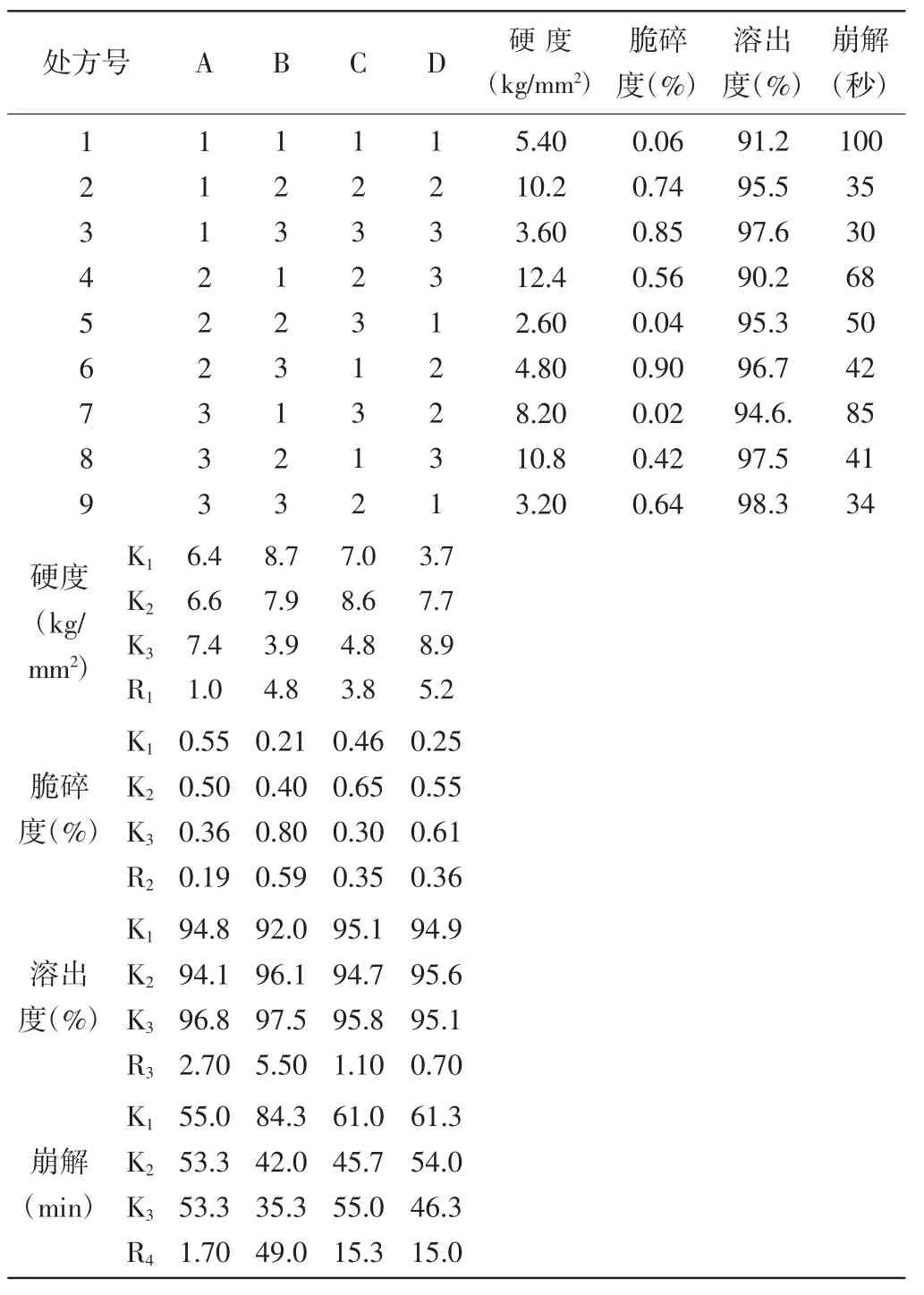
表2 L9(34)正交实验结果分析
3.2分散均匀性:按选定处方制得分散片,照“2.3”项下操作,分散片在1.5min内全部崩解并通过筛网。
3.3溶出度试验[3]:分别取卡莫氟分散片与卡莫氟片各6片,按照2015年版《中国药典》四部通则0931第一法,参照2015年版《中国药典》二部(P190)卡莫氟片溶出度检查法进行测定,在10、20、40、60min时,分别取两种溶液20mL滤过,并及时补加溶出介质20mL,取续滤液作为供试品溶液;另取卡莫氟对照品,精密称定,加少量乙醇使溶解并用溶出介质定量稀释制成每1mL中约含50μg的溶液,作为对照品溶液。照含量测定项下的色谱条件,精密量取供试品溶液与对照品溶液各10μL,分别注入液相色谱仪,记录色谱图,按外标法以峰面积计算每片的溶出量,并绘制溶出曲线如下:
溶出曲线表明,在60min内,卡莫氟分散片各时间点溶出度均远高于卡莫氟片,体外溶出趋势明显优于普通片剂。
4 稳定性试验[4]
4.1加速试验:取样品,置恒温40℃±2℃、相对湿度75%±5%条件下放置6个月。分别在1、2、3、6个月末取样检查,结果外观无明显变化,各项指标与原样品基本一致。
4.2长期试验:取样品,置温度25℃±2℃、相对湿度60%±10%条件下放置24个月。分别在3、6、9、12、18、24个月末取样检查,结果外观无明显变化,各项指标与原样品基本一致。
5 讨论
5.1压片硬度影响分散片的分散均匀度。因此应控制硬度,一般宜控制在6~8kg/mm2。
5.2采用2%PVPk30溶液制粒有利于控制分散均匀度和溶出度,但粘合剂浓度对分散片分散均匀度和溶出度的影响有待研究。
5.3分散片常采用MCC、L-HPC、PVPP等作为崩解剂,本方采取MCC与CMS-Na联合内加方式,片子可压性和分散均匀度俱佳,但不同崩解剂及其用量对该品种的崩解效果有待研究。
[1]杨继泰.正交试验设计与分析.医药应用数理统计[M].河南大学出版社,第八章P137.
[2]国家药典委员会.分散均匀性检查0101.中国药典2015年版四部[M].北京:中国医药科技出版社,制剂通则0101.
[3]国家药典委员会.溶出度测定法.中国药典2015年版二部[M].北京:中国医药科技出版社,2015.
[4]国家药典委员会.原料药物与制剂稳定性试验指导原则9001.中国药典2015年版四部[M].北京:中国医药科技出版社,制剂通则指导原则9000.
R943
B
1672-8351(2016)02-0125-02

