β -环糊精增敏荧光法测定β -雌二醇
陈金娥, 吴玉芳, 张海容
(忻州师范学院生化分析技术研究所,山西忻州 034000)
雌二醇是一种类固醇雌激素,是雌激素中活性最强的激素,在许多生理过程中起着非常重要的作用。雌二醇[1]可以补充女性卵巢分泌的17-β-雌二醇的不足,能促使细胞合成DNA、RNA和相应组织内各种不同的蛋白质,同时它也是一种具有较强雌性活力的内分泌干扰物,并可产生代谢产物雌三醇。β-雌二醇在人体中含量的偏高或偏低均会引起相关疾病,如女性性腺功能不良、乳腺癌、前列腺癌、骨质疏松、白细胞减少症等,给人体健康带来重大隐患。
目前,用于检测β-雌二醇的方法主要有高效液相色谱法[2]、气相色谱-质谱法[3]、高效液相色谱-串联质谱法[4]、电化学分析法[5]、荧光免疫法[6]、反相高效液相色谱-荧光检测法[1]等。这些分析方法操作繁琐,成本较高,时间冗长[7]。β-环糊精(β-CD)是一类具有“内疏水外亲水”特殊分子结构的大环化合物[8],其有序的微环境可对荧光客体分子起到保护作用,减少客体分子各种猝灭过程及辐射与非辐射去活化过程,提高荧光量子产率[9]。本实验利用β-CD结构特性,建立了一种简单、快速的检测鸡蛋样品中β-雌二醇的分析方法,尚未见有关此类报道。
1 实验部分
1.1 仪器与试剂
F-4600型荧光分光光度计(日本,日立公司);KQ-400KDE型高功率数控超声波清洗器(江苏省昆山市超声仪器有限公司);pHS-3B型pH计(上海精密科学仪器有限公司);AB204-N型电子分析天平(Mettler-Toledo Group公司);85-2型磁力搅拌器(巩义市予华仪器有限责任公司);LC-4016型低速离心机(安徽中科中佳科学仪器有限公司)。
β-雌二醇(Sigma公司);十二烷基硫酸钠(SDS)(分析纯,天津市风船化学试剂科技有限公司);十六烷基三甲基溴化铵(CTMAB)(分析纯,天津市光复精细化工研究所);聚氧乙烯月桂醚(Brij35,Alfa Aesar公司);β-环糊精(β-CD)(分析纯,天津市光复精细化工研究所);无水乙醇(分析纯,天津市风船化学试剂科技有限公司);甲醇(分析纯,天津市风船化学试剂科技有限公司);硼酸(天津市北辰方正试剂厂);磷酸(天津市北辰方正试剂厂);36%乙酸(西陇化工股份有限公司);氢氧化钠(分析纯,天津市风船化学试剂科技有限公司);乙腈(分析纯,天津市福晨化学试剂厂)。实验用水为二次蒸馏水。
1.2 实验方法
1.2.1β-雌二醇贮备液的配制准确称取0.0136 g雌二醇于烧杯中,用无水乙醇溶解后,移入50 mL容量瓶中用乙醇定容,浓度为1.0×10-3mol/L。
1.2.2有序介质溶液的配制用水分别配制0.1 mol/L的SDS溶液、1.0×10-2mol/L CTMAB溶液、1.0×10-2mol/L Brij35溶液和1.0×10-2mol/Lβ-CD溶液,胶束体系浓度均大于其临界胶束浓度。
1.2.3三酸缓冲溶液的配制[10]准确称取2.4745 g硼酸及2.71 mL磷酸(85%)与2.35 mL乙酸(36%),用水定容至1 L,再用0.2 mol/L NaOH溶液调节至实验所需pH值。
1.2.4试样制备与荧光测定参考文献方法[11],将新鲜鸡蛋打碎搅匀,称取样品10.0 g,加入20.0 mL乙腈,在磁力搅拌器上混合搅匀,超声20 min,于3 800 r/min条件下离心10 min,移出上清液。残渣中加入20.0 mL乙腈后做同样处理,合并上清液。上清液用0.45 μm微孔滤膜过滤,滤液备用。
在10 mL比色管中加入适量β-雌二醇溶液,再依次加入2 mL三酸缓冲溶液,适量有序介质溶液,超声15 min,静置20 min后,在荧光光度计上测量荧光强度。荧光激发和发射通带均为2.5 nm,扫描速度设定为1 200 nm/min。
2 结果与讨论
2.1 β -雌二醇荧光光谱
按照实验方法,测定β-雌二醇以及β-CD存在时的荧光激发和发射,发现在λex/λem=278/307 nm处出现强的荧光激发和发射峰,加入β-CD后荧光强度显著增加,荧光光谱如图1所示。
2.2 外界因素对β -雌二醇荧光强度的影响
2.2.1不同介质的影响实验探究了在水、乙醇、甲醇、SDS、CTMAB、Brij35、β-CD七种不同介质中β-雌二醇的荧光强度。结果表明:在酸性环境中,SDS、CTMAB、Brij35、β-CD对β-雌二醇均有荧光增敏作用,其中β-CD对雌二醇的荧光增敏效果最显著。因此,本文选择β-CD作为增敏介质。表1列出了β-雌二醇在不同介质中的荧光特性。
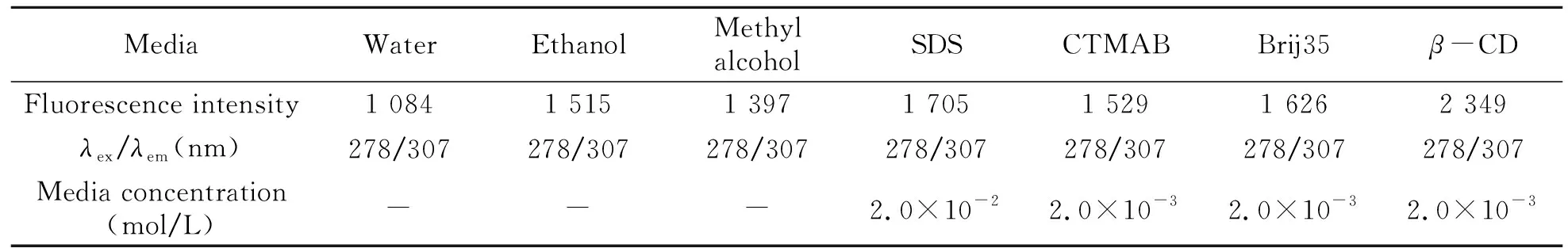
表1 不同介质中雌二醇的荧光特性
2.2.2pH的影响在β-雌二醇、β-CD体系中分别用pH从1.95到12.02的三酸缓冲溶液控制溶液酸度,然后测定其荧光强度,结果见图2。在pH为1.95~8.09范围内荧光强度较强且比较稳定,当pH超过9.17时,随着pH值的增大体系的荧光强度呈下降趋势。这可能是由于pH的变化使得β-雌二醇的活性部位羟基结构发生变化,导致体系共轭电子云密度变化,进而引起荧光强度值的改变[11]。因此实验选取pH=6.93的三酸缓冲溶液控制体系的酸度。
2.2.3稳定性测量按照前述实验条件,以10 min为测量间隔,连续测定2 h内体系的荧光强度,实验结果如图3所示。在2 h内荧光强度保持稳定不变,说明测量体系稳定性良好。
2.2.4β-CD浓度的影响选取pH=6.93的三酸缓冲溶液,固定β-雌二醇的浓度为1.0×10-5mol/L,改变β-CD浓度,测量体系的荧光强度。结果表明,β-CD浓度在2.0×10-4~1.0×10-3mol/L范围内,随着β-CD浓度的增加,荧光强度迅速增大;当浓度超过1.0×10-3mol/L时,荧光强度增长呈平缓趋势。本文选择β-CD浓度为2.0×10-3mol/L。
2.2.5金属离子对β-雌二醇荧光干扰测定实验测定了10种不同金属离子对体系荧光强度的影响。结果显示:当金属离子浓度为β-雌二醇浓度的20倍时,Ca2+、Mg2+、Al3+、Zn2+、Hg2+、Co2+对体系荧光强度无影响;Cu2+、Cd2+、Pb2+浓度降低为β-雌二醇浓度的5倍时对体系无影响;Ce3+影响较大,测量结果显示体系在307 nm和345 nm处出现两个荧光发射峰,可能生成了新的配合物,其作用机理尚待进一步研究。
2.3 工作曲线、检出限与精密度
在最佳实验条件下绘制工作曲线,β-雌二醇浓度在6.0×10-7~4.0×10-5mol/L 范围内呈良好线性关系,回归方程为:lgF=0.8181lgc+7.5124,相关系数R2=0.995,方法检出限(3σ/k)为1.36×10-8mol/L(k为工作曲线斜率),对1.0×10-5mol/Lβ-雌二醇溶液平行7次测量的相对标准偏差(RSD)为1.83%。
2.4 实际样品分析及回收率测定
按照实验方法,测定3种鸡蛋样品(均购自本地超市)中β-雌二醇的含量,并进行加入回收实验,取6份样品平行测定,结果见表2。

表2 鸡蛋中β -雌二醇含量测定结果
2.5 主客体分子的作用机理
2.5.1β-CD对β-雌二醇荧光强度的影响在β-雌二醇中加入β-CD后,随着β-CD浓度的增加体系的荧光强度逐渐增大,形成了主客体包合物,其激发波长和发射波长基本保持不变。结果见图4。
2.5.2包合比及其包合常数的测定Benes-Hildebrand双导数法[11]是利用光谱法(包括吸收光谱法和荧光光谱法)测定主客体络合物形成常数的经典方法,本实验采用荧光法来测定包合物成及常数。实验结果表明,1/△F对1/[CD]作图呈良好线性关系,说明β-雌二醇与β-CD形成1∶1的稳定的包合物。根据截距和斜率即可求得包合常数Kf=7.0×103。
2.5.3热力学函数△G⊖、△H⊖、△S⊖测定实验选取25 ℃、30 ℃、35 ℃不同温度,用双导数法求得不同温度下的包合常数Kf值,见表3。包合过程中△G⊖<0,△H⊖<0,说明该过程是一个可以自发进行的放热反应,升高温度包合物的稳定性下降,不利于反应正向进行;△S⊖<0,说明β-雌二醇进入β-CD分子中,使体系中分子的有序度增加[8]。研究结果表明,由于客体分子进入β-CD空腔运动受限,使其荧光强度增大。
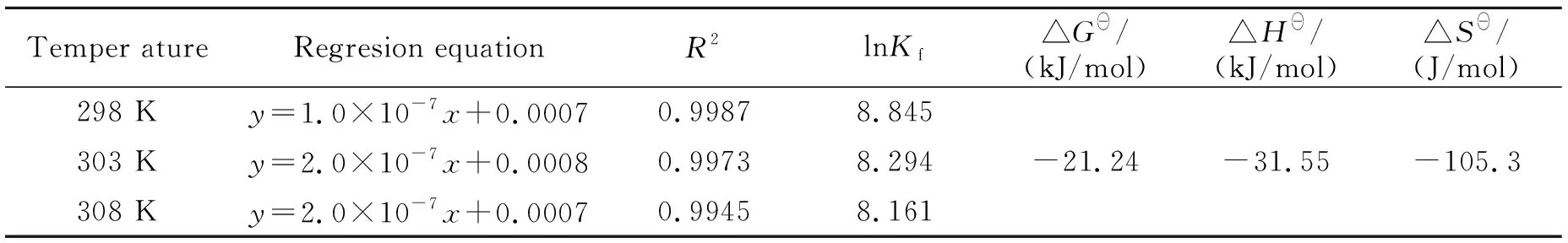
表3 热力学函数测定
3 结论
本文通过β-CD增敏荧光法测定鸡蛋样品中β-雌二醇的含量,方法的线性范围为6.0×10-7~4.0×10-5mol/L,检出限为1.36×10-8mol/L,相对标准偏差(RSD)为1.83%。同时采用Benes-Hildebrand双倒数法研究了主客体包合物包合比、包合常数Kf及热力学函数△G⊖、△H⊖、△S⊖变化,探讨了雌二醇在环糊精体系中发光机理。

