改良胸腔镜下胸膜纤维板剥脱术治疗慢性脓胸31例
邓勇军刘焕鹏 喻应洪 李 珏 汪 颖 邹建彬
(昆明医科大学第四附属医院胸外科,昆明 650021)
·临床研究·
改良胸腔镜下胸膜纤维板剥脱术治疗慢性脓胸31例
邓勇军*刘焕鹏 喻应洪 李 珏 汪 颖 邹建彬
(昆明医科大学第四附属医院胸外科,昆明 650021)
目的 探讨改良胸腔镜下胸膜纤维板剥脱术治疗慢性脓胸的可行性。 方法 2013年10月~2015年11月对31例脓胸行改良两孔胸腔镜下胸膜纤维板剥脱术,做长约4 cm操作口,紧贴壁层纤维板表面进行胸膜下钝性分离,从闭锁的胸膜之间形成扩大的间隙,随后做长约1.5 cm观察孔,置入胸腔镜进行纤维板剥脱。 结果 27例在胸腔镜下完成胸膜纤维板剥脱术,4例因病程较长,脏层纤维板与肺组织致密粘连中转为胸腔镜辅助下保留肌肉小切口开胸手术完成胸膜纤维板剥脱术。手术时间120~185 min,(145±42)min;术中出血量(380±100)ml;术后胸腔闭式引流管留置时间4~16 d,(10±6)d。术后肺持续漏气>7 d 1例,胸腔积液>7 d 1例。术后住院时间(14.0±1.5)d。31例术后随访3~6个月,1例发生中等量胸腔积液,其余患者未发现脓胸复发。 结论 改良胸腔镜下胸膜纤维板剥脱术治疗慢性脓胸可行。
电视胸腔镜手术; 胸膜纤维板剥脱术; 脓胸
电视胸腔镜手术(video-assisted thoracoscopic surgery,VATS)的应用范围几乎涉及到普胸外科领域的各种手术。以往的观点认为脓胸是胸腔镜手术禁忌证,传统治疗方法为开胸胸膜纤维板剥脱术,病灶清除彻底,操作方便,但手术切口大,胸部肌肉切断多,术后恢复较慢。随着胸外科微创技术的不断发展,胸腔镜技术逐渐应用于早期脓胸的治疗,并取得一定的疗效[1~3]。目前,VATS对慢性脓胸的应用范围有限,胸腔镜下剥脱较厚的纤维板较为困难;另一方面,慢性脓胸由于胸膜腔闭锁,膈肌与肺组织或胸膜紧密粘连,做胸腔镜观察孔探查时容易损伤肺组织、膈肌,甚至进入腹腔损伤腹腔脏器;此外,传统胸腔镜脓胸手术切口多为3~4个。基于以上问题,我科在传统开胸手术和VATS基础上,融合两者的优点进行改良,2013年10月~2015年11月采用改良两孔胸腔镜下胸膜外纤维板剥脱术治疗慢性脓胸31例,现报道如下。
1 临床资料与方法
1.1 一般资料
本组31例,男17例,女14例。年龄21~54岁,(35.5±4.5)岁。临床表现为发热、胸痛。病程4周~3个月,(9.5±4.5)周。左侧19例,右侧12例。肺部炎症所致15例,胸膜炎所致14例,胸部外伤所致2例。既往有呼吸道感染病史15例。根据患者发热、乏力、消瘦、贫血、胸痛、胸闷等症状、体征,胸片、胸部CT、胸腔超声等检查及胸腔穿刺,临床诊断为慢性脓胸(Ⅲ期)。15例发热,术前经抗感染治疗至体温正常;9例结核性脓胸经抗结核治疗2周以上;16例营养不良接受支持治疗。术前采用胸腔穿刺抽液治疗13例,行胸腔闭式引流术8例(引流液为稠厚脓液或稀薄脓液中检出大量白细胞)。
病例选择标准:术前胸片及胸部CT显示包裹性积液,胸膜不同程度增厚,脓腔均位于患侧胸腔的后、外、下方及膈面,行胸腔穿刺抽脓或胸腔闭式引流等治疗无效,排除胸膜间皮瘤或恶性肿瘤胸膜转移所致恶性胸水。
1.2 方法
双腔气管插管全麻,健侧90°折刀卧位。操作口位于第6肋间隙腋后线前后,观察口位于腋前线第7肋间隙(图1A)。首先,于第6肋间隙腋后线前后做长约4 cm切口,切开皮肤皮下组织,以手指将背阔肌前缘向后推以免损伤。沿肌纤维走行方向切开前锯肌,随后紧贴第7肋骨上缘切开肋间肌及壁层胸膜到达纤维板表面,此时不再继续切开纤维板,改为以食指或镊子柄紧贴纤维板表面进行胸膜外钝性分离,将切口周围纤维板从胸壁上分离下来,尽量保留壁层胸膜(图1B),此时胸膜外腔隙已形成,切口放入塑料切口保护套(规格为70/70-35/25,江苏常州威克医疗器械有限公司,批文号:苏械注准20152660911)将切口撑开(图1C),继续以手指钝性分离胸膜向观察孔处延伸,随后于腋前线第7肋间隙处做长约1.5 cm切口为观察口,进入胸膜外腔隙后以食指钝性分离胸膜,将观察口周围胸膜外间隙扩大,放置套管并置入胸腔镜。弯头吸引器配合卵圆钳夹持折叠纱布进一步胸膜外剥离壁层胸膜及纤维板,随后切开壁层胸膜及纤维板(图2A),显露脓腔,吸净脓腔内脓液及坏死组织并冲洗脓腔,以电钩或剪刀切除壁层胸膜及纤维板,此时剩下肺表面脏层纤维板需剥脱,操作方法与常规开胸手术类似,电刀切开脏层纤维板达脏层胸膜表面,以弯头吸引器配合剥离子逐渐剥离脏层纤维板,尽量保留脏层胸膜(图2B)。剥离完毕后创面止血,3-0可吸收线8字缝合漏气及出血处肺组织。观察孔处常规留置胸腔闭式引流管。如果无法完成VATS,中转为胸腔镜辅助下保留肌肉小切口开胸手术(muscle-sparing thoracotomy, MST),沿原切口向后及向前切开皮肤皮下组织,长10~12 cm,并游离皮下组织,沿背阔肌前缘进行游离并向后牵开背阔肌,沿前锯肌肌纤维走行方向延长切开前锯肌及肋间肌,以中、小开胸器十字撑开,胸腔镜辅助下继续行胸膜纤维板剥脱术。
2 结果
4例(12.9%)由于脏层纤维板过厚,与肺组织粘连紧密,剥离困难,且剥离过程中肺组织损伤严重,出血较多,中转为胸腔镜辅助下MST。手术时间120~185 min,(145±42)min;术中出血量(380±100)ml;术后胸腔闭式引流管留置时间4~16 d,(9.5±5.8)d。术后肺持续漏气>7 d 1例,胸腔积液>7 d 1例,均经持续胸腔闭式引流后治愈。术后住院(14.0±1.5)d,出院前常规胸片检查显示患侧脓腔基本消失。术后病理:结核性脓胸9例,化脓性脓胸14例,感染性血胸2例,无法明确病因6例。31例术后随访时间3~6个月,平均4.5月,1例结核性脓胸术后4周再次出现中等量胸腔积液,经胸腔穿刺引流治疗后治愈,其余患者未见脓胸复发。
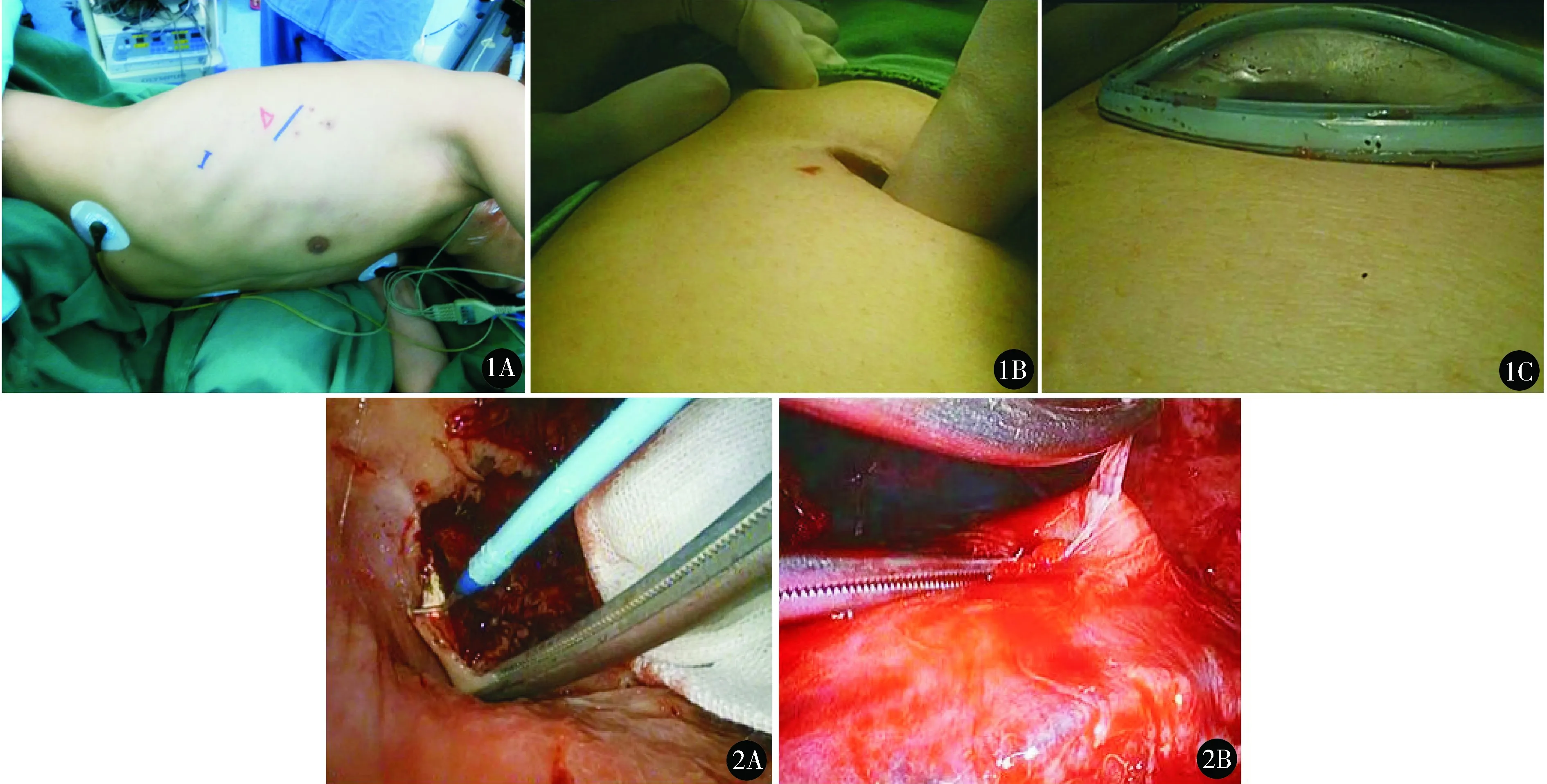
图1 A.体位及切口;B.主操作口以食指胸膜外钝性分离;C.放入切口保护套 图2 A.切除壁层纤维板;B.切除脏层纤维板
3 讨论
1998年Striffeler等[4]报道将VATS应用于脓胸的治疗,目前,采用VATS治疗脓胸已逐渐被广大胸外科医师所接受。但并不是所有脓胸都适用于VATS,部分机化晚期的脓胸仍需传统开胸胸膜纤维板剥脱术。一般认为脓胸的分期不同治疗方法也不同,因此,大部分胸外科医师认为脓胸的分期对选择脓胸的治疗方法具有一定的指导意义。
脓胸是一个逐步发展的过程,为指导各期脓胸的治疗,美国胸科协会(American Thoracic Society, ATS)根据脓胸的自然病程对脓胸进行病理分期,将其分为急性渗出期(急性期,Ⅰ期)、纤维素期(亚急性期,Ⅱ期)以及机化期(慢性期,Ⅲ期)[5]。美国胸科医师协会(American College of Chest Physician, ACCP)根据脓胸患者预后不良的相关风险将其进行分期[6]。也有学者认为除病程对胸膜病变的影响外,不同的病因以及致病因素的量对胸膜病变也存在不同影响,主张按照脓胸形成的不同病因来选择治疗方式[7]。由此可见,脓胸的病理生理转变过程受到多个因素的影响,病理分期界限不是非常明显,临床上也不乏病程很短但术中发现已形成增厚纤维板的病例,或纤维板虽厚,但与肺组织或者胸壁结合疏松。因此,仅依靠自然病程来进行脓胸的分期并指导治疗存在一定的片面性,需要结合影像学(包括胸部CT、B超及胸片)、病因、引流液的性状以及术中探查情况等因素来进行判断,所以有时脓胸的分期对胸腔镜手术的应用并没有直接的影响[8],各期脓胸都可以尝试VATS,且取得了一定的疗效[9,10]。韦鸣等[3]报道应用VATS最多的是亚急性期脓胸,还有部分机化早期的慢性脓胸也适合VATS。在手术方式的选择上,选择单纯胸腔镜或胸腔镜辅助小切口进行手术都是可行的。
本组27例完成改良胸腔镜下胸膜纤维板剥脱术,手术时间、出血量、中转开胸率、术后胸腔闭式引流时间、围手术期并发症等临床指标与Tong等[11]和金明华等[12]报道的基本一致,显示本术式安全可靠,在操作流程上具有可行性。本组4例中转为胸腔镜辅助下MST,表明胸腔镜技术不论如何改良,都存在一定局限性,仍然不能完全替代开胸手术。
本改良术式的要点:①操作切口位于第6肋间隙腋后线前后,靠后、外、下,位于脓腔所在处的中心,实际上是一个缩小的开胸手术切口;②操作口长约4 cm左右,体位为折刀位,壁层纤维板剥脱后肋间隙变宽,经切口保护套撑开后,切口操作空间变大,可同时放置3种以上手术器械进行操作,常规手术器械也可使用。本改良术式与传统VATS不同之处:①操作流程上与常规开胸手术类似,首先,切开操作口,以手指进行胸膜外剥离形成胸膜外腔隙后再切开观察孔,避免传统VATS首先做操作孔时因胸膜腔闭锁可能造成的肺组织及膈肌等脏器损伤。②进行胸膜纤维板剥脱时,将病变壁层胸膜及纤维板连续完整切除,其操作便利性不亚于常规开胸手术。③切口选择上,与传统VATS相比切口数量更少,与传统开胸手术有相似之处,而且易于中转为MST。
综上所述,本术式一方面在手术切口选择、操作流程以及病灶切除彻底性上更接近常规开胸手术,具有开胸手术的优势;另一方面,切口小、切口数量少,胸壁的完整性得以保留,且胸腔镜下操作视野更广阔,纤维板剥脱彻底,具有微创手术的特点,是微创手术与传统开胸手术的结合,兼具两者的优点,因此,可以将本术式理解为胸腔镜辅助微创小切口开胸的胸膜纤维板剥脱术,该术式扩大了脓胸的VATS适应证,各期脓胸都可尝试该术式。
1 Chambers A, Routledge T, Dunning J, et al. Is video-assisted thoracoscopic surgical decortication superior to open surgery in the management of adults with primary empyema? Interact Cardiovasc Thorac Surg, 2010,11(2):171-177.
2 黄 镇,张 奕,黄荣智,等.电视胸腔镜手术治疗脓胸的体会.齐齐哈尔医学院学报,2014,35(3):355-356.
3 韦 鸣,廖 勇,黄喜峰,等.电视胸腔镜胸膜纤维板剥脱术治疗机化初期脓胸.微创医学,2010,5(4):324-326.
4 Striffeler H, Gugger M, Im Hof V, et al. Video-assisted thoracoscopic surgery for fibrinopurulent pleural empyema in 67 patients. Ann Thorac Surg,1998,65(2):319-323.
5 Lee SF,Lawrence D,Booth H,et al.Thoracic empyema: current opinions in medical and surgical management. Curr Opin Pulm Med,2010,16(3):194-200.
6 Hecker E, Hamouri S, Müller E, et al. Pleural empyema and lung abscess: current treatment options. Zentralbl Chir,2012,137(3):248-256.
7 Hecker E, Hecker HC, Hecker KA. Pleural empyema treatment strategies in light of etiology. Zentralbl Chir,2013,138(3):353-377.
8 Cameron RJ. Management of complicated parapneumonic effusions and thoracic empyema. Int Med J,2002,32(8):408-414.
9 Davies HE, Davies RJ, Davies CW. Management of pleural infection in adults: British Thoracic Society Pleural Disease Guideline 2010. Thorax,2010,65(Suppl 2):S41-S53.
10 Bender MT, Ferraris VA, Saha SP. Modern management of thoracic empyema. South Med J, 2015, 108(1):58-62.
11 Tong BC, Hanna J, Toloza EM, et al. Outcomes of video-assisted thoracoscopic decortication. Ann Thorac Surg,2010, 89(1):220-225.
12 金明华,王 伟,王传庆,等.电视胸腔镜脓胸廓清术治疗结核性脓胸.中国微创外科杂志,2012,12(6):524-526.
(修回日期:2016-08-02)
(责任编辑:李贺琼)
Treatment of Chronic Empyema with Modified Decortication of Pleural Fibreboard Under Video-assisted Thoracoscopic Surgery: Report of 31 Patients
DengYongjun,LiuHuanpeng,YuYinghong,etal.
DepartmentofThoracicSurgery,TheFourthAffiliatedHospitalofKunmingMedicalUniversity,Kunming650021,China
Correspondingauthor:DengYongjun,E-mail:thoraces@163.com
Objective To explore the clinical application of modified decortication of pleural fibreboard with video-assisted thoracoscopic surgery (VATS) for chronic empyema. Methods From October 2013 to November 2015, a total of 31 cases of chronic empyema were treated with modified decortication of pleural fibreboard under two-trocar VATS. Firstly an operating incision about 4 cm in length was made and the fiber plate of the wall layer was separated from the pleural surface. Then an enlarged gap was formed from pleural atresia. Finally an observation hole about 1.5 cm in length was made and the thoracoscope was put into the thoracic cavity to strip the fiber board. Results The modified decortication of pleural fibreboard under VATS was successfully performed in 27 cases, while conversions to video-assisted muscle-sparing thoracotomy was required in 4 cases because of close adhesion between the fiber board and the lung tissue due to long course of disease. The operation time was 120-185 min (145±42 min), the blood loss was (380±100) ml, and the time of thoracic drainage was 4-16 days (10±6 days). Persistent lung leakage for more than 7 days happened in 1 case. Pleural effusion for more than 7 days occurred in 1 case. The length of postoperative hospital stay was (14.0±1.5) days. All the patients were followed up for 3-6 months, and 1 patient was found with middle amount of pleural effusion and the rest of these patients had no empyema recurrence. Conclusion The modified method of decortication of pleural fibreboard under two-trocar VATS is feasible in the treatment of chronic empyema.
Video-assisted thoracoscopy; Decortication of pleural fibreboard; Chronic empyema
A
1009-6604(2016)11-1009-04
10.3969/j.issn.1009-6604.2016.11.014
2016-03-07)
* 通讯作者,E-mail:thoraces@163.com

