顺序注射阻抑动力学光度法测定环境水样中的对苯二酚
吴春来,王涛,张士苹,樊静,
1. 河南师范大学环境学院 河南省环境污染控制重点实验室 黄淮水环境与污染防治教育部重点实验室,新乡 453007 2. 洛阳理工学院环境工程与化学学院,洛阳 471023
顺序注射阻抑动力学光度法测定环境水样中的对苯二酚
吴春来1,2,王涛1,张士苹1,樊静1,
1. 河南师范大学环境学院 河南省环境污染控制重点实验室 黄淮水环境与污染防治教育部重点实验室,新乡 453007 2. 洛阳理工学院环境工程与化学学院,洛阳 471023
在酸性条件下,利用对苯二酚能够阻抑碱性藏花红和溴酸钾反应的原理,联用顺序注射分析技术建立了快速测定环境水样中对苯二酚的新方法。在最佳实验条件下,对苯二酚的线性范围为0.05~1.50 μg·mL-1,检出限为0.02 μg·mL-1,完成一次分析循环总的试剂消耗仅为0.125 mL。该方法用于自来水、地表水和河水中对苯二酚的测定,结果与HPLC法所得结果对照,无显著性差异。
对苯二酚;环境水样;顺序注射;动力学光度法
Received 24 November 2015 accepted 29 December 2015
对苯二酚又名氢醌,属于不挥发性酚,是一种重要的化工原料,广泛应用于显影剂、合成染料、合成氨助溶剂、橡胶防老剂、涂料和香精中的抗氧化剂和稳定剂等[1]。对苯二酚具有一定的毒性且难降解,不仅污染环境,而且会对人体的肝、肾、造血系统、中枢系统造成损害,当2个羟基被氧化成氢醌,会造成更大的损害[2]。对苯二酚是环境和食品等领域重点检测的有机污染物,而且酚类化合物也被各国政府列为优先控制污染物。因此,建立环境中痕量对苯二酚的测定具有重要意义。
目前用来测定对苯二酚的方法主要有分光光度法[3]、荧光法[4]、色谱法[5-6]、电化学法[7-8]和化学发光法[9]等。色谱法虽然灵敏度高,检出限低,但是仪器价格较贵,测定成本高;分光光度法和荧光法等操作繁琐,测定效率低。
顺序注射分析是由Ruzicka和Marshall[10]于1990年提出的,作为第二代流动注射分析,硬件简单可靠,技术更加成熟,具有分析速度快、试剂消耗少、稳定性好等优点。由于顺序注射可以在非平衡状态下检测的特性,已广泛应用于化学分析等领域。研究发现,在酸性条件下,对苯二酚能够抑制溴酸钾氧化碱性藏花红的反应,利用顺序注射可以在非平衡态检测的优势,建立了一种快速、简便检测对苯二酚的新方法。
1 实验部分(Experiment)
1.1 仪器和试剂
FIAlab-3500顺序注射分析仪(FIAlab Instruments Inc. USA);2.5 mL注射泵,八通道选择阀。储存管为0.7 mm×200 cm,反应管为0.5 mm×90 cm,其他聚四氟乙烯管均为0.5 mm内径。系统由计算机程序控制,采用FIAlab软件(FIAlab 5.0E)进行数据采集和处理。USB2000-UV/VIS分光光度计(Analytical Instruments Inc. USA);10 mm长的光纤SMAZ型流通池。
对苯二酚(Hyd)标准溶液:用对苯二酚配制成1.0 g·L-1的储备液,使用时逐级稀释成所需的浓度;溴酸钾溶液:0.17 mol·L-1;碱性臧花红溶液:1×10-4mol·L-1;盐酸:0.6 mol·L-1。
实验所用试剂均为分析纯,水为二次蒸馏水。

图1 顺序注射分析系统 注:C,载流;SP,注射泵;SV,注入阀;MV,多位选择阀;HC,储存管;RC,反应管;R1,碱性藏花红-溴酸钾混合溶液;R2,盐酸;S,样品溶液;ZFC,Z-流通池;VIS,可见光检测器;DET,检测器;W,废液;PC,电脑。Fig. 1 Sequence injection analysis system Note: C, carrier; SP, syringe pump; SV, syringe pump valve; MV,multi-position valve; HC, holding coil; RC, reaction coil; R1, Safranine and KBrO4; R2, HCl; S, samples; ZFC, Z- flow cell; VIS, Visible light detector; DET, detector; W, waste; PC, personal computer.

表1 顺序注射控制程序
注:a,多位选择阀;b,注入阀;c,“+” 为吸入,“-”为推出。
Note: a, Multi bit selector valve; b, Injection valve; c, “+” stands for injection, “-” stands for push off.
1.2 实验方法
顺序注射分析系统的流路示意图如图1。实验操作步骤如下:首先经注射泵吸入一定体积的去离子水作为载流,然后通过八通道选择阀依次吸入碱性藏花红和溴酸钾的混合溶液、样品溶液(空白或标准溶液)、盐酸进入到储存管中,然后反方向经反应管推至检测器,在波长517 nm处分别测量非阻抑体系和阻抑体系的吸光度A0和A,计算ΔA=A- A0。顺序注射分析控制程序如表1,利用八通道选择阀,通过程序设计控制上述操作,可以连续测定多份样品,如图2所示,进样频率为50 h-1。

图2 程序控制流程图 注:S0,试剂空白;S1,0.5 μg·mL-1 的Hyd;S2,1.0 μg·mL-1 的Hyd;S3,1.5 μg·mL-1 的Hyd。Fig. 2 The flow chart for system controlNote: S0, reagent blank; S1, 0.5 μg·mL-1 of Hyd; S2, 1.0 μg·mL-1 of Hyd; S3, 1.5 μg·mL-1 of Hyd.
2 结果与讨论(Result and discussion)
为了使反应体系的灵敏度最高,必须对影响反应的各因素进行优化。我们采用单因素变换法对反应体系所用的试剂和顺序注射流路参数进行了优化。反应试剂的影响包括参加反应的各试剂的浓度和体积,顺序注射参数包括储存管和反应管内径和长度、流速和推出体积的影响等。
2.1 顺序注射参数的优化
2.1.1 试样注入顺序的影响
由于顺序注射分析系统是按照一定顺序吸取试剂和样品溶液到储存管中,因此不同的进样顺序就会导致区带之间相互渗透的程度不同,从而影响反应的灵敏度。本实验研究了多种区带对灵敏度的影响,发现碱性藏花红-溴酸钾混合溶液、盐酸、样品这3个区带进样时体系的峰型较好。对这3个区带的不同进样顺序进行了研究,结果发现,当加入顺序依次为碱性藏花红-溴酸钾混合溶液、样品、盐酸时,反应的灵敏度最好。
2.1.2 储存管和反应管的影响
管长和管径影响试剂和试样的重叠分散程度,从而影响体系的灵敏度。比较了内径分别为0.5 mm和0.7 mm两种储存管对体系灵敏度的影响,结果表明0.7 mm的储存管灵敏度更好。因此本实验选用内径为0.7 mm长度为200 cm的储存管。又考察了反应管内径和长度对体系灵敏度的影响。当选用内径为0.5 mm的反应管时,体系的灵敏度更大。在50~110 cm范围内研究了长度的影响,如图3所示,随着反应管长度的增加,体系的ΔA先增加后减小,当长度为90 cm时,ΔA最大,故实验选用内径为0.5 mm长度为90 cm的反应管。
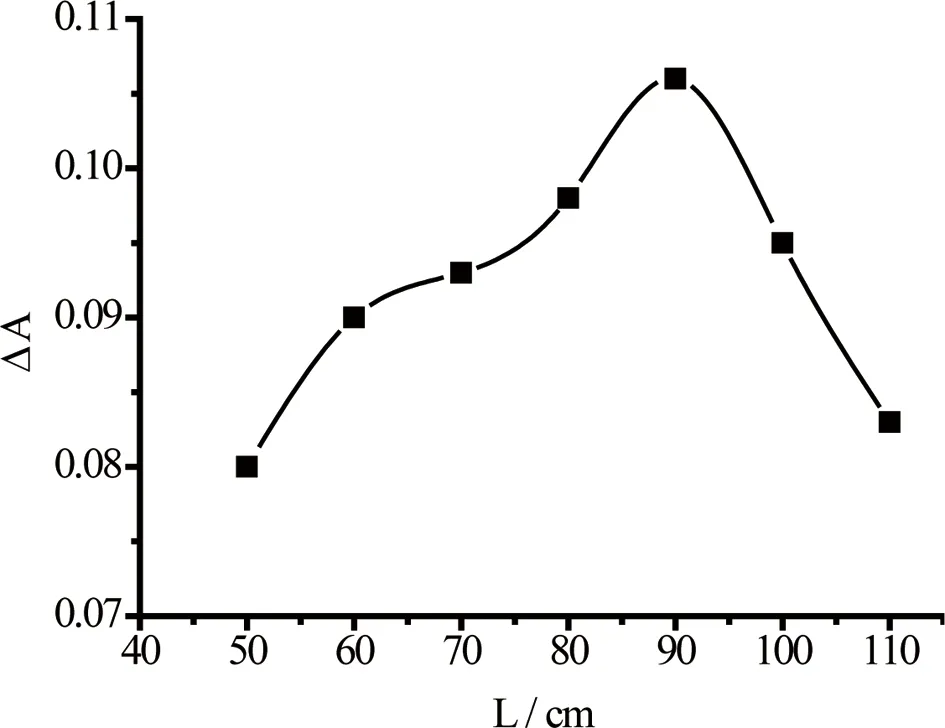
图3 反应管长度的影响 注:碱性藏花红,2.0×10-4 mol·L-1;KBrO3,0.17 mol·L-1;HCl,0.60 mol·L-1;Hyd,0.5 μg·mL-1。Fig. 3 Effect of length of reaction tubeNote: Safranine, 2.0×10-4 mol·L-1; KBrO3, 0.17 mol·L-1; HCl, 0.60 mol·L-1; Hyd, 0.5 μg·mL-1.
2.1.3 流速的影响
在顺序注射系统中,流速是一个重要的参数,它影响着试剂在管道中的留存时间以及各试剂区带之间相互渗透的程度,从而影响反应时间和反应的进行程度。从物理因素考虑,要尽量减少分散所产生的稀释效应而导致的吸光度降低,此时要增加流速;从化学因素考虑,要加大混合程度以利于反应产物的形成,此时要降低流速。合适的流速是这两种因素综合作用的结果。本实验在20~50 μL·s-1范围内考察了不同流速对体系灵敏度的影响,如图4所示,当流速为30 μL·s-1时,灵敏度最好。所以试验选取30 μL·s-1作为反应的最佳流速。

图4 流速的影响 注:碱性藏花红,2.0×10-4 mol·L-1;KBrO3,0.17 mol·L-1;HCl,0.60 mol·L-1;Hyd,0.5 μg·mL-1。Fig. 4 Effect of flow rate Note: Safranine, 2.0×10-4 mol·L-1; KBrO3, 0.17 mol·L-1; HCl, 0.60 mol·L-1; Hyd, 0.5 μg·mL-1.

图5 推出体积的影响 注:碱性藏花红,2.0×10-4 mol·L-1;KBrO3,0.17 mol·L-1;HCl,0.60 mol·L-1;Hyd,1.0 μg·mL-1。Fig. 5 Effect of sample volume Note: Safranine, 2.0×10-4 mol·L-1; KBrO3, 0.17 mol·L-1; HCl, 0.60 mol·L-1; Hyd, 1.0 μg·mL-1.
2.1.4 推出体积的影响
在500-~800 μL内考察了推出体积对灵敏度的影响,如图5所示,当推出体积为750 μL时,ΔA最大,表明此时试剂和样品已充分混合并反应。因此,实验选择750 μL为最佳推出体积。

图6 溴酸钾浓度的影响 注:碱性藏花红,2.0×10-4 mol·L-1;HCl,0.60 mol·L-1;Hyd,0.5 μg·mL-1。Fig. 6 Effect of the concentration of potassium bromate Note: Safranine, 2.0×10-4 mol·L-1; HCl, 0.60 mol·L-1; Hyd, 0.5 μg·mL-1.

图7 盐酸浓度的影响 注:碱性藏花红,2.0×10-4 mol·L-1;KBrO3,0.17 mol·L-1;Hyd,1.0 μg·mL-1。Fig. 7 Effect of the concentration of HClNote: Safranine, 2.0×10-4 mol·L-1; KBrO3, 0.17 mol·L-1; Hyd, 1.0 μg·mL-1.
2.2 反应试剂参数的优化
2.2.1 碱性藏花红-溴酸钾浓度的影响
碱性藏花红是指示剂,它的浓度对吸光度值有直接影响。本文研究发现,随着碱性藏花红浓度的增加,体系的吸光度值一直增大,但浓度过大时,阻抑反应的吸光度值就超出了仪器的线性响应范围,综合考虑选择藏花红的浓度为2.0×10-4mol·L-1。固定藏花红的浓度后,考察了溴酸钾浓度在0.1~0.2 mol·L-1范围内体系的相对吸光度值变化,如图6,当溴酸钾浓度为0.17 mol·L-1时,体系的ΔA最大,故实验选择碱性藏花红的浓度为2.0×10-4mol·L-1,溴酸钾的浓度为0.17 mol·L-1。
2.2.2 反应介质及浓度的影响
分别考察了同浓度的硫酸、盐酸、硝酸、磷酸、醋酸对反应体系灵敏度的影响,结果表明在盐酸中对苯二酚的阻抑作用最明显,重现性最好。本实验选用盐酸作为反应介质,在0.4~0.8 mol·L-1浓度之间考察了酸度对灵敏度的影响,如图7所示。当浓度为0.6 mol·L-1时,ΔA达到最大,故实验选用0.6 mol·L-1的盐酸溶液作为反应酸度。

图8 反应试剂体积的影响 注:a盐酸溶液; b, 碱性藏花红-溴酸钾混合溶液; c,样品溶液。碱性藏花红,2.0×10-4 mol·L-1;KBrO3,0.17 mol·L-1;HCl,0.60 mol·L-1;Hyd,1.0 μg·mL-1。Fig. 8 Effect of the volume of reaction regent Note: a, HCl; b, Safranine and KBrO4; c, samples; Safranine, 2.0×10-4 mol·L-1; KBrO3, 0.17 mol·L-1; HCl, 0.60 mol·L-1; Hyd, 1.0 μg·mL-1.

图9 对苯二酚标准工作曲线 注:碱性藏花红,2.0×10-4 mol·L-1;KBrO3,0.17 mol·L-1;HCl,0.60 mol·L-1。Fig. 9 Standard working curve for hydroquinone Note: Safranine, 2.0×10-4 mol·L-1; KBrO3, 0.17 mol·L-1; HCl, 0.60 mol·L-1.
2.2.3 各试剂体积的影响
在不同的范围内分别考察了碱性藏花红-溴酸钾混合溶液、盐酸溶液、样品吸入体积对体系灵敏度的影响,结果如图8所示,当吸入碱性藏花红-溴酸钾混合溶液45 μL、盐酸溶液30 μL、样品溶液50 μL时,体系的灵敏度最好,因此选用上述体积作为反应的最佳体积。
2.3 工作曲线和精密度
在上述最佳实验条件下绘制工作曲线,如图9所示,对苯二酚的质量浓度在0.05~1.50 μg·mL-1范围内与ΔA呈线性关系,其线性回归方程为ΔA=0.07893+0.07762C(μg·mL-1),检出限(3Sb/斜率,Sb为11份空白溶液的的标准偏差)为0.02 μg·mL-1,对浓度为0.5 μg·mL-1和1.0 μg·mL-1的对苯二酚溶液进行了11次平行测定,其相对标准偏差分别为1.79%和2.13%。

表3 样品中对苯二酚的测定结果(n=5)
2.4 共存离子和化合物的影响

2.5 样品分析
用玻璃器皿取自来水、地表水和雨水样品。准确移取250 mL水样按上述方法进行蒸馏,然后准确量取一定量馏出液按1.2方法测定,3种水样品中均未检测出对苯二酚,然后在上述实际水样中进行加标回收实验,结果见表3,经t检验表明2种方法无显著性差异。
本实验将灵敏度较高的动力学分析方法联合顺序注射分析系统,建立了一种快速简便测定痕量对苯二酚的新方法,通过实验得到以下结论:
(1)方法简便快速,自动化程度高,减少了人为操作可能带来的误差,每小时可测定50个样品;
(2)直接排除了大多数共存物的影响,选择性高;
(3)试剂消耗少,每次分析仅消耗0.125 mL试剂,对环境二次污染小。
[1] Zhang H Q, Huang Y H, Hu S R, et al. Self-assembly of graphitic carbon nitride nanosheets-carbon nanotube composite for electrochemical simultaneous determination of catechol and hydroquinone [J]. Electrochimica Acta, 2015, 176: 28-35
[2] Huang Y H, Chen J H, Sun X, et al. One-pot hydrothermal synthesis carbon nanocages-reduced graphene oxide composites for simultaneous electrochemical detection of catechol and hydroquinone [J]. Sensors and Actuators B: Chemical, 2015, 212: 165-173
[3] Khoshneviszadeh R, Bazzaz B S F, Housaindokht M R, et al. UV spectrophotometric determination and validation of hydroquinone in liposome [J]. Iranian Journal of Pharmaceutical Research, 2015, 14: 473-478
[4] Ni P J, Dai H C, Li Z. Carbon dots based fluorescent sensor for sensitive determination of hydroquinone [J]. Talanta, 2015, 144: 258-262
[5] Abbas S S, Elghobashy M R, Lories I, et al. Stability-indicating chromatographic determination of hydroquinone in combination with tretinoin and fluocinolone acetonide in pharmaceutical formulations with a photodegradation kinetic study [J]. RSC Advances, 2015, 5: 43178-43194
[6] Xu S J, Chen F N, Deng M, et al. Simple simultaneous determination of butylated hydroquinone (TBHQ) and butylated hydroxyanisole (BHA) antioxidants in oil using high-performance liquid chromatography with chemiluminescence detection [J]. Luminescence, 2014, 29: 1027-1032
[7] Huang Y H, Chen J H, Ling L J, et al. Simultaneous electrochemical detection of catechol and hydroquinone based on gold nanoparticles@carbon nanocages modified electrode [J]. Analyst, 2015, 140: 7939-7947
[8] Zhou J, Li X, Yang L L, et al. The Cu-MOF-199/single-walled carbon nanotubes modified electrode for simultaneous determination of hydroquinone and catechol with extended linear ranges and lower detection limits [J]. Analytica Chimica Acta, 2015, 29: 57-65
[9] Wang Z C, Tang Y H, Hu H, et al. Chemiluminescence detection of hydroquinone with flow-injection analysis of luminol-hydrogen peroxide system catalyzed by Jacobsen's catalyst [J]. Journal of Luminescence, 2014, 145: 818-823
[10] Ruzicka J, Marshall G D. Sequential injection: A new concept for chemical sensors, process analysis and laboratory assays [J]. Analytica Chimica Acta, 1990, 237: 329-343
[11] 黄志勇, 陈国树, 彭在姜. 阻抑动力学光度法测定痕量间苯二酚[J]. 分析化学, 1998, 26(11): 1298-1302
Huang Z Y, Chen G S, Peng Z J.Inhibitory kinetic -spectrophotometric determination of trace resorcinol [J]. Chinese Journal of Analytical Chemistry, 1998, 26(11): 1298-1302 (in Chinese).
◆
Inhibition Kinetic Spectrophotometric Determination of Hydroquinone in Environmental Water Samples by Sequential Injection
Wu Chunlai1,2, Wang Tao1, Zhang Shiping1, Fan Jing1,*
1. School of Environment, Henan Normal University, Henan Key Laboratory for Environmental Pollution Control, Key Laboratory for Yellow River and Huai River Water Environment and Pollution Control, Ministry of Education, Xinxiang 453007, China 2. School of Environmental Engineering and Chemistry, Luoyang Institute of Science and Technology, Luoyang 471023, China
A new method for rapid determination of trace hydroquinone in environmental water samples is established by coupling the inhibition effect of hydroquinone on the rate of the reaction between potassium bromate and safranine in acid medium with sequential injection technology. Different sequential injection analysis parameters such as reagent concentration, injection sequence of reagent and sample, flow speed and coexisting species effect have been investigated in detail. It is found that under the optimum conditions, the linear range for hydroquinone determination is 0.05 - 1.50 μg·mL-1, and the detection limit is 0.02 μg·mL-1. Only 0.125 mL of reagent is needed in a single analysis cycle. The method has been used for the determination of trace hydroquinone in tap water, ground water and river water samples, and the results are in good agreement with those obtained from HPLC.
hydroquinone; environmental water sample; sequential injection; kinetic inhibition spectrophotometry
10.7524/AJE.1673-5897.20151124001
国家自然科学基金(21377036);河南省科技创新杰出人才计划(144200510004);河南省软科学研究项目(102400440069)
吴春来(1979-),男,博士研究生,研究方向为环境分析化学,E-mail: chunlaiwu@126.com
*通讯作者(Corresponding author), E-mail: fanjing@htu.cn
2015-11-24 录用日期:2015-12-29
1673-5897(2016)2-749-06
X171.5
A
简介:樊静(1956-),女,教授,博士,博士生导师,主要研究方向环境分析化学,发表SCI论文90余篇。
吴春来, 王涛, 张士苹, 等. 顺序注射阻抑动力学光度法测定环境水样中的对苯二酚[J]. 生态毒理学报,2016, 11(2): 749-754
Wu C L, Wang T, Zhang S P, et al. Inhibition kinetic spectrophotometric determination of hydroquinone in environmental water samples by sequential injection [J]. Asian Journal of Ecotoxicology, 2016, 11(2): 749-754 (in Chinese)

