纳米氧化锌修饰玻碳电极–电化学法测定水中的对苯二酚与邻苯二酚
尚永辉,刘鑫雨,李子媛,谢华萍,乔姣姣,张世叶,张一驰,张恒
(咸阳师范学院化学与化工学院,陕西咸阳 712000)
邻苯二酚和对苯二酚是一种被广泛应用于化工、医药和食品等领域中的化工原料[1],由于邻苯二酚和对苯二酚均对环境有严重的危害且难以降解,已被环保部门限制排放[2–3]。邻苯二酚和对苯二酚均属于苯二酚的同分异构体,分子结构、物理性质、化学性质均十分接近,在测定过程中相互干扰难以同时准确测定[4–5],因此探索能够同时测定对苯二酚和邻苯二酚的新方法具有非常重要的现实意义。文献报道邻苯二酚和对苯二酚同时测定的方法主要有高效液相色谱法[6]、比色法[7]、紫外分光光度法[8]、荧光光谱法[9–10]等,而电化学方法可以利用修饰工作电极提高测定灵敏度、降低检出限,且操作方便,已建立了多种对苯二酚和邻苯二酚同时测定的方法[11–14]。
纳米氧化锌因其特殊的尺寸、形貌和内部结构,具有独特的物理和化学性质而被广泛应用于修饰电极[15–16]。本实验通过考察邻苯二酚和对苯二酚在纳米氧化锌修饰玻碳电极上的直接电化学行为,建立了同时测定邻苯二酚和对苯二酚的电化学新方法。
1 实验部分
1.1 主要仪器与试剂
电子天平:CH2250型,北京赛多利斯仪器系统有限公司。
电化学工作站:CHI660C型,上海辰华仪器公司。
三电极系统:纳米氧化锌修饰玻碳电极为工作电极,Hg/Hg2Cl2为参比电极,铂电极为辅助电极。
实验用水为去离子水。
实验所用其它试剂均为分析纯。
邻苯二酚溶液:1.00×10–3mol/L,准确称取0.0110 g邻苯二酚于小烧杯中,用水溶解后定量转入100 mL容量瓶中,摇匀,用水定容,保存备用。同法配制1.00×10–3mol/L对苯二酚溶液,保存备用。
1.2 修饰电极的制备及活化
玻碳电极处理:用粒径0.05 μm的Al2O3抛光粉充分抛光,依次用无水乙醇–硝酸溶液(体积比为1∶1)、二次蒸馏水超声清洗2~3 min,自然风干,备用。
氧化锌修饰电极的制备:准确称量5.0 mg纳米氧化锌粉末[17],加入1.00 mLN,N-二甲基甲酰胺(DMF),超声分散6 h。用移液器准确移取2.0 μL分散液于处理过的玻碳电极表面,以红外灯烘干,备用。
修饰电极的活化:使用循环伏安法将制作好的修饰电极在pH 3.00的B–R缓冲溶液中以50 mV/s的扫描速度,在–1.0~1.4 V区间连续扫描25个循环,使电极活化。
1.3 电化学测定
在室温(25℃)下,分别准确移取一定量的对苯二酚和邻苯二酚标准溶液于10 mL比色管中,加入3.00 mL pH 1.89的B–R缓冲溶液,定容至10.0 mL,摇匀,以三电极系统进行测定并绘制循环伏安或差分脉冲曲线。
2 结果与讨论
2.1 对苯二酚、邻苯二酚在氧化锌修饰玻碳电极上的电化学行为
准确移取2.00 mL 1.00×10–3mol/L邻苯二酚溶液于10 mL比色管中,加入3.00 mL pH 1.89的B–R缓冲溶液,定容至10 mL标线,分别采用玻碳电极和氧化锌修饰玻碳电极测定并绘制体系的循环伏安(CV)和差分脉冲(DPV)曲线,结果如图1所示。
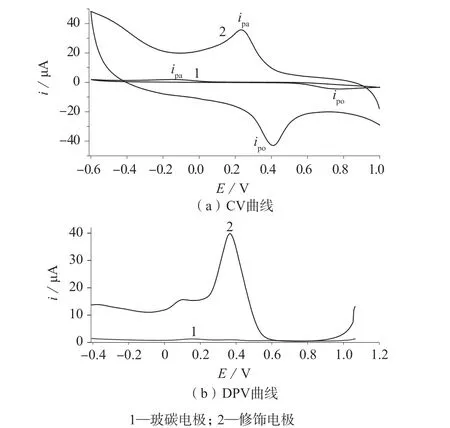
图1 对苯二酚的CV曲线及DPV曲线
由图1(a)可知,对苯二酚在玻碳电极以及纳米氧化锌修饰玻碳电极上均能产生良好的电化学信号,在修饰电极上的氧化信号、还原信号强度分别是玻碳裸电极的10倍和19倍,且在修饰电极上的氧化峰电位明显负移,还原峰电位明显正移,氧化峰与还原峰之间的电位差值(ΔE)由裸电极上的0.9139 V降到0.0840 V,氧化峰电流与还原峰电流的比值ipa/ipo由裸电极的2.37降至1.08。由图1(b)可知,对苯二酚在修饰电极上的差分脉冲(DPV)峰电流是裸电极上的188倍,表明对苯二酚在纳米氧化锌上具有更快的反应速率,且反应可逆性增强;纳米氧化锌对对苯二酚具有明显的催化效果,在纳米氧化锌修饰玻碳电极上对苯二酚的可逆性增强;
准确移取2.00 mL 1.00×10–3mol/L对苯二酚溶液于10 mL比色管中,加入3.00 mL pH 1.89的B–R缓冲溶液,定容至10 mL标线,分别采用玻碳电极和氧化锌修饰玻碳电极测定并绘制CV和DPV曲线,结果见图2。
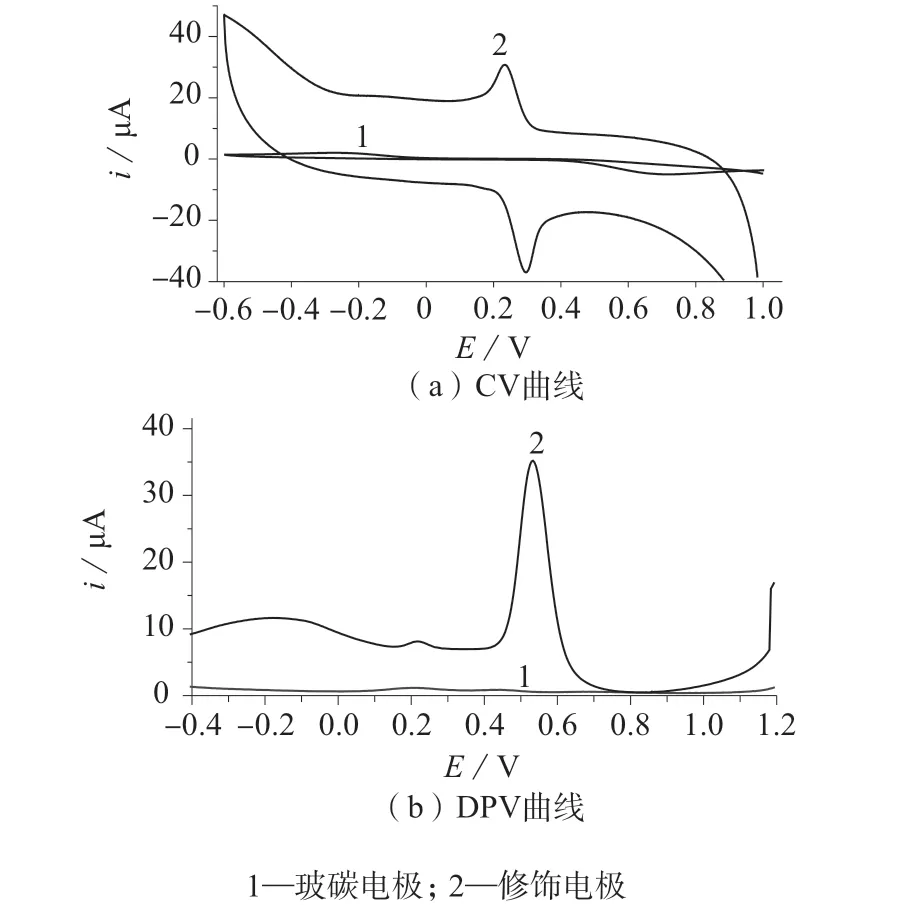
图2 邻苯二酚的CV曲线及DPV曲线
由图2(a)可知,邻苯二酚在玻碳电极以及纳米氧化锌修饰玻碳电极上也均能产生良好的电化学信号,在修饰电极上的氧化信号、还原信号强度分别是玻碳裸电极的7倍和15倍,在修饰电极上的氧化峰电位明显负移,还原峰电位明显正移,氧化峰与还原峰之间的电位差值(ΔE)由裸电极上的0.977 V降至0.063 V,氧化峰电流与还原峰电流强度比值ipa/ipo由裸电极的2.48降至1.20。由图2(b)中可知,邻苯二酚在修饰电极上的差分脉冲(DPV)峰电流强度是裸电极上的180倍,表明邻苯二酚在纳米氧化锌上具有更快的反应速率,且反应可逆性增强,说明纳米氧化锌对对苯二酚具有明显的催化效果,在纳米氧化锌修饰玻碳电极上对苯二酚的可逆性增强。
实验进一步考察了对苯二酚、邻苯二酚混合液的CV曲线和DPV曲线,结果见图3。CV曲线中对苯二酚,邻苯二酚的还原峰电位相差130 mV,氧化峰电位相差101 mV;DPV曲线中峰电位相差108 mV,且两者的谱图明显区分,可实现对苯二酚,邻苯二酚的同时测定。
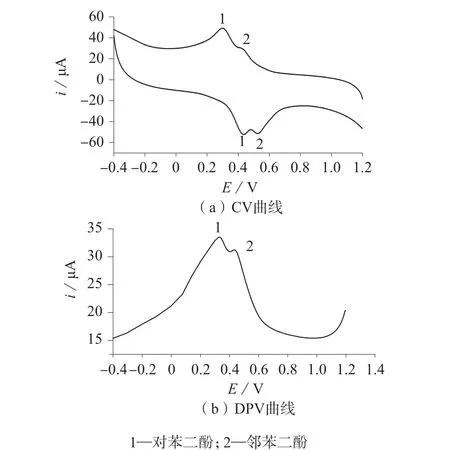
图3 对苯二酚和邻苯二酚混合物在电极上的CV、DPV曲线
纳米氧化锌修饰玻碳电极的优势,源于纳米氧化锌与碳纳米管分散均匀,羧基化的碳纳米管表面带有亲水性的羧基和羟基,能与氧化锌的氧原子结合成氢键,碳纳米管的强物理吸附能力使纳米氧化锌也能同时吸附在玻碳电极上,纳米氧化锌增大了电催化面积,从而提高了邻苯二酚和对苯二酚检测的灵敏度和修饰电极的稳定性。
2.2 邻苯二酚及对苯二酚最佳测定条件的选择
2.2.1 底液的选择
实验考察了pH 6.80的不同底液对邻苯二酚(对苯二酚)电化学行为的影响,结果见图4。
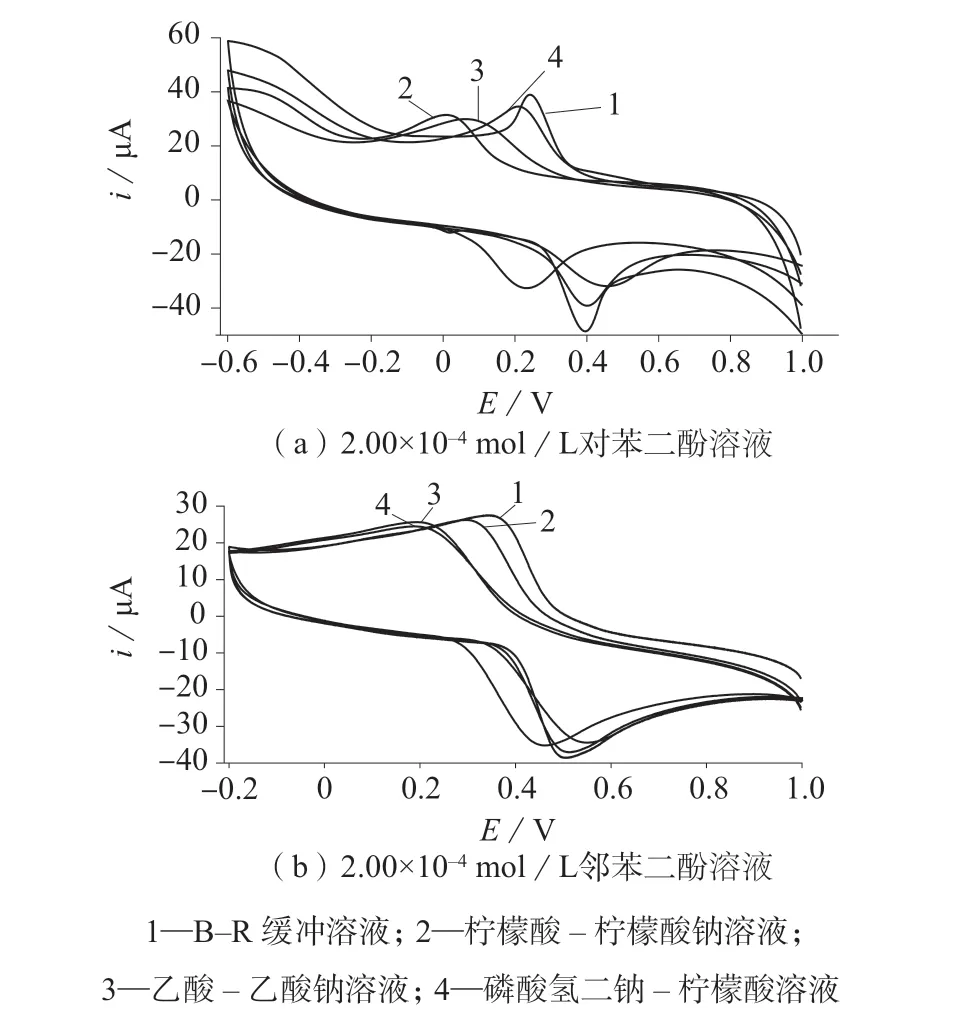
图4 对苯二酚和邻苯二酚在不同缓冲溶液中的CV曲线
根据图4对比发现,对苯二酚、邻苯二酚均在B–R缓冲液中电化学信号最为明显,因此实验选择在B–R缓冲溶液中进行测定。
2.2 pH的选择
分别考察了不同pH的B–R缓冲溶液对邻苯二酚和对苯二酚CV曲线的影响,如图5所示。
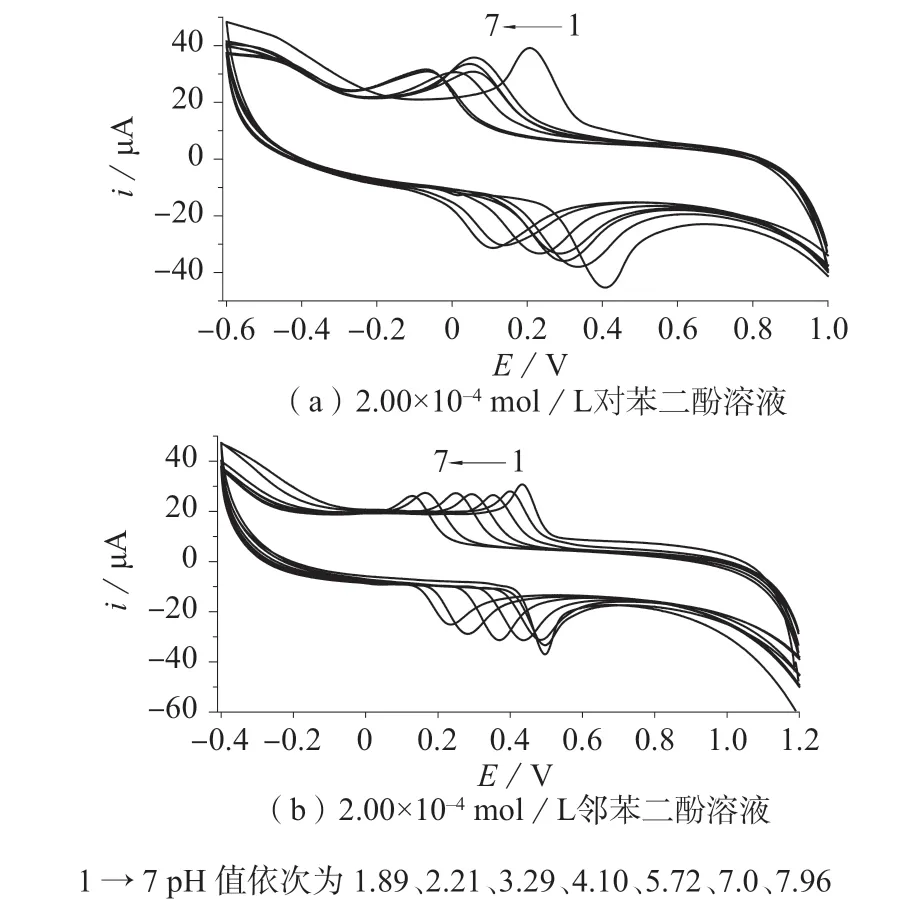
图5 不同pH值下邻苯二酚和对苯二酚的CV曲线
通过对比发现,对苯二酚、邻苯二酚氧化峰电位(EP)均随pH增加线性负移,其中对苯二酚:EP=–0.046 3pH+0.4668(r=0.996 4),邻 苯 二 酚:EP=–0.048 3pH+0.510 3(r=0.994 0),表明在电极上的反应过程均有质子参与,依据峰电位与pH之间的经验公式,Ep与pH函数关系斜率为0.059(m/n,m为质子转移数,n为电子转移数),计算得电极反应过程对苯二酚、邻苯二酚的m/n接近于1,即对苯二酚、邻苯二酚电极反应过程m=n,表明对苯二酚,邻苯二酚电极反应过程为等质子、等电子反应过程;根据对苯二酚峰电位差值(ΔE)为0.074 V,邻苯二酚峰电位差值(ΔE)为0.063 V,对于可逆体系,氧化还原峰电位之差为Epa–Epc=59 mV/n,求得对苯二酚n=0.80≈1,邻苯二酚n=0.94≈1,说明对苯二酚、邻苯二酚在纳米氧化锌修饰玻碳电极上发生单电子、单质子电极反应过程。在pH 1.89的B–R底液中对苯二酚、邻苯二酚峰电流最大,峰型最佳,实验选择pH 1.89的B–R缓冲溶液为底液。
2.2.3 扫描速率对酚类物质电化学信号的影响
在实验选择的pH 1.89的B–R底液中,考察了扫描速率对邻苯二酚、对苯二酚电化学行为的影响,结果见图6。
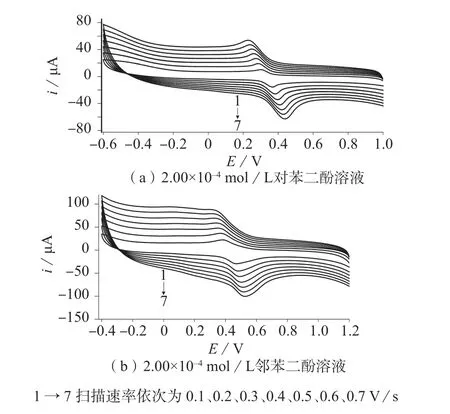
图6 不同扫描速率下对苯二酚和邻苯二酚的CV曲线
图6结果表明,实验条件下对苯二酚、邻苯二酚氧化峰电流ipo(μA)、还原峰电流ipa(μA)均与扫描速率ν(V/s)线性关系良好,对苯二酚:ipo=72.075ν+4.385 7(r=0.998 0);ipa=–78.46 4ν–9.3571(r=0.996 6);邻苯二酚:ipo=112.31ν+11.374(r=0.995 2);ipa=–117.66ν–20.534(r=0.997 6),表明对苯二酚、邻苯二酚在纳米氧化锌修饰玻碳电极上的电极反应过程主要受吸附控制[18]。
实验进一步考察了扫描次数对测定结果的影响,分别测定2.00×10–4mol/L的对苯二酚和溶液2.00×10–4mol/L邻苯二酚溶液CV曲线20次,发现随扫描次数的增加,对苯二酚和邻苯二酚的峰电位无明显变化,但氧化峰电流、还原峰电流逐渐增加至稳定;将测定过对苯二酚或邻苯二酚的电极用水冲洗后在pH 1.98的B–R缓冲的空白底液中继续扫描,发现随着扫描次数的增加,对苯二酚、邻苯二酚的电化学信号强度逐渐降低至几乎消失,进一步表明对苯二酚、邻苯二酚在纳米氧化锌修饰玻碳电极表面的电化学过程受吸附控制。
2.3 标准曲线
配制1.00×10–6~5×10–4mol/L区间的邻苯二酚(对苯二酚)标准溶液,按照实验方法进行DPV扫描。以峰电流i对邻苯二酚(对苯二酚)浓度(mmol/L)作图得到标准曲线,发现对苯二酚及邻苯二酚浓度均在1.00×10–3~0.5 mmol/L范围内与其还原峰电流i(μA)呈良好的线性关系,线性方程分别为i=0.921 9c+2.057 3(r=0.998 1,对苯二酚),i=0.540 1c+2.370 6(r=0.995 6,邻苯二酚)。以3倍信噪比(3S/N)计算得邻苯二酚、对苯二酚的检出限均为3.3×10–4mmol/L。
2.4 稳定性和重现性试验
考察了浓度均为2.00×10–4mol/L的对苯二酚和邻苯二酚溶液分别在修饰电极上的DPV信号,每隔1 h重新测定1次,结果发现对苯二酚和邻苯二酚的DPV信号至少在12h之内无显著变化。6次平行测定结果的相对标准偏差为对苯二酚样品溶液不超过4.8%,邻苯二酚样品溶液不超过5.6%,表明纳米氧化锌修饰玻碳电极性能稳定且重现性良好。
2.5 样品测定及回收试验
实验选择在渭河某段处水样,静置待杂质沉降后,依次用0.45 μm,0.22 μm滤膜过滤后,准确移取3.00 mL处理后的水样于10 mL比色管中,按照实验方法测定DPV图谱,分别带入2.3线性方程中计算对苯二酚、邻苯二酚的含量;采用标准加入法进行加标回收试验,结果如表1所示。由表1可知,对苯二酚、邻苯二酚的回收率分别为96.8%~103.0%、96.4%~104.3%,说明该方法具有较高的准确度。
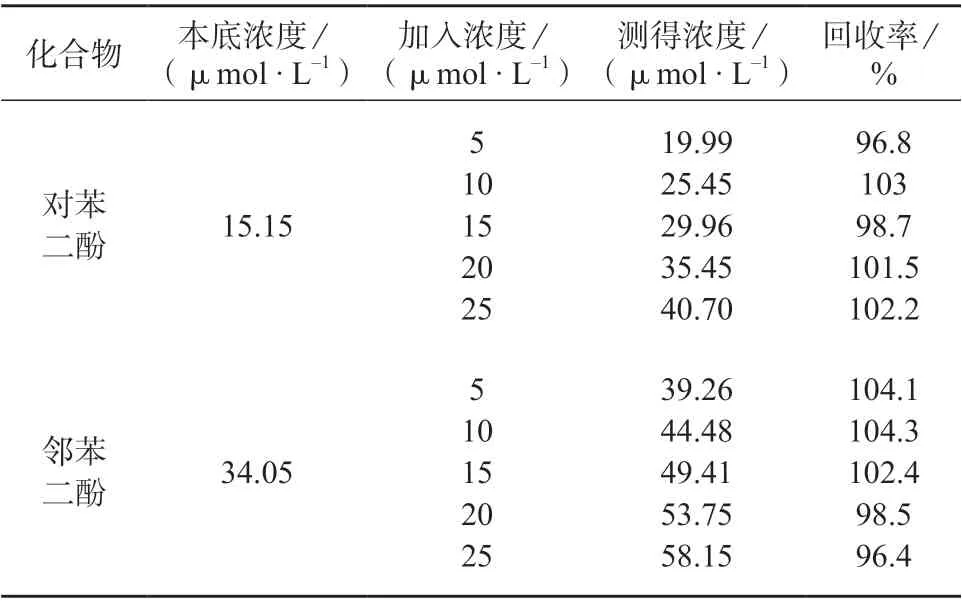
表1 加标回收试验结果
3 结语
通过考察对苯二酚和邻苯二酚在纳米氧化锌修饰玻碳电极的电化学行为,发现这两种酚类化合物均在pH 1.89的B–R缓冲溶液中具有良好的电化学信号,且峰电位有明显区别,据此建立了同时测定对苯二酚和邻苯二酚的电化学新方法。该方法灵敏度较高,样品无需特殊处理,简单快速,准确度高,可实现酚类样品的分别检测,具有重要的应用价值。

