有机污染物在碳纳米管上的吸附解吸动力学研究
卢妙杰,王 方,王中良
(天津师范大学a.天津市水资源与水环境重点实验室,b.城市与环境科学学院,天津 300387)
有机污染物在碳纳米管上的吸附解吸动力学研究
卢妙杰a,b,王 方a,王中良a,b
(天津师范大学a.天津市水资源与水环境重点实验室,b.城市与环境科学学院,天津 300387)
为了分析研究有机物在碳纳米管上的吸附/解吸动力学机理,选用原始单壁碳纳米管(r-SWNTs)和氧化单壁碳纳米管(O-SWNTs)作为吸附剂,对比了2种碳纳米管对1,3-二氯苯(1,3-DCB)、2,4-二氯酚(2,4-DCP)和硝基苯(NBZ)3种不同污染物的吸附和解吸行为.研究结果表明:与非极性有机污染物相比,极性有机污染物具有相对较快的快吸附/解吸阶段和相对缓慢的慢吸附/解吸阶段.有机污染物在氧化碳纳米管上的吸附解吸动力学速率比在原始碳纳米管上缓慢,这主要是由于碳纳米管与有机污染物间的氢键和π-π电子供受体等的特殊作用所致.研究结果对碳纳米管在废水处理中的应用具有指导意义,同时可为评价碳纳米管的环境风险提供重要的技术参考.
有机污染物;碳纳米管;吸附动力学;解吸动力学
自1991年被Iijima[1]发现,碳纳米管以其独特的物理化学性质和优异的电化学性能被广泛关注,并被大量应用于光学、电学、生物医学和传感器等领域[2-3].碳纳米管的大量生产和使用不可避免地造成这些材料进入到环境中,因此,其环境行为已经引起国内外学者的广泛关注[4-5].由于具有较高的比表面积和孔体积,碳纳米管对环境中很多有机污染物具有很强的吸附能力,可大量地富集有机污染物,并极大地改变污染物的迁移性和生物可利用性[4-6].因此,了解碳纳米管对有机污染物的吸附解吸机理对于正确评价其环境风险非常重要.
近十多年来,碳纳米管对有机污染物的吸附热力
学研究已有很多[7-11].这些研究表明,碳纳米管对多环芳烃、酚类有机物和硝基类化合物等具有很强的吸附能力,远高于环境中的溶解性有机质、粘土颗粒等环境介质[9-11].然而有关碳纳米管对有机污染物吸附动力学尤其是解吸动力学的研究还非常有限.污染物在碳纳米管上的动力学过程能够更直接地影响污染物的迁移性和生物可利用性,且其动力学过程与污染物的性质和碳纳米管的表面化学性质直接相关[12].Pan等[13]研究发现雌二醇和双酚A在碳纳米管上的吸附和解吸过程很快达到平衡,且很难从碳纳米管上解吸下来;而Sheng等[7]的研究发现污染物的硝基官能团越多,其在碳纳米管上的吸附动力学速率越慢.
为了进一步明确碳纳米管的表面化学性质与污染物的理化性质对吸附解吸动力学的影响,本研究选用原始单壁碳纳米管(r-SWNTs)和氧化单壁碳纳米管(O-SWNTs)作为吸附剂,对比了2种碳纳米管对1,3-二氯苯(1,3-DCB)、2,4-二氯酚(2,4-DCP)和硝基苯(NBZ)3种不同污染物的吸附和解吸动力学行为,旨在探索碳纳米管对有机污染物的吸附解吸机理,为评价碳纳米管的环境风险提供技术参考.
1 材料与方法
1.1 实验材料与试剂
实验所用的原始单壁碳纳米管购买自深圳市纳米港有限公司,外径≤2 nm,长5~15 μm,纯度≥95%.氧化单壁碳纳米管采用Yang等[14]的方法,用体积比为3∶1的浓硫酸和浓硝酸氧化处理原始单壁碳纳米管得到.
实验所用1,3-二氯苯(99%)、2,4-二氯酚(99%)和硝基苯(99%)均购买自SigmaAldrich公司(St.Louis,MO),其水溶解度Csat、辛醇-水分配系数KOW和酸解离常数pKa等理化性质如表1所示.
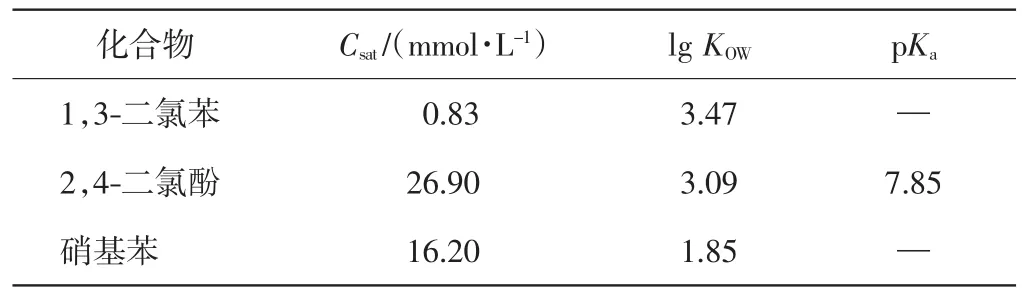
表1 1,3-二氯苯、2,4-二氯酚和硝基苯的基本理化性质Tab.1 Basic physical and chemical properties of 1,3-DCB,2,4-DCP and NBZ
表1中数据均出自文献[15].浓硫酸(分析纯)、浓硝酸(分析纯)、盐酸(分析纯)和氢氧化钠(分析纯)均购自天津市嬴达稀贵化学试剂厂,氯化钠(分析纯)购自天津市津科精细化工公司,甲醇(色谱纯)和正己烷(色谱纯)购自天津康科德科技有限公司.
1.2 实验方法
1.2.1 吸附动力学实验
采用摇瓶法进行有机污染物在碳纳米管上的吸附动力学实验,具体操作如下:准确称取100 mg碳纳米管置于200 mL玻璃反应瓶中,加入预先配制好的pH值为5的背景电解液(含0.02 mg/L NaCl和200 mg/L叠氮化钠),以保证实验条件下所有吸附质都是分子状态.润湿24 h后,用微量注射器分别加入预先配制的有机污染物甲醇储备液(甲醇加入量不超过溶液总体积的0.5%),使1,3-二氯苯、2,4-二氯酚和硝基苯的初始质量分数分别为28、100和20 mg/L,加盖密封后快速摇匀,并放入恒温摇瓶柜中以140 r/min的速度在25℃下恒温震荡,分别在0.25、0.5、1、2、4、10、24、48、72和120 h等时间点取出玻璃反应瓶,以3 000 r/min的速率离心5 min,取上清液测定其浓度. 1.2.2 解吸动力学实验
解吸动力学实验与吸附动力学实验类似.首先取吸附平衡后离心过的反应瓶,去掉90%左右的上清液,称重确定剩余的电解液重量,并计算确定剩余液体的体积;然后重新向瓶中加满不含污染物的电解液,开始进行解吸动力学实验,分别在解吸进行了0.25、0.5、1、2、4、10、24、48、72和120 h等时间点取出玻璃反应瓶,以3 000 r/min的速率离心5 min,取上清液测定其浓度.
1.3 分析方法和质量保证
实验中1,3-二氯苯的浓度采用Aglient GC 6890N型气相色谱仪自动进行分析,使用30 m×0.32 mm× 0.25 μm的J&W Scientific HP-5色谱柱和电子捕获检测器(electron capture detector,ECD).分析条件为:进样口温度为200℃;柱起始温度为80℃,保留1 min,以10℃/min的速率升温至160℃后,以50℃/min的速率升到240℃;检测器温度为300℃;高纯氮载气流速为1.0 mL/min,不分流进样.
2,4-二氯酚和硝基苯的浓度采用配备有3 mm× 100 mm SunFire C18反相柱的Merck Hitachi L-2000型高效液相色谱仪测定.测定2,4-二氯酚的流动相为水和甲醇混合液(体积比为40∶60),流速为0.4mL/min,紫外检测波长为280 nm;测定硝基苯的流动相仍为水和甲醇混合液(体积比为65∶35),流速为0.4mL/min,紫外检测波长为305 nm.
在背景电解液中添加叠氮化钠作为抑菌剂,可以避免微生物对有机污染物的降解.吸附和解吸动力学实验均在密封、避光的条件下进行,以防止有机污染
物的挥发和光降解.所有吸附和解吸动力学实验数据点为2个平行样,并设有空白对照.
1.4 数据拟合
采用两阶段一级动力学模型[12,16-17]分别对吸附动力学和解吸动力学实验数据进行拟合.此模型将污染物的吸附过程分为初始的快吸附阶段和后续的慢吸附阶段2个过程,分别使用2个一级动力学方程进行模拟,其动力学模型分别为

式(1)和式(2)中:C0(mg/L)和Ct(mg/L)分别为有机污染物在起始时刻和时间t时的水相浓度;Fr1和Fs1为有机污染物在碳纳米管上快吸附和慢吸附部分分别所占的比例;kr1(h-1)和ks1(h-1)为有机污染物在碳纳米管上快吸附和慢吸附的速率常数;q0(mg/kg)和qt(mg/ kg)分别为解吸过程中起始时刻和时间t时碳纳米管上有机污染物的固相浓度;Fr2和Fs2为有机污染物在碳纳米管上快解吸和慢解吸部分分别所占的比例;kr2(h-1)和ks2(h-1)为有机物在碳纳米管上快解吸和慢解吸的速率常数.
2 结果与讨论
2.1 碳纳米管的性质与表征
2种碳纳米管的表面元素含量、孔径结构和零电荷点等性质如表2所示.表2中碳纳米管的表面元素含量采用X线光电子能谱分析得到,BET比表面积和平均孔径由N2吸附方法测定,零电荷点由pH漂移法测定.
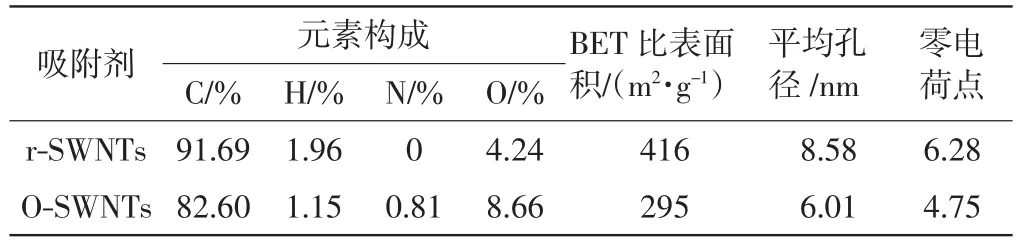
表2 r-SWNTs和O-SWNTs的元素分析、孔径分析和零电荷点分析结果Tab.2 Results of elemental analysis,pore width analysis and pHPZC analysis of r-SWNTs and O-SWNTs
由表2可知,氧化单壁碳纳米管的含氧量为8.66%,与原始单壁碳纳米管4.24%的含氧量相比明显增加,这与图1所示的傅里叶-红外光谱的测定结果一致.由图1可知,经氧化处理后,碳纳米管表面的含氧官能团增多,其—OH峰(3 450 cm-1)、—COOH峰(1 700~1 750 cm-1)、CO峰(1 550~1 650 cm-1)和C—O峰(1 450 cm-1)更为明显.

图1 r-SWNTs和O-SWNTs的傅里叶-红外光谱图Fig.1 Fourier transform infrared(FTIR)spectra of r-SWNTs and O-SWNTs
表3为碳纳米管表面官能团的含量,其中表面酸碱度采用Boehm滴定法测得,总官能团密度为总酸碱度与BET比表面积的比值.
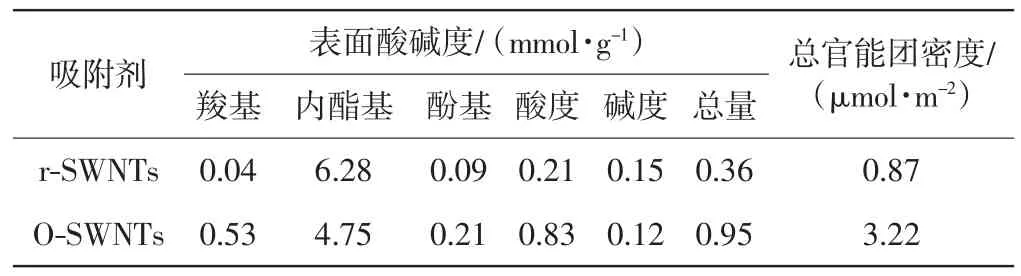
表3 r-SWNTs和O-SWNTs的表面官能团含量Tab.3 Content of surface functional group of r-SWNTs and O-SWNTs
由表3中结果可知,氧化处理后的碳纳米管的表面酸性官能团含量由0.21 mmol/g提高至0.83 mmol/g.氧化碳纳米管表面酸性官能团的增加,一方面表明了其表面含氧量的增加;另一方面也导致了氧化碳纳米管零电荷点(pHPZC)的降低.同时,氧化后碳纳米管的比表面积由416 m2/g降至295 m2/g,平均孔径由8.58 nm降至6.01nm,都明显低于原始碳纳米管.
2.2 有机污染物的吸附动力学
1,3-二氯苯、2,4-二氯酚和硝基苯3种有机污染物在原始单壁碳纳米管和氧化单壁碳纳米管上的吸附动力学的模型拟合曲线如图2所示.从图2中可以看出,3种有机物在碳纳米管上的吸附动力学均表现出明显的两阶段特征,即初始的快吸附阶段和后续的慢吸附阶段,且3种有机物在2种碳纳米管上的吸附均能很快达到平衡.
采用两阶段一级动力学模型(式(1))对3种有机污染物的吸附动力学曲线进行拟合,拟合结果如表4所示.由表4可知,3种有机物的拟合相关性系数
R2均大于0.97,说明两阶段一级动力学模型对吸附动力学数据拟合良好.此外,3种有机物在2种不同碳纳米管上拟合得到的快吸附速率常数kr1的大小顺序一致,由大到小的顺序依次为:1,3-二氯苯>2,4-二氯酚>硝基苯;而慢吸附速率常数ks1由大到小的顺序依次为:硝基苯>2,4-二氯酚>1,3-二氯苯,与快吸速率常数kr1的趋势相反,且同一种污染物对应的快吸附速率常数kr1均比慢速率吸附常数ks1高1到2个数量级.3种有机污染物在2种碳纳米管上的快吸附部分Fr1所占比例均大于相应的慢吸附部分Fs1,这说明3种有机污染物在2种碳纳米管上的吸附均以快吸附为主.对于同一种污染物,在原始碳纳米管上的快吸附速率kr1和慢吸附速率ks1均大于氧化碳纳米管,且氧化碳纳米管上的慢吸附比例Fs1更高,说明与原始碳纳米管相比,3种有机污染物在氧化碳纳米管上的吸附平衡时间相对较长.

图2 1,3-二氯苯,2,4-二氯酚和硝基苯在r-SWNTs和O-SWNTs上吸附的两阶段一级动力学模型拟合曲线Fig.2 Fitting curves of 1,3-DCB,2,4-DCP and NBZ adsorption on r-SWNTs and O-SWNTs by two-compartment first-order kinetic model
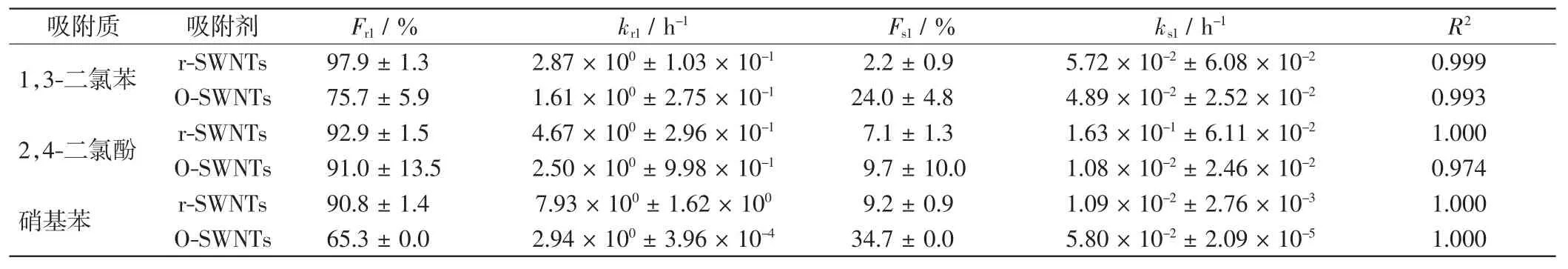
表4 1,3-二氯苯,2,4-二氯酚和硝基苯在r-SWNTs和O-SWNTs上吸附的两阶段一级动力学模型拟合参数Tab.4 Two-compartment first-order kinetic model parameters for 1,3-DCB,2,4-DCP and NBZ adsorption on r-SWNTs and O-SWNTs
2.3 有机污染物的解吸动力学
1,3-二氯苯、2,4-二氯酚和硝基苯3种有机污染物在原始单壁碳纳米管和氧化单壁碳纳米管上的解吸动力学模型拟合曲线如图3所示.由图3可以看出,与吸附动力学曲线类似,3种有机物在碳纳米管上的解吸动力学也表现出明显的两阶段特征,即初始的快解吸阶段和后续的慢解吸阶段.
采用两阶段一级动力学模型(式(2))对3种污染物的解吸动力学曲线进行拟合,结果如表5所示.由表5可知,3种有机物的拟合的相关性系数R2均大于0.99,说明两阶段一级动力学模型对解吸动力学数据进行拟合的效果良好.3种有机污染物在2种碳纳米管上拟合得到的快解吸速率常数kr2和慢解吸速率常数ks2的大小规律均与吸附动力学拟合得到的结果类似.值得注意的是,在解吸动力学中,快解吸速率常数kr2比慢解吸速率常数ks2高4到5个数量级,远大于吸附动力学中的差距.相对于吸附动力学,有机污染物在2种碳纳米管上的慢解吸部分Fs2所占比例大大提高,这说明有机污染物在碳纳米管上的解吸动力学以慢解吸为主.
2.4 吸附解吸动力学机理探讨
碳纳米管可看作由片层石墨结构卷曲而成的中空管,主要由sp2杂化碳原子构成,可以形成高度离域化的π电子共轭体系,既可以成为π电子供体,也可以成为π电子受体[10].研究表明,除疏水性作用外,碳纳米管还可通过π-π共轭作用、π-π电子供受体作用和氢键作用等极大地促进有机污染物的吸附[5].
1,3-二氯苯、2,4-二氯酚和硝基苯在2种碳纳米管上的吸附/解吸动力学速率的差异主要由有机污染物的性质决定.1,3-二氯苯不含极性官能团,
主要通过疏水作用和π电子共轭作用吸附在碳纳米管表面.而对于2,4-二氯酚,由于其羟基为供电子基团,造成与之相连的苯环上的电荷密度增加,此时碳纳米管的石墨化表面可作为π电子受体,与其发生π电子供受体作用,此外,2,4-二氯酚还可与碳纳米管上的官能团发生氢键作用,增强其在碳纳米管上的吸附[11].硝基苯的硝基为强吸电子基团,造成苯环上的电荷密度降低,因此,硝基苯可以作为π电子受体,与碳纳米管间发生π-π电子供受体作用,这大大增强了硝基苯在碳纳米管上的吸附[10].Zhang等[12]的研究结果表明,与非极性有机物相比,极性污染物普遍具有更大的快吸附速率kr和更小的慢吸附速率ks,这与本研究的结果一致.上述研究结果均表明极性有机污染物与碳纳米管的特殊作用加快了其在碳纳米管上的快吸附/解吸速率,但同时减慢了其慢吸附/解吸速率.
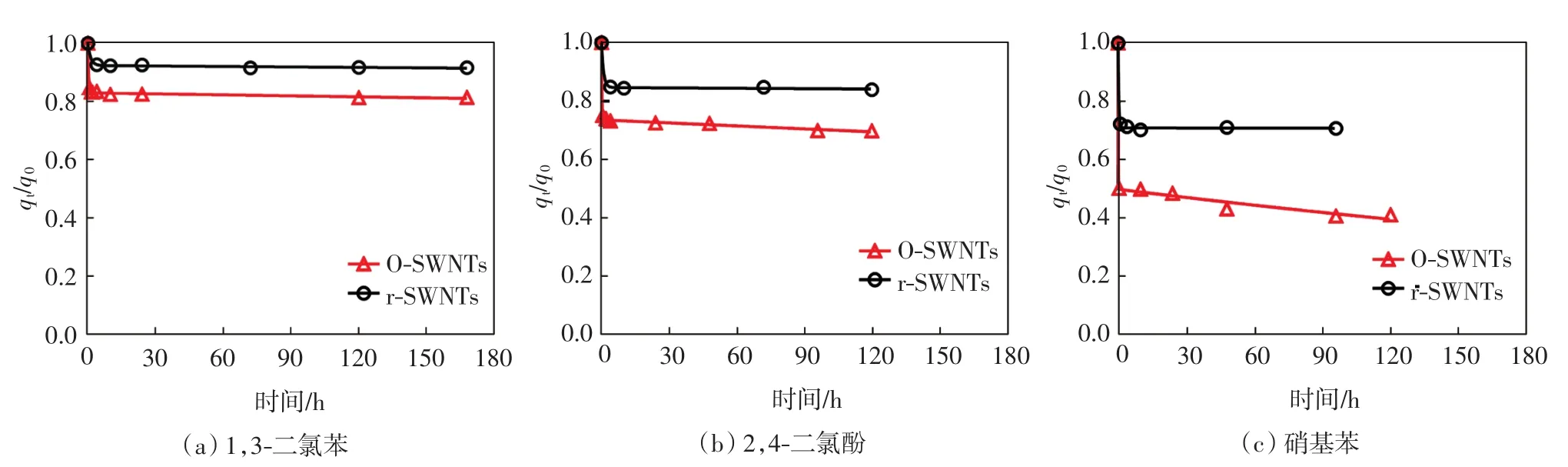
图3 1,3-二氯苯,2,4-二氯酚和硝基苯在r-SWNTs和O-SWNTs上解吸的两阶段一级动力学模型拟合曲线Fig.3 Fitting curves of 1,3-DCB,2,4-DCP and NBZ desorption on r-SWNTs and O-SWNTs by two-compartment first-order kinetic model

表5 1,3-二氯苯,2,4-二氯酚和硝基苯在r-SWNTs和O-SWNTs上解吸的两阶段一级动力学模型拟合参数Tab.5 Two-compartment first-order model parameters for 1,3-DCB,2,4-DCP and NBZ desorption on r-SWNTs and O-SWNTs
3种污染物在氧化碳纳米管上快吸附/解吸速率和慢吸附/解吸速率均有所降低,这主要是因为氧化处理后的碳纳米管的表面性质发生了化学变化.一方面,氧化碳纳米管的表面官能团间可能存在交联(cross-linking)现象[18],造成碳纳米管的比表面积和平均孔径变小,有机污染物较难进入较小的孔径或缝隙,导致吸附/解吸速率降低.另一方面,氧化处理后的碳纳米管表面引入的含氧酸性官能团为亲水性基团,使得碳纳米管本身的疏水作用减弱.同时,氧化处理破坏了碳纳米管石墨化表面完整的π键结构,影响了π电子分布,在一定程度上减弱了碳纳米管与有机污染物的π-π共轭作用,所以有机污染物在氧化碳纳米管需要更长的时间达到吸附平衡.此外,氧原子具有供电子属性,虽然氧化碳纳米管的比表面积低于原始碳纳米管,但由于极性化合物2,4-二氯酚和硝基苯本身的供电子羟基基团和吸电子硝基基团具有很强的提供电子和接受电子的能力,很容易与具有得失电子属性的碳纳米管产生电子供受体作用,因此,极性有机污染物2,4-二氯酚和硝基苯在氧化碳纳米管和原始碳纳米管上的吸附和解吸速率差小于非极性有机污染物1,3-二氯苯在氧化碳纳米管和原始碳纳米管上的吸附和解吸速率差.
3 结论
(1)有机污染物在碳纳米管上的吸附解吸动力学表现出明显的两阶段特征,即初始的快吸附/解吸阶段和后续的慢吸附/解吸阶段.
(2)两阶段一级动力学模型的拟合结果表明:极性污染物普遍具有更大的快吸附解吸速率常数和更小的慢吸附解吸速率常数;与非极性有机污染物相
比,极性有机污染物的吸附动力学速率相对缓慢,这主要是由于碳纳米管与极性有机污染物间的特殊作用所致,表明有机污染物的极性和分子结构对其吸附解吸动力学行为具有显著的影响.
(3)有机污染物在氧化碳纳米管上的吸附解吸动力学速率慢于在原始碳纳米管上的吸附解吸动力学速率,这表明吸附剂的表面化学性质对污染物的吸附解吸动力学行为具有显著影响.
[1] IIJIMA S.Helical microtubules of graphitic carbon[J].Nature,1991,354(6348):56-58.
[2]MAUTER M S,ELIMELECH M.Environmental applications of carbonbased nanomaterials[J].Environmental Science&Technology,2008,42(16):5843-5859.
[3]REN X M,CHEN C L,NAGATSU M,et al.Carbon nanotubes as adsorbents in environmental pollution management:a review[J].Chemical Engineering Journal,2011,170(2):395-410.
[4] KLAINE S J,ALVAREZ P J,BATLEY G E,et al.Nanomaterials in the environment:behavior,fate,bioavailability,and effects[J].Environ Toxicol Chem,2008,27(9):1825-1851.
[5] PAN B,XING B S.Adsorption mechanisms of organic chemicals on carbon nanotubes[J].Environmental Science&Technology,2008,42(24):9005-9013.
[6] JI L L,CHEN W,DUAN L,et al.Mechanisms for strong adsorption of tetracycline to carbon nanotubes:a comparative study using activated carbon and graphite as adsorbents[J].Environmental Science&Technology,2009,43(7):2322-2327.
[7]SHENG G D,SHAO D D,REN X M,et al.Kinetics and thermodynamics of adsorption of ionizable aromatic compounds from aqueous solutions by as-prepared and oxidized multiwalled carbon nanotubes[J]. Journal of Hazardous Materials,2010,178(1/2/3):505-516.
[8]张伟,施周,徐舜开.多壁碳纳米管吸附水中三氯苯动力学及热力学研究[J].上海环境科学,2010,29(6):231-235. ZHANG W,SHI Z,XU S K.Kinetic and thermodynamic studies on the adsorption of trichlorobenzene in water onto multiwalled carbon nanotubes[J].Shanghai Environmental Sciences,2010,29(6):231-235(in Chinese).
[9] LIN D H,XING B S.Adsorption of phenolic compounds by carbon nanotubes:Role of aromaticity and substitution of hydroxyl groups[J]. Environmental Science&Technology,2008,42(19):7254-7259.
[10]CHENW,DUANL,ZHUDQ.Adsorptionofpolar and nonpolar organic chemicalstocarbonnanotubes[J].EnvironmentalScience&Technology,2007,41(24):8295-8300.
[11]CHEN W,DUAN L,WANG L L,et al.Adsorption of hydroxyl-and amino-substituted aromatics to carbon nanotubes[J].Environmental Science&Technology,2008,42(18):6862-6868.
[12]ZHANG D M,HOU L,ZHU D Q,et al.Synergistic role of different soil components in slow sorption kinetics of polar organic contaminants [J].Environmental Pollution,2014,184:123-130.
[13]PAN B,SUN K,XING B S.Adsorption kinetics of 17α-ethinyl estradiol and bisphenol A on carbon nanomaterials.II.concentration-dependence[J].Journal of Soils Sediments,2010,10(5):845-854.
[14]YANG C M,PARK J S,AN K H,et al.Selective removal of metallic single-walled carbon nanotubes with small diameters by using nitric and sulfuric acids[J].Journal of Physical Chemistry B,2005,109(41):19242-19248.
[15]SCHWARZENBACH R P,GSCHWEND P M,IMBODEN D M.Environmental Organic Chemistry[M].New York:Wiley-Inter-Science,2003.
[16]CORNELISSEN G,RIGTERINK H,VAN NOORT P C M,et al.Slowly and very slowly desorbing organic compounds in sediments exhibit Langmuir-type sorption[J].Environmental Toxicology and Chemistry,2000,19(6):1532-1539.
[17]JOHNSON M D,KEINATH T M,WEBER W J.A distributed reactivity model for sorption by soils and sediments.14.characterization and modeling of phenanthrene desorption rates[J].Environmental Science& Technology,2001,35(8):1688-1695.
[18]ZHANG X F,SREEKUMAE T V,LIU T,et al.Properties and structure of nitric acid oxidized single wall carbon nanotube films[J].Journal of Physical Chemistry B,2004,108(42):16435-16440.
(责任编校 亢原彬)
Adsorption and desorption kinetics of organic contaminants on carbon nanotubes
LU Miaojiea,b,WANG Fanga,WANG Zhonglianga,b
(a.Tianjin Key Laboratory of Water Resources and Environment,b.College of Urban and Environmental Sciences,Tianjin Normal University,Tianjin 300387,China)
In order to study the adsorption/desorption kinetics mechanism of organic contaminants on carbon nanotubes,the raw single-walled carbon nanotubes(r-SWNTs)and oxidized single-walled carbon nanotubes(O-SWNTs)were selected as the adsorbents,1,3-dichlorobenzene(1,3-DCB),2,4-dichlorophenol(2,4-DCP)and nitrobenzene(NBZ)were selected as the adsorbates,and the adsorption/desorption behaviors of these organic contaminants on r-SWNTs and O-SWNTs were compared.The results show that the rapid adsorption/desorption stage of the polar contaminants is relatively faster than that of nonpolar contaminants,and slow adsorption/desorption stage of the polar contaminants is relatively slower than that of nonpolar contaminants.The adsorption/desorption rate of all organic contaminants on O-SWNTs are slower than those on r-SWNTs. This is likely because of the specific interaction force(H-bonding,π-π electron donor-acceptor interactions,etc.)between organic contaminants and CNTs.It is important for CNTs in their application in wastewater treatment and assessment of their environmental risk.
organic contaminants;carbon nanotubes;adsorption kinetics;desorption kinetics
X131,O64
A
1671-1114(2016)06-0023-06
2016-07-11
天津市高等学校创新团队培养计划资助项目(TD12-5037);天津师范大学博士基金资助项目(52XB1403).
卢妙杰(1992—),女,硕士研究生.
王 方(1984—),女,助理研究员,主要从事环境有机化学方面的研究.

