利用SPR检测26肽与β1-肾上腺素受体自身抗体的相互作用
董 玉 吕婷婷 徐文丽 白 燕 武 烨 刘慧荣 王 雯
(首都医科大学基础医学院生理学与病理生理学系 代谢紊乱相关心血管疾病北京市重点实验室,北京 100069)
· 心血管疾病的病理生理机制 ·
利用SPR检测26肽与β1-肾上腺素受体自身抗体的相互作用
董 玉 吕婷婷 徐文丽 白 燕 武 烨 刘慧荣 王 雯*
(首都医科大学基础医学院生理学与病理生理学系 代谢紊乱相关心血管疾病北京市重点实验室,北京 100069)
目的 探讨根据β1肾上腺素受体细胞外第二环(β1-adrenergic receptor,β1-AR-ECⅡ)的氨基酸序列合成的26肽与β1-肾上腺素受体β1-AR-ECⅡ的单克隆抗体(β1-adrenergic receptor autoantibodies,β1-AA)的相互作用。方法 根据人β1-肾上腺素受体细胞外第二环(β1-AR-ECⅡ)的氨基酸序列合成26肽;采用杂交瘤细胞融合的方法获得针对β1-AR-ECⅡ的单克隆抗体(β1-AA);利用表面等离子共振(surface plasmon resonance,SPR)检测该合成的26肽与β1-AA的亲和力;利用乳鼠心肌细胞跳动频率实验验证该合成26肽对β1-AA的中和作用。结果 提取的β1-AA可以使乳鼠心肌细胞跳动频率增加(P<0.05),提示该β1-AA具有生物学活性;合成26肽与β1-AA结合的亲和力(KD)为4.44 μmol/L,属于中等强度结合;较β1-AA组相比,26肽处理后可明显降低心肌细胞跳动频率(P<0.05)。结论 该合成26肽与β1-肾上腺素受体自身抗体之间存在相互作用,并且可以拮抗β1-AA引起的乳鼠心肌细胞跳动频率的增加。
β1-肾上腺素受体自身抗体; 26肽; 表面等离子共振
研究[1]显示,多种心血管疾病患者血清中都存在针对β1-肾上腺素受体细胞外第二环的自身抗体(β1-adrenergic receptor autoantibodies,β1-AA),这提示免疫功能的紊乱可以加速心力衰竭进程。以往研究[2-6]显示,β1-肾上腺素受体自身抗体的长期存在可以引起心功能下降、炎性反应、心肌重塑以及心律失常等,参与心力衰竭事件的发生。
针对β1-AA引起的心力衰竭,中和抗体法已成为近年研究的热点[7-9]。这种方法是基于合成特异性肽与β1-AA结合以消除其对心脏的有害刺激作用。β1-AA主要与β1-肾上腺素受体的细胞外第二环(β1-adrenergic receptor,β1-AR-ECⅡ)结合,β1-AR-ECⅡ由26个氨基酸构成。然而该类肽与β1-AA的结合特征并不清楚,因此本课题根据人β1-肾上腺素受体细胞外第二环的氨基酸序列,应用固相合成法合成26肽,通过表面等离子共振(surface plasmon resonance,SPR)检测该合成26肽与β1-AA之间的相互作用,观察两者相互结合的动力学特征,同时应用乳鼠心肌细胞跳动频率实验验证26肽对β1-AA下游激动效应的拮抗作用。
1 材料与方法
1.1 实验动物
20只SPF级健康雌性BalB/C小鼠,8周龄,体质量(20±2)g;15只SPF级健康SD大鼠的乳鼠,0~3 d,均购自北京维通利华实验动物技术有限公司,实验动物许可证号:SCXK(京)2012-0001。
1.2 主要试剂与仪器
胰蛋白酶 1∶250(Trypsin Powder, Porcine 1∶250,Sigma公司,美国);Ⅱ型胶原酶(Collagenase type 2,Worthington公司,美国);美托洛尔(Metoprolol tartrate, Abcam公司,美国); 枸橼酸钠溶液(Sodium Acetate Buffer,pH 5.5)、HBS-EP运行缓冲液以及甘氨酸盐酸缓冲液(Glycine-HCl,pH 1.5)均购自美国GE Healthcare公司。
1.3 实验方法
1)肽段的合成:根据人β1-AR-ECⅡ氨基酸序列,委托上海强耀生物科技有限公司采用固相合成多肽法合成26肽(HWWRAESDEARRCYNDPKCCDFVTNRC),运用高效液相色谱(HPLC)进行纯度检测,纯度大于98%。
2)单克隆抗体的制备:采用杂交瘤细胞融合的方法获得分泌单克隆β1-AA的杂交瘤细胞株,对杂交瘤细胞进行克隆筛选,选择1株杂交瘤细胞进行培养,按照1×106/只接种BalB/C雌性小鼠,在第10~14天收集腹水,Protein G亲和柱纯化腹水进行β1-AA单克隆抗体的提纯,并用乳鼠心肌细胞跳动频率实验评价提取β1-AA的功能。
3)表面等离子共振:运用Biacore T200 (GE Healthcare)检测26肽与β1-AA的相互作用。将β1-AA用pH为5.5的枸橼酸钠溶液稀释成10 mmol/L,应用胺偶联试剂盒将β1-AA偶联到CM5传感芯片上,捕获信号为2655RU。以HBS-EP作为仪器运行缓冲液,将分析物(26肽)稀释成6个浓度(0.437 5~14 μmol/L),选定“Kinetics”程序进行上机实验。每个浓度循环之后,芯片表面注入10 mmol/L pH值为1.5的Glycine-HCl运行30 s以再生,循环完毕,获得动力学参数。一般认为亲和力(Affinity KD)为10-3mol/L时,两者为弱结合,KD为10-6mol/L时为中等强度结合,KD为10-9mol/L时为强结合。
4)乳鼠心肌细胞培养:取正常SD大鼠0~3 d的乳鼠,用75%(体积分数) 乙酸消毒后用剪刀从剑突左缘剪开胸骨,取出心脏置于冰冷PBS中充分清洗,眼科剪剪碎后吸入离心管,加入PBS,1 000 r/min, 离心5 min。弃掉PBS,加入1 mL酶混合液,置37 ℃水浴中摇动消化3 min,将酶悬液吸出加入到含10%(体积分数)FBS的DMEM培养基中终止消化,如此反复加酶混合液至组织消化完全。收集消化液与培养基混合液,1 000 r/min,离心5 min,加入新鲜培养基贴壁1.5 h后,将培养基转到新的离心管中,1 000 r/min,离心5 min收集细胞,弃上清,加入新鲜培养基于培养皿中进行细胞培养。
1.4 统计学方法
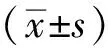
2 结果
2.1 β1-AA能够增加乳鼠心肌细胞的跳动频率
与Vehicle组相比,β1-AA组的心肌细胞跳动频率明显升高[(125.33±11.678)min-1vs(101.23±13.205)min-1,P<0.05)],提示其具有生物学活性,详见图1。
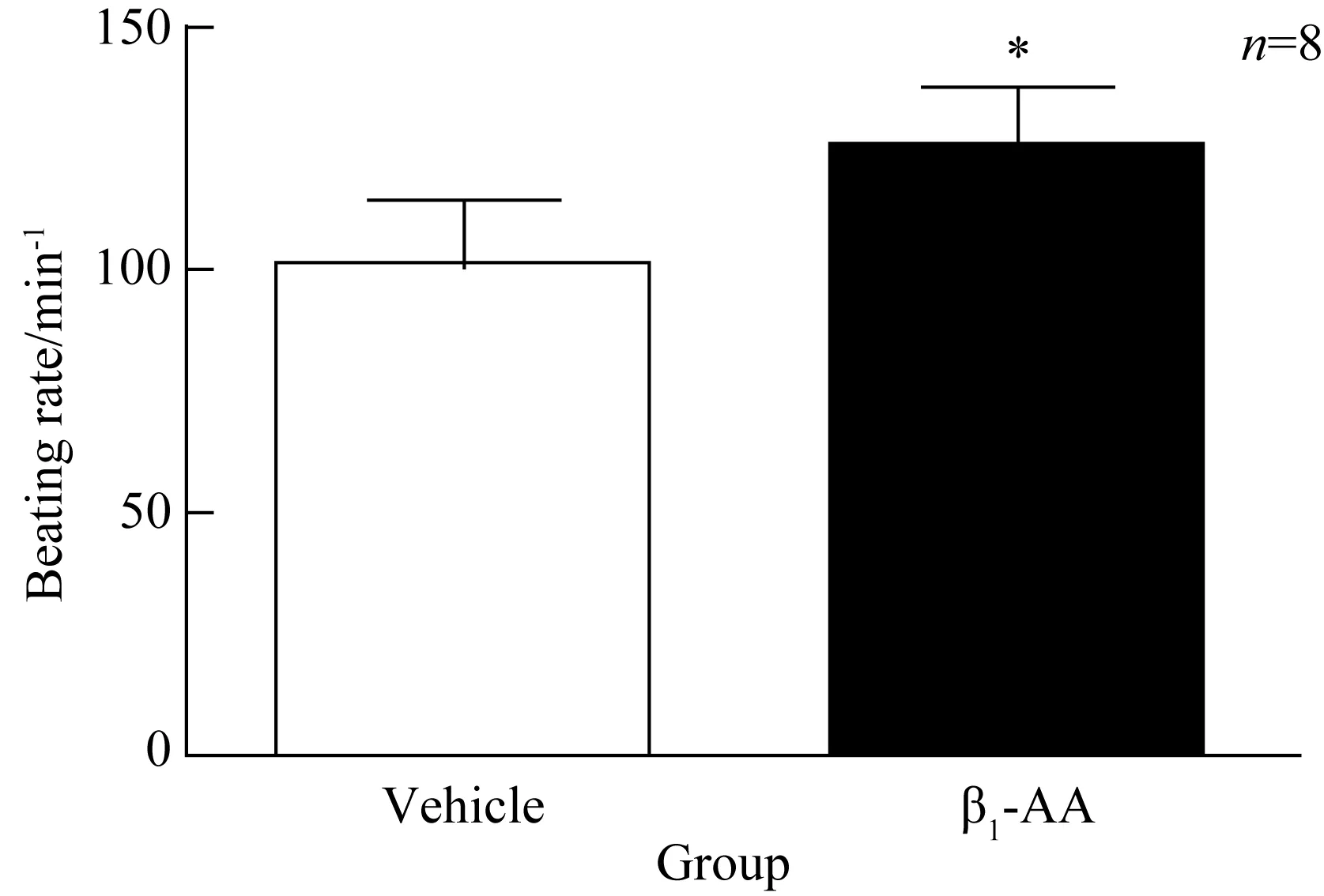
图1 β1-AA使乳鼠心肌跳动频率增加
Fig.1 β1-AA increased the beating frequency of neonatal rat cardiomyocytes
β1-AA:β1-adrenergic receptor autoantibodies;*P<0.05vsvehicle group.
2.2 该合成26肽与β1-AA具有较强亲和力
26肽与β1-AA以1∶1比例结合,pH=1.5的Glycine-HCl再生30 s,得到动力学参数:ka=7.34×103/m·s-1, kD=3.26×10-2/s, KD=4.44 μmol/L, Rmax=68.9 RU;该合成26肽与β1-AA有中等强度的结合(图2)。
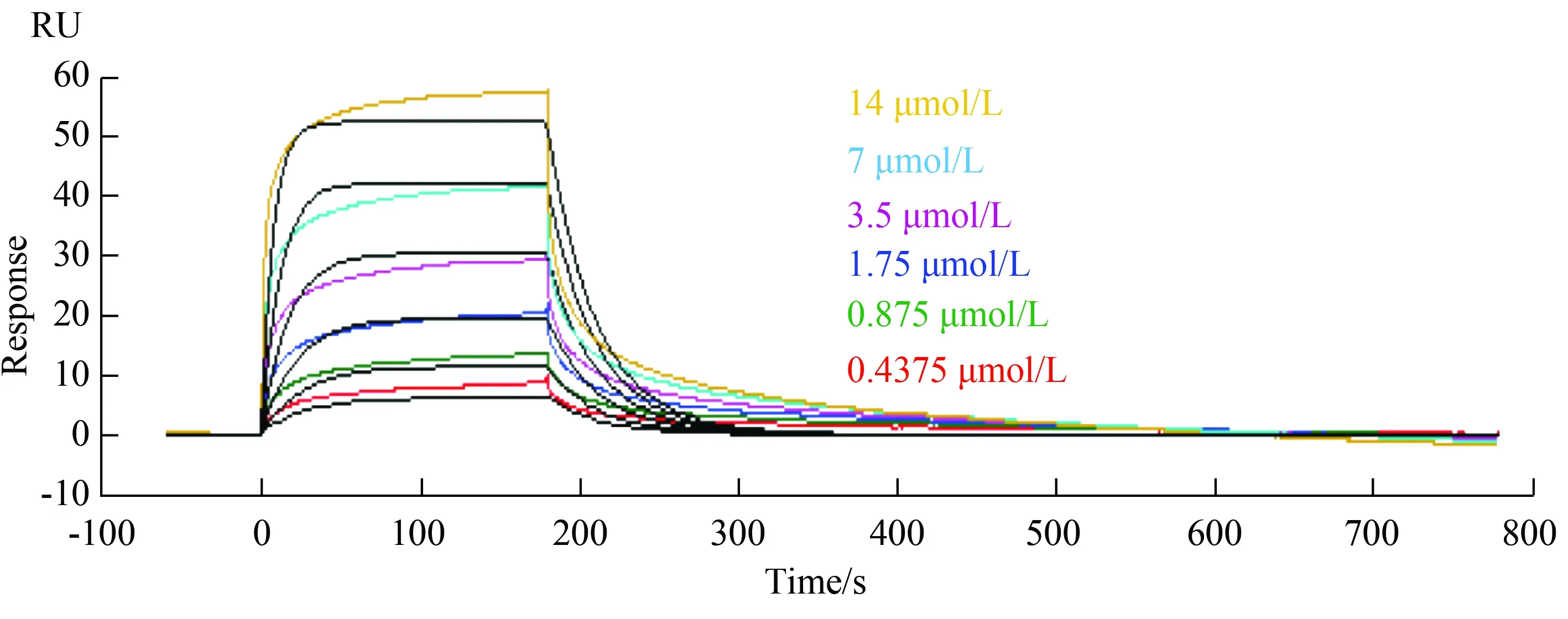
图2 26肽与β1-AA结合的亲和力
Fig.2 Binding affinity(KD) of the peptide and β1-AA
β1-AA:β1-adrenergic receptor autoantibodies.
2.3 26肽可降低β1-AA引起的乳鼠心肌细胞跳动频率增加
β1-AA可引起乳鼠心肌细胞跳动频率增加[(118.67±2.309)min-1vs(97.33±2.309)min-1,P<0.05];与β1-AA组相比,用26肽处理后乳鼠心肌细胞跳动频率显著降低[(81.33±2.309)min-1vs(118.67±2.309)min-1,P<0.05]。该26肽能够拮抗β1-AA引起的乳鼠心肌细胞跳动频率增加,详见图3。
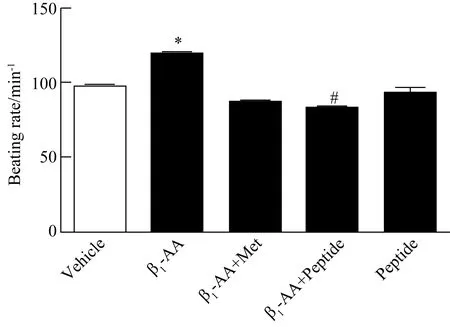
图3 26肽处理可显著降低β1-AA引起的乳鼠心肌细胞跳动频率增加
Fig.3 Peptide decreased the beating frequency of neonatal rat cardiomyocytes induced by β1-AA(n=6)
β1-AA:β1-adrenergic receptor autoantibodies;*P<0.05vsvehicle group,#P<0.05vsβ1-AA group.
3 讨论
本研究利用固相合成多肽法成功合成了模拟β1-AR-ECⅡ的26肽,采用杂交瘤细胞融合的方法获得了针对β1-AR-ECⅡ的单克隆抗体,表面等离子共振的结果证实合成的26肽与β1-AA具有相互作用,且能够拮抗其引起的下游类激动剂样效应。
β1-AA激活β1-AR后,可启动G蛋白-腺苷酸环化酶-环磷酸腺苷-蛋白激酶A(Gs-AC-cAMP-PKA)信号转导通路,引起cAMP升高、正性变时、变力、变传导等类激动剂样效应。在乳鼠心肌细胞跳动频率实验中,β1-AA增加了心肌细胞的跳动频率,这与前期实验[3]结果一致;26肽处理后,心肌细胞跳动频率较β1-AA组下降。有研究[10]报道体外实验预孵育β1-AA后加入特异性肽可减弱受体信号、降低80%以上的β1-AA引起的cAMP的产生,大鼠注射此类肽24 h后明显降低了cAMP的下游反应[11]。Li等[12]研究发现,针对β1-AA合成的10肽可以延长家兔心律失常时心房有效不应期;另外,β1-AA阳性心肌病大鼠长期注射此类肽可以反转心脏扩张并且改善心功能[13]。近期,此类肽化合物在人体的临床I期已完成[14],结果表明模拟β1-AR-ECⅡ结构合成的肽具有良好的耐受性和高度特异性且作用安全。以上结果提示,根据β1-AR-ECⅡ合成的此类肽可以拮抗β1-AA引起的下游有害效应。
目前研究证实,此类肽可以缓解或反转由β1-AA所致的心脏疾病,但未有文献报道β1-AA与肽的直接作用。既然此类肽的临床效果已初见成效,根据β1-AA的免疫原性特点,合成稳定且无不良反应的肽类药物必将为临床β1-AA所致的自身免疫疾病提供广阔的治疗前景。由此可见,阐明肽与β1-AA的分子间相互作用是未来药物研发的必由之路。传统研究分子间相互作用的方法有多种, 如酵母双杂交、放射免疫分析、酶连结免疫分析、免疫共沉淀等方法,但操作耗时费力、步骤繁琐、需要标记且假阳性率高[15]。表面等离子共振可以实现无须标记分子, 动态监控两者结合与解离过程, 低样品消耗以及灵敏度高等优点,其原理是:通过一定的化学反应将β1-AA单克隆抗体固定在传感器芯片上,当分析物流过芯片表面时,通过免疫反应与固定的抗体结合,引起芯片表面光学参数变化,这一变化与芯片表面结合的物质的质量有关[16-17]。因此,本实验首次应用SPR技术,证实了合成26肽与β1-肾上腺素受体自身抗体之间直接相互作用的动力学特征,得到其结合速率常数、解离速率常数以及亲和力,乳鼠心肌细胞跳动频率实验进一步证明,26肽中和β1-AA之后,其下游类激动剂样效应明显减弱。本研究为后续深入探索两者之间作用的机制以及肽类药物在生物医学、药学领域的研发提供了依据。
致谢:感谢首都医科大学医学实验与测试中心的杨颖老师在表面等离子共振检测方面提供的技术支持和帮助。
[1] Fiore G, Suppress P, Triggiani V, et al. Neuroimmune activation in chronic heart failure[J]. Enocr Metab Immun Disord Drug Targets, 2013,13(1): 68-75.
[2] Wang L, Lu K, Hao H, et al. Decreased autophagy in rat heart induced by anti-β1-adrenergic receptor autoantibodies contributes to the decline in mitochondrial membrane potential[J]. PLoS One, 2013,8(11):e81296.
[3] Du Y, Yan L, Wang J, et al. β1-Adrenoceptor autoantibodies from DCM patients enhance the proliferation of T Lymphocytes through the β1-AR/cAMP/PKA and p38 MAPK Pathways[J]. PLoS One, 2012,7(12): e52911.
[4] Du Y, Yan L, Du H, et al. β1-adrenergic receptor autoantibodies from heart failure patients enhanced TNF-α secretion in RAW264.7 macrophages in a largely PKA-dependent fashion[J]. J Cell Biochem, 2012, 113(10): 3218-3228.
[5] Zuo L, Du Y, Ma J, et al. Pro-arrhythmic action of autoantibodies against the second extracellular loop of β1-adrenoceptor and its underlying molecular mechanisms[J]. Int J Cardiol, 2015,198: 251-258.
[6] Zhao Y, Huang H, Du Y, et al.β1-Adrenoceptor autoantibodies affect action potential duration and delayed rectifier potassium currents in guinea pigs[J]. Cardiovasc Toxicol, 2015,15(1):1-9.
[7] Nitsche A, Kurth A, Dunkhorst A, et al. One-step selection of vaccinia virus-binding DNA aptamers by MonoLEX[J].BMC Biotechnol, 2007,7: 48.
[8] Haberland A, Wallukat G, Dahmen C, et al. Aptamer neutralization of beta1-adrenoceptor autoantibodies isolated from patients with cardiomyopathies[J]. Circ Res, 2011,109(9): 986-992.
[9] Haberland A, Wallukat G, Berg S, et al. Neutralization of pathogenic beta1-receptor autoantibodies by aptamers in vivo: the first successful proof of principle in spontaneously hypertensive rats[J]. Mol Cell Biochem, 2014,393(1-2): 177-180.
[10]Jahns R, Schlipp A, Boivin V, et al. Targeting receptor antibodies in immune cardiomyopathy[J]. Semin Thromb Hemost, 2010,36(2):212-218.
[11]Pei J, Li N, Chen J, et al. The predictive values of beta1-adrenergic and M2muscarinic receptor autoantibodies for sudden cardiac deathin patients with chronic heart failure[J]. Eur J Heart Fail, 2012,14(8): 887-894.
[12]Li H, Zhang L, Huang B, et al.A peptidomimetic inhibitor suppresses the inducibility of β1-adrenergic autoantibody-mediated cardiac arrhythmias in the rabbit[J]. J Interv Card Electrophysiol, 2015,44(3):205-212.
[13]Jahns R, Boivin V, Hein L, et al. A new cyclic receptor peptide prevents development of heart dilatation and failure induced by antibodies activating cardiac beta1-adrenergic receptors[J]. Circulation, 2005,112(17): U53-U53.
[14]Munch G, Boivin-Jahns V, Holthoff HP, et al. Administration of the cyclic peptide COR-1 in humans (phase I study): ex vivo measurements of anti-beta1-adrenergic receptor antibody neutralization and of immune parameters[J]. Eur J Heart Fail, 2012,14(11):1230-1239.
[15]陈丽华, 苏忠民, 王荣顺. 用表面等离子共振仪进行生物分子相互作用研究的评述[J]. 分子科学学报, 2004,20(4):44-49.
[16]吴世康, 汪鹏飞. 表面等离子共振(SPR)—一种新型化学检测方法的原理[J].影像科学与光化学, 2008,26(2):157-168.
[17]徐江敏,张丽丽,李桂芬. 利用表面等离子体共振仪检测黄瓜花叶病毒[J]. 生物技术通讯, 2013,24(6):847-849.
编辑 慕 萌
Detection of the interaction between the peptide and β1-adrenergic receptor autoantibodies using surface plasmon resonance
Dong Yu, Lyu Tingting, Xu Wenli, Bai Yan, Wu Ye, Liu Huirong, Wang Wen*
(DepartmentofPhysiologyandPathophysiology,SchoolofBasicMedicalSciences,CapitalMedicalUniversity,BeijingKeyLaboratoryofMetabolicDisordersRelatedCardiovascularDiseases,CapitalMedicalUniversity,Beijing100069,China)
Objective To investigate the interaction between the peptide which mimic the structure of the second extracellular loop of the β1-adrenergic receptor (β1-AR-ECⅡ) and β1-adrenergic receptor autoantibodies (β1-AA). Methods Peptide was synthesized according to the amino acid sequence of human β1-AR-ECⅡ; a hybridoma fusion method was used to obtain anti-β1-AR-ECⅡmonoclonal antibody; the interaction between the peptide and β1-AA was detected by surface plasmon resonance (SPR); and the beating frequency experiment of neonatal rat cardiomyocytes was explored to test the neutralization of the peptide to β1-AA. Results β1-AA enhanced the beating frequency of neonatal rat cardiomyocytes (P<0.05), indicating that the β1-AA we obtained has biological activity; SPR results showed that there was a moderate binding affinity (KD) of 4.44 μmol/L between the synthetic peptide and β1-AA. Conclusion There was interaction between the synthesized peptide and β1-adrenergic receptor autoantibodies.
β1-adrenergic receptor autoantibodies(β1-AA); 26 peptide; surface plasmon resonance
973计划前期研究专项(2014CB560704),北京市自然科学基金重点项目(7151001)。This study was supported by 973 Special Preliminary Study Plan(2014CB560704), Natural Science Foundation of Beijing(7151001).
时间:2016-12-14 20∶19
http://www.cnki.net/kcms/detail/11.3662.r.20161214.2019.034.html
10.3969/j.issn.1006-7795.2016.06.004]
R 971
2016-10-03)
*Corresponding author, E-mail:wangwen@ccmu.edu.cn

