肺癌第8版TNM分期解读与展望
刘宝东 支修益
(首都医科大学宣武医院胸外科,北京 100053)
· 肺癌精准治疗 ·
肺癌第8版TNM分期解读与展望
刘宝东 支修益*
(首都医科大学宣武医院胸外科,北京 100053)
在过去的6年多时间里,肺癌的诊断和治疗研究取得了巨大的进步,但是第7版肺癌TNM分期难以满足目前的临床需求。于是国际肺癌研究协会(International Association for the Study of Lung Cancer,IASLC)收集了1999年至2010年间94 708例新确诊的肺癌患者,患者来自16个国家的35个中心,形成第8版肺癌TNM分期。第8版肺癌TNM分期较第7版TNM分期能够更好地反映不同分期患者的预后。
肺癌;肺癌分期;TNM分期
恶性肿瘤TNM分期系统是进行肿瘤诊断、治疗及临床研究的“国际语言”,一个理想的TNM分期系统应能够正确地反映患者病情,准确地判断预后。随着肺癌筛查、诊断、分期和治疗等技术的进步,需要不断更新分期标准以适应疗效及预后的评估。
1 肺癌TNM分期的历史
国际抗癌联盟(International Union Against Cancer,UICC)自1968年提出了“恶性肿瘤TNM分期法”第1版肺癌TNM分期以来[1], 到目前为止共进行了5次修订[2]。1998年,国际肺癌研究协会(International Association for the Study of Lung Cancer,IASLC)组织了一个国际分期委员会(International Staging Committee,ISC)旨在全世界范围内收集肺癌患者的大样本,建立一个国际数据库。国际协会肺癌研究会在1990年至2000年间评估了大约8.1万名确诊为肺癌患者,制定了第7版修订的肺癌TNM分期[3-7]。
在过去的6年多时间里,肺癌的诊断和治疗研究取得了巨大的进步,特别是薄层高分辨计算机横断层扫描(computed tomography ,CT)及正电子发射计算机断层显像(positron emission tomography/computer tomography,PET-CT)等分期手段的多样化,胸腔镜技术等手术技术的微创化和中晚期肺癌靶向治疗的精准化,旧的分期标准已经难以满足目前的临床需求。于是IASLC数据库搜集了1999年至2010年间94 708例新确诊的肺癌患者,包括原先已建立的数据库(90 014例)和通过电子数据收集系统(electronic data capture system,EDC)提交给癌症研究及生物统计学(cancer research and biostatistics,CRAB)的数据(4 667例)。通过EDC收集的数据包含了肺癌TNM分期所有必需的元素,尽管数据库规模稍小,但细节更多,使得研究人员对不同描述的分析及改进成为可能。患者来源于16个国家的35个中心,其中欧洲贡献了46 560例患者,亚洲41 705例患者,北美4 660例患者,澳大利亚1 593例患者和南美190例患者。欧洲仍然是贡献病例最多的地区,而亚洲由于日本的巨大贡献而紧随其后,相对于以前的数据库,来自北美洲和澳洲的病例数减少了,南美洲首次提供了病例。CRAB在已经建立的TNM分期基础上对经过筛选后的77 156例 (70 967例非小细胞肺癌和6 189例小细胞肺癌)进行分析,形成第8版肺癌TNM分期,修订稿已发表于《Journal of Thoracic Oncology》[8-18],并于2017年1月正式开始实施。新的第8版肺癌TNM分期较第7版TNM分期能够更好的反映不同分期患者的预后。
2 第7版肺癌TNM分期的争议
2.1 数据库
1)回顾性数据:第7版肺癌TNM分期完全建立在回顾性数据基础上。此研究收集的是1990年至2000年间的数据,该数据库包括19个国家46个医疗中心的100 869例的临床分期与治疗方案评价的数据,其中满足TNM分期、病理和生存期随访要求的 81 015例被纳入分析,67 725例为非小细胞肺癌,小细胞肺癌13 290例。新辅助化学治疗病例纳入临床治疗部分但不纳入病理分期部分,CT分期只见于纳入阶段(1990年至2000年)的病例。分期信息来自手术(41%)、放射治疗(11%)、化学药物治疗(23%)、多方法(25%),主要以手术病例作为分期参考。IASLC数据库由CRAB进行存储、处理及分析[3]。通过对不同TNM定义的统计分析, 2007年在第12届世界肺癌大会上报告了对第7版肺癌TNM分期系统的修订建议[4-7],2009年在第13届世界肺癌大会上,IASLC公布了国际肺癌分期系统第7版,被UICC和美国癌症联合会(American Joint Committee on Cancer,AJCC)修改并采纳。第7版肺癌TNM分期也适用小细胞分期等,首次将恶性肿瘤及肺支气管良性肿瘤进行形态学分期。此外,提出了新的淋巴结分布图,解决了早前版本的分歧。
2)数据来源不均衡:数据来源于全球19个国家的46个研究中心(包括58%来自欧洲、21%来自北美、14%来自亚洲、7%来自澳洲),尚没有来源于非洲、南美及印度次大陆的数据;一些人口巨大的国家(如中国、俄罗斯、印度尼西亚)其所提供的数据占总体的比例太小,不具有代表性。各个研究机构的治疗模式有很大的不同,导致了治疗结果的差异,对患者生存率的最终统计也产生了一些影响。而各研究中心在提交数据时难免会有所侧重,影响到了统计结果的随机性和客观性。此外研究者还认为需要更多的前瞻性数据来验证修订内容的可靠性[3]。
2.2 T、N、M定义的局限性
1)T分期:除肿瘤大小因素以外的T2、T3,同一肺叶内的其他转移和胸膜转移以外的T4,目前均缺乏特异性数据验证。将肺原发肿瘤侵犯大血管规定为T4,但未明确规定哪些血管属于大血管,孤立的肿瘤病灶位于同一肺叶定义为T3,位于同侧不同肺叶定义为T4,但未规定病灶的数量[4]。
2)N分期:根据淋巴结转移程度进行的N分期亚分类也因缺乏证据而无法提出[5]。
3)M分期:由于有转移的患者极少手术,因此,对侧肺或胸外转移的数量对预后是否有影响尚不清楚。同样是单发脑转移和肾上腺转移,手术治疗效果较好[6]。
2.3 其他病理学类型
1)第7版肺癌TNM分期是基于非小细胞肺癌的回顾性数据分析,虽然也建议可应用于小细胞肺癌与类癌,但这并非该研究项目的主要目的[7]。
2)第7版肺癌TNM分期用于一些肿瘤组织亚型时局限性明显,特别是涉及不典型腺瘤样增生(atypical adenomatous hyperplasia,AAH)、原位腺癌(adenocarcinoma in situ,AIS)和微浸润腺癌(minimally invasive adenocarcinoma,MIA)时。
3 第8版肺癌TNM分期的解读
与第7版肺癌TNM分期相比,第8版分期能够更好地反映病情和估计预后,详见表1、2、3。
3.1 T分期
肿瘤最大径≤3 cm及>3 cm生存差异很大,因此仍将3 cm作为T1、T2的分界点;对于肿瘤最大径>5 cm,但≤7 cm的患者生存率变化不大,因此将其统称为T3;肿瘤最大径>7 cm患者预后与第7版肺癌TNM分期的T4患者生存率类似,因此第8版分期将>7 cm归为T4[16]。累及主支气管且距离隆突≥2 cm与其他因素T2预后一致,生存差异并无统计学意义,而累及主支气管且距离隆突<2 cm但未累及隆突者,预后明显好于其他因素T3,因此第8版分期对于主支气管受累,只要未侵犯隆突,无论距离隆突多远均归为T2。合并部分肺不张或阻塞性肺炎的患者预后与其他因素的T2预后一致,但合并全肺不张或阻塞性肺炎患者预后明显好于其他因素的T3,因此第8版分期无论肺不张或阻塞性肺炎范围大小、累及全肺与否均归为T2。侵犯膈肌的患者要比其他pT3患者预后更差,类似于pT4患者,因此第8版分期将侵犯膈肌归为T4。和壁层胸膜不同,纵隔胸膜受累没有明显征象,当发现纵隔胸膜受累时往往肿瘤已越过胸膜侵犯到胸膜内组织或脏器,而且病理界定有一定困难,在病理分期中极少见仅单独纵隔胸膜受侵而没有浸润到纵隔内组织的情况,因此将纵隔胸膜受累纳入临床分期并不可靠,故而在新版分期中删除了纵隔胸膜受累的T分期因素。
表1 肺癌第7版、第8版TNM定义变更比较
Tab.1 The change between IASLC-seventh and eighth edition of the TNM descriptors for lung cancer
表2 肺癌第7版、第8版TNM组合变更比较
Tab.2 The change between IASLC-seventh and eighth edition of the TNM classification for lung cancer
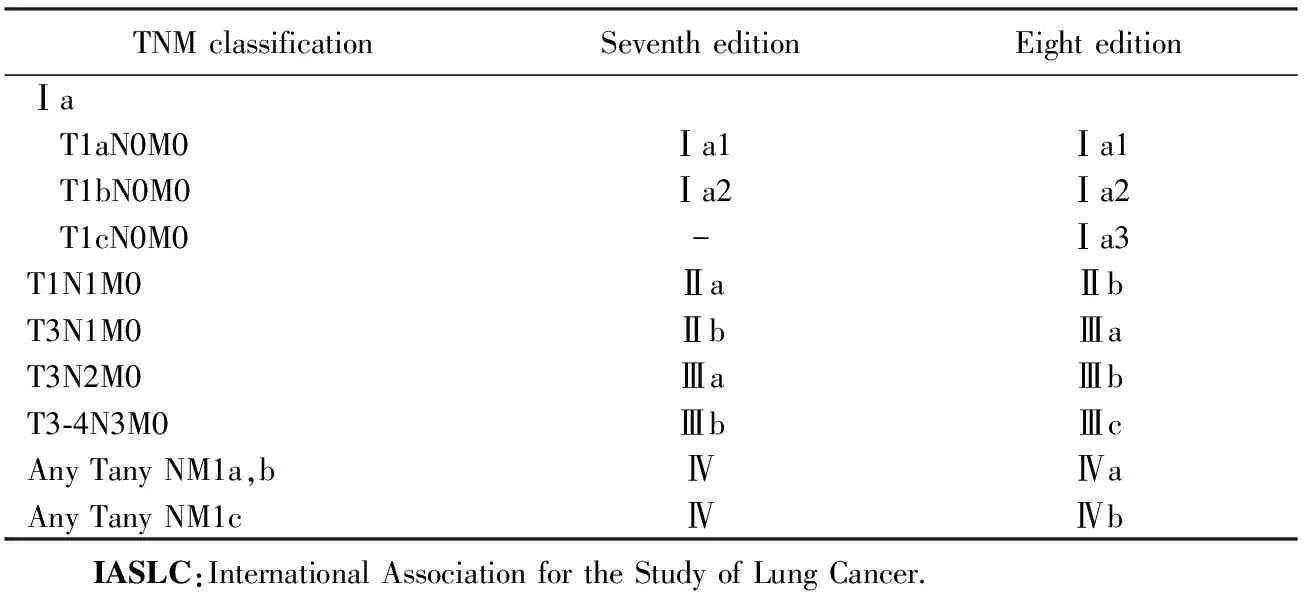
TNMclassificationSeventheditionEighteditionⅠa T1aN0M0Ⅰa1Ⅰa1 T1bN0M0Ⅰa2Ⅰa2 T1cN0M0-Ⅰa3T1N1M0ⅡaⅡbT3N1M0ⅡbⅢaT3N2M0ⅢaⅢbT3⁃4N3M0ⅢbⅢcAnyTanyNM1a,bⅣⅣaAnyTanyNM1cⅣⅣb IASLC:InternationalAssociationfortheStudyofLungCancer.
表3 肺癌第8版TNM分期
Tab.3 The eighth edition of the TNM classification for lung cancer

T/MSubclassificationN0N1N2N3T1T2aⅡa1T1a≤1cmⅡa1ⅡbⅢaⅢb1cm 3.2 N分期 由于以往不同N分期之间生存率差异已经能够很好地反映肺癌患者分期与预后的关系,因此第8版分期建议继续沿用原来第7版N分期。但是研究[15]显示对于同一级别的N分期中,临床分期与病理分期生存率差异较大,而病理分期往往能够更真实地反映分期情况,研究[15]显示淋巴结转移站数及是否存在跳跃性转移对预后会产生重要影响,伴有多站转移及存在跳跃性转移的患者预后明显变差,因此推荐将原来的N1细分为N1a(单站转移)和N1b(多站转移);N2分为N2a1(无N1转移,直接跳跃到N2的淋巴结)、N2a2(有N1淋巴结转移,同时发生单站N2淋巴结转移)和N2b(多站N2淋巴结转移)。 3.3 M分期 由于寡转移概念的引入,将M分期进一步细分为M1a、M1b和M1c,其中M1a与第7版定义一致,将M1b细分,单器官转移独列为新的M1b[14]。 3.4 TNM分期组合 第8版TNM分期将原来的Ⅰa期进一步细分为Ⅰa1、Ⅰa2、Ⅰa3期,T1N1由Ⅱa期改为Ⅱb期;T3N1由Ⅱb期改为Ⅲa期;T3N2 由Ⅲa期改为Ⅲb期;T3-4N3更新为Ⅲc期;M1a和M1b更新为Ⅳa,M1c更新为Ⅳb[12]。 4.1 入选人群的代表性 第8版肺癌TNM分期虽然增加了亚洲病例的比例,但主要来自日本,中国作为肺癌大国,病例数较少,而且主要为上海和广东病例,不具有代表性。另外虽然首次将南美病例纳入研究,但仍然缺乏来自非洲、俄罗斯及印度的病例。因为不同地域的肺癌病例生物学行为存在差异,对治疗的反应不一样,因此预后也不同[8]。所以在将来的分期研究中病例要有人群的代表性。 4.2 数据收集的前瞻性 第8版肺癌TNM分期的数据库主要来自IASLC数据库,属于回顾性病例[8]。将来的分期研究中需要增加病例的前瞻性研究,进一步确认新版分期的可行性。 4.3 分期手段的多样性 薄层高分辨CT、PET-CT、纵膈镜、支气管内超声引导针吸活检(endobronchial ultrasound guided tranbronchial needle aspiration,EBUS-TBNA)、电磁导航支气管镜(electromagnetic navigation bronchoscopy)等的广泛应用使肺癌的形态学分期越来越精确化,但是在将来的分期研究中应该对微转移的问题进一步研究,如液体活检,检测包括循环肿瘤细胞(circulating tumor cells,CTC)、循环肿瘤DNA(circulating tumor DNA,ctDNA)、循环游离DNA(circulating free DNA,cfDNA)。 4.4 生物特征的精确性 在过去的几十年里,由于基因分析和分子诊断技术的不断发展,基于基因特征的肺癌分期研究也相继开展。但是目前已知驱动基因的非小细胞肺癌比例不足50%,随着二代测序(next-generation sequencing,NGS)等检测技术的推广运用,可以发现更多未知突变基因。在将来的分期研究中,肺癌的驱动基因突变状态和程序性死亡受体配体(programmed death ligand-1,PDL-1)表达水平等生物学特征应该有所体现,即肿瘤的生物学行为将应用于基于形态学为特征的肺癌分期系统,逐步过渡到成熟的肺癌形态-生物分期系统。 总之,第8版肺癌TNM分期最主要的变更内容是对T分期和M分期的改变,与第7版肺癌TNM分期相比能更好地反映不同分期肺癌患者的预后。但是肺癌分期必将由基于形态学为特征的肺癌分期系统,逐步过渡到肺癌形态-生物分期系统。 [1] Mountain C F.Revisions in the international system for staging lungcancer[J].Chest,1997,111(6):1710-1717. [2] UICC. TNM classification of malignant tumours[M]. Geneva: UICC, 1968. [3] Groome P A,Bolejack V,Crowley J J,et al.The IASLC lung cancer staging project: validation of the proposals for revision of the T, N, and M descriptors and consequent stage groupings in the forthcoming (seventh) edition of the TNM classification of malignant tumours[J]. J Thorac Oncol,2007,2(8):694-705. [4] Rami-Porta R,Ball D,Crowley J,et al.The IASLC lung cancer staging project: proposals for the revision of the T descriptors in the forthcoming (seventh) edition of the TNM classification for lung cancer[J]. J Thorac Oncol,2007,2(7):593-602. [5] Rusch V W,Crowley J,Giroux D J,et al.The IASLC lung cancer staging project: proposals for the revision of the N descriptors in the forthcoming seventh edition of the TNM classification for lung cancer[J]. J Thorac Oncol,2007,2(7):603-612. [6] Postmus P E,Brambilla E,Chansky K,et al.The IASLC lung cancer staging project: proposals for revision of the M descriptors in the forthcoming (seventh) edition of the TNM classification of lung cancer[J]. J Thorac Oncol,2007,2(8):686-693. [7] Goldstraw P,Crowley J,Chansky K,et al.The IASLC lung cancer staging project: proposals for the revision of the TNM stage groupings in the forthcoming (seventh) edition of the TNM Classification of malignant tumours[J]. J Thorac Oncol,2007,2(8):706-714. [8] Rami-Porta R,Bolejack V,Giroux D J,et al.The IASLC lung cancer staging project: the new database to inform the eighth edition of the TNM classification of lung cancer[J]. J Thorac Oncol,2014,9(11):1618-1624. [9] Rami-Porta R,Bolejack V,Crowley J,et al.The IASLC lung cancer staging project: proposals for the revisions of the T descriptors in the forthcoming eighth edition of the TNM classification for lung cancer[J]. J Thorac Oncol,2015,10(7);990-1003. [10]Eberhardt W E,Mitchell A,Crowley J,et al.The IASLC lung cancer staging project: proposals for the revision of the M descriptors in the forthcoming eighth edition of the TNM classification of lung cancer[J]. J Thorac Oncol,2015,10(11):1515-1522. [11]Nicholson A G,Chansky K,Crowley J,et al.The International association for the study of lung cancer staging project: proposals for the revision of the clinical and pathologic staging of small cell lung cancer in the forthcoming eighth edition of the TNM classification for lung cancer[J]. J Thorac Oncol,2016, 11(3):300-311. [12]Goldstraw P,Chansky K,Crowley J,et al. The IASLC lung cancer staging project: proposals for revision of the TNM stage groupings in the forthcoming (eighth) edition of the TNM classification for lung cancer[J]. J Thorac Oncol,2016,11(1):39-51. [13]Detterbeck F C,Marom E M,Arenberg D A,et al.The IASLC lung cancer staging project: background data and proposals for the application of TNM staging rules to lung cancer presenting as multiple nodules with ground glass or lepidic features or a pneumonic type of involvement in the forthcoming eighth edition of the TNM classification[J]. J Thorac Oncol,2016,11(5):666-680. [14]Detterbeck F C,Nicholson A G,Franklin W A,et al. The IASLC lung cancer staging project: summary of proposals for revisions of the classification of lung cancers with multiple pulmonary sites of involvement in the forthcoming eighth edition of the TNM classification[J]. J Thorac Oncol,2016,11(5):639-650. [15]Detterbeck F C,Bolejack V,Arenberg D A,et al.The IASLC lung cancer staging project: background data and proposals for the classification of lung cancer with separate tumor nodules in the forthcoming eighth edition of the TNM classification for lung cancer[J]. J Thorac Oncol,2016,11(5):681-692. [16]Detterbeck F C,Franklin W A,Nicholson A G,et al.The IASLC lung cancer staging project: background data and proposed criteria to distinguish separate primary lung cancers from metastatic foci in patients with two lung tumors in the forthcoming eighth edition of the TNM classification for lung cancer[J]. J Thorac Oncol,2016,11(5):651-665. [17]Travis W D,Asamura H,Bankier A A,et al.The IASLC lung cancer staging project: proposals for coding T categories for subsolid nodules and assessment of tumor size in part-solid tumors in the forthcoming eighth edition of the TNM classification of lung cancer[J]. J Thorac Oncol,2016,11(8):1204-1223. [18]Detterbeck F C,Chansky K,Groome P,et al.The IASLC lung cancer staging project: methodology and validation used in the development of proposals for revision of the stage classification of NSCLC in the forthcoming (eighth) edition of the TNM classification of lung cancer[J].J Thorac Oncol,2016, 11(9):1433-1446. 编辑 孙超渊 Interpretation and prospect of the eighth edition of TNM staging for lung cancer Liu Baodong,Zhi Xiuyi* (DepartmentofThoracicSurgery,XuanwuHospital,CapitalMedicalUniversity,Beijing100053,China) Over the past six years, with the diagnosis and treatment of lung cancer has meaningful advances, the 7th edition of lung cancer TNM staging is difficult to meet the current clinical needs. Therefore, International Association for the Study of Lung Cancer (IASLC) has information on 94 708 new patients diagnosed as lung cancer originated from 35 sources in 16 countries between 1999 and 2010, forming the eighth edition of TNM staging of lung cancer. The new edition of the classification will then be enacted in January 2017. The advantages of the new staging has higher value in prognosis and clinical guidance of different patients. lung cancer;lung cancer stage;TNM classification 国家自然科学基金(81572704)。This study was supported by National Natural Science Foundation of China (81572704). 时间:2016-12-14 20∶10 http://www.cnki.net/kcms/detail/11.3662.r.20161214.2010.008.html 10.3969/j.issn.1006-7795.2016.06.007] R 73 2016-10-03) *Corresponding author, E-mail:xiuyizhi2015@163.com4 肺癌TNM分期的展望

