一种新纳米乳作为流感疫苗佐剂的效果
, ,,,
(南华大学病原生物学研究所,特殊病原体防控湖南省重点实验室,湖南 衡阳 421001)
·技术与方法·
一种新纳米乳作为流感疫苗佐剂的效果
赵兰华,刘玮,唐双阳,李冉辉,曾焱华*
(南华大学病原生物学研究所,特殊病原体防控湖南省重点实验室,湖南 衡阳 421001)
目的筛选有佐剂效果的纳米乳新配方,并从稳定性、粒径大小、载水范围、佐剂效果与安全性等方面评价其作为疫苗佐剂的可行性。方法依据伪三元相图筛选出能被水大量稀释的配方,测定基本性质如pH,黏度,粒径,长期保存或离心条件下是否保持稳定等。将其做为佐剂与流感疫苗混合进行动物实验。25只ICR小鼠随机分为生理盐水组、单独疫苗组、铝佐剂对照组、弗氏佐剂组和纳米乳佐剂组,每组5只,经大腿腓肠肌注射流感H3N2裂解疫苗。第三周加强免疫一次,初次免疫后一周内观察各组小鼠的体重变化,每周收集血清以检测血凝抑制抗体的效价,用SPSS18.5软件分析比较各组小鼠产生的抗体水平。最大给药量实验评价其安全性。结果该纳米乳理化性质稳定,pH值为7.5,黏度与水接近,平均粒径为56.3 nm,离心及长期保存不破乳。纳米乳佐剂组小鼠能产生更高水平的血凝抑制抗体,在0.25 mg/10 g给药量下无小鼠死亡。结论该纳米乳配方作为流感疫苗佐剂具有良好的稳定性、安全性及佐剂效果。
纳米乳; 佐剂; 流感疫苗
传统流感疫苗生产工艺繁杂,生产成本高,在储备不足或致病亚型突变的情况下,很难应对流感大流行爆发[1],加入佐剂能增强抗原的免疫原性,既节约疫苗用量,又能有效应对流感爆发,因此,研究新型的疫苗佐剂意义重大。纳米乳是一类由表面活性剂、助表面活性剂、油相、水相按一定比例混合形成的透明、澄清、稳定的运载系统。纳米乳作为载药系统已有大量研究[2],作为疫苗佐剂则研究较少。现已有MF59、AS03、AF03等乳佐剂被批准用于人体,限于安全等因素考虑,目前仍只是作为某些特定疫苗的储备佐剂,没有得到普遍认可和使用。大量关于纳米乳的载药研究表明纳米乳佐剂具有可观的应用前景[3]。
为筛选到安全、有效能作为佐剂的纳米乳新配方,本研究拟依据伪三元相图筛选出能被水大量稀释的纳米乳新配方,并从稳定性、粒径大小、载水范围等方面评价其作为疫苗佐剂的可行性。
1 材料与方法
1.1实验疫苗及毒株流感病毒:H3N2A/Victoria/210/2009NYMC X-187来源于WHO/NIBSC。H3N2流感病毒灭活疫苗单价原液由中国医学科学院医学生物学研究所提供,血凝素含量为325 μg/mL。
1.2实验动物ICR雌性小鼠,体重18~22 g,由中国医学科学院医学生物学研究所动物实验中心提供,合格证号:SCXK(滇)2010-0003。
1.3实验试剂Tween-80购自上海生工生物工程有限公司;Span-80购自天津市光复精细化工研究所;1,2-丙二醇和液体石蜡为天津市风船化学试剂科技有限公司产品;氢氧化铝佐剂(原始浓度16.31 mg/mL)由中国医学科学院医学生物学研究所制备;完全弗氏佐剂购自Sigma公司;受体破坏酶购自东京生研株式会社。
1.4纳米乳的配制称取Tween-20 0.94 g,Span-80 0.94 g,1,2-丙二醇0.94 g,液体石蜡1.2 g,在700 r/min的转速下搅拌均匀,边搅拌边以每分钟100 μL的速度加入生理盐水,待形成澄清透明的纳米乳后,改为每分钟500 μL继续添加生理盐水至16 000 μL。取1 mL纳米乳,加入28.5 μL的流感疫苗原液,混匀。
1.5纳米乳理化性质测定与观察观察纳米乳的外观,检测其pH值和黏度,电镜下观察粒子形态,用马尔文粒度仪测其粒径大小,在4 ℃、25 ℃和37 ℃环境中储存3个月后观察其是否破乳。
1.6实验分组与免疫将28日龄,体重18~22 g的雌性小鼠随机分为生理盐水组(每只注射0.2 mL生理盐水)、单独疫苗组(每只注射0.2 mL疫苗,其中含血凝素1.8 μg)、铝佐剂对照组(每只注射0.2 mL疫苗,其中含血凝素1.8 μg,氢氧化铝0.2 mg)、完全弗氏佐剂组(每只注射0.2 mL完全弗氏佐剂,其中含血凝素1.8 μg)和纳米乳佐剂组(每只注射0.2 mL纳米乳,其中含水80%,Tween-20为4.7%(w/w),Span-80 为4.7%(w/w),1,2-丙二醇为4.7%(w/w),液体石蜡油6%(w/w),含血凝素1.8 μg)。每组5只,饲养1周后,分别于0天和21天分别经大腿腓肠肌进行免疫,并于初次免疫后的一周内隔天监测小鼠体重。
1.7血凝抑制抗体滴度的测定免疫一周后开始每周采集分离血清,用受体破坏酶处理19 h以去除非特异性抑制剂,然后56 ℃灭活1 h,血清倍比稀释后加入等量8个血凝单位的病毒液,结合1 h后加入1%的鸡红细胞,静置30 min,判定血凝抑制抗体的滴度。
1.8最大给药量试验随机选取10只ICR小鼠,在0.25 mg/10g的最大给药量下进行一次性腹腔注射,观察其注射一周内的存活情况。
2 结 果
2.1纳米乳的理化性质经测定,该纳米乳pH为7.5,黏度与水接近,经4 ℃,25 ℃,37 ℃储存3个月后未见分层破乳,经10 000 r/min离心后仍然能保持稳定,表明该纳米乳具有动力学稳定性。通过伪三元相图(图1)可知,该配方成乳面积大,即载水范围较大,被大量的水稀释后无明显破乳现象,由此也能证明其动力学稳定性[4]。
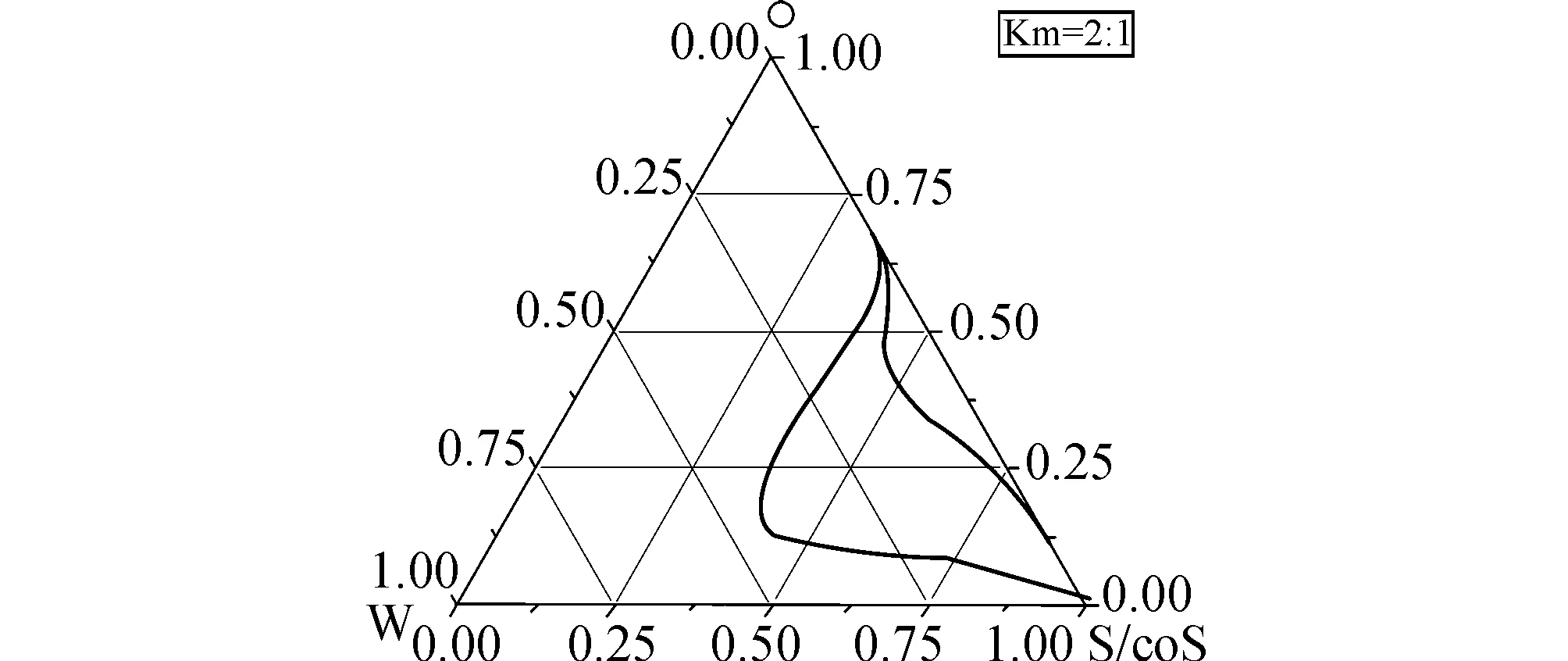
图1 纳米乳的伪三元相图(×10 000)
2.2电镜观察磷钨酸负染后用透射电子显微镜进行观察,如图2所示:纳米乳的颗粒呈球形,易堆积聚集,粒径大小约在50 nm左右,分布较为均匀。
2.3马尔文粒度仪检测用马尔文粒度仪测定纳米乳的粒径大小和均匀度,如图3所示,该纳米乳平均粒径大小为56.3 nm,多分散性系数(PDI值)为0.302。由粒径强度曲线图可知,该纳米乳的粒子呈正态分布[5]。该检测结果与用电子显微镜观察的结果基本一致。
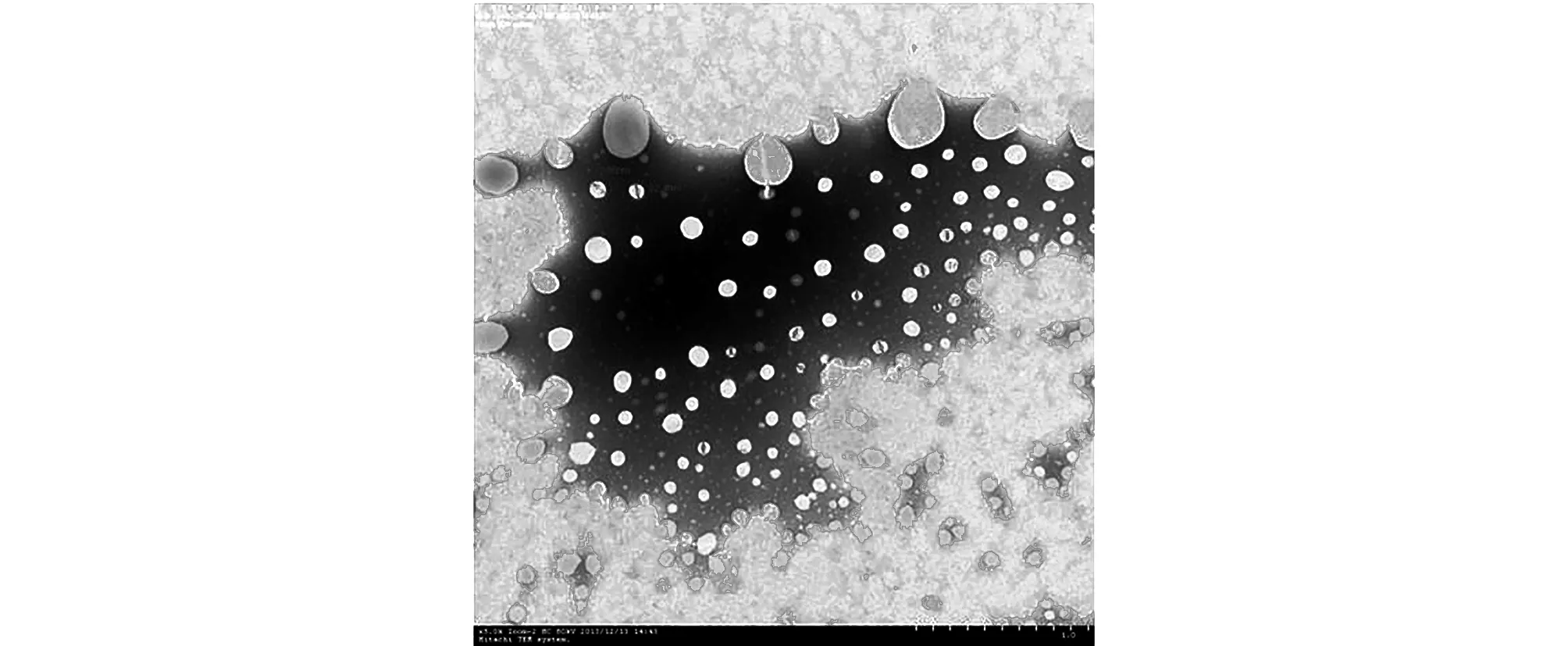
图2 电子显微镜观察纳米乳颗粒
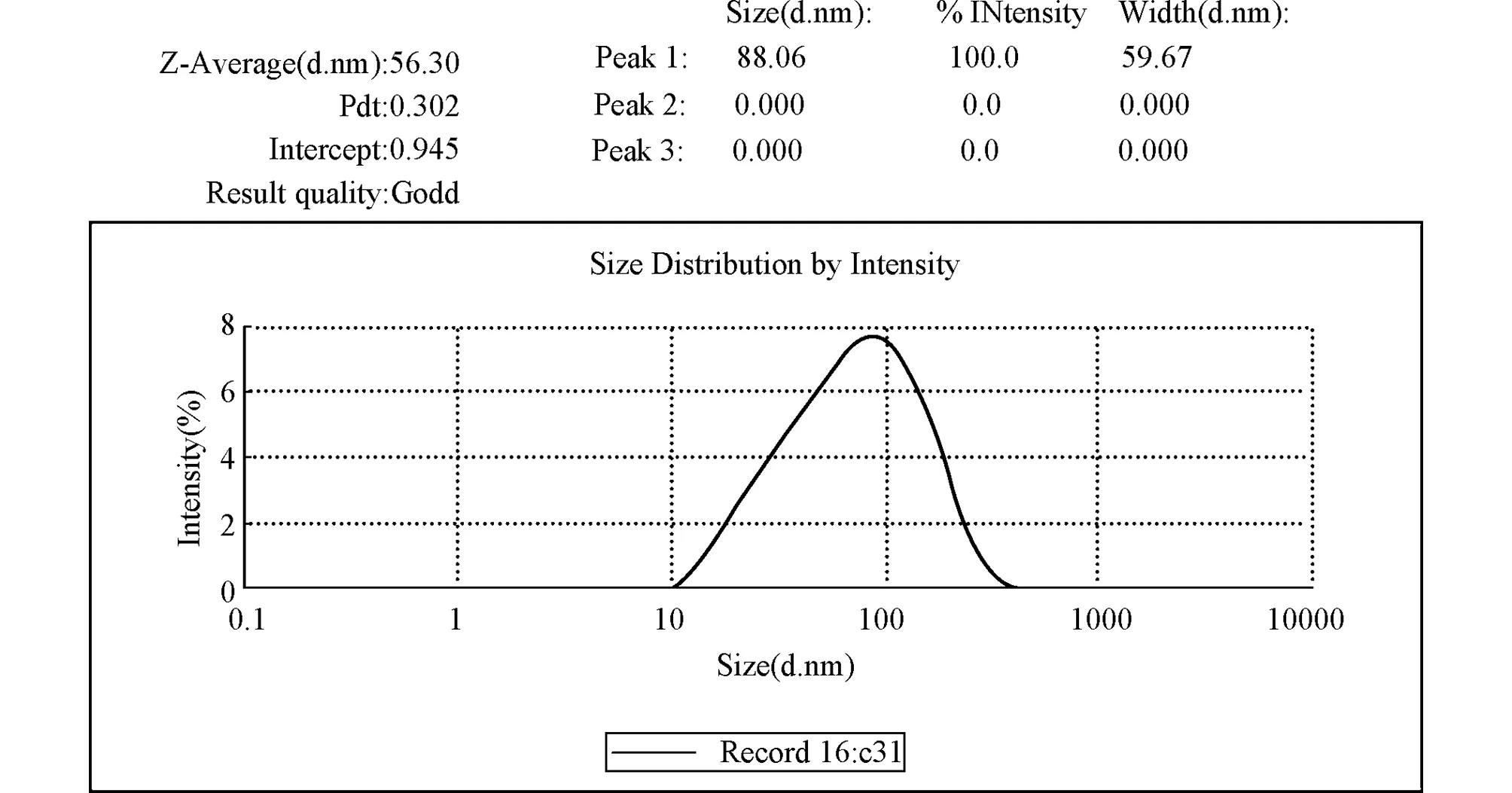
图3 纳米乳粒径大小与分布
2.4小鼠体重监测不同组别小鼠在初次免疫后一周内,其体重增长情况如图4所示,所有组别小鼠在免疫前体重均约为20 g,初次免疫后一周内各组小鼠体重稳定增长,其中纳米乳佐剂组小鼠平均体重最高,但与对照组小鼠体重和生理盐水组比较,差异无显著性(P>0.05),即纳米乳对小鼠没有明显的毒副作用。

图4 小鼠初次免疫后一周内的体重变化
2.5小鼠血清中血凝抑制抗体的滴度由图5可知:各组小鼠血清中HI抗体均在初次免疫后第四周达到峰值,纳米乳佐剂组平均抗体滴度为1∶5 632,铝佐剂组为1∶2 662,完全弗氏佐剂组为1∶1 446,单独疫苗组为1∶934,对比可知,纳米乳佐剂组的抗体峰值分别约为铝佐剂组、完全弗氏佐剂组和单独疫苗组的2倍、4倍和6倍,表明该纳米乳佐剂具有明显的增强免疫的效果,且纳米乳佐剂组在抗体达峰值后能持续较长时间。

图5 各组小鼠血清中HI抗体滴度的比较
2.6最大给药量实验在0.25 μg/10 g的给药量下,小鼠均无死亡,活动力与生理盐水对照组相比没有明显差异,一周后解剖小鼠,未发现脏器异常,说明该纳米乳具有较好的安全性。
3 讨 论
本实验得出的纳米乳配方含水量80%(w/w),Tween-20为4.7%(w/w),Span-80 为4.7%(w/w),1,2-丙二醇为4.7%(w/w),液体石蜡油6%(w/w)。目前的同类佐剂中,完全弗氏佐剂只能在使用前即时乳化,其过程需要在一定摩擦力或剪切力下长时间进行[6],期间可能会有大量的抗原损失,而该纳米乳与疫苗简单混合就能直接使用,避免了繁杂的乳化过程,相较于完全弗氏佐剂具有一定优势。铝佐剂作为全世界范围内认可的疫苗佐剂,因只能激发机体的体液免疫,故其佐剂效果不如纳米乳佐剂[7]。因此,开发工艺简单、安全性高的纳米乳佐剂具有一定的现实意义。
在佐剂效果方面,该纳米乳免疫机体产生的血凝抑制抗体成倍高于以上两种对照佐剂,显示出极大的佐剂优势[8]。与已报道的纳米乳佐剂[9]相比,本研究将Tween-20改为Tween-80,其成乳的Km值就由1∶1变为2∶1。根据相关研究,纳米乳的组分极大的影响其粒径大小、稳定性[10]与载水量。首先,粒径大小是微观颗粒的最重要性质和评价指标之一,可能影响纳米乳体系的某些物理化学性质(如光学性质和重力稳定性),而作为佐剂,粒径大小影响免疫反应的类型和反应强度,如Kanchan V和Panda AK[11]发现200~600 nm大小的颗粒容易通过淋巴结利用抗原提呈细胞(Antigen Presenting Cell,APC)激发Th1型细胞免疫反应,而2~8 μm的颗粒则是经巨噬细胞的吞噬或胞饮作用运输至淋巴结而激发体液免疫。本研究获得的纳米乳粒径约为50 nm,是一种严格意义上的纳米乳,相比完全弗氏佐剂(粒径大于1 000 nm)能激发机体产生更高的抗体水平,说明这种粒径大小的纳米乳能激发较强的体液免疫,而对细胞免疫的影响则有待进一步研究。其次,纳米乳的组成影响其稳定性,复合乳化剂比单一乳化剂更易形成稳定纳米乳[12],单一表面活性剂所制备的乳剂易出现混浊,不同亲水亲油平衡(HLB)值的乳化剂形成纳米乳的性质不同,HLB值在8~18内的表面活性剂形成O/W型纳米乳,本实验的纳米乳由Span-80(HLB值为4.3)和Tween-80(HLB值为15)形成复合乳化剂,因而稳定性高;能被水大量稀释,说明是O/W型,这两个特征为其作为佐剂候选配方提供了基础。
由于该配方纳米乳化学组分含量极低,不易对人体产生毒副作用,具有较好的安全性。其中的非离子型乳化剂Tween-80和Span-80具有毒性低,溶血作用小,能与大多数药物配伍等特点,因此常作为纳米乳的乳化剂。然而,Tween-80也存在一定的急性超敏反应和外周神经毒性[13],其余化学组分的引入也可能形成一定毒副作用,因此探索更高含水量的制剂以降低其毒性是未来研究的重点。
[1] Jackson L,Jackson ML,Phillips CH.Interim adjusted estimates of seasonal influenza vaccine effectiveness(D)-United States[J].Morbidity and Mortality Weekly Report (MMWR),2013,2(7):119-123.
[2] Jaworska M,Sikora E,Ogonowski J,et al.Study of O/W micro and nano-emu-lsions based on propylene glycol diester as a vehicle for geranic acid.Biochimica Polonica[J].Acta Biochim Pol,2015,62(2):229-233.
[3] Hörmann,KZimmer A.Drug delivery and drug targeting with parenteral lipid nanoemulsions [J].J Control Release,2016,10(223):85-98.
[4] Niederquell A1,Kuentz M.Proposal of stability categories for nanodispersions obtained from pharmaceutical self-emulsifying formulations[J].Int J Pharm,2013,446(1-2):70-80.
[5] Shah RR,Dodd S,Schaefer M,et al.The development of self-emulsifying oil-in-water emulsion adjuvant and an evaluation of the impact of droplet size on performance[J].J Pharm Sci,2015,104(4):1352-1361.
[6] 黄小荣,梁昌盛,骆晓枫,等.抗原-弗氏佐剂乳化实验技术的改进与技巧[J].实验室研究与探索,2013,32(8):265-266,285.
[7] Jafari M,Moghaddam PM,Taghizadeh M.Comparative assessment of humoral immune responses of aluminum hydroxide and oil-emulsion adjuvants in Influenza (H9N2) and Newcastle inactive vaccines to chickens[J].Artif Cells Nanomed Biotechnol,2016,13:1-6.
[8] Deng J,Cai W,Jin F.A novel oil-in-water emulsion as a potential adjuvant for infuenza vaccine:development,characterization,stability and in vivo evaluation[J].Int J Pharm,2014,468(1-2):187-195.
[9] 刘洪卿,毕湖冰,赵兰华,等.纳米乳作为流感疫苗佐剂的免疫效果及安全性的初步研究[J].生物制品学,2013,42(7):33-37.
[10] Fox CB,Barnes VL,Evers T,et al.Adjuvanted pandemic influenza vaccine:variation of emulsion components affects stability,antigen structure,and vaccine efficacy[J].Influenza and Other Respiratory Viruses,2013,7(5):815-826.
[11] Kanchan V,Panda AK.Interactions of antigenloaded polylactide particles with macrophages and their correlation with the immune response[J].Biomaterials,2007,28(35):5344-5357.
[12] Li P,Ghosh A,Wagner RF,et al.Effect of combined use of nonionic surfactant on formation of oil-in-water microemulsions.International journal of pharmaceutics[J].2005,288(1):27-34.
[13] 王辉.蛋白制剂中Tween80含量检测研究[J].河北化工,2011,34(3):44-47,78.
EfficacyofaNewNano-EmulsionasInfluenzaVaccineAdjuvant
ZHAO Lanhua,LIU Wei,TANG Shuangyang,et al
(InstitueofPathogenicBiology,UniversityofSouthChina,HunanProvincicalKeyLaboratoryforSpecialPathogensPreventionandControl,Hengyang,Hunan421001,China)
ObjectiveTo screen a new Nano-emulsion fomula with good efficiency,high stability,good safety,suitable particle size and large water capacity to evaluate its feasibility when used as vaccine adjuvant.MethodsNano-emulsions that can be diluted by plenty of water was selected based on pseudo-ternary phase diagram,the basical properties such as PH,viscosity,partical size,stability when centrifuged or long-stem storedweretested.And the emulsion was mixed with influenza vaccine for animal experiments.ICR mice were randomly divided intonormal saline group,single vaccine group,aluminium adjuvant control group,Freund’s adjuvant group and nano emulsion adjuvant group.All mice were immuned by gastrocnemius muscle and weighed within a week.The second immunization was performed at the third week.Sera were collected every week after the second immunization.Finally,the titer of hemagglutination inhibition (HI) antibody was detected and analyzed by SPSS 18.5 software.The maximum dosage experiment was performed to evaluate its safety.ResultsThe emulsion showed stable physical and chemical properties,the PH value was 7.5,viscosity close to water,and the average particle size was 56.3 nm,no demulsification was observed when centrifugedor long-term stored.The mice of Nano emulsion adjuvant group had a significantly higher antibody level than that of other groups in animal test.Finally,the dosage of 0.25 mg/10 g caused no mice death.ConclusionsThe nano-emulsion formula was a good adjuvant with stability,safety and good efficacy.
nano emulsion; adjuvant; influenza vaccine
10.15972/j.cnki.43-1509/r.2016.05.024
2016-04-05;
2016-06-30
衡阳市科学技术发展计划项目(NO:2016KJ67);国家自然科学基金资助(NO:2013GZK09),特殊病原体防控湖南省重点实验室资助项目(湘科计字[2014]5号);湖南省分子靶标新药研究协同创新中心资助项目(湘教通[2015]351号).
*通讯作者,E-mail:zengyihua21cn@126.com.
R392-33
A
蒋湘莲)

