文冠果子壳活性炭对Pb2+的吸附及解吸
郝一男,王喜明,红岭,赵家祺
(内蒙古农业大学材料科学与艺术设计学院,呼和浩特010018)
文冠果子壳活性炭对Pb2+的吸附及解吸
郝一男,王喜明*,红岭,赵家祺
(内蒙古农业大学材料科学与艺术设计学院,呼和浩特010018)
以废弃的文冠果子壳为原料,通过ZnCl2活化法制备活性炭。利用SEM-EDX技术,对文冠果子壳活性炭吸附前后元素组成进行分析。探讨吸附时间、吸附温度、pH以及Pb2+初始浓度对吸附的影响,考察时间、温度、稀硝酸浓度对解吸的影响,分析其吸附热力学性质和动力学特性,初步探讨吸附机理。研究结果表明:在吸附温度30℃,Pb2+初始浓度0.003 2 mol/L,pH 5.0,吸附40 min,吸附量最大可达656.54 mg/g;当稀HNO3浓度0.06 mol/L,温度60℃,解吸40 min,解吸率最大可达96.13%;活性炭对Pb2+吸附等温线符合Langmuir模型,其吸附动力学过程以准二级动力学方程拟合效果最好;在303~323 K温度范围内,活性炭吸附Pb2+的吉布斯自由能ΔGo<0、焓变ΔHo<0、熵变ΔSo<0,表明活性炭对Pb2+吸附是一个自发的放热过程。
文冠果子壳;活性炭;Pb2+;吸附;解吸
重金属污染早已引起国内外广泛关注,其含量超标对水资源、空气和人体健康都会造成严重的危害。铅(Pb)如果不经过处理便排入到环境中,通过水体迁移、土壤和食物链的积累和放大效应,将对人体产生极大的伤害,因此降低或去除水中铅离子显得非常重要和迫切[1]。采用廉价高效的吸附剂去除废水中的铅,是国内外研究人员需要解决的问题,应用最广泛的就是利用生物质资源制备活性炭,如大蒜皮[2]、梧桐叶[3]、杏壳[4]和甘蔗渣[5]等。
文冠果广泛分布于内蒙古赤峰、通辽、鄂尔多斯等地,对文冠果的研发主要以文冠果种仁油的提取及制备生物柴油为主,通常文冠果子壳(XSBH)未被利用而被丢弃。经课题组前期研究发现[6],文冠果子壳活性炭(XSBHAC)对有机染料具有很好的吸附效果,亚甲基蓝吸附量为591.47 mg/g,碱性品红吸附量为359.52 mg/g,对碘吸附量为1 438.05 mg/g,远高于大麻杆[7]、废弃木材[8]等原料所制得的活性炭。鉴于此,本试验选用废弃的文冠果子壳为原料,采用65%的ZnCl2活化制备活性炭,研究pH、Pb2+初始浓度、时间及温度对吸附量的影响,对吸附等温线及动力学方程进行拟合,研究吸附机制,为处理废水中Pb2+提供一种高效的吸附剂,并为其实际应用提供理论依据。
1 材料与方法
1.1 原料、药品及仪器
原料:文冠果采购于内蒙古赤峰市。
药品:氯化锌、硝酸铅、二甲酚橙、六次甲基四胺、盐酸、硝酸、邻二氮菲等化学试剂均为分析纯,试验用水为去离子水。
仪器:BZN-1.5制氮机(杭州市博达华工科技发展有限公司);ML802电子天平(北京梅特勒公司);DHG-9035型电热恒温鼓风干燥箱(上海一恒科学仪器有限公司);TU-1901双光束紫外分光光度计(北京普析仪器有限公司);SHA-C恒温振荡仪(金坛市荣华仪器制造有限公司);6309POT pH测定仪(深圳市长利来科技有限公司);25-10型箱式电阻炉(上海娥江仪器设备有限公司);L5042V低速离心机(上海知信实验仪器技术有限公司);S-3400N扫描电子显微镜和X射线能量色散光谱仪(日本日立公司)。
1.2 文冠果子壳活性炭制备
将XSBH粉碎,称取一定量的粒径为0.25 mm粉末于烧杯内,放入110℃干燥箱内干燥12 h;加入65%的ZnCl2溶液,搅拌1 h后,放入200℃的箱式电阻炉中炭化4 h,继续升至500℃活化2 h,并通入N2;用去离子水反复清洗至中性,抽滤,得到XSBHAC,放入110℃干燥箱中干燥12 h,研磨后密封保存。
1.3 吸附试验
在100 mL锥形瓶中,准确称量0.05 g XSBHAC,加入50 mL已知浓度的硝酸铅溶液和适量的六次甲基四胺缓冲溶液,分别在30,40和50℃下以120 r/min振速恒温振荡40 min;振荡结束后离心分离,取适量上层清液,用紫外分光光度计(吸收波长574 nm)测Pb2+平衡浓度,根据公式(1)计算活性炭平衡吸附量Q:
(1)
式中:C0为吸附前溶液中Pb2+质量浓度,mg/L;Ce为吸附平衡后溶液中Pb2+质量浓度,mg/L;Q为单位质量活性炭对Pb2+平衡时的吸附量,mg/g;V为溶液的体积,L;m为活性炭的质量,g。
1.4 解吸试验
用移液管量取50 mL稀硝酸溶液,加入到50 mL锥形瓶中,加入吸附Pb2+后的活性炭,在不同的酸浓度、时间、温度条件下进行解吸,根据公式(2)计算解吸率:
(2)
式中:C0为吸附前溶液中Pb2+质量浓度,mg/L;C2为解吸溶液中Pb2+质量浓度,mg/L;C1为吸附后溶液中Pb2+浓度,mg/L;P为解吸率,%。
2 结果与讨论
2.1 文冠果子壳及其活性炭表征
对文冠果子壳及其活性炭进行扫描电镜观察如图1~2所示。由图1可见,XSBH中存在一定的大孔结构,且表面较为平滑疏松,从而有利于活化剂快速进入进行疏松孔内,活化造孔。由图2可见,经高温ZnCl2溶液活化后,XSBHAC表面被侵蚀,原先的大孔,向内部延伸,形成丰富的无规则孔隙结构,孔隙内壁光滑,无沉积,并且连通性较好,具有较大的孔隙率, 同时有大量的微小孔存在,构成了空间网状结构[9-10],吸附后的活性炭孔被Pb2+充填,所以XSBHAC存在丰富的微孔或者中孔结构。

图1 XSBH扫描电镜图 Fig. 1 SEM image of XSBH

图2 Pb2+吸附前后XSBHAC的SEM图Fig. 2 SEM images of XSBHAC before and after adsorption of Pb2+
对XSBHAC吸附Pb2+前后元素进行分析如图3所示。由图3a和3b可知,吸附Pb2+的电子能谱分析图(EDX)表明吸附前后XSBHAC表面的元素含量出现了明显变化。吸附前,活性炭表面由C、O、N、Cl、Na等元素组成,其质量分数分别为80.26%,12.92%,5.62%,0.75%和0.46%。吸附后,活性炭表面由C、O、N、Pb、Cl、Na等元素组成,其质量分数分别为75.58%,9.42%,4.19%,10.34%,0.35%和0.12%,这也证实Pb2+在吸附过程中发生了表面沉淀。

图3 XSBHAC吸附Pb2+前后的电子能谱分析图Fig. 3 EDX patterns of XSBHAC before and after the adsorption of Pb2+
2.2 Pb2+初始浓度对吸附的影响
在30℃、pH 5.0、吸附60 min条件下,分析Pb2+初始浓度对吸附效果的影响,结果见图4a。由图4a可知,随着Pb2+初始浓度的增加,XSBHAC对Pb2+的吸附量逐渐增大,当Pb2+浓度为0.003 2 mol/L时,吸附量最大,随后趋于平衡。这是由于随着Pb2+浓度的增加,溶液中单位体积内的所含有的溶质数也将相应的增加,因而单位时间内能够与活性炭接触的溶质分子数也增加[11],吸附量增大;当Pb2+增加到一定浓度时,溶质分子占满活性炭接触位点后,吸附量不再发生变化。
2.3 pH对吸附的影响
在30℃、Pb2+初始浓度0.003 2 mol/L、吸附60 min条件下,分析pH对吸附效果的影响,结果见图4b。由图4b可知,当溶液pH从3.0升至5.0,XSBHAC对Pb2+的吸附量从336.48 mg/g增加到649.38 mg/g,当溶液pH>5.0时,吸附量有所下降。这是因为溶液pH影响活性炭表面电性以及溶液中Pb2+的存在形式,活性炭表面的含氧基团在溶液中H+作用下含有正电性,使活性炭带正电[11],pH越低,越不利于活性炭对Pb2+的吸附。当pH>6.0时,Pb2+将形成Pb(OH)2沉淀,不利于XSBHAC对Pb2+的吸附。由此可得,吸附体系的最佳pH应为5.0。
2.4 吸附温度对吸附的影响
在Pb2+初始浓度0.003 2 mol/L,pH 5、吸附40 min条件下,分析温度对吸附效果的影响,结果见图4c。由图4c可知,当温度从20℃升至70℃时,XSBHAC对Pb2+吸附量从656.54 mg/g下降到549.46 mg/g,即随着温度升高,吸附量逐渐下降,由于活性炭吸附Pb2+是放热反应,因此,温度升高不利于活性炭表面吸附Pb2+,低温利于对Pb2+的吸附。虽然高温有利于Pb2+在活性炭表面的扩散速率,激发活性炭表面的官能团与Pb2+发生反应,但是如果温度升至30℃以上,吸附量会急剧下降,解吸能高于吸附能[12],Pb2+比较活跃,在活性炭边界层中的传质阻力减弱,导致已吸附的Pb2+从活性炭表面脱附下来,从而导致吸附量下降。因此,活性炭吸附Pb2+体系的最佳温度为30℃。
2.5 吸附时间对吸附的影响
在温度为30℃、Pb2+溶液初始浓度0.003 2 mol/L、pH为5.0时,分析时间对吸附效果的影响,见图4d。由图4d可以看出,吸附随时间的延长呈先增大后趋于平缓的趋势,当吸附时间为40 min时,Pb2+吸附量最大。这是因为随着时间的延长,溶液中Pb2+占据活性炭吸附位点的接触时间越长,在40 min时,XSBHAC对Pb2+的吸附量基本趋于稳定。初始时,Pb2+吸附量增加迅速,此时由于XSBHAC上吸附点位较多,伴随着吸附的进行,吸附点位缓慢减少,Pb2+吸附量增速减慢。另外,由于Pb2+液相浓度与活性炭表面Pb2+浓度差越来越小,传质推动力减弱,吸附速率降低。因此,吸附体系的最佳吸附时间为40 min。

图4 Pb2+初始浓度,pH,温度和时间对XSBHAC吸附量的影响Fig. 4 The effects of initial Pb2+ concentration, pH, temperature and time on the adsorption capacity of XSBHAC
2.6 吸附动力学
分别运用准一级动力学方程(3)和准二级动力学方程(4)描述XSBHAC吸附Pb2+的速率快慢[2],通过动力学模型进行拟合,研究吸附机理。
准一级动力学方程:
(3)
准二级动力学方程:
(4)
式中:Qe和Qt为吸附平衡和t时刻单位质量活性炭Pb2+的吸附量,mg/g;K1为准一级动力学速率常数,min-1;K2为准二级动力学速率常数,g/(mg·min)。
XSBHAC吸附Pb2+的准一级动力学和准二级动力学模型见图5,动力学相关参数见表1。可以看出,在0.000 5~0.005 0 mol/L Pb2+浓度范围内,303~323 K实验温度条件下,准二级动力学方程的线性决定系数R2均高于0.99,相关性明显高于准一级动力学模型,而且由准二级动力学方程计算吸附量与实验测得吸附量接近。这表明,XSBHAC吸附Pb2+符合准二级动力学方程,属于化学吸附,吸附速率取决于活性炭表面的吸附位点。
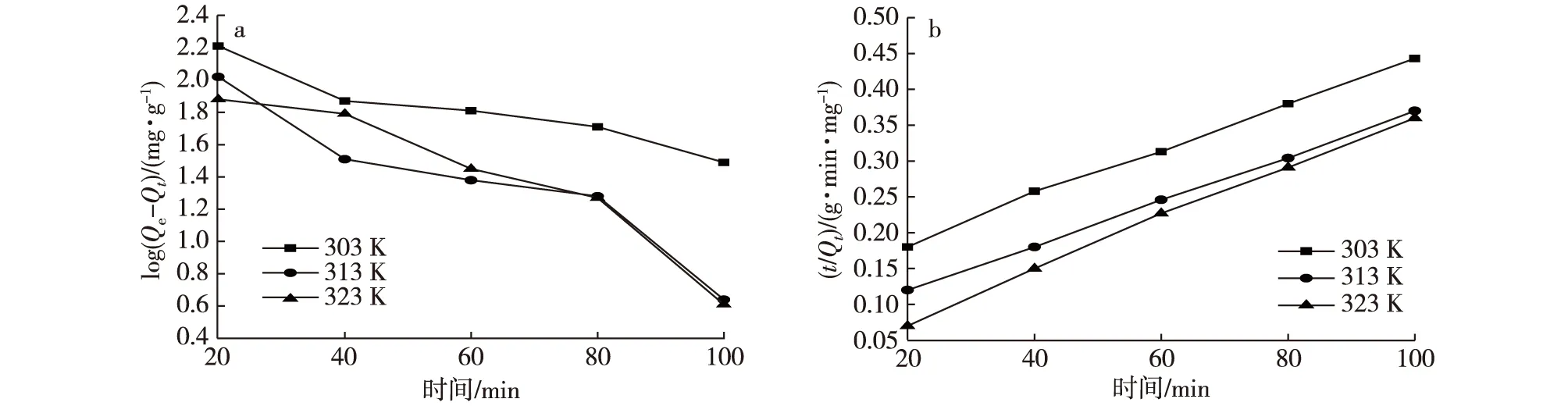
图5 XSBHAC吸附Pb2+的准一级、准二级动力学模型Fig. 5 Pseudo-first-order and pseudo-second-order adsorption kinetic equations of Pb2+ by XSBHAC

T/K准一级动力学方程准二级动力学方程R2Qe/(mg·g-1)K1/min-1R2Qe/(mg·g-1)K2/(g·mg-1·min-1)303092869678400077099773114250825133130909410723100154099963134500193204323091268465800095099803030275354331
2.7 吸附等温线
分别用Langmuir和Freundlich吸附模型拟合不同温度下XSBHAC吸附Pb2+的实验数据[13]。吸附等温线方程如式(5)和(6)所示:
(5)
(6)
式中:Qm为活性炭对Pb2+的饱和吸附量,mg/g;Qe为单位质量活性炭对Pb2+平衡时的吸附量,mg/g;Ce为吸附平衡后溶液中Pb2+浓度,mg/L;KF和n为Freundlich方程经验常数;KL为Langmuir方程常数,L/mg。
XSBHAC对Pb2+的Langmuir吸附等温线和Freundlich吸附等温线见图6,拟合的回归参数见表2。可以看出,在303~323 K实验温度范围内,Langmuir吸附等温线决定系数R2均高于0.99,吸附属于单分子层吸附。Frendlich 吸附等温线决定系数R2与Langmuir吸附等温线相比较低, Fre-undlich方程经验常数1/n值在0.463 8~0.494 1之间,一般认为0.1<1/n<0.5时,易于吸附,1/n>2时,吸附较为困难[14],说明XSBHAC比较容易吸附溶液中的Pb2+。
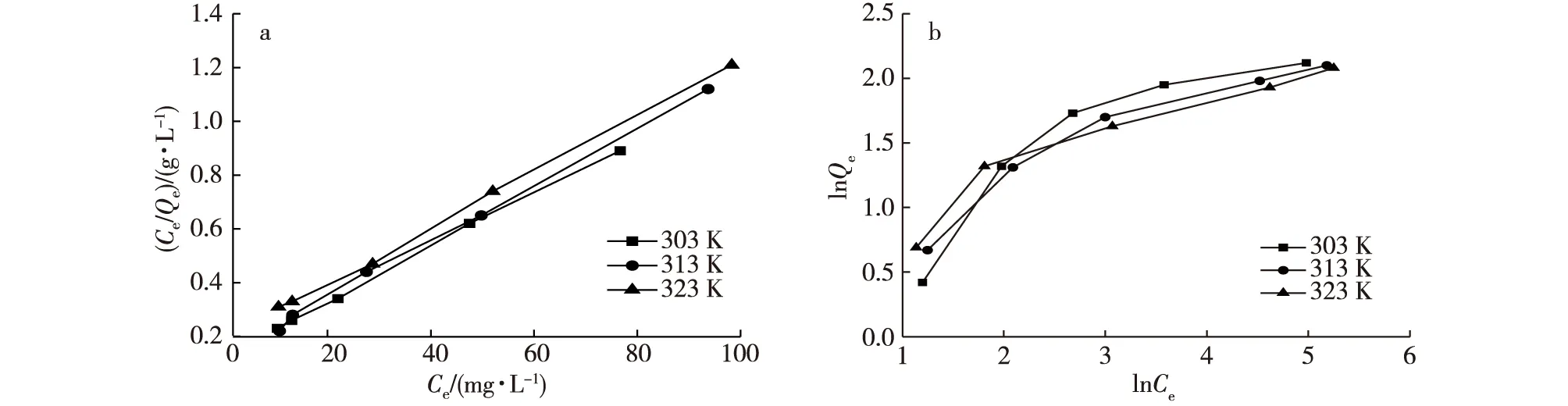
图6 Langmuir和Freundlich吸附等温线Fig. 6 The adsorption isothermal curve of Langmuir and Freundlich

T/KLangmuir等温式Freundlich等温式R2KLRLKFR21/n303099880468800032307330798504941313099800463000032303620904004779323099900498100030308530905004638
2.8 吸附热力学参数
XSBHAC吸附Pb2+热力学参数,吉布斯自由能(ΔGo)、熵(ΔSo)、焓(Ho)分别用(7~9)公式[15]计算:
(7)
ΔGo=-R·T·lnK
(8)
K=Qe/Ce
(9)

图7 HNO3浓度、时间和温度对XSBHAC解吸率的影响Fig. 7 The effect of HNO3 concentration, time and temperature on the desorption efficiency of XSBHAC
式中:ΔGo为吉布斯自由能,kJ/mol;ΔSo为熵,J/(mol·K);ΔHo为反应焓,kJ/mol;R为气体摩尔常数,8.314 J/(mol·K);T为绝对温度,K;K是Langmuir平衡常数,L/mol。
lnK对1/T作图由斜率和截距得出ΔSo和ΔHo见表3。由表3可知,ΔHo<0,说明是一个放热反应,ΔGo<0,表明溶液中的Pb2+容易被吸附到XSBHAC的表面,活性炭吸附Pb2+是自发进行的,ΔSo<0,说明在吸附过程中XSBHAC与Pb2+溶液界面上分子的运动无序性下降。所以XSBHAC吸附Pb2+是一个自发放热熵降低过程。

表3 XSBHAC吸附Pb2+热力学参数
2.9 硝酸浓度对解吸的影响
在30℃、取吸附Pb2+后的XSBHAC 0.05 g、解吸60 min条件下,考查稀硝酸浓度对解吸效果的影响,结果见图7a。由图7a可知,稀硝酸浓度达0.06 mol/L时解吸率最大,随着浓度的增加,解吸率基本不变,这是因为Pb2+与活性炭发生了化学反应,单纯的改变HNO3浓度不能提高解吸率。本试验结果以取0.06 mol/L为最佳解吸硝酸浓度。
2.10 时间对解吸的影响
在30℃、取吸附Pb2+后的XSBHAC 0.05 g、稀硝酸浓度0.06 mol/L条件下,考查时间对解吸效果的影响,结果见图7b。由图7b可知,在20~40 min内解吸率增加缓慢,40 min时达到最大,40 min后解吸趋于平衡。主要是因为在解吸反应过程中,溶液中的Pb2+与XSBHAC表面的Pb2+之间的浓度梯度逐渐减小,反应推动力逐渐减小,解吸速率越来越慢,直到解吸反应达到平衡。
2.11 温度对解吸的影响
在稀硝酸浓度0.06 mol/L、取吸附Pb2+后的XSBHAC 0.05 g、解吸40 min条件下,考查温度对解吸效果的影响,结果见图7c。由图7c可知,当温度从30℃升至60℃时,Pb2+解吸率从92.80%增加至96.13%,即解吸率随着温度的升高而增加,Pb2+从XSBHAC上的解吸是吸热过程,温度升高向着解吸方向进行,这是因为温度升高,溶液黏度逐渐降低,活性炭中的Pb2+与H+的碰撞机会逐渐增加,从而导致解吸率增大;溶液中的Pb2+与XSBHAC表面的Pb2+之间的浓度差变大,传质推动力增大,传质速率提高, Pb2+在溶液中的溶解度增加[15]。因此,随着温度的上升,利于Pb2+在活性炭表面的解吸,与较低温利于XSBHAC吸附Pb2+正好相反。
3 结 论
1)通过SEM-EDX分析,XSBHAC存在丰富的微孔或者中孔结构,吸附前后XSBHAC表面的元素含量出现了明显变化,证实了Pb2+在吸附过程中发生了表面沉淀。
2)进行了XSBHAC吸附Pb2+的试验,研究了时间、Pb2+初始浓度、pH、温度对吸附效果的影响,得到了最佳工艺条件:当时间40 min,Pb2+初始浓度0.003 2 mol/L,pH=5.0,温度30℃条件下,吸附量最大为656.54 mg/g;当稀硝酸浓度0.06 mol/L,温度60℃,时间40 min,解吸率最大为96.13%。
3)在Pb2+初始浓度0.000 5~0.005 0 mol/L范围内,XSBHAC吸附Pb2+等温线符合Langmuir方程,准二级动力学方程能够较好地描述其吸附的动力学过程;在303~323 K实验温度范围内,XSBHAC吸附Pb2+热力学参数ΔGo<0、ΔHo<0、ΔSo<0,说明该吸附是一个自发的放热过程,温度的升高不利于XSBHAC对Pb2+的吸附。
[1]MOYERS B, WU J S. Removal of organic precursors by permanganate oxidation and alum coagulation[J]. Water Research, 1985, 19(3):309-314.
[2]HAMEED B H, AHMAD A A. Batch adsorption of methylene blue from aqueous solution by garlic peel, an agricultural waste biomass[J]. Journal of Hazardous Materials, 2009, 164(2/3):870-875.
[3]HAN R P, ZOU W H, YU W H. Biosorption of methylene blue from aqueous solution by fallen phoenix tree’s leaves[J]. Journal of Hazardous Materials, 2007, 141(1):156-162.
[4]杨继亮, 岳贤田, 周建斌. 活性炭对卷烟烟气中汞和铅的吸附[J]. 林业工程学报, 2016, 1(1):68-73. YANG J L, YUE X T, ZHOU J B. The adsorption of Hg and Pb in the cigarette mainstream smoke by activated carbon[J]. Journal of Forestry Engineering, 2016, 1(1):68-73.
[5]CRONJE K J, CHETTY K, CARSKY M, et al. Optimization of chromium (VI) sorption potential using developed activated carbon from sugarcane bagasse with chemical activation by zinc chloride[J]. Desalination, 2011, 275(1/2/3):276-284.
[6]郝一男. 文冠果种仁油的提取及其生物柴油合成的研究[D]. 呼和浩特:内蒙古农业大学, 2011. HAO Y N. Study on extraction of xanthoceras sorbiflia bunge seed oil and preparation of biodiesel fromXanthocerassorbifliabunge seed oil[D]. Hohhot:Inner Mongolia Agricultural Univer-sity, 2011.
[7]蒋志茵, 杨儒, 张建春, 等. 大麻杆活性炭对染料吸附性能的研究[J]. 北京化工大学报(自然科学版), 2010, 37(2):83-89. JIANG Z Y, YANG R, ZHANG J C, et al. Adsorption studies of dyes on hemp haulm-based activated carbon[J]. Journal of Beijing University of Chemical Technology(Natural Science Edition), 2010, 37(2):83-89.
[8]TSANG D C W, HU J, LIU M Y. Activated carbon produced from waste wood pallets:adsorption of three classes of dyes[J]. Water Air & Soil Pollution, 2007, 184(1):141-155.
[9]XU J, ZHOU P Y, LIN Y Z, et al. Influence of activator on porous structure of activated carbon derived from tung-nut-shell[J]. Advances in Fine Petrochemicals, 2012, 12(9):54-58.
[10]张晓雪, 王欣. 磷酸活化沙柳制备活性炭工艺[J]. 林业工程学报, 2016, 1(3):58-62. ZHANG X X, WANG X. Study of preparation of salix psammophila activated carbons by the activation of H3PO4[J]. Journal of Forestry Engineering, 2016, 1(3):58-62.
[11]YU J F, CHEN P R, YU Z M, et al. Preparation and characteristic of activated carbon from sawdust bio-char by chemical activation with KOH[J]. Acta Agronomica Sinica, 2013, 30(9):1017-1022.
[12]KUMAR K V, Ramamurthi V, SIVANESAN S. Modelling the mechanism involved during the sorption of methylene blue onto fly ash[J]. Journal of Colloid Interface, 2005, 284(1):14-21.
[13]杨军, 张玉龙, 杨丹, 等. 稻秸对Pb2+的吸附特性[J]. 环境科学研究, 2012, 25(7):815-819. YANG J, ZHANG Y L, YANG D, et al. Adsorption characteristics of Pb2+on rice straw[J]. Research of Environmental Sciences, 2012, 25(7):815-819.
[14]刘斌, 顾洁, 屠扬艳, 等. 梧桐叶活性炭对不同极性酚类物质的吸附[J]. 环境科学研究, 2014, 27(1):92-98. LIU B, GU J, TU Y Y, et al. Adsorption property of activated carbon from leaves of phoenix tree on different polarity phenols[J]. Research of Environmental Sciences, 2014, 27(1):92-98.
[15]张晓涛, 王喜明. 木质纤维素/纳米蒙脱土复合材料对废水中Cu(Ⅱ)的吸附及解吸[J]. 复合材料学报, 2015, 32(2):385-394. ZHANG X T, WANG X M. Adsorption and desorption of Cu(Ⅱ) in wastewater by lignocellulose nano-montmorillonite composites[J]. Acta Materiae Compositae Sinica, 2015, 32(2):385-394.
Adsorption and desorption of Pb2+byXanthocerassorbifoliabunge hull activated carbon
HAO Yinan, WANG Ximing*, HONG Ling, ZHAO Jiaqi
(CollegeofMaterialsScienceandArtDesign,InnerMongoliaAgriculturalUniversity,Hohhot010018,China)
Mesoporous activated carbon with high surface area was prepared from wasteXanthocerassorbifoliabunge hull by ZnCl2activation. The elemental composition ofX.sorbifoliabunge hull activated carbon(XSBHAC)before and after adsorption were analyzed by SEM-EDX. The adsorption process were carried out including initial Pb2+concentration,adsorption time,pH and temperature, while the desorption experiments were investigated in order to analyze the influences of HNO3concentration, time and temperature, the thermodynamic, and kinetic parameters. The adsorption mechanism was discussed preliminarily. The results showed that the maximum adsorption capacity of Pb2+reached 656.54 mg/g at an initial Pb2+concentration, solution pH value, temperature, and adsorption time of 0.003 2 mol/L, 5.0, 30℃, and 40 min, respectively. The satisfactory effect of the best desorption efficiency was 96.13% at HNO3concentration, desorption temperature, and desorption time of 0.06 mol/L, 60℃, and 40 min, respectively. The modeling of adsorption kinetics indicated good agreement of experimental data with the pseudo-second-order kinetic model. Langmuir equilibrium isotherm fitted the experimental data reasonable well. The calculated values of the Gibbs free energy ΔGo<0,enthalpy change ΔHo<0, entropy change ΔSo<0 when temperature were in range of 303 K to 323 K,which revealed the adsorption was a spontaneous and exothermic process.
Xanthocerassorbifoliabunge hull; activated carbon; Pb2+; adsorption; desorption
2016-06-01
2016-09-09
内蒙古人才开发基金项目;内蒙古农业大学科技成果转化项目(CGZH2014009);内蒙古科技创新引导奖励项目(20131506,20140609)。
郝一男,男,博士,研究方向为生物质能源。通信作者:王喜明,男,教授。E-mail:w_ximing@263.net
TQ424.1+5
A
2096-1359(2017)01-0078-06

