MgO-B2O3-SiO2-CaO-Al2O3体系富硼渣表面张力的计算
许继芳,李建朝,翁文凭,盛敏奇,陈 栋,张捷宇,陈 瑶
(1. 苏州大学 沙钢钢铁学院,苏州 215021;2. 上海大学 省部共建高品质特殊钢冶金与制备国家重点实验室,上海 200072;3. 河北工业职业技术学院 材料工程系,石家庄 050091)
MgO-B2O3-SiO2-CaO-Al2O3体系富硼渣表面张力的计算
许继芳1,李建朝2,3,翁文凭1,盛敏奇1,陈 栋1,张捷宇2,陈 瑶1
(1. 苏州大学 沙钢钢铁学院,苏州 215021;2. 上海大学 省部共建高品质特殊钢冶金与制备国家重点实验室,上海 200072;3. 河北工业职业技术学院 材料工程系,石家庄 050091)
基于熔渣结构的离子与分子共存理论和Butler方程建立了MgO-B2O3-SiO2-CaO-Al2O3体系表面张力计算模型,计算了该体系及其子体系表面张力值,考察了熔渣表面张力随熔渣组分的变化规律,以期为富硼渣调控和综合利用提供参考。结果表明:本模型计算的熔渣表面张力值与实验值吻合较好,模型平均相对误差为9.03%。含B2O3的二元体系中,B2O3组元显著降低熔渣表面张力,纯氧化物表面张力值与形成氧化物阳离子的静电势及氧化物中离子键的分数有关。含B2O3的多元体系中,熔渣表面张力随着B2O3含量的增加而显著降低,但随着MgO和SiO2质量比、CaO含量和Al2O3含量的增加而逐渐增大,且CaO和Al2O3含量对含B2O3渣表面张力的影响基本相当。
MgO-B2O3-SiO2-CaO-Al2O3熔渣;表面张力;组分含量;共存理论;计算模型
我国蕴藏丰富的硼铁矿资源,硼铁精矿高炉冶炼后得到含硼生铁和富硼渣[1]。富硼渣中主要物相为遂安石(2MgO…B2O3)、镁橄榄石(2MgO…SiO2)以及少量的钙黄长石(2CaO…Al2O3…SiO2)[2]。其化学成分约为B2O314%~17%、MgO 43%~46%、SiO220%~23%、CaO 4%~6%、Al2O36%~8%(质量分数)[3]。硼铁矿高炉铁硼分离过程中,表面张力过小时,渣铁分离困难,金属熔体容易进入熔渣中,不利于硼铁分离提取。富硼渣是宝贵的二次资源,富硼渣主要通过碳碱法、硫酸法、熔态钠化-热处理-加压水浸法等方法用来生产硼砂、硼酸和一水硫酸镁等[4-6]。富硼渣还可通过多组分整体转型,制备具有富硼渣资源特点的含硼复合材料[7]。
硼铁矿火法分离工艺中铁硼分离程度决定富硼渣中有价硼、镁等资源的品味,对富硼渣中有价元素的分离利用产生重要影响。而富硼渣的熔体物性对铁硼分离提取具有显著影响,其中表面张力对渣金界面反应、硼铁分离提取等过程具有决定作用[8]。目前,虽然一些研究者研究了含硼渣的表面张力[9-10],但鉴于熔渣表面张力测定的实验难度大,富硼渣成分复杂且变化范围广,因此,利用模型对多元富硼渣体系表面张力进行计算和预测很有必要,目前关于多元含硼渣体系的表面张力计算模型尚未见报道。
BULTER[11]根据化学势和表面能建立了熔体表面张力计算方程(Butler方程)。成国光等[12]基于熔渣结构离子和分子共存理论以及Butler方程,提出了一个热力学模型计算熔渣的表面张力,该模型计算过程中基于纯组分的表面张力和摩尔体积,结合实际熔渣结构合理假设,模型简单且适用性强,在多组元熔渣表面张力计算中得到广泛验证和推广[13-14]。因此,本文作者基于含B2O3熔渣结构的离子与分子共存理论和熔体表面张力的Butler方程,建立MgO-B2O3- SiO2-CaOAl2O3富硼渣体系表面张力的计算模型,并将计算结果与对应的实验测量值进行对比,以验证模型的准确性;并在此基础上,计算1873K下MgO-B2O3-SiO2-CaO-Al2O3渣系及其子体系的熔渣表面张力,考察熔渣表面张力随熔渣组分的变化规律,以期为富硼渣调控和综合利用提供参考。
1 MgO-B2O3-SiO2-CaO-Al2O3体系熔渣结构单元的确定
本模型的关键环节即为依据熔渣结构离子与分子共存理论确定熔渣中离子、简单分子和复杂分子。目前,MgO-B2O3-SiO2-CaO-Al2O3五元富硼渣体系相图及物相关系未见文献报道,本文作者通过相关的含硼三元体系确定富硼渣体系的物相。MgO-B2O3-SiO2三元相图显示,渣系中存在众多物相,但三元渣系中不存在三元复杂化合物[15]。MgO-SiO2二元体系中,确定的主要物相为2MgO…SiO2和MgO…SiO2两种复杂化合物,B2O3-SiO2二元体系中无复杂化合物,B2O3-MgO二元体系中确定存在3MgO…B2O3和2MgO…B2O3复杂化合物,但对是否存在MgO…B2O3和MgO…2B2O3物相是否稳定存在尚存在争议[16-18],在MgO-B2O3二元体系物相尚存争议的情况下,本研究中确定MgO-B2O3-SiO2三元体系熔渣高温下稳定存在2MgO…SiO2、MgO…SiO2、3MgO…B2O3和2MgO…B2O34种复杂化合物。CaO-B2O3-SiO2三元体系中,CaO…SiO2、3CaO…2SiO2、2CaO…SiO2和3CaO…SiO24种复杂化合物确定存在于CaO-SiO2二元体系中,B2O3-CaO二元体系中存在的复杂化合物为3CaO…B2O3、2CaO…B2O3、CaO…B2O3和CaO…2B2O3,三元复杂化合物B2O3…CaO…2SiO2作为自然矿物(硅酸硼钙石,又称赛黄晶)存在,MOREY等[19]通过水热法合成了该复杂化合物。FLINT等[20]报道了B2O3…5CaO…2SiO2复杂化合物的存在,但SUZUKI等[21]否定B2O3…5CaO…2SiO2存在,而认为存在1713K(1440 ℃)以下稳定存在的B2O3…11CaO…4SiO2复杂化合物。目前,相关CaO-B2O3-SiO2三元优化相图对B2O3…5CaO…2SiO2和B2O3…11CaO…4SiO2是否稳定存在也没有定论[22-23]。在此情况下,本研究中规定CaO-B2O3-SiO2三元体系熔渣高温下稳定存在CaO…SiO2、3CaO…2SiO2、2CaO…SiO2、3CaO…SiO2、3CaO…B2O3、2CaO…B2O3、CaO…B2O3、CaO…2B2O3和B2O3…CaO…2SiO29种复杂化合物[24-25]。Al2O3-B2O3-SiO2三元体系中不存在三元复杂化合物[26],Al2O3-SiO2二元体系中确定的主要物相为3Al2O3…2SiO2,Al2O3-B2O3二元体系中确定的主要物相为9Al2O3…2B2O3和2Al2O3…B2O3。本研究中确定Al2O3-B2O3-SiO2三元体系熔渣高温下稳定存在3Al2O3…2SiO2、9Al2O3…2B2O3和2Al2O3…B2O33种复杂化合物。另外,MgO-SiO2-CaO-Al2O3体系[27]中确定的主要物相为3CaO…Al2O3、12CaO…7Al2O3、CaO…Al2O3、 CaO…2Al2O3、CaO…6Al2O3、MgO…Al2O3、CaO…Al2O3…SiO2、2CaO…Al2O3…SiO2、CaO…MgO…SiO2和2CaO…MgO…2SiO2。综上所述,本研究中确定MgO-B2O3-SiO2-CaO-Al2O3体系熔渣中存在的结构单元包括Mg2+、Ca2+和O2-3种简单离子,B2O3、SiO2和Al2O33种简单分子以及上述26个复杂化合物分子。
2 MgO-B2O3-SiO2-CaO-Al2O3体系熔渣表面张力模型的建立
Butler假设熔体表面相内组分与体相内组分在热力学上都达到平衡,推导出表面张力与热力学性质之间的关系(Butler方程)[11]。本模型基于Butler方程计算熔渣表面张力,熔渣表面相和体相内组分通过熔渣结构离子与分子共存理论来确立。本模型主要假设如下:1) 熔渣表面相与体相都遵守熔渣结构离子与分子共存理论,即组元结构都由简单离子、分子和复合分子组成,熔渣表面相和体相中简单离子和分子进行着形成复合分子的动力学质量平衡反应,且表面相和体相中形成复合分子的反应都遵守质量作用定律;2) 熔渣表面相和体相中各组元的质量作用浓度和熔渣表面张力符合Butler方程:

式中:σipure表示纯组元和Al2O3)的表面张力;Ai为纯组元i的摩尔表面积,其中L为校正因子,熔渣中设为1.091; N0为阿伏加德罗常数,Vi为组元i的摩尔体积);R和 T分别表示摩尔气体常数和绝对温度;为组元i在表面相或体相的质量作用浓度。
根据共存理论[28]以及上述确定的MgO-B2O3-SiO2-CaO-Al2O3富硼渣体系熔渣中存在的结构单元,定义熔渣中成分分别为。结构组元作用浓度符号表示为:
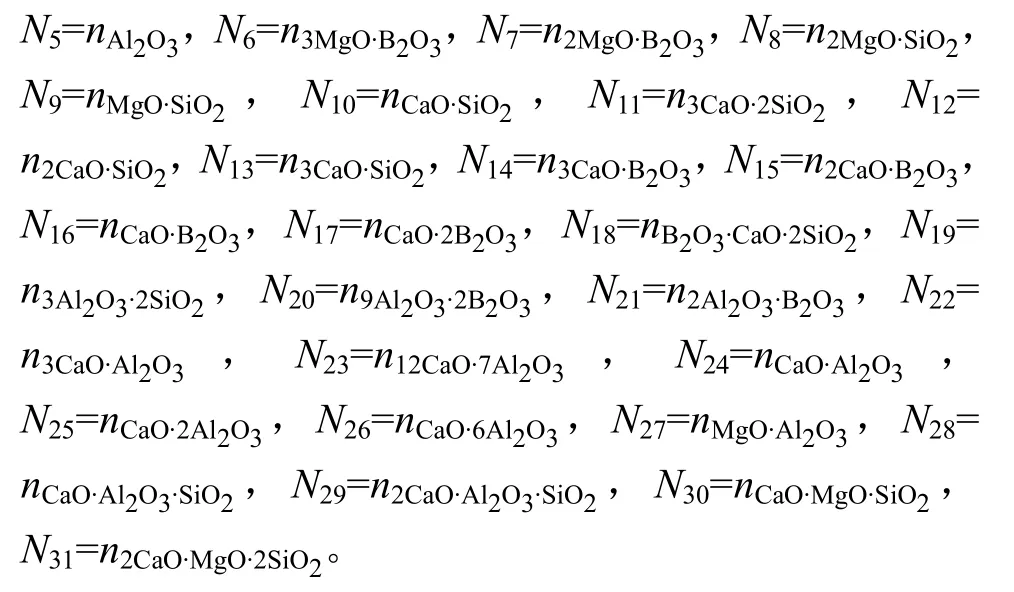
所有组元总平衡摩尔数表示为∑ni。各组元作用浓度表达式为:
在1773~1873 K温度范围内,熔渣中各组分之间形成复杂分子的反应式及其达到平衡时的标准Gibbs自由能(以纯物质为标准态)和质量作用浓度的表达式如表1所列,其中所有反应的平衡常数可通过的关系式进行计算。
MgO-B2O3-SiO2-CaO-Al2O3渣系中质量平衡公式如下:
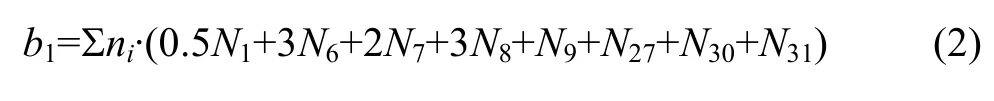
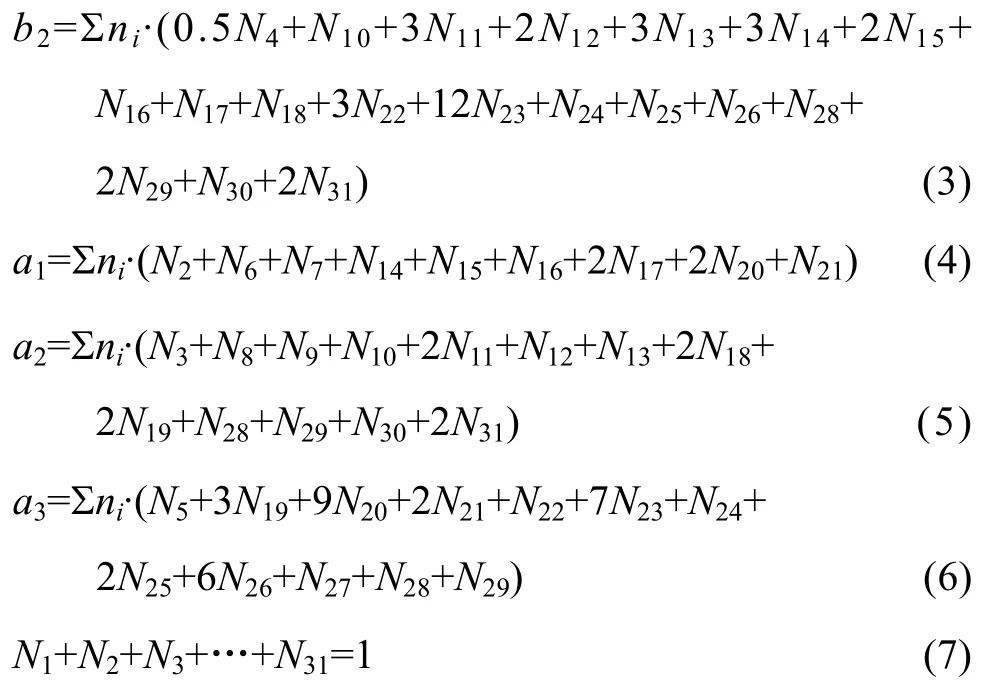
因此,由表1和式(2)~(7)建立计算MgO-B2O3-SiO2-CaO-Al2O3渣系中结构组元和离子对作用浓度Ni的控制方程,其中N6~N31由N1~N5表示出来。在一定温度下,熔渣成分代入该方程组,采用迭代法计算出所有结构组元和离子对的作用浓度。
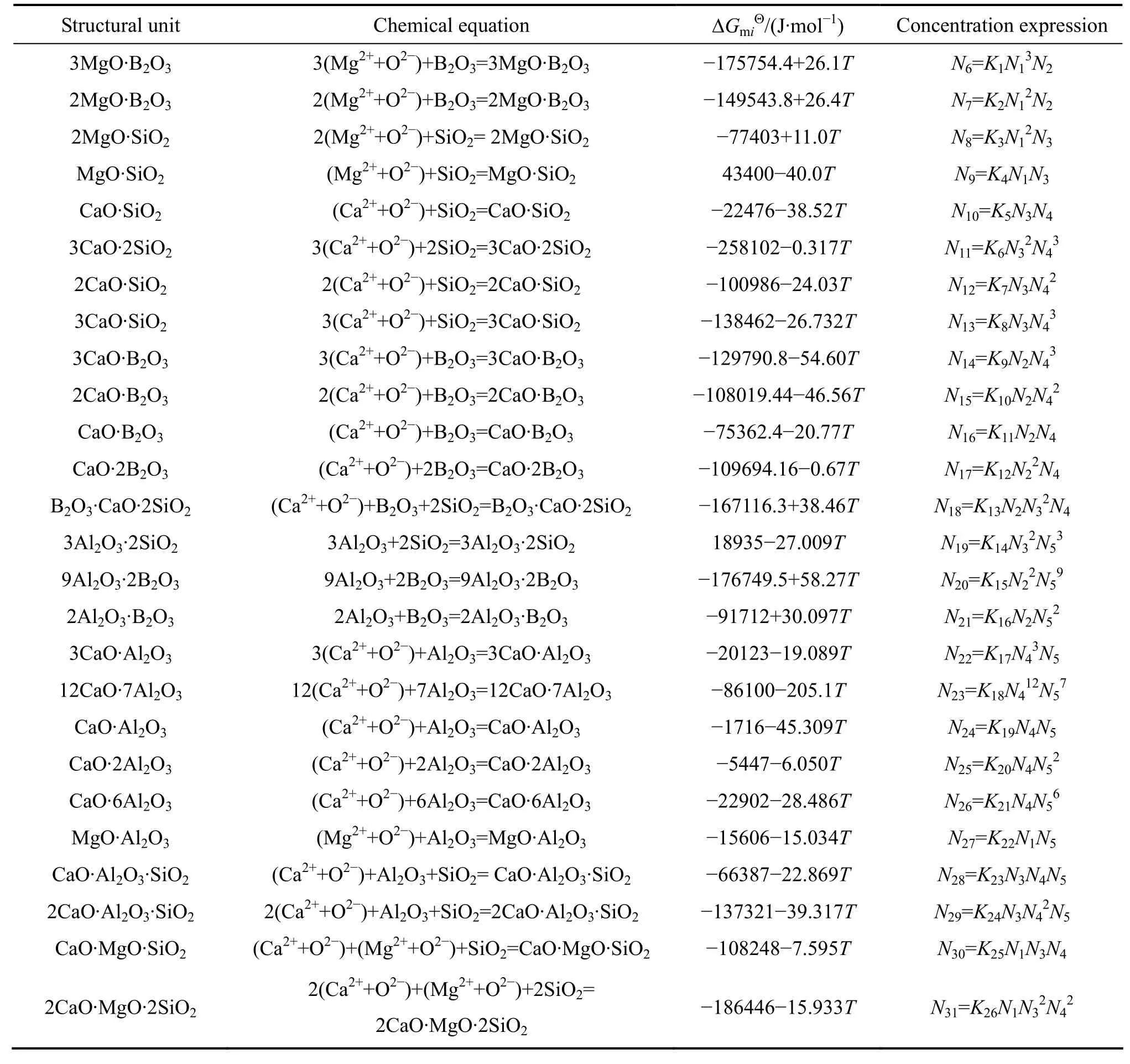
表1 MgO-B2O3-SiO2-CaO-Al2O3渣系中复杂分子的化学反应及标准Gibbs自由能和作用浓度的表达式Table 1 Formulas of action concentrations, standard Gibbs free energies and chemical reactions of complex molecules in MgO-B2O3-SiO2-CaO-Al2O3slag system
对于MgO-B2O3-SiO2-CaO-Al2O3体系,依据Bulter方程,其表面张力可以分别表示为
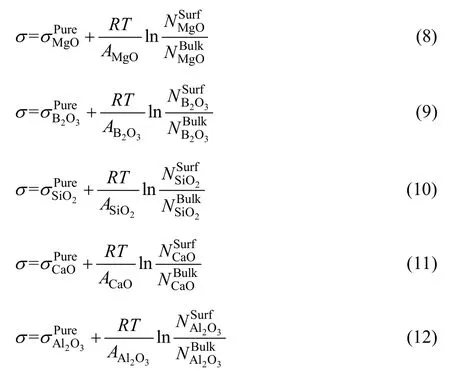
依据上述描述,建立模型可计算熔渣表面张力,其中,NiBulk可以通过熔渣成分的摩尔分数和基于熔渣结构离子与分子共存理论的形成复合分子的化学平衡计算得出。然后进一步基于共存理论和Butler方程,通过已知量NiSurf、σiPure和Ai,利用方程(8)~(12)可计算出σ和NiSurf值。MgO-B2O3-SiO2-CaO-Al2O3渣系中σiPure和Ai数据可见表2和3[29-30]。
3 计算结果及讨论
3.1 表面张力的计算值与实测值对比
为了验证本模型计算结果的准确性,需将计算结果与文献实验数据进行对比。富硼渣相关体系中,已有B2O3-CaO体系、B2O3-SiO2-CaO体系、B2O3-CaOAl2O3体系、B2O3-SiO2-CaO-Al2O3体系和MgOB2O3-SiO2-CaO-Al2O3体系的表面张力实验数据的报道[9-10],相关体系的组分范围及温度范围如表4所列。本研究中计算了上述体系的表面张力计算值,并与文献实验数据进行了对比,对比结果如图1和表4所示。5个体系文献实验结果与计算结果总平均相当误差为9.03%。大多数熔渣的表面张力实验误差一般为±5%~10%,由此可知,本模型计算的熔渣表面张力值与实验值吻合较好。比较结果显示,B2O3-SiO2-CaO体系和B2O3-CaO-Al2O3体系偏差较大,这一方面可能与表面张力高温测量难度和精度导致的误差有关,另一方面本模型未考虑熔渣中部分组元会存在饱和现象。由于氧化物纯物质的熔点偏高,计算温度下采用的氧化物纯组分表面张力数据由已有纯物质的实验数据进行合理的外推得到,这些也可能对模型计算结果带来一定的误差。
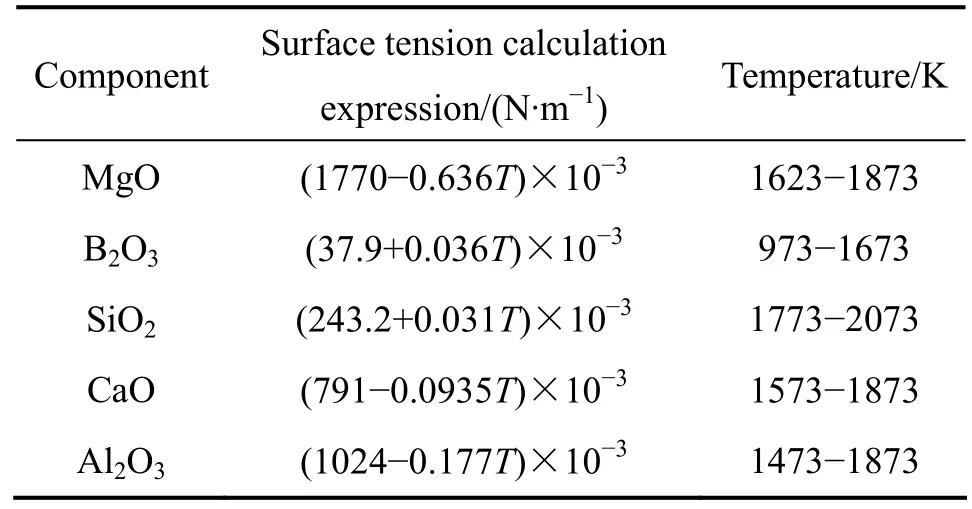
表2 纯组元表面张力与温度的关系Table 2 Temperature dependence of surface tension of pure components

表3 纯组元摩尔体积与温度的关系Table 3 Relationship between molar volume of pure components and temperature
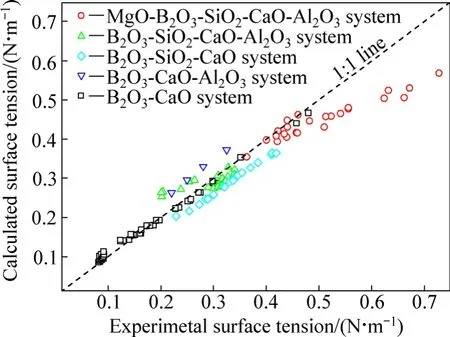
图1 MgO-B2O3-SiO2-CaO-Al2O3体系相关渣系表面张力计算值与文献实验数据的比较Fig. 1 Comparison between calculated values with measured values from literature for MgO-B2O3-SiO2-CaO-Al2O3related system
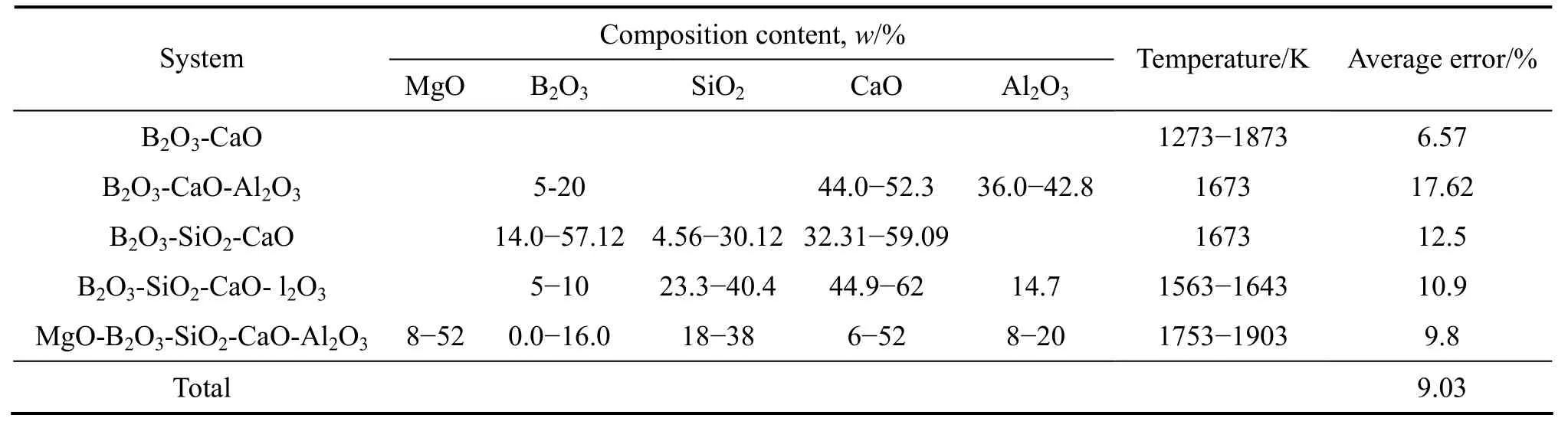
表4 富硼渣相关实验渣系组分、温度及相对平均误差Table 4 Composition content, temperature and relative error average error for B2O3-riched related experimental system
3.2 含B2O3二元体系熔渣表面张力
采用本模型计算1873K下含B2O3二元体系熔渣表面张力,考察B2O3含量对熔渣表面张力的影响。MgO-B2O3体系中,1873K时,在富MgO区(B2O3含量(质量分数)小于28%),存在MgO相和液相的固液两相区(L2+MgO),在富B2O3区(B2O3含量(质量分数)大于70%)存在两液相不互溶区(L1+L2),且该区处于亚稳态,有关该亚稳态区,其边界、体系热力学性质等研究尚不清楚,因此,本研究中虽然计算了MgO-B2O3渣系全浓度范围内的表面张力变化情况,但仅B2O3含量在28%~70%范围内熔渣处于单一液相区(L2)范围[31];CaO-B2O3体系中,在富B2O3区同样存在两液相不互溶区,在不互溶区存在温度相对较低(<1490 ℃),因此,1873 K时,仅在富CaO区(B2O3含量小于22%)存在氧化钙相和液相的固液两相区(L+CaO)[24-25]。B2O3-SiO2二元体系中,熔渣液相区(L)范围比较大,仅富SiO2区(B2O3含量(质量分数)小于3%)存在方英石相和液相的固液两相区(L+方英石)[9]。Al2O3-B2O3二元体系中,熔渣液相区(L)范围较窄,仅在富B2O3区(B2O3含量大于85%)存在液相区[26]。含B2O3二元体系熔渣表面张力计算结果如图2所示。结果表明,作为表面活性物质,B2O3组元能够显著降低熔渣表面张力。熔渣表面张力随着B2O3含量的增加而显著降低。MgO-B2O3体系和CaO-B2O3体系中,酸性氧化物B2O3的增加,将导致阴离子结构复杂化,阴离子团聚合程度增强,对阳离子的静电引力减弱,从而降低了体系的表面张力[32]。B2O3-SiO2体系和Al2O3-B2O3体系中,B2O3对表面张力的降低作用,则可能与硼氧阴离子团与硅氧阴离子团、铝氧阴离子团之间的差异有关[10]。

图2 1873 K时含B2O3二元熔渣表面张力Fig. 2 Surface tension of molten binary system containing B2O3at 1873 K: (a) B2O3-CaO and B2O3-MgO binary systems; (b) Al2O3-B2O3and B2O3-SiO2binary systems
纯氧化物表面张力主要与离子间的键能有关,形成氧化物的离子的静电势(Z/r)大,且离子键分数高的氧化物有较大的表面张力[33]。纯组分氧化物的静电势和离子键分数如图3所示[34]。纯液态B2O3属于表面活性物质,在1873 K时的表面张力约为0.104 N/m,仅为MgO、CaO、Al2O3和SiO2同温度纯物质表面张力数据的1/6~1/3。Si4+和B3+离子虽然静电势很高,但其离子键分数较低(<50%),易形成共价键高、静电势小的络离子,从而其表面张力值较小;Mg2+、Ca2+和Al3+离子虽然静电势较小,但离子键分数较高,从而具有较高的表面张力值。
3.3 含B2O3三元体系熔渣表面张力

图3 1873K下纯氧化物的表面张力值与离子键分数和阳离子静电势(Z/r)Fig. 3 Relationships between surface tension and ion bond fraction (a) and electrostatic potential (b) of cations for pure oxide at 1873 K
1873K时含B2O3三元体系等温相图及液相线如图4所示。实际条件下,Si常存在于金属相中,而SiO2则以硼硅酸盐的形式存在于熔渣中,因此,SiO2添加对含B2O3三元体系热力学性质的影响仍有待确定,MgO-B2O3-SiO2、CaO-B2O3-SiO2和Al2O3-B2O3-SiO2三元系相图也需要进一步优化[11]。1873K时含B2O3三元体系熔渣等表面张力线如图4所示。结果表明,在MgO-B2O3-SiO2体系和CaO-B2O3-SiO2体系1873K完全液相区(Liquid II)范围内,熔渣表面张力值在0.15~0.45 N/m范围内;随着B2O3含量的增加,表面张力显著降低;随着SiO2含量、MgO含量和CaO含量的增加,熔渣表面张力逐渐增大,但MgO含量和CaO含量对表面张力的影响更加显著。在Al2O3-B2O3-SiO2体系1873K完全液相区(Liquid)范围内,熔渣表面张力在0.10~0.30 N/m范围内;熔渣表面张力随B2O3含量的增加而逐渐减小,随SiO2含量和Al2O3含量的增加而逐渐增大。
3.4 MgO-B2O3-SiO2-CaO-Al2O3体系中组分含量对熔渣表面张力的影响
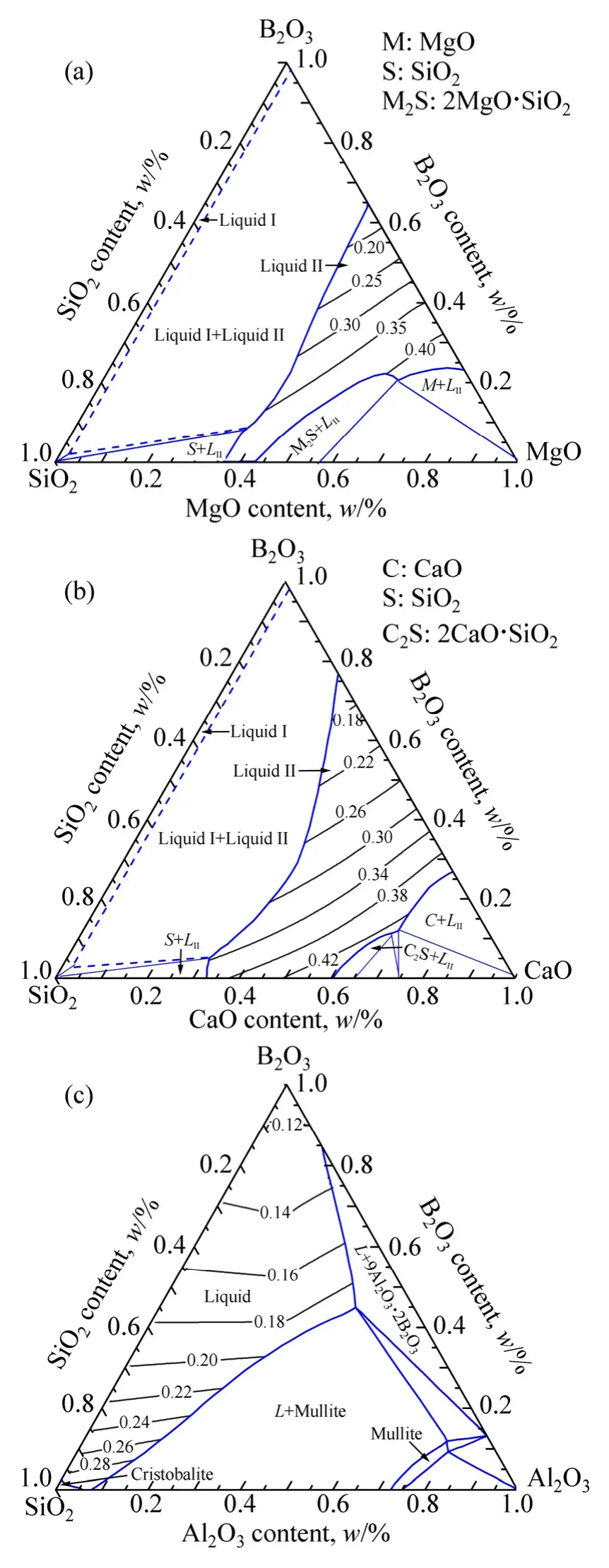
图4 1873K时含B2O3三元系等表面张力线的计算结果Fig. 4 Calculated iso-surface tension lines of ternary system containing B2O3at 1873K: (a) MgO-B2O3-SiO2ternary system; (b) CaO-B2O3-SiO2ternary system; (c) Al2O3-B2O3-SiO2ternary system
采用本模型,考察1873K时组分含量对典型富硼渣表面张力的影响,计算结果如图5所示。图5(a)为1873K时渣中CaO含量和Al2O3含量分别为10%和5%(质量分数),MgO和SiO2质量比为1.0~2.5时,不同B2O3含量(分别为10%、15%、20%和25%(质量分数))下熔渣表面张力与MgO和SiO2的质量比的关系。计算结果显示,熔渣表面张力随着MgO和SiO2的质量比的增加而逐渐增大,但变化的幅度逐渐降低;熔渣表面张力随着B2O3含量的增加而逐渐降低,且B2O3含量对表面张力的影响对MgO和SiO2的质量比更加显著。图5(b)为1873K时渣中MgO和SiO2的质量比为1.5、B2O3含量为15%、Al2O3含量在1%~15%时(质量分数),不同CaO含量(分别为1%、5%、9%和13%(质量分数))下熔渣表面张力与Al2O3含量的关系。计算结果显示,熔渣表面张力随CaO含量和Al2O3含量的增加而逐渐增大,不同CaO含量下表面张力随Al2O3含量变化的趋势基本一致,CaO含量对表面张力的影响与Al2O3含量对表面张力的影响基本相当。

图5 1873K下MgO-B2O3-SiO2-CaO-Al2O3体系熔渣表面张力与组分含量的关系Fig. 5 Relationships between surface tension of MgO-B2O3-SiO2-CaO-Al2O3system with composition at 1873K: (a) Effects of m(MgO)/m(SiO2) and B2O3content; (b) Effects of CaO content and Al2O3content
综上所述,硼铁矿火法分离工艺中利用铁水和熔渣在密度、表面张力等方面的差异,实现铁与富硼渣的分离。通过减少硼铁矿中脉石含量,提高富硼渣中MgO/SiO2比值,合理控制CaO和Al2O3含量,从而提高富硼渣表面张力,有利于使渣金间具有足够大的界面张力,提高渣铁分离提取效率。
4 结论
1) 基于熔渣结构离子与分子共存理论和Butler方程建立MgO-B2O3-SiO2-CaO-Al2O3体系熔渣表面张力计算模型,模型计算结果与实验测量值吻合较好。
2) 含B2O3二元体系中,熔渣表面张力随B2O3含量的增加而降低,作为表面活性物质,B2O3组元能显著降低熔渣表面张力。纯氧化物表面张力值与形成氧化物的阳离子静电势及氧化物中离子键分数有关。
3) 含B2O3三元体系熔渣表面张力随着B2O3含量的增加而显著降低;随着SiO2含量、Al2O3含量、MgO含量和CaO含量的增加,熔渣表面张力逐渐增大。
4) MgO-B2O3-SiO2-CaO-Al2O3体系熔渣表面张力随着MgO和SiO2质量比的增加而增大,但变化的幅度逐渐降低;B2O3组元能够显著降低熔渣表面张力;熔渣表面张力随CaO含量和Al2O3含量的增加而逐渐增大,且两者对表面张力的影响基本相当。
REFERENCES
[1] SUI Zhi-tong, ZHANG Xian-peng, YAMAUCHI C. Precipitation selectivity of boron compounds from slags[J]. Acta Materialia, 1999, 47(4): 1337-1344.
[2] 李 杰, 樊占国. 富硼渣钠化法制备硼砂的实验研究[J]. 材料科学与工艺, 2011, 19(1): 144-148. LI Jie, FAN Zhan-guo. Experimental study on preparation of borax from boron-rich slag by adding sodium carbonat[J]. Materials Science & Technology, 2011, 19(1): 144-148.
[3] FU Xiao-jiao, ZHAO Jia-qi, CHEN Shuang-yin, LIU Zheng-gen, GUO Tong-lai, CHU Man-sheng. Comprehensive utilization of ludwigite ore based on metallizing reduction and magnetic separation[J]. Journal of Iron and Steel Research, International, 2015, 22(8): 672-680.
[4] WANG Guang, XUE Qing-guo, WANG Jing-song. Effect of Na2CO3on reduction and melting separation of ludwigite/coal composite pellet and property of boron-rich slag[J]. Transactions of Nonferrous Metals Society of China, 2016, 26(1): 282-293.
[5] 李 杰, 郭学东, 光 明, 姜 涛. 富硼渣硫酸法制取硼酸和一水硫酸镁[J]. 中国有色金属学报, 2014, 24(11): 2943-2949. LI Jie, GUO Xue-dong, GUANG Ming, JIANG Tao. Preparation of boric acid and magnesium sulfate monohydrate from boron-rich slag by sulfuric acid leaching method[J]. The ChineseJournal of Nonferrous Metals, 2014, 24(11): 2943-2949.
[6] LI Jie, FAN Zhan-guo, LIU Yan-li, LIU Su-lan, JIANG Tao, XI Zheng-ping. Preparation of boric acid from low-grade ascharite and recovery of magnesium sulfate[J]. Transactions of Nonferrous Metals Society of China, 2010, 20(6): 1161-1165.
[7] JIANG Tao, XUE Xiang-xin. Synthesis of (Ca, Mg)-α′-Sialon-AlN-BN powders from boron-rich blast furnace slag by microwave carbothermal reduction-nitridation[J]. Transactions of Nonferrous Metals Society of China, 2012, 22(12): 2984-2990.
[8] MILLS K C, KEENE B J. Physical properties of BOS slags[J]. International Materials Reviews, 1987, 32(1/2): 1-120.
[9] Verein Deutscher Eisenhuttenleute. Slag atlas[M]. 2nd ed. Düsseldorf: Verlag Stahleisen GmbH, 1995: 424-425, 436, 454.
[10] 崔传孟, 徐秀光, 张显鹏, 王魁汉, 韩维儒. B2O3-MgO-SiO2-Al2O3-CaO系渣组成对熔体物性的影响[J].金属学报, 1996, 32(6): 637-641. CUI Chuan-meng, XU Xiu-guang, ZHANG Xian-peng, WANG Kui-han, HAN Wei-ru. Effect of composition of B2O3-MgO-SiO2-Al2O3-CaO slag system on physical properties of melt[J]. Acta Metallurgica Sinica, 1996, 32(6): 637-641.
[11] BUTLER J A V. The thermodynamics of the surfaces of solutions[J]. Proceedings of the Royal Society A, 1932, 135(827): 348-375.
[12] CHENG Guo-guang, LIAO Neng-bin. Calculation model for surface tension of slag melt[J]. Journal of Iron and Steel Research, International, 1999, 6(2): 17-20.
[13] 吴铖川, 成国光, 马琦琦. CaF2-CaO-Al2O3-MgO-SiO2渣系表面张力计算模型[J]. 上海金属, 2014, 36(3): 33-36. WU Cheng-chuan, CHENG Guo-guang, MA Qi-qi. Calculating model on the surface tension of CaF2-CaO-Al2O3-MgO-SiO2slag system[J]. Shanghai Metals, 2014, 36(3): 33-36.
[14] CHENG Guo-guang, LIAO Neng-bin. Calculation model for surface tension of slag melt[J]. Transactions of Nonferrous Metals Society of China, 1998, 8(3): 5-10.
[15] SUNKAR A S, MORITA K. Thermodynamic Properties of the MgO-BO1.5, CaO-BO1.5, SiO2-BO1.5, MgO-BO1.5-SiO2and CaO-BO1.5-SiO2slag systems at 1873K[J]. ISIJ international, 2009, 49(11): 1649-1655.
[16] TOROPOV N A, KONOVALOV P F. Binary system magnesium oxide-boric anhydride[J]. Russian Journal of Physical Chemistry, 1940, 14(3): 1103-1109.
[17] MIYAGAWA S, HIRANO S, SOMIYA S. Phase relations in the system MgO-B2O3and effects of boric oxide on grain growth of magnesia[J]. Journal of the Ceramic Association Japan, 1972, 80(2): 53-63.
[18] MUTLUER T, TIMUCIN M. Phase equilibria in the system MgO-B2O3[J]. Journal of the American Ceramic Society, 1975, 58(5/6): 196-197.
[19] MOREY G W, INGERSON E. The melting of danburite: a study of liquid immiscibility in the system, CaO-B2O3-SiO2[J]. American Mineralogist, 1937, 22(1): 37-47.
[20] FLINT E P, WELLS L S. The system lime-boric oxide-silica[J]. Journal of Research of the National Bureau of Standards, 1936, 17(5): 727-752.
[21] SUZUKI K, HIRA I. Study on the system of 2CaO…SiO2-3CaO…B2O3[J]. Journal of the Ceramic Association, Japan, 1970, 78(6): 189-195.
[22] GIULI G, BINDI L, BONAZZI P. Rietveld refinement of okayamalite, Ca2SiB2O7: Structural evidence for the B/Si ordered distribution[J]. American Mineralogist, 2000, 85(10): 1512-1515.
[23] FLETCHER J G, GLASSER F P. Phase relations in the system CaO-B2O3-SiO2[J]. Journal of Materials Science, 1993, 28(10): 2677-2686.
[24] KIM Y J, MORITA K. Relationship between molten oxide structure and thermal conductivity in the CaO-SiO2-B2O3system[J]. ISIJ International, 2014, 54(9): 2077-2083.
[25] SAKAMOTO M, YANABA Y, YAMAMURA H, MORITA K. Relationship between structure and thermodynamic properties in the CaO-SiO2-BO1.5slag system[J]. ISIJ International, 2013, 53(7): 1143-1151.
[26] SWAMY V, JUNG I H, DECTEROV S A. Thermodynamic modeling of the Al2O3-B2O3-SiO2system[J]. Journal of Non-Crystalline Solids, 2009, 355(47): 1679-1686.
[27] ZHANG Jian. Coexistence theory of slag structure and its application to calculation of oxidizing capability of slag melts[J]. Journal of Iron and Steel Research, International, 2003, 10(1): 1-10.
[28] ZHANG Jian. The application of the law of mass action in combination with the coexistence theory of slag structure to the multicomponent slag systems[J]. Acta Metallurgica Sinica (English Letters), 2001, 14(3): 177-190.
[29] NAPOLITANO A, MACEDO P B, HAWKINS E. Viscosity and density of boron trioxide[J]. Journal of the American Ceramic Society, 1965, 48(12): 613-616.
[30] NAKAMOTO M, KIYOSE A, TANAKA T, HOLAPPA L, HÄMÄLÄINEN M. Evaluation of the surface tension of ternary silicate melts containing Al2O3, CaO, FeO, MgO or MnO[J]. ISIJ International, 2007, 47(1): 38-43.
[31] 王 广, 王静松, 薛庆国, 丁银贵. MgO-B2O3二元系熔渣质量作用浓度计算模型[J]. 中国有色金属学报, 2011, 21(12): 3144-3148. WANG Guang, WANG Jing-song, XUE Qing-guo, DING Yin-gui. Mass action concentration calculation model for MgO-B2O3slag melt[J]. The Chinese Journal of NonferrousMetals, 2011, 21(12): 3144-3148.
[32] MILLS K C. The influence of structure on the physico-chemical properties of slags[J]. ISIJ International, 1993, 33(1): 148-155.
[33] DUFFY J A, INGRAM M D. An interpretation of glass chemistry in terms of the optical basicity concept[J]. Journal of Non-Crystalline Solids, 1976, 21(3): 373-410.
[34] HWANG C, RYUA B K, FUJINO S. Surface tension of bismuth borosilicate melts[J]. Thermochimica Acta, 2012, 531: 70-74.
Calculation of surface tension for MgO-B2O3-SiO2-CaO-Al2O3molten boron-rich slag system
XU Ji-fang1, LI Jian-chao2,3, WENG Wen-ping1, SHENG Min-qi1, CHEN Dong1, ZHANG Jie-yu2, CHEN Yao1
(1. School of Iron and Steel, Soochow University, Suzhou 215021, China; 2. State Key Laboratory of Advanced Special Steel, Shanghai University, Shanghai 200072, China; 3. Department of Materials Engineering, Hebei Institute of Vocational and Technique, Shijiazhuang 050091, China)
Based on the coexistence theory of ions and molecules of molten melt structure and Butler’s equation, a thermodynamic model was developed to establish the surface tension of MgO-B2O3-SiO2-CaO-Al2O3system and its sub-system. The relationship between the composition and surface tension was investigated, which provided reference for the regulation and comprehensive utilization of boron-rich slag. The results indicate that the calculated value of surface tension agrees well with the literature data, and the average error is about 9.03%. The surface tension of molten slag decreases with increasing the B2O3component significantly in binary system. The surface tension value of pure oxide is related to the electrostatic potential of cations and the ion bond percentage in oxide. The surface tension in multi-component system increases with increasing the mass ratios of MgO to SiO2, the CaO content and Al2O3content, and the effect of CaO on surface tension is the same as that of Al2O content.
MgO-B2O3-SiO2-CaO-Al2O3molten slag; surface tension; component content; coexistence theory; calculating model
WENG Wen-ping; Tel: +86-13776085647; E-mail: wenpingweng@suda.edu.cn
TF01
A
1004-0609(2017)-01-0206-09
Foundation item: Projects(BK20130308; BK20140337) supported by the Basic Research Program of Jiangsu Province, China; Projects(50874072, 51504155) supported by the National Science Foundation of China; Project(2014M561710) supported by the China Postdoctoral Science Foundation
(编辑 李艳红)
江苏省基础研究计划(自然科学基金)资助项目(BK20130308);国家自然科学基金资助项目(50874072,51204115);中国博士后科学基金资助项目(2014M561710)
2015-12-15;
2016-04-15
翁文凭,副教授,博士;电话:13776085647;E-mail:wenpingweng@suda.edu.cn
Received date: 2015-12-15; Accepted date: 2016-04-15

