血液病毒核酸筛查系统室内质控方法的建立及评价
蒋义,张钢,郭咚,张会平
(湖南省血液中心检验科,长沙 410000)
·质量管理研究·
血液病毒核酸筛查系统室内质控方法的建立及评价
蒋义,张钢,郭咚,张会平
(湖南省血液中心检验科,长沙 410000)
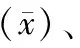
室内质控;病毒核酸;血液筛查
目前全国采供血机构核酸检测(nucleic acid test,NAT)技术已经全面普及,其涉及到许多环节,而室内质量控制对于保证NAT结果的可靠性具有重要意义。然而各血站实验室尚未建立较统一的NAT质量控制体系。由于各实验室使用的检测系统、人员操作及结果判断等不同,导致各实验室间结果差异较大,可比性较差。建立本实验室可行的核酸标准化质量控制方法是实验结果准确可靠的有力保障。《血站核酸检测实验室质量保证指南》中提到血站核酸检测室内质控的基本要求:每一批检测应至少有一个弱阳性室内质控品,基于PCR原理的检测方法可以用循环阈值(Ct值)作为检测值做质控图[1]。本实验室结合检测系统的混样方式及检测下限,设计出阳性室内质控品与阴性质控品检测方案,评价该室内质控模式的可行性,监控室内质控体系的运行情况。
1 材料与方法
1.1 试剂与仪器 质控品标准物质采用北京康切斯特HBV/HCV/HIV(批号:201601001),每支1.5 mL,浓度分别为200 IU/mL、2 000 IU/mL及2 000 IU/mL;NAT阴性质控品采用国家卫生和计划生育委员会临床检验中心室间质评结果阴性的质控品,-20 ℃保存备用。HBV、HCV、HIV(1型)核酸检测试剂盒(PCR-荧光法,批号:20160514,含提取、扩增试剂以及阴、阳性对照,上海科华公司);全自动核酸提取仪STAR(HAMILTON公司);ABI 7500荧光PCR仪(美国ABI公司)。
1.2 质控品检测 按照科华公司试剂说明书的操作步骤,质控品与献血员血液标本在同样条件下进行8混样汇集检测。在汇于1个汇集管的特定位置分别放入HBV DNA、HCV RNA及HIV RNA质控品与5份已知阴性标本,另在汇入1个汇集管的特定位置放入1个阴性质控及7个未知检测结果的献血者标本,同时每批实验含1个阴性对照和1个阳性对照。阴性质控及阴、阳性对照物结果均应符合实验要求,该批次实验结果才有效。
1.3 Ct值与质控品浓度的相关性分析 以HBV DNA为例,将已知浓度的HBV DNA质控品用阴性血清倍比稀释,对每一浓度梯度的血清进行检测(方法同1.2),所得Ct值与各浓度作相关性分析[2]。

1.5 室内质量控制结果分析 得出质控品的最适合浓度,在同一批号下再检测180次,检测方法同1.2。分析并评价该室内质控模式的可行性。
1.6 实验有效性判断 结合Westgard多规则质控方法,判断每批实验的有效性。此外,将阴性质控和7份献血者标本一起检测时,如结果为阴性,实验有效;如为阳性,第2天继续将此孔所含的阴性质控及7份样本单独检测,若阴性质控为阴性,则实验有效。阴、阳性对照物结果均符合实验要求,该批次实验有效。只有满足以上所有条件,实验结果才有效与可信。

2 结果
2.1 HBV DNA室内质控品浓度与Ct值检测关系 质控品倍比稀释后Ct值数据见表1。室内质控品浓度与Ct值的相关系数r=-0.920,在0.05水平达到高度相关。
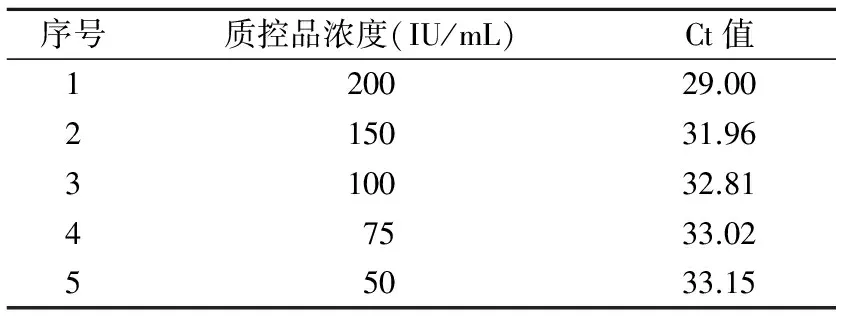
表1 HBV DNA室内质控品浓度与Ct值检测结果


图1 Levey-Jennings质控框架图

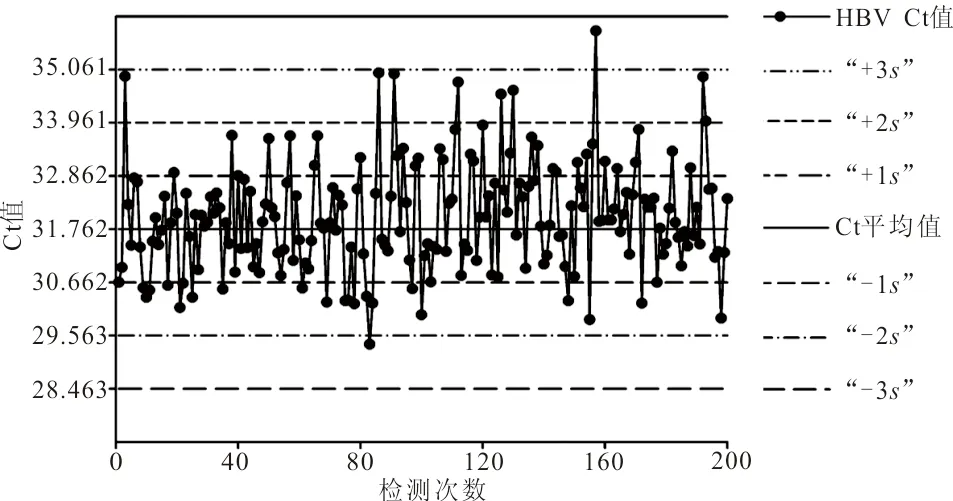
图2 180次质控品的质控图
2.4 室间质评结果 在进行室内质控期间,本实验室参加了澳大利亚NRL国家室间质评(委托上海血液中心提供)及国家卫计委核酸实验室室间质评活动,在阳性室内质控Ct值在控、阴性质控及阴、阳性对照有效的情况下,室间质控结果与靶值完全一致。
3 讨论
Ct值指在PCR扩增过程中,荧光信号由本底进入指数增长阶段的阈值所对应的循环次数。核酸检测的扩增循环数与病毒载量存在一定的线性关系,在指数扩增的开始阶段进行检测,此时样品间的误差尚未放大,因此该Ct值具有很好的重复性[4]。由表1可知,质控品浓度与Ct值呈高度相关。
质控品检测结果是核酸提取和检测有效性的综合反映。科华核酸检测试剂盒说明书提供的8人份混检献血员血浆的HBV DNA 95%置信区间的检出限为50 IU/mL。本实验室购买的HBV DNA室内质控品的浓度为200 IU/mL。在前期实验时此浓度阳性质控品全部检出阳性,浓度过高,质控品则失去其应有的监控意义。有相当一部分HBV“窗口期”和隐匿性感染者中的病毒载量甚至低于10 IU/mL,室内质控浓度越接近最低检测限,反映测定操作变异的灵敏度越高,故我们认为室内质控浓度应尽可能接近试剂与系统最低检测限,但实际工作发现,检测用低检测限浓度的质控品检测的稳定性较差[5]。最终我们实验探索出浓度为100 IU/mL的HBV DNA室内质控品,连续测定20次后计算出Ct值的平均值和标准差,绘制出Levey-Jennings质控图。
由结果可知Ct值质量控制有很好的重复性、稳定性。据有关报道,自行配制的室内质控品随保存时间延长,其病毒载量降低,建议室内质控品解冻后最好在72 h内使用[6],我们实验室自行配制的质控品能在48 h内用完,因此能保证质控品的稳定性。以此框架下进行的卫生部室间质评,结果与靶值完全一致,证明用该浓度下Ct值建立核酸检测室内质量控制模式完全可行与可靠。
本实验室室内质控其有效CV为3.53%,批间差异较小,测定结果较稳定。实验过程中若更换试剂批号,则重新用即刻法计算得出20次的Ct值和CV。此次分析过程中,未出现试剂及质控品批号更换。在此后又进行180次检测,有1次未检出阳性,检出符合率为99.5%。未检出可能原因为:(1)核酸提取过程中的随机误差,如核酸提取中的靶核酸丢失、有机溶剂的去除不彻底、标本中扩增抑制物的残留,耗材有PCR抑制物等;(2)仪器的问题,如扩增仪孔间温度的不均一;(3)试剂问题,如反转录酶的失活[1];(4)人员操作问题,如磁珠未混匀。结果表明,室内质控品的Ct值有2次超过了2s,根据Westgard多规则质控方法,当室内质控品测定值超出12S告警规则时,可启动其他规则如R4S、22S、41S、10X判断其是否有效[7]。
阴性质控样本失控的原因主要为扩增产物的污染或者是核酸提取过程中发生的标本间交叉污染。在此过程中本实验室未出现阴性质控无效情况。
本实验室选择的弱阳性质控品能增强当次实验结果的可靠性,可以排除因人员更换等实验条件的差异而导致的误差,可用于日常监控核酸提取扩增检测的有效性。
[1]李金明. 我国血站核酸检测及质量管理的现状与展望[J]. 中国输血杂志, 2012, 25(10): 933-934.
[2]于洋, 马春娅, 冯倩, 等. 自制输血相容性检测室内质控品保存条件的研究[J]. 中国实验血液学杂志, 2010, 18(3): 780-784.
[3]刘保廷, 雷桂华. 应用 Levey-Jennings质控图结合Westgard 多规则进行临床化学室内质控[J]. 现代检验医学杂志, 2004, 19(6): 43-44.
[4]庄乃保, 叶贤林, 李活, 等. 血液乙型肝炎核酸筛查质量控制方法的研究[J]. 中国输血杂志, 2008, 21(11): 844-845.
[5]陈少彬, 何子毅, 余霖, 等. 多标记室内质控品在血液核酸筛查的应用分析[J]. 中国输血杂志, 2016, 29(4): 423-426.
[6]熊玉娟, 周华友. 不同保存条件对丙型肝炎病毒核酸稳定性的影响[J]. 中国输血杂志, 2012, 25(6): 549-552.
[7]吴亚玲, 祝宏, 董杰, 等. 血液核酸筛查室内质控品浓度选择的探讨[J]. 中国输血杂志, 2013, 26(2): 170-171.
(本文编辑:刘群)
10.13602/j.cnki.jcls.2017.07.17
蒋义,1987年生,女,主管技师,硕士研究生,主要从事核酸检测工作。
张钢,主任技师,大学本科,E-mail:781451761@qq.com。
R446
A
2017-05-16)

