水中亚硝胺类消毒副产物的污染现状、形成与控制
李志刚,鲜啟鸣
(污染控制与资源化研究国家重点实验室,南京大学环境学院,江苏 南京 210023)
·前沿评述·
水中亚硝胺类消毒副产物的污染现状、形成与控制
李志刚,鲜啟鸣*
(污染控制与资源化研究国家重点实验室,南京大学环境学院,江苏 南京 210023)
综述了水中亚硝胺类消毒副产物的来源、浓度水平及限定标准,以及亚硝胺类物质(NAs)的生成机制、分析检测技术、控制与去除方法。指出,随着人们对饮用水安全消毒的重视和污水消毒的推广,应增加大范围水中NAs污染水平的调查工作,以及对复杂污水体系中NAs生成前体物的研究,优化和改进消毒工艺,减少NAs的生成,针对复杂水样建立准确可靠的NAs检测方法。
亚硝胺;消毒副产物;污染现状;形成机制;检测方法;控制与消除
1 亚硝胺类消毒副产物
水是生命之源,是人类生存不可或缺的物质之一,饮用水的安全与人类的生命健康和社会经济可持续发展息息相关。水源水中一般含有病原微生物,直接饮用可能会导致伤寒、霍乱及甲肝等传染性疾病的爆发和流行。为了保障饮用水安全,出厂水在进入输水管网前需要进行消毒处理。消毒包括物理消毒和化学消毒,在消毒过程中,化学消毒剂会与水中的天然有机质以及水中的污染物发生一系列的反应,生成有毒有害的消毒副产物(Disinfection By-products, DBPs)。目前世界范围内发现的DBPs有600多种[1-6],主要分含碳消毒副产物、含氮消毒副产物以及含卤素消毒副产物等。除了受管控的三卤甲烷、卤乙酸、溴酸盐、亚氯酸盐之外,还有很多新型的消毒副产物,如亚硝胺、卤代乙腈、卤代苯醌、卤代乙酰胺等[7-10]。
亚硝胺类(N-Nitrosamines,NAs)化合物是一种新型的消毒副产物,根据国际致癌研究机构的分类,大部分亚硝胺类化合物被列为可疑致癌物。继1994年首次于加拿大安大略湖饮用水中发现亚硝基二甲胺(N-Nitrosodimethylamine,NDMA)之后,至今发现的亚硝胺类消毒副产物主要有9种,见表1和图1,分别为:亚硝基二甲胺(N-Nitrosodimethylamine,NDMA)、亚硝基甲乙胺(N-Nitrosodimethylethylamine,NMEA)、亚硝基二乙胺(N-Nitrosodiethylamine,NDEA)、亚硝基二丙胺(N-Nitrosodinpropylamine,NDPA)、亚硝基二正丁胺(N-Nitrosodinbutylamine,NDBA)、亚硝基吡咯烷(N-Nitrosopyrrolidine,NPYR)、亚硝基吗啉(N-Nitrosomorpholine,NMOR)、亚硝基哌啶(N-Nitrosopiperidine,NPIP)和亚硝基二苯胺(N-Nitrosodiphenylamine,NDPhA)。

表1 亚硝胺类消毒副产物的理化性质
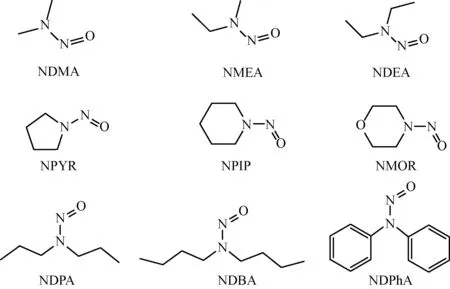
图1 9种亚硝胺类消毒副产物化学结构简式
继1956年Magee[11]报道了亚硝胺类物质具有致癌作用以后,人们开始对亚硝胺类物质进行了广泛研究。研究表明,亚硝胺类化合物绝大部分能够诱发癌症,目前饮用水中发现的9种亚硝胺类消毒副产物,NDMA检出率最高,NDEA和NDMA的毒性比较高,被国际癌症研究署定为2A级致癌物质,其中NDMA的致癌风险要显著高于三卤甲烷。虽然目前报道显示,饮用水中的亚硝胺类消毒副产物含量为ng/L水平,但依然具有引发癌症的风险,不容忽视。
2 亚硝胺类物质的浓度水平及限定标准
2.1 水中的NAs浓度水平
目前,加拿大、美国、西班牙、日本、英国和中国等国家对水中亚硝胺类物质的研究报道较多,这些国家饮用水中均检测到亚硝胺类消毒副产物。近年来,世界各地不断有文献报道水中NAs的污染状况,不仅在供水系统中的进水、出水、管网水、龙头水中发现不同浓度的NAs,甚至在水源水中发现NAs的存在。
2009年,日本夏季31个出厂水水样NDMA检出率为30%,最高值为2.2 ng/L,冬季28个出厂水水样检出率为23%,最高值为10 ng/L[12];2010年,美国近2万水样NDMA检出率为10%,最高值为630 ng/L;在土耳其的一个水源水中,检出2~164.8 ng/L的NDMA生成潜能[13];2013年,加拿大魁北克省195个水样中,NDMA的检出率低于10%,最高值为3.3 ng/L[14];2013年,韩国沿洛东江的水样中,检出6种亚硝胺,总亚硝胺的最大值为735.7 ng/L[15]。
2012年,本课题组在江苏选定不同水源的9家饮用水厂,分别在丰水期和枯水期采集饮用水厂的源水、出厂水和管网水,测定水样中的9种亚硝胺类消毒副产物[16]。结果显示,江苏地区8个城市9个饮用水厂的出水与管网水中NDMA的总质量浓度为未检出~45.3 ng/L,均值为19 ng/L,出厂水中9种亚硝胺类消毒副产物的总质量浓度为未检出~765 ng/L,均值为42 ng/L。其中,枯水期中检出的NAs种类较多,9种亚硝胺中,NDMA、NDEA、NPYR和NPIP检出率较高。对南京市场上的10种瓶装饮用水做了亚硝胺消毒副产物的检测,检测到NDMA的质量浓度为未检出~4.8 ng/L, NMOR的质量浓度为未检出~36.2 ng/L。
2012年,北京大学胡建英团队对中国河南贾鲁河流域河水中7种亚硝胺的污染水平进行了分析检测[17]。结果显示,NDMA、NDEA、NMOR、NPIP和NDBA的平均值>5 ng/L,NPYR和NDPA的平均值分别为2.8和1.7 ng/L。2016年,清华大学陈超团队[18]利用3年时间,分别对中国23个省,44个大中小城镇供水系统的155个采样点的166个出厂水、龙头水、水源水水样中的亚硝胺类消毒副产物进行检测,在已检测的全部水样中,出厂水和龙头水中的NDMA平均值分别为11 和13 ng/L,水源水中的NDMA生成潜能平均为66 ng/L。文献显示,检测到NDMA质量浓度0~189 ng/L,平均值11 ng/L;相对WHO标准NDMA 100 ng/L,只有很少一部分水样超过WHO标准;26%的出厂水中NDMA的质量浓度超过10 ng/L;29%的龙头水中NDMA的质量浓度超过10 ng/L。国内各区域龙头水中NDMA的平均质量浓度除东北地区,其他地区均超过10 ng/L,长江三角洲地区NDMA含量和生成势最高。
2.2 水中NAs的限定标准
2002年,美国加利福尼亚健康服务部制定了NAs的控制标准,规定饮用水中NDMA、NDEA、NDPA的限定标准为10 ng/L;2012年,加拿大安大略省环境部限定本省饮用水中NDMA的质量浓度不能高于9 ng/L;2004年,荷兰限定饮用水中的NDMA质量浓度为12 ng/L;2007年德国卫生服务部限定饮用水中NDMA、NMOR质量浓度为10 ng/L;2008年,WHO限定饮用水中NDMA的标准为100 ng/L;2009年美国马萨诸塞州限定饮用水中NDMA质量浓度不得超过10 ng/L;2009年澳大利亚限定饮用水中NDMA质量浓度不能超过100 ng/L;2010年加拿大卫生部限定饮用水中NDMA质量浓度上限为40 ng/L。截止目前,《生活饮用水卫生标准》(GB 5749—2006)中,并未对饮用水中亚硝胺类消毒副产物的浓度设定标准。
3 亚硝胺类物质的生成机制
目前研究认为,NAs主要是由水中天然有机质,尤其是含氮物质,在消毒剂、光照等条件下生成的一系列亚硝胺类消毒副产物[19-27],而这些消毒副产物中研究最多,检出率最高的为NDMA,因此,NAs的形成机制主要以NDMA为研究对象。
3.1 亚硝化反应生成途径
在早期的研究中,NDMA 被认为是在强酸性条件下通过二甲胺(DMA)的亚硝化途径生成的,反应途径见图2[28]。

对NDMA的亚硝化反应途径的进一步研究发现,磷酸盐缓冲溶液会抑制 NDMA 的生成,主要原因是 NaH2PO4和NaNO2相互作用,从而对二甲胺(DMA )发生亚硝化反应生成 NDMA 的过程产生抑制作用。
3.2 自由氯催化亚硝化反应途径
在实际消毒过程中,自由氯可催化亚硝化反应,促进 DMA 反应生成 NDMA[29],反应途径见图3。
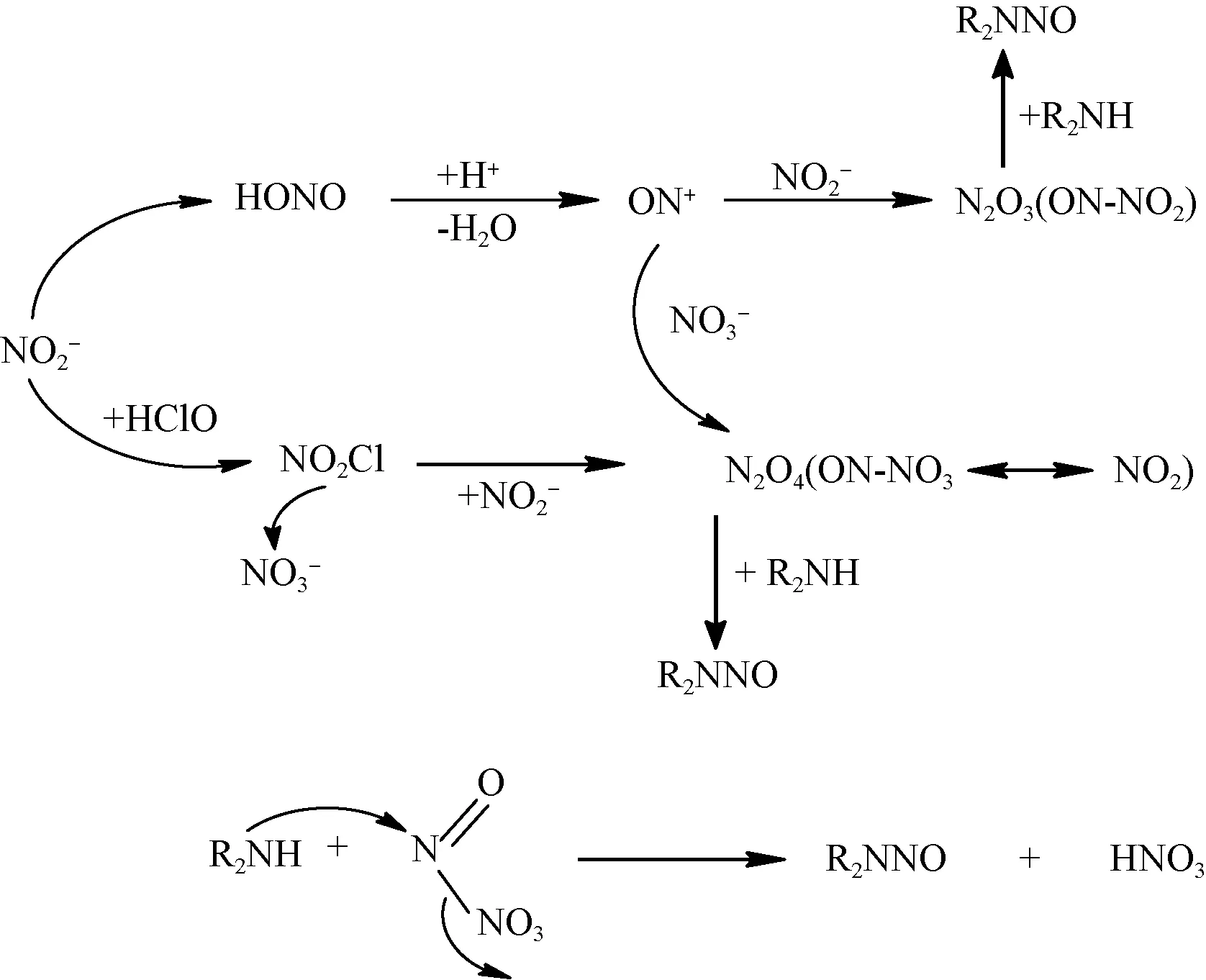
图3 NDMA自由氯催化亚硝化反应生成途径
3.3 氯化偏二甲肼途径
实际水体多为中性偏碱条件,亚硝化反应的速率较慢,随后的研究表明,使用氯胺消毒的饮用水中,DMA 也可以先与二氯胺反应生成中间产物偏二甲肼(UDMH)[30-31],UDMH 不稳定,可被一氯胺或溶解氧等进一步氧化,生成包含 NDMA 在内的一系列产物,NDMA 的产量占所有生成物总量的 5%左右,反应途径见图4。
3.4 O3氧化生成途径
虽然自由氯消毒和氯胺消毒是饮用水中 NDMA 生成的主要来源,但部分研究发现,水处理过程中
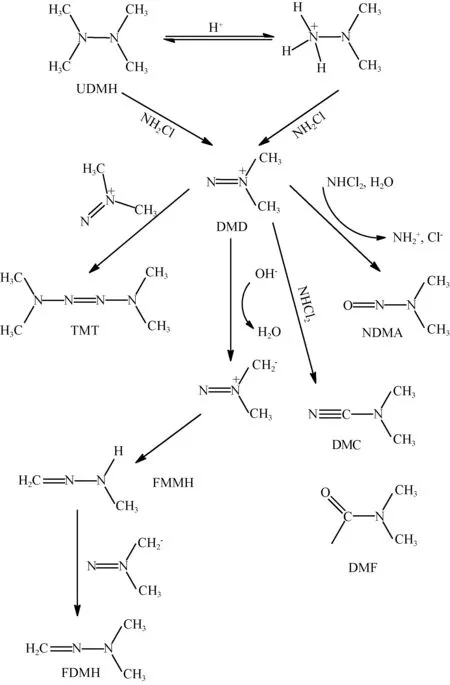
图4 NDMA氯化偏二甲肼反应生成途径
使用其他强氧化剂时也可能生成 NDMA,如O3、ClO2、KMnO4等[32-33]。图5为可能的O3氧化 DMA 生成 NDMA 的反应途径。
图5NDMAO3氧化生成途径
3.5 氯胺消毒生成途径
已有研究表明,DMA与二氯胺作用时可生成 NDMA(图6),是NDMA的重要前体物[28]。
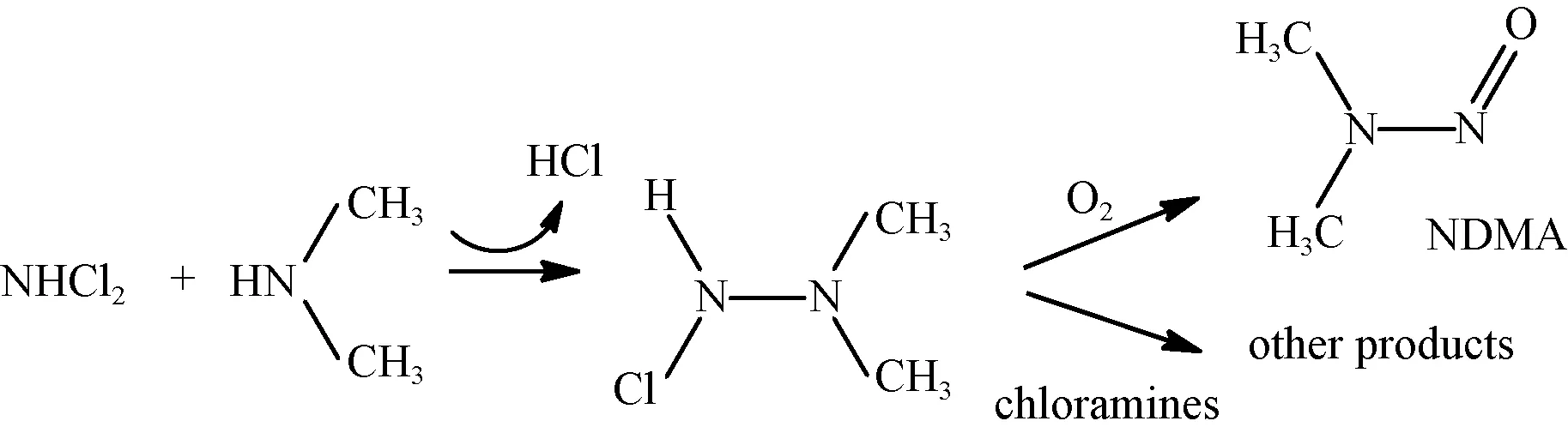
图6 NDMA氯胺消毒生成途径
4 NAs分析检测技术
水中亚硝胺类消毒副产物的含量很低,一般在ng/L水平,其具有亲水性,难以从复杂的水样中分离出来。因此,亚硝胺类物质通常不能直接用仪器检测,需要对样品预处理。常用的水样预处理方法包括:液液萃取,固相萃取,固相微萃取,其中固相萃取作为预处理的主流方法[34-39]。目前,水中亚硝胺类化合物的检测方法主要集中在气相色谱-质谱联用法和液相色谱-质谱联用法[40-44]。
EPA521的方法是利用椰壳活性炭固相萃取柱进行富集浓缩,利用GC-MS/MS检测9种NAs中的7种,亚硝基二苯胺(NDPhA)热不稳定,容易分解。文献[16]显示,EPA521方法同样适用于9种NAs的检测,对于热不稳定的亚硝基二苯胺,采取测其分解产物二苯胺(DPhA),同样可以较为准确地对亚硝基二苯胺进行准确定量。Li等[16]采用固相萃取GC-MS检测方法,检测水中的亚硝胺类消毒副产物,方法检测限为0.8~4.3 ng/L,除NDPhA外,平均回收率86%~97%,相对标准偏差12%。
近年来,不少科研工作者尝试使用液质联用检测分析亚硝胺得到了较好的效果,能有较低的检测限,可同时测定9种亚硝胺类消毒副产物,对于热不稳定的亚硝基二苯胺能够直接检测而不同于气质联用仪检测其分解产物。2009年,Asami等[45]利用SPE-LC-MS/MS检测方法检测水中NAs,检测限为1 ng/L。
5 NAs的控制与去除方法
由于NAs具有不同程度的致癌性,对人类健康有危害,饮用水中的亚硝胺类消毒副产物的控制与去除技术受到国内外研究者的广泛关注,目前文献报道主要去除方法有吸附法、氧化法、光解法、反渗透膜法、化学还原以及生物降解等方法[46]。
5.1 吸附法
吸附法是一种比较传统的去除环境污染物的方法,分为物理吸附和化学吸附。物理吸附主要是由活性炭一类材料对污染物进行吸附解吸;化学吸附一般是由合成的新型吸附材料进行吸附降解。亚硝胺类消毒副产物是水溶性的极性小分子,所以亚硝胺类物质的吸附材料要求亲水性比较好。研究表明,沸石、果壳活性炭、大孔树脂等对亚硝胺有较好的吸附潜质,EPA521方法中作为SPE填料的就是改性椰壳活性炭,能够较好地吸附亚硝胺类消毒副产物,目前的研究也有将金属氧化物嵌入活性炭表面,来增加材料的最大吸附量[47-48]。
5.2 氧化法
氧化法是处理大多数有机污染物常用的方法,用于氧化的试剂有臭氧、双氧水、芬顿试剂等,也有利用紫外光照和超声等技术手段进行亚硝胺的氧化消除,这些技术和试剂主要是在介质中生成新的自由基进而进行自由基反应,来消除水中的亚硝胺[49-50]。研究显示,在亚硝胺的形成中,二级胺或者是含有二级胺的物质生成亚硝胺的潜能不容忽视[51-52],所以在氧化法除去亚硝胺的同时,能够有效控制二级胺类亚硝胺前驱物也是关键的一步,对二级胺类物质也需要进行一定程度的关注[53]。徐冰冰等[54]在亚硝胺类物质的控制与消除中,使用紫外结合双氧水和紫外结合O32种高级氧化的技术手段,在其研究中发现紫外结合双氧水进行氧化消除亚硝胺实验中,能够有效降低NDMA和NDEA的浓度,但是不能有效控制和消除二甲胺和二乙胺的生成;但是在紫外结合O3进行氧化处理时,发现这种技术手段能够有效控制NDMA和NDEA的生成,并且有效地减弱了二甲胺和二乙胺这2种前驱物的形成,对这2种技术手段进行对比,紫外结合O3对消除亚硝胺的生成作用要强于紫外结合双氧水的技术手段。国内外也有不少科研工作者利用芬顿试剂进行NDMA的去除,由于芬顿试剂去除水中的NAs主要是依靠自由基反应,而在水体中,由于水体的酸碱环境条件难以获取足够多的自由基,因此依靠自由基进行氧化反应去除亚硝胺的方法推广应用难度较大。
5.3 光解法
亚硝胺类消毒副产物对紫外光比较敏感,长时间光照不稳定能够分解,导致亚硝胺中的N-N键断裂,进而使亚硝胺类化合物分解[55]。研究结果表明,紫外光可以去除水体中的NDMA,能够有效降低NDMA在水体中的含量,紫外光光解NDMA与水体环境条件有关,水体的酸碱度、浊度、色度等因素能够影响紫外光解的效率,紫外光解可以有效去除水体中的NDMA,但是利用紫外光解去除NAs的经济成本也是需要考虑的一个方面。
5.4 反渗透膜法
有研究表明,由于伯胺和叔胺在中性的溶液中带有正电荷,反渗透膜技术可以利用这一类物质带正电的特点对其进行有效拦截[56]。而对于NAs来说,NDMA分子质量比较小,而且其在中性水溶液中不带电呈现电中性,反渗透膜对其去除效率并不高,美国加利福尼亚的一家污水处理厂利用反渗透技术对水中的NDMA的去除率为24%~56%;但是将反渗透技术和紫外光解技术结合起来的话,饮用水中的NDMA能够控制在限定标准10 ng/L。亚硝胺类消毒副产物是极性小分子化合物,不同NAs分子大小也不尽相同,在研究中发现,反渗透技术对于分子质量较大的NPIP、NMOR、NDBA可以完全去除,但对于分子质量比较小的NDMA去除效率相对较低,然而NDMA是目前检出率最高的一种亚硝胺类消毒副产物,因此,反渗透技术在实际应用中仍然需要有更进一步的研究。
5.5 化学还原法
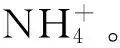
5.6 生物降解法
生物降解处理环境中的有机污染物在环境领域应用比较广泛,尤其是废水处理中,利用生物降解能够有效去除污染物。已有结果显示,利用好氧生物可以有效去除水体中的NDMA,说明生物降解对消除水体中的亚硝胺类消毒副产物有较好的应用前景[58]。研究发现,有一些菌株在有氧或者厌氧条件下能够将NDMA转化为毒性较弱的化合物,如门多萨假单胞菌KR1以甲苯作为初级营养物质,在有氧条件下能够将NDMA氧化为硝基二甲胺,并进一步降解为硝基甲烷[59]。此外,也有研究发现红球菌属RhodococusRuberENV425 能够在厌氧条件下将NDMA降解为CO2,其他降解产物包括甲烷、亚硝酸盐、硝酸盐、甲酸盐等[60-61]。
6 水中亚硝胺类物质研究的展望
随着人们对饮用水安全消毒的重视,需要增加大范围水中NAs污染水平的调查工作,关注NAs的污染水平和健康风险。由于水源水中发现亚硝胺类消毒副产物,天然有机质的光解转化形成NAs的研究应该受到更多的关注。随着污水消毒的推广,需要增加对复杂污水体系中NAs生成前体物的研究,优化和改进消毒工艺,减少NAs的生成,针对复杂水样建立准确可靠的NAs检测方法。
[1] BEI E, LIAO X, MEMG X, et al.Identification of nitrosamine precursors from urban drainage during storm events: A case study in southern China[J].Chemosphere, 2016, 160: 323-331.
[2] BOND T, HUANG J, TEMPLETON M R, et al.Occurrence and control of nitrogenous disinfection by-products in drinking water-a review[J].Water Research, 2011, 45 (15): 4341-4354.
[3] DAI N, MITCH W A. Relative importance of N-nitrosodimethylamine compared to total N-nitrosamines in drinking waters[J].Environmental Science & Technology, 2013, 47 (8): 3648-3656.
[4] VENTANAS S, RUIZ J.On-site analysis of volatile nitrosamines in food model systems by solid-phase microextraction coupled to a direct extraction device[J].Talanta, 2006, 70 (5): 1017-1023.
[5] YOON S, TANAKA H.Formation of N-nitrosamines by chloramination or ozonation of amines listed in Pollutant Release and Transfer Registers (PRTRs)[J].Chemosphere, 2014, 95: 88-95.
[6] ZENG T, PLEWA M J, MITCH W A.N-Nitrosamines and halogenated disinfection byproducts in U.S. Full Advanced Treatment trains for potable reuse[J].Water Research, 2016, 101: 176-186.
[7] QIAN Y, WU M, WANG W, et al.Determination of 14 nitrosamines at nanogram per liter levels in drinking water[J]. Analytical Chemistry, 2015, 87 (2): 1330-1336.
[8] SAKAI H, TOKUHARA S, MURAKAMI M, et al.Comparison of chlorination and chloramination in carbonaceous and nitrogenous disinfection byproduct formation potentials with prolonged contact time[J].Water Research, 2016, 88: 661-670.
[9] VENKATESAN A K, PYCKE B F, HALDEN R U.Detection and occurrence of N-nitrosamines in archived biosolids from the targeted national sewage sludge survey of the U.S. Environmental Protection Agency[J].Environmental Science & Technology, 2014, 48 (9): 5085-5092.
[10] WEST D M, WU Q, DONOVAN A, et al.N-nitrosamine formation by monochloramine, free chlorine, and peracetic acid disinfection with presence of amine precursors in drinking water system[J].Chemosphere, 2016, 153: 521-527.
[11] MAGEE P N.Toxic liver injury metabolism of dimethylnitrosamine[J]. Journal of Biochemical, 1956, 64 (4): 676-682.
[12] CHIKAN N A, SHABIR N, SHAFFI S, et al.N-Nitrosodimethylamine in the kashmiri diet and possible roles in the high incidence of gastrointestinal cancers[J].Asian Pacific Journal of Cancer Prevention, 2012, 13 (3): 1077-1079.
[13] AYDIN E, YAMAN F B, GENCELI E A, et al.Occurrence of THM and NDMA precursors in a watershed: Effect of seasons and anthropogenic pollution[J].Journal of Hazardous Materials, 2012, 221: 86-91.
[14] BRISSON I J, LEVALLOIE P, TREMBLAY H, et al.Spatial and temporal occurrence of N-nitrosamines in seven drinking water supply systems[J].Environmental Monitoring and Assessment, 2013, 185 (9): 7693-7708.
[15] KIM G A, SON H J, KIM C W, et al. Nitrosamine occurrence at Korean surface water using an analytical method based on GC/LRMS[J].Environmental Monitoring and Assessment, 2013, 185 (2): 1657-1669.
[16] LI T, YU D, XIAN Q, et al.Variation of levels and distribution of N-nitrosamines in different seasons in drinking waters of East China[J].Environ Sci Pollut Res Int, 2015, 22 (15): 11792-11800.
[17] MA F, WAN Y, YUAN G, et al.Occurrence and source of nitrosamines and secondary amines in groundwater and its adjacent Jialu River basin, China[J].Environmental Science & Technology, 2012, 46 (6): 3236-3243.
[18] BEI E, SHU Y, LI S, et al.Occurrence of nitrosamines and their precursors in drinking water systems around mainland China[J].Water Research, 2016, 98: 168-175.
[19] CHEN W H, WANG C Y, HUANG T H.Formation and fates of nitrosamines and their formation potentials from a surface water source to drinking water treatment plants in Southern Taiwan[J].Chemosphere, 2016, 161: 546-554.
[20] GAO P F, ZHANG Z X, GUO X F, et al.Determination of primary and secondary aliphatic amines with high performance liquid chromatography based on the derivatization using 1,3,5,7-tetramethyl-8-(N-hydroxysuccinimidyl butyric ester)-difluoroboradiaza-s-indacene[J].Talanta, 2011, 84 (4): 1093-1098.
[21] HUI Y, ZHOU L, CHEN X G.Analysis of ammonia and aliphatic amines in environmental water by micellar electrokinetic chromatography and QSPR modeling of electrophoretic migration time[J].Talanta, 2010, 80 (5): 1619-1625.
[22] LEAVEY-ROBACK S L, KRASNER S W.Suffet I M, Veterinary antibiotics used in animal agriculture as NDMA precursors[J].Chemosphere, 2016, 164: 330-338.
[23] SHEN R, ANDREWS S A.NDMA formation from amine-based pharmaceuticals-impact from prechlorination and water matrix[J].Water Research, 2013, 47 (7): 2446-2457.
[24] SHEN R, ANDREWS S A.NDMA formation kinetics from three pharmaceuticals in four water matrices[J].Water Research, 2011, 45 (17): 5687-5694.
[25] UZUN H, KIM D, KARANFIL T.Seasonal and temporal patterns of NDMA formation potentials in surface waters[J].Water Research, 2015, 69: 162-172.
[26] WANG X, YANG H, ZHOU B, et al.Effect of oxidation on amine-based pharmaceutical degradation and N-Nitrosodimethylamine formation[J].Water Research, 2015, 87: 403-411.
[27] WOODS G C, DICKENSON E R.Natural attenuation of NDMA precursors in an urban, wastewater-dominated wash[J].Water Research, 2016, 89: 293-300.
[28] KRASNER S W, MITCH W A, MCCURRY D L, et al. Formation, precursors, control, and occurrence of nitrosamines in drinking water: a review[J].Water Research, 2013, 47: 4433-5033.
[29] CHOI J H, VALENTINE R L.N-nitrosodimethylamine formation hy free-chlorine-enhanced nitrosation of dimethylamine[J].Environmental Science & Technology, 2003, 37 (21): 4871-4876.
[30] CHOI J H, VALENTINE R L.Formation of N-nitrosodimethylamine (NDMA) from reaction of monochloramine: a new disinfection by-product[J].Water Research, 2002, 36 (4): 817-824.
[31] SHARMA V K.Kinetics and mechanism of formation and destruction of N-nitrosodimethylamine in water - A review[J].Separation and Purification Technology, 2012, 88: 1-10.
[32] SCHINDLER W Y, MESTANKOVA H,SCHARER M, et al.Novel test procedure to evaluate the treatability of wastewater with ozone[J].Water Research, 2015, 75: 324-335.
[33] YANG L, CHEN Z L, SHEN J M, et al. Reinvestigation of the nitrosamine-formation mechanism during ozonation[J].Environmental Science & Technology, 2009, 43 (14): 5481-5487.
[34] ARAGON M, MARCE R M, BORRULL F.Determination of N-nitrosamines and nicotine in air particulate matter samples by pressurised liquid extraction and gas chromatography-ion trap tandem mass spectrometry[J].Talanta, 2013, 115: 896-901.
[35] DAVARANI S S, MASOOMI L, BANITABA M H, et al.Determination of N-nitrosodiethanolamine in cosmetic products by headspace solid phase microextraction using a novel aluminum hydroxide grafted fused silica fiber followed by gas chromatography-mass spectrometry analysis[J].Talanta, 2013, 105: 347-353.
[36] JURADO-SANCHEZ B, BALLESTEROS E, GALLEGO M.Automatic screening method for the preconcentration and determination of N-nitrosamines in water[J].Talanta, 2007, 73 (3): 498-504.
[37] JURADO-SANCHEZ B, BALLESTEROS E, GALLEGO M.Comparison of several solid-phase extraction sorbents for continuous determination of amines in water by gas chromatography-mass spectrometry[J].Talanta, 2009, 79 (3): 613-620.
[38] LEE H L, WANG C, LIN S, et al.Liquid chromatography/tandem mass spectrometric method for the simultaneous determination of tobacco-specific nitrosamine NNK and its five metabolites[J].Talanta, 2007, 73 (1): 76-80.
[39] PLANAS C, PALACIOS O, VENTURA F, et al.Analysis of nitrosamines in water by automated SPE and isotope dilution GC/HRMS Occurrence in the different steps of a drinking water treatment plant, and in chlorinated samples from a reservoir and a sewage treatment plant effluent[J].Talanta, 2008, 76 (4): 906-913.
[40] FUJIOKA T, TAKEUCHI H, TANAKA H, et al.A rapid and reliable technique for N-nitrosodimethylamine analysis in reclaimed water by HPLC-photochemical reaction-chemiluminescence[J].Chemosphere, 2016, 161: 104-111.
[41] MCDONALD J A, HARDEN N B, NGHIEM L D, et al.Analysis of N-nitrosamines in water by isotope dilution gas chromatography-electron ionisation tandem mass spectrometry[J].Talanta, 2012, 99: 146-154.
[42] SPAHR S, BOLOTIN J, SCHLEUCHER J, et al.Compound-specific carbon, nitrogen, and hydrogen isotope analysis of N-nitrosodimethylamine in aqueous solutions[J].Analytical Chemistry, 2015, 87 (5): 2916-2924.
[43] WU Q, SHI H, MA Y, et al.Determination of secondary and tertiary amines as N-nitrosamine precursors in drinking water system using ultra-fast liquid chromatography-tandem mass spectrometry[J].Talanta, 2015, 131: 736-741.
[44] YOON S, NAKADA N. Tanaka H.A new method for quantifying N-nitrosamines in wastewater samples by gas chromatography-triple quadrupole mass spectrometry[J].Talanta, 2012, 97: 256-261.
[45] ASAMI M, OYA M. A nationwide survey of NDMA in raw and drinking water in Japan[J].Science of the Total Environment, 2009, 407(11), 3540-3545
[46] KOROLCZUK M, GRABARCZYK M, RUTYNA I.An adsorptive stripping voltammetry procedure for ultra-trace determination of U(VI) using double accumulation step on two lead-film working electrodes[J].Talanta, 2014, 130: 342-346.
[47] GUO X, LI Q, ZHANG M, et al.Enhanced photocatalytic performance of N-nitrosodimethylamine on TiO2nanotube based on the role of singlet oxygen[J].Chemosphere, 2015, 120: 521-526.
[48] HE Y, CHENG H.Degradation of N-nitrosodimethylamine (NDMA) and its precursor dimethylamine (DMA) in mineral micropores induced by microwave irradiation[J].Water Research, 2016, 94: 305-314.
[49] CHEN H W, CHEN C Y, WANG G S.Performance evaluation of the UV/H2O2process on selected nitrogenous organic compounds: reductions of organic contents vs. corresponding C-, N-DBPs formations[J].Chemosphere, 2011, 85 (4): 591-597.
[50] CHU W, YAO D, GAO N, et al.The enhanced removal of carbonaceous and nitrogenous disinfection by-product precursors using integrated permanganate oxidation and powdered activated carbon adsorption pretreatment[J].Chemosphere, 2015, 141: 1-6.
[51] CHANG H, CHEN C, WANG G.Identification of potential nitrogenous organic precursors for C-, N-DBPs and characterization of their DBPs formation[J].Water Research, 2011, 45 (12): 3753-3764.
[52] WANG W, REN S, ZHANG H, et al.Occurrence of nine nitrosamines and secondary amines in source water and drinking water: Potential of secondary amines as nitrosamine precursors[J].Water Research, 2011, 45 (16): 4930-4938.
[53] ZHOU W, CHEN C, LOU L, et al.Formation potential of nine nitrosamines from corresponding secondary amines by chloramination[J].Chemosphere, 2014, 95: 81-87.
[54] XU B, CHEN Z.Comparison of N-nitrosodiethylamine degradation in water by UV irradiation and UV/O-3: Efficiency, product and mechanism[J].Journal of Hazardous Materials,2008,179(13),976-982.
[55] CHEN Z, FANG J, FAN C, et al.Oxidative degradation of N-Nitrosopyrrolidine by the ozone/UV process: Kinetics and pathways[J].Chemosphere, 2016, 150: 731-739.
[56] PLUMLEE M H, LOPEZ-Mesas M, HEIDLBERGER A, et al.N-nitrosodimethylamine (NDMA) removal by reverse osmosis and UV treatment and analysis via LC-MS/MS[J].Water Research, 2008, 42 (1-2): 347-355.
[57] HAN Y, CHEN Z L, SHEN J M, et al. The role of Cu(II) in the reduction of N-nitrosodimethylamine with iron and zinc[J].Chemosphere, 2017, 167: 171-177.
[58] CHUNG J, AHN C H, CHEN Z, et al.Bio-reduction of N-nitrosodimethylamine (NDMA) using a hydrogen-based membrane biofilm reactor[J].Chemosphere, 2008, 70 (3): 516-520.
[59] FOURNIER D, HAWARI J, STREGER S H, et al.Biotransformation of N-nitrosodimethylamine by Pseudomonas mendocina KR1[J].Applied and Environment Microbiology, 2006, 72 (10): 6693-6698.
[60] FOURNIER D, HAWARI J, HALASZ A, et al.Aerobic biodegradation of N-nitrosodimethylamine by the propanotroph Rhodococcus ruber ENV425[J].Applied and Environment Microbiology, 2009, 75 (15): 5088-5093.
[61] SHARP J O, SALES C M, LEBLANC J C, et al.An inducible propane monooxygenase is responsible for N-nitrosodimethylamine degradation by Rhodococcus sp.strain RHA1[J].Appliedand Environment Microbiology, 2007, 73 (21): 6930-6938.
Occurrence,FormationMechanismandControlofNitrosaminesDisinfectionBy-productsinWater
LI Zhi-gang, XIAN Qi-ming*
(StateKeyLaboratoryofPollutionControlandResourcesReuse,SchoolofEnvironment,NanjingUniversity,Nanjing,Jiangsu210023,China)
This paper summarized the sources, concentrations and the standard limit of Nitrosamines (NAs), the formation mechanism, the analysis and detection techniques, the control and removal methods of NAs were also mentioned. With the emphasis on the disinfection of drinking water and the promotion of sewage disinfection, it is necessary that surveys on NAs levels in water in a wide range should be taken and precursors of NAs in complex sewage systems should be investigated, and then optimize and improve the disinfection technologies to reduce the formation of NAs and establish accurate and reliable detection methods of NAs in complex water samples.
Nitrosamines;Disinfection by-product; Occurrence; Formation mechanism;Detection method;Control and elimination
2017-08-31
江苏省重点研发计划-社会发展面上基金资助项目(BE2017711)
李志刚(1989—), 男,博士生,研究方向为水中亚硝胺类物质的分析技术。
*通讯作者:鲜啟鸣 E-mail: xianqm@nju.edu.cn
10.3969/j.issn.1674-6732.2017.06.001
X592
A
1674-6732(2017)06-0001-07
栏目编辑 李文峻

