硫酸盐还原菌附着对阴极保护条件下钙质沉积层形成及其对金属保护性能的影响
, ,,3,,
(1. 中国科学院海洋研究所 海洋环境腐蚀与生物污损重点实验室,青岛 266071; 2. 中国科学院大学,北京 100049; 3. 中国海洋大学 材料科学与工程研究院,青岛 266100)
金属在海洋环境中的腐蚀很大程度上是由于微生物引起的,因此微生物腐蚀会对海洋金属构筑物的安全造成严重危害,而硫酸盐还原菌(SRB)被认为是造成微生物腐蚀最主要的原因之一[1-4]。钢结构在含硫酸盐还原菌海洋环境中的腐蚀也越来越受到人们的重视[5-6]。硫酸盐还原菌是一种兼性厌氧菌,广泛存在于厌氧和缺氧的环境中(如海泥)。它能够利用硫酸盐作为电子受体,将硫酸盐还原为硫离子,然后利用氢化酶消耗积累在阴极的氢原子,同时与金属离子反应形成金属硫化物,加速金属腐蚀,造成严重的危害[7-10]。
阴极保护是海上石油平台、钢桩码头等大型金属构筑物防止微生物腐蚀最为常用的方法之一[11]。在阴极保护条件下,钢结构表面能够形成一层以CaCO3和Mg(OH)2为主要成分的致密的钙质沉积层[12-13]。钙质沉积层能够限制海水中的溶解氧扩散到钢结构表面,降低保护电流密度,增强阴极保护的效果[14-15]。因此,钙质沉积层对于海洋环境中金属构筑物阴极保护的有效性和效率十分重要[16-17]。
在实际海洋环境中,细菌在钢结构表面附着并形成生物膜是一种非常普遍的现象,这会影响钙质沉积层的形成[18]。因此,当钢结构被施加阴极保护时,为形成有效的钙质沉积,提高阴极保护的效果,应尽可能避免细菌生物膜的形成。目前,关于微生物附着以及海洋生物膜与钙质沉积层之间的相互作用的研究较少,关于硫酸盐还原菌与钙质沉积层之间的相互关系的研究则更有限。本工作结合电化学相关知识、表面分析以及微生物相关理论研究了硫酸盐还原菌附着对Q235碳钢表面钙质沉积层形成及其对金属的保护性能的影响。
1 试验
1.1 电极制备
电极材料选用Q235碳钢,其化学成分(质量分数)为99.31% Fe,0.1% C,0.4% Mn,0.12% Si,0.02% S,0.05% P。将Q235碳钢制成尺寸为10 mm×10 mm×10 mm的正方体试样。将新开封Q235碳钢试样用丙酮清洗去除防锈油,然后使用蒸馏水冲洗,最后使用无水乙醇超声清洗,吹风机吹干后放入干燥器中备用。选取正方体试样的一面作为工作面,工作面背面用φ2.5 mm铜芯导线焊接,再将试样(除工作面)用环氧树脂密封在φ25 mm聚氯乙烯管中,自然固化24 h,完成工作电极的制备。依次用400号、600号、800号、1 000号砂纸逐级打磨工作面,然后用丙酮超声清洗,再依次用蒸馏水、无水乙醇清洗,吹风机吹干后放入干燥器中备用。
1.2 硫酸盐还原菌的活化、培养和附着
试验所用的硫酸盐还原菌是从青岛胶州湾海域的铁锈中提取的,经过不断分离纯化并确定为纯种的硫酸盐还原菌后,将其放置在-20 ℃的冰箱中保种。硫酸盐还原菌使用时需先使用修正的Postgate′s培养基进行活化、富集培养。修正的Postgate′s培养基组分为:0.25 g KH2PO4,0.5 g NH4Cl,0.03 g CaCl2·6H2O,0.03 g MgSO4·7H2O,3.0 mL乳酸钠,0.5 g酵母膏,0.15 g柠檬酸钠,500 mL过滤后的陈海水[19]。硫酸盐还原菌的活化、富集培养过程如下:将配制好的培养基放入高压灭菌锅中高温(121 ℃)灭菌30 min,再将经过紫外光照射30 min后的铁屑加入到冷却的培养基中;按照5%的接种量将冷冻的硫酸盐还原菌接入到培养基中,再放入30 ℃的生化恒温培养箱中培养,培养3 d左右,硫酸盐还原菌开始进入指数生长期,且生长情况良好。在30 ℃的生化恒温培养箱中,用经活化和富集培养的硫酸盐还原菌对Q235碳钢电极进行附着,附着时间分别为0 h,12 h,1 d,3 d,5 d。附着前Q235碳钢电极需经紫外线照射30 min。
1.3 电化学沉积
采用电化学沉积法将经不同时间硫酸盐还原菌附着的工作电极于新鲜海水中制备钙质沉积层。新鲜海水取自青岛汇泉湾并经过过滤,其氧溶解度为5.95 mg/L,pH为8.1。整个体系为三电极敞开体系,石墨板为辅助电极,由DJS-292E型恒电位仪作为极化电源[20]。电化学沉积过程中,极化电流密度为-30 μA/cm2,沉积时间为72 h,每隔12 h更换一次溶液以保证溶液中氧含量稳定。在此条件下形成的钙质沉积层表面平整光滑,具有良好的结晶[21],其化学成分以CaCO3为主,并含有少量Mg(OH)2[20],钙质沉积层在金属基体表面具备良好的附着力,对金属的保护性优良[22]。将制备好的钙质沉积层用氮气干燥,然后放入干燥器中备用。
1.4 电化学测试
电化学测试采用三电极体系:饱和甘汞电极(SCE)作为参比电极;铂电极作为辅助电极;工作电极为此前制备好的表面含有钙质沉积层的Q235碳钢。整个体系处于过滤的天然海水环境中。电化学测试仪器为Gamry 1000电化学工作站,在开路电位(OCP)条件下,对试样施加幅值为10 mV扰动交流信号进行电化学阻抗(EIS)测试,EIS测试的频率范围为10-2~105Hz。所有电化学测试数据通过ZSimpWin软件进行拟合处理。
1.5 表面形貌观察和钙质沉积层成分表征
电化学沉积后,将环氧树脂和铜导线与Q235碳钢剥离,用50%(体积分数,下同),60%,70%,80%,90%,100%酒精逐次脱水15 min,然后,采用二氧化碳临界点干燥,对试样表面喷金,使用日立高新技术有限公司S-3400N型扫描电镜(SEM)及附带的能谱仪(EDS)对钙质沉积层进行表面形貌观察和成分分析。
2 结果与讨论
2.1 钙质沉积层成分
经硫酸盐还原菌附着不同时间后Q235碳钢表面钙质沉积层的EDS谱以及其钙元素和镁元素的质量分数分别如图1和表1所示。由图1和表1可见:经硫酸盐还原菌附着不同时间后Q235碳钢表面钙质沉积层中主要元素都是钙,并伴有少量镁;镁元素的含量随着附着时间的延长先增加后减小,当附着时间为5 d时,镁含量最低。钙质沉积层主要由CaCO3和Mg(OH)2组成,Mg(OH)2含量的增加会使钙质沉积层的附着力下降,对碳钢的保护效果下降[22]。硫酸盐还原菌附着5 d形成的钙质沉积层中Mg(OH)2含量最少,其保护性能最佳。
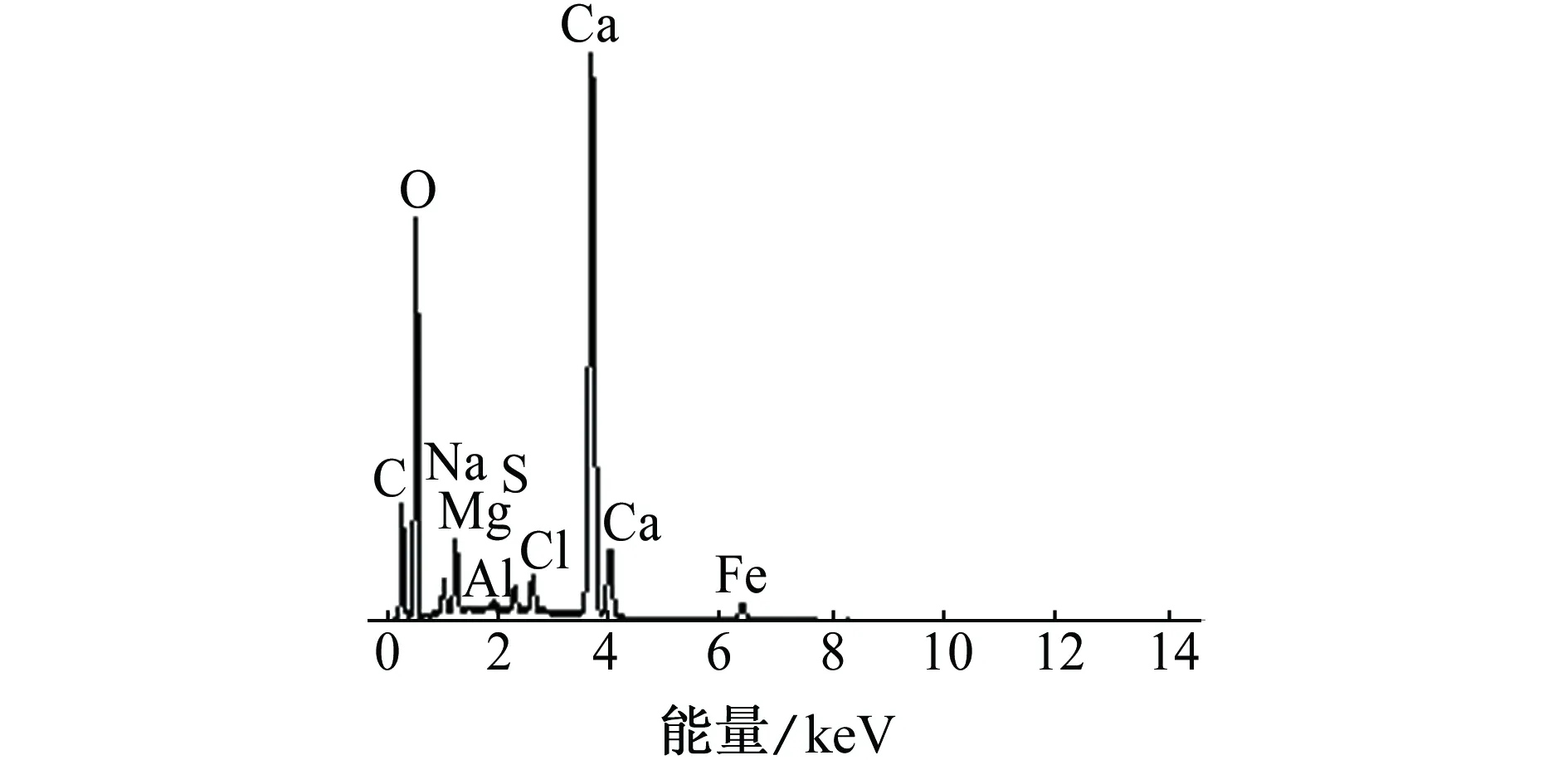
(a) 12 h
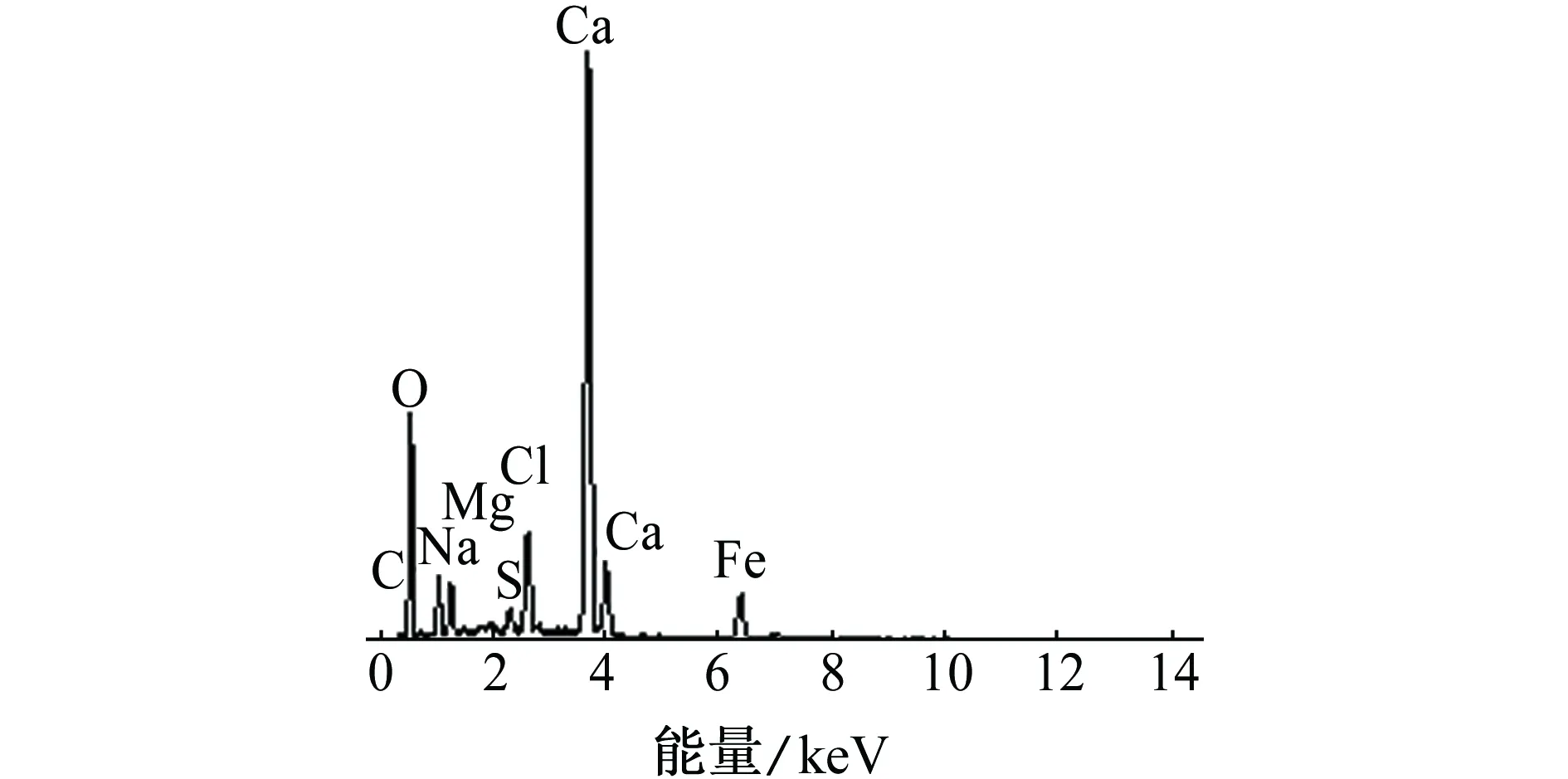
(b) 1 d
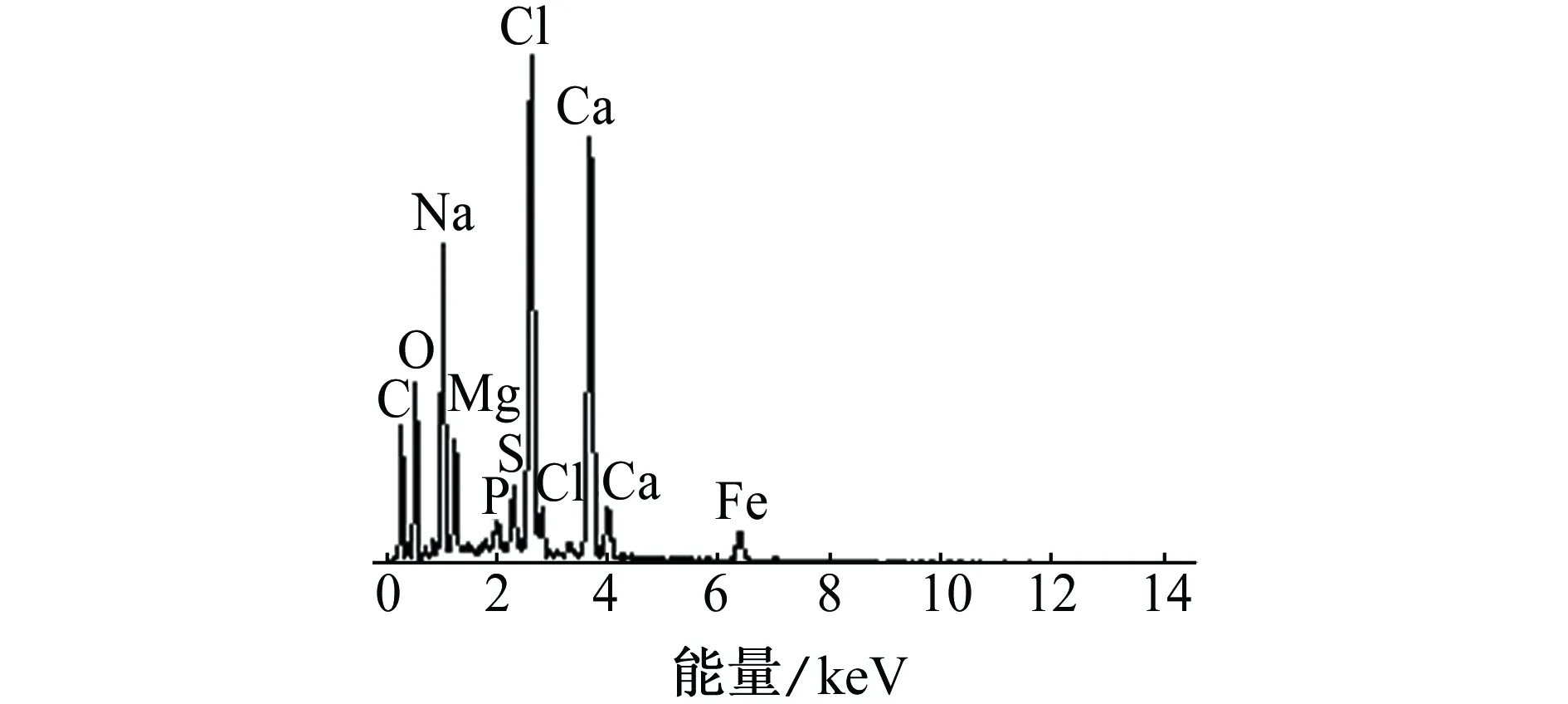
(c) 3 d
(d) 5 d 图1 经硫酸盐还原菌附着不同时间后Q235碳钢表面 钙质沉积层的EDS谱Fig. 1 EDS spectra of calcareous deposits on the surface of Q235 carbon steel after adhesion of sulfate reducing bacteria for different periods of time

表1 钙质沉积层中钙元素和镁元素的含量 (质量分数)Tab. 1 Content of calcium and magnesium in calcareous deposits (mass) %
2.2 钙质沉积层表面形貌
经硫酸盐还原菌附着不同时间后Q235碳钢表面钙质沉积层的表面形貌如图2所示。从图2中可以看到:硫酸盐还原菌附着时间为12 h时,制备的钙质沉积层较均匀、致密,表面晶体较小,呈三角形状并且排列规整;硫酸盐还原菌附着时间为1 d时,制备的钙质沉积层不均匀也不致密,表面晶体依然比较小,呈三角形状并且排列规整;硫酸盐还原菌附着时间为3 d时,制备的钙质沉积层不均匀也不致密,表面晶体依然较小,但晶体形状发生改变;硫酸盐还原菌附着时间为5 d时,制备的钙质沉积层比较疏松,表面晶体比较大,晶体形状呈现类似圆形。
2.3 电化学阻抗谱
经硫酸盐还原菌附着不同时间后Q235碳钢表面钙质沉积层的电化学阻抗谱如图3所示,而不同试验条件下电化学阻抗谱的等效电路以及拟合后得到电化学参数分别如图4和表2所示。其中,Rsol代表溶液电阻,CPEdl代表电极表面双电层的常相位角元件,Rct代表电极表面电荷转移电阻,CPEf代表电极表面膜层的常相位角元件,Rf代表电极表面膜层电阻。
从Bode图可见:硫酸盐还原菌附着时间为12 h,1 d以及3 d时,制备的钙质沉积层只出现了一个峰,表明测试体系中只含有一个时间常数,选择图4(a)所示的等效电路拟合;硫酸盐还原菌附着时间为5 d和没有细菌附着(附着时间为0 h)时,制备的钙质沉积层出现了两个峰,说明体系中含有两个时间常数,选择图4(b)所示的等效电路拟合。
从Nyquist图可见:随附着时间的延长,各钙质沉积层容抗弧半径逐渐变小,附着时间为5 d时,容抗弧半径又增大;附着时间为0 h时制备的钙质沉积层的容抗弧半径远大于硫酸盐还原菌附着后制备的钙质沉积层的容抗弧半径;同时,对于经硫酸盐还原菌附着后制备的钙质沉积沉积层,其最大的Rct值出现在附着时间为5 d时,但是该值远小于附着时间为0 h时制备的钙质沉积层的(9 282 Ω·cm2),这主要是由于金属表面生物膜的形成抑制了钙质沉积层的形成,使硫酸盐还原菌局部腐蚀加速[23]。

(a) 12 h

(b) 1 d

(c) 3 d

(d) 5 d 图2 经硫酸盐还原菌附着不同时间后Q235碳钢表面 钙质沉积层的表面形貌Fig. 2Surface morphology of calcareous deposits on the surface of Q235 carbon steel after adhesion of sulfate reducing bacteria for different periods of time

(a) Nyquist图
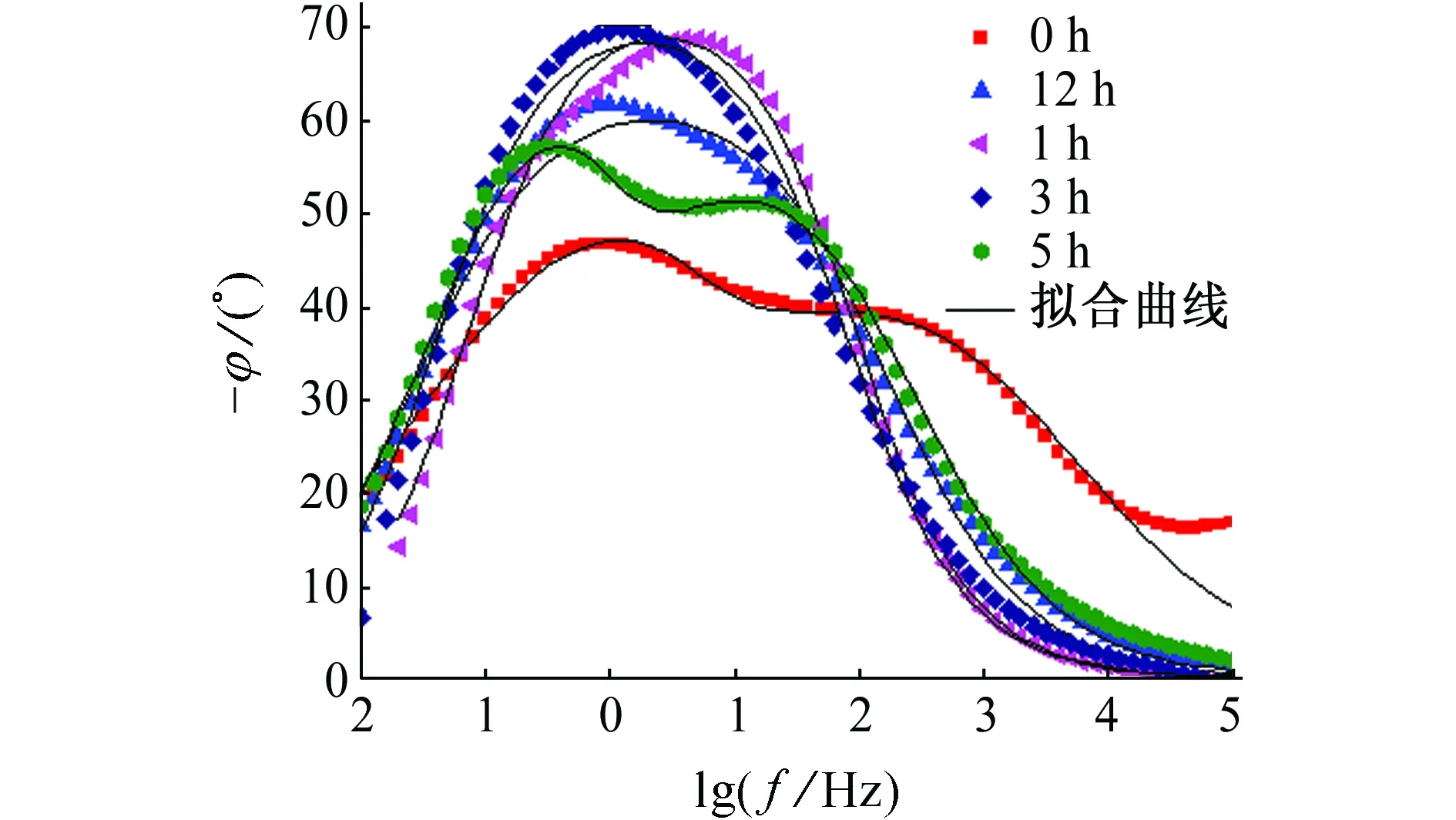
(b) Bode图 图3 经硫酸盐还原菌附着不同时间后Q235碳钢表面 钙质沉积层的电化学阻抗谱Fig. 3 EIS of calcareous deposits on the surface of Q235 carbon steel after adhesion of sulfate reducing bacteria for different periods of time: (a) Nyquist plots; (b) Bode plots
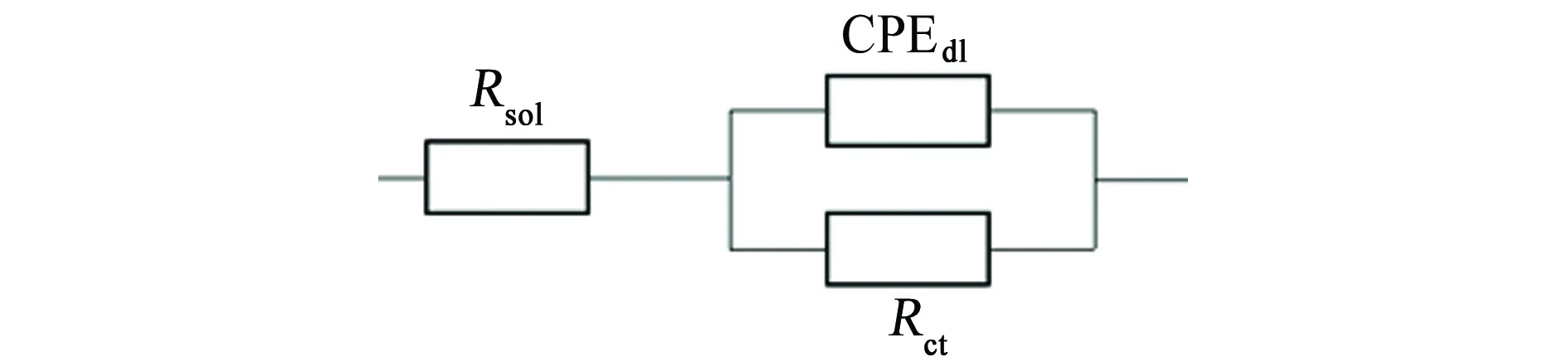
(a) 0 h,5 d

(b) 12 h,1 d,3 d 图4 拟合图3中电化学阻抗谱的等效电路Fig. 4 Equivalent circuits for fitting the EIS in Fig. 3
3 结论
(1) 硫酸盐还原菌在碳钢表面附着形成生物膜之后,钙质沉积层仍能沉积于碳钢表面。

表2 电化学阻抗谱的拟合参数Tab. 2 Fitted parameters of EIS
(2) 在金属表面被硫酸盐还原菌附着形成生物膜的情况下,采用-30 μA/cm2电流密度,极化72 h获得的钙质沉积层主要成分为CaCO3,几乎不含Mg(OH)2。
(3) 无论硫酸盐还原菌附着时间长短,生物膜的形成,都会使所需初始保护电流密度和局部pH降低,导致金属表面钙质沉积层的量减少,对基体的保护性减弱,硫酸盐还原菌局部腐蚀加速。
参考文献:
[1] VENZLAFF H,ENNING D,SRINIVASAN J,et al. Accelerated cathodic reaction in microbial corrosion of iron due to direct electron uptake by sulfate-reducing bacteria[J]. Corrosion Science,2013,66:88-96.
[2] SHENG X X,TING Y P,PEHKONEN S O. The influence of sulphate-reducing bacteria biofilm on the corrosion of stainless steel AISI 316[J]. Corrosion Science,2007,49:2159-2176.
[3] SANDERS P F,STOTT J F D. Assessment,monitoring and control of microbiological corrosion hazards in offshore oil production systems[C]//Corrosion 1987. Houston,TX:NACE,1987:870314.
[4] WIKIEL A J,DATSENKO I,VERA M,et al. Impact of desulfovibrio alaskensis biofilms on corrosion behaviour of carbon steel in marine environment[J]. Bioelectrochemistry,2014,97:52-60.
[5] YUAN S,LIANG B,ZHAO Y,et al. Surface chemistry and corrosion behaviour of 304 stainless steel in simulated seawater containing inorganic sulphide and sulphate-reducing bacteria[J]. Corrosion Science,2013,74:353-366.
[7] LIU F L,ZHANG J,SUN C X,et al. The corrosion of two aluminium sacrificial anode alloys in SRB-containing sea mud[J]. Corrosion Science,2014,83:375-381.
[9] JACK T R. Biological corrosion failures[M]//ASM Handbook:Failure Analysis and Prevention. [S.l.]:ASM International,2002:882-890.
[10] CHEN X,WANG G,GAO F,et al. Effects of sulphate-reducing bacteria on crevice corrosion in X70 pipeline steel under disbonded coatings[J]. Corrosion Science,2015,101:1-11.
[11] WAGNER P,LITTLE B,HART K,et al. Environmental fate of sacrificial zinc anodes and influence of a biofilm[J]. International Biodeterioration & Biodegradation,1996,37(3):151-157.
[12] BARCHICHE C,DESLOUIS C,FESTY D,et al. Characterization of calcareous deposits in artificial seawater by impedance techniques:3-deposit of CaCO3in the presence of Mg (II)[J]. Electrochimica Acta,2003,48(12):1645-1654.
[13] LUO J S,LEE R U,CHEN T Y,et al. Formation of calcareous deposits under different modes of cathodic polarization[J]. Corrosion,1991,47(3):189-196.
[14] GABRIELLI C,KEDDAM M,KHALIL A,et al. Study of calcium carbonate scales by electrochemical impedance spectroscopy[J]. Electrochimica Acta,1997,42(8):1207-1218.
[15] REFAIT P,JEANNIN M,SABOT R,et al. Corrosion and cathodic protection of carbon steel in the tidal zone:products,mechanisms and kinetics[J]. Corrosion Science,2015,90:375-382.
[16] WOLFSON S L,HARTT W H. An initial investigation of calcareous deposits upon cathodic steel surfaces in sea water[J]. Corrosion,1981,37(2):70-76.
[17] HARTT W H,CULBERSON C H,SMITH S W. Calcareous deposits on metal surfaces in seawater-a critical review[J]. Corrosion,1984,40(11):609-618.
[18] DEC W,MOSIALEK M,SOCHA R P,et al. The effect of sulphate-reducing bacteria biofilm on passivity and development of pitting on 2205 duplex stainless steel[J]. Electrochimica Acta,2016,212:225-236.
[19] ZHENG F,WEN G M,FANG B F,et al. Influence of cathodic polarization mode on the formation of calcareous deposits[J]. Corrosion Science,1995,6:253-256.
[20] 汪江伟,张杰,陈守刚,等. 钙质层对Q235碳钢在含双眉藻f/2培养基中腐蚀行为的影响[J]. 中国腐蚀与防护学报,2016,35(6):535-542.
[21] DESLOUIS C,FALARAS P,GIL O,et al. Influence of clay on calcareous deposit in natural and artificial sea water[J]. Electrochimica Acta,2006,51(15):3173-3180.
[22] 温国谋,郑辅养. 海水中阴极保护时钙质沉积层的形成及其应用[J]. 腐蚀与防护,1995,16(1):50-53.
[23] EDYVEAN R G J,MAINES A D,HUTCHINSON C J,et al. Interactions between cathodic protection and bacterial settlement on steel in seawater[J]. International Biodeterioration & Biodegradation,1992,29(3/4):251-271.

