响应面法优化纳米Fe3O4/CaO2处理含PAEs废水的研究
朱峥嵘,石 崇,朱颖一,王彩彩,王明新
(1.常州大学环境与安全工程学院,江苏 常州,213164;2.江苏龙环环境科技有限公司,江苏 常州,213022)
邻苯二甲酸酯(Phthalates,PAEs)是一类使用广泛的增塑剂,广泛存在于地下水和土壤环境中[1-2]。它是一种潜在的内分泌干扰物,已先后被世界卫生组织、欧盟、美国和中国列入“优先控制污染物名单”[3-5]。国内外学者针对水环境中PAEs类污染物的去除进行了大量的研究,并取得了一定的成果[6-11]。
高级氧化技术因其能够高效去除多种有机污染物而备受关注,包括臭氧催化氧化、光催化氧化、芬顿氧化和超声波/微波氧化以及过渡金属元素催化氧化等[12-18]。其中,芬顿氧化因其具有反应快、易操作等优点而在废水处理中得到了广泛的应用,但也存在过氧化氢(H2O2)容易无效分解,导致利用率不高、反应体系需保持低pH值、铁泥易造成二次污染等缺点。有研究表明,固体过氧化物如过氧化钙(CaO2)在水化介质中可以缓慢释放H2O2,能克服H2O2容易无效分解的问题[19-20]。此外,采用比表面积大、比表面能高的纳米四氧化三铁(纳米Fe3O4)作为铁源来代替经典芬顿试剂中的Fe2+,可大大提高催化活性,且对反应体系pH值的适应性较大,磁性容易分离和重复利用,有利于降低成本。因此,本研究以邻苯二甲酸二甲酯(DMP)、邻苯二甲酸二乙酯(DEP)、邻苯二甲酸丁苄酯(BBP)和邻苯二甲酸二丁酯(DBP)4种邻苯二甲酸酯(PAEs)模拟废水为处理对象,采用纳米Fe3O4作为催化剂、CaO2作为氧化剂组成新型非均相类芬顿试剂,研究其对模拟废水中4种PAEs的降解效果,并采用Box-Behnken响应面法对反应条件进行了拟合与优化,旨在为该方法的实际应用提供科学依据和设计参数。
1 材料与方法
1. 1 试验试剂与仪器
(1) 试验试剂:邻苯二甲酸二甲酯(DMP)、邻苯二甲酸二乙酯(DEP)、邻苯二甲酸丁苄酯(BBP)、邻苯二甲酸二丁酯(DBP)、异丙醇、盐酸、氢氧化钠、四氯化碳、氯化钠,均为分析纯;纳米Fe3O4(20~30 nm,98%)、CaO2(65%)、乙腈(HPLC)、甲醇(HPLC),均为色谱纯;试验用水为超纯水。
(2) 试验仪器:LC-20AT高效液相色谱仪(日本岛津公司);BT224S电子天平;FE28 pH计;KH-500DB数控超声波清洗器;THZ-C恒温振荡器;GT16-3高速台式离心机等。
1. 2 试验方法
1.2.1 模拟废水中4种PAEs的降解试验
采用批处理试验,在250 mL锥形瓶中室温条件下进行。用盐酸和氢氧化钠调节溶液pH值,在250 mL锥形瓶中加入100 mL的PAEs混合溶液,DMP、DEP、BBP、DBP 4种污染物初始浓度均设定为100 mg/L,分别加入不同摩尔比例的纳米Fe3O4和CaO2,置于恒温振荡器中,调节转速为180 r/min,反应12 h后取样测定其去除率。
1.2.2 响应面法优化试验设计
根据纳米Fe3O4和CaO2单独试验的条件和结果,采用Box-Behnken模型设计中心组合试验,通过三次平行试验的平均值建立二次回归模型。在单因素试验的基础上,选取纳米Fe3O4投加量(X1)、CaO2投加量(X2)和初始pH值(X3)3个主要因素,并以+1、0、-1分别代表各因素的高、中、低水平,响应值为4种PAEs的去除率。应用Design Expert 8.0.5软件进行响应面法优化试验设计,见表1。
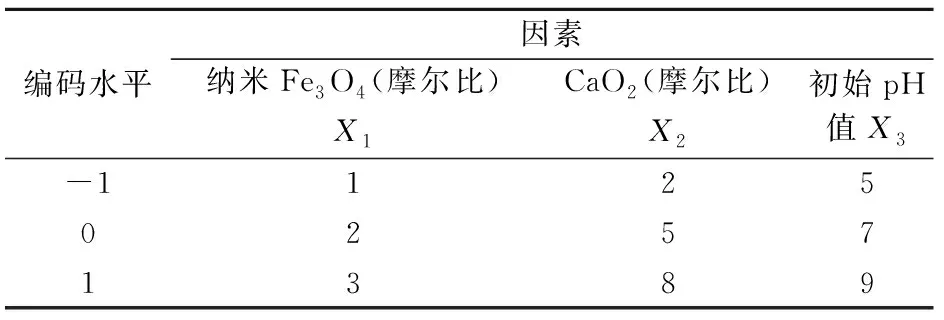
表1 响应面法优化试验设计Table 1 Design of the response surface methodology experiment
1. 3 分析方法
模拟废水中4种PAEs的浓度采用LC-20AT高效液相色谱仪进行测定,样品预处理采用超声辅助液液微萃取方法,经膜过滤后直接进样。
测试条件:紫外检测器;色谱柱为SinChrom ODS-BP(5 μm,4.6×250 mm);流动相为乙腈/水(75/25,体积比),等速洗脱,流速为1 mL/min;进样体积为20 μL,检测波长为225 nm,保留时间为15 min。
2 结果与讨论
2. 1 单因素试验结果与分析
2.1.1 纳米Fe3O4和CaO2的投加量对模拟废水中4种PAEs去除率的影响
2.1.1.1 等比例纳米Fe3O4和CaO2的投加量对模拟废水中4种PAEs去除率的影响
设置纳米Fe3O4∶CaO2∶PAEs(摩尔比)分别为0.5∶0.5∶1、1∶1∶1、2∶2∶1、5∶5∶1、10∶10∶1,反应条件是:摇床转速为180 r/min、初始pH值为中性条件、反应温度为室温、反应时间为12 h,考察等比例纳米Fe3O4和CaO2的投加量对模拟废水中4种PAEs去除率的影响,其试验结果见图1。
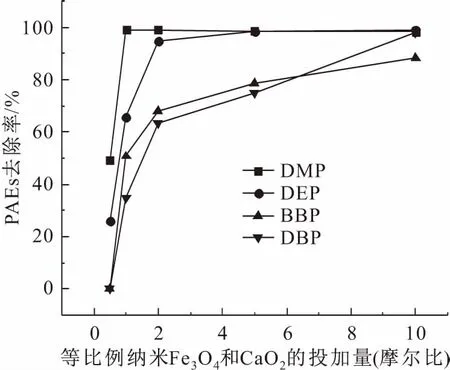
图1 等比例纳米Fe3O4和CaO2的投加量对模拟废水中4种PAEs去除率的影响Fig.1 Effects of equal dosage of nano Fe3O4 and CaO2 on removal rate of PAEs in model wastewater
由图1可见:在纳米Fe3O4/CaO2反应体系中,当等比例纳米Fe3O4和CaO2的投加量较低时,模拟废水中4种PAEs的去除率均随投加量的增加呈迅速上升趋势;当等比例纳米Fe3O4和CaO2的投加量增加到2倍摩尔比时,模拟废水中DMP和DEP的去除率已经达到90%以上并趋于平衡,继续加大投加量效果不大;当等比例纳米Fe3O4和CaO2的投加量逐渐增加时,模拟废水中BBP和DBP的去除率随之增大,但降解速率有所降低;当等比例纳米Fe3O4和CaO2的投加量为5倍摩尔比时,模拟废水中BBP和DBP的去除率达到70%以上,当投加量继续增加到10倍摩尔比时,模拟废水中DBP的去除率可达到90%以上,BBP的去除率可达到80%以上。
2.1.1.2 CaO2投加量对模拟废水中4种PAEs去除率的影响
设置纳米Fe3O4∶CaO2∶PAEs(摩尔比)分别为5∶0.5∶1、5∶1∶1、5∶2∶1、5∶5∶1、5∶10∶1,反应条件是:摇床转速为180 r/min、初始pH值为中性条件、反应温度为室温、反应时间为12 h,考察CaO2投加量对模拟废水中4种PAEs去除率的影响,其试验结果见图2。
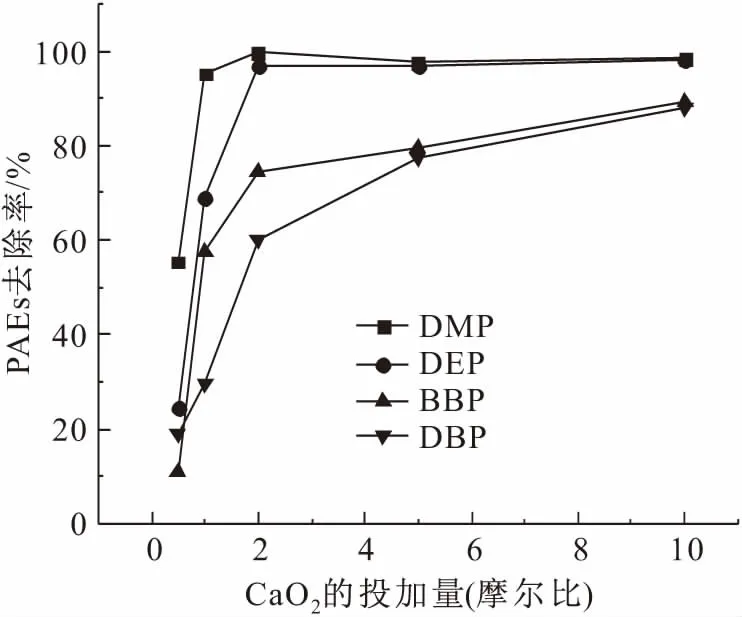
图2 CaO2投加量对模拟废水中4种PAEs去除率的影响Fig.2 Effects of dosage of CaO2 on removal rate of the 4 kinds of PAEs
CaO2投入到反应体系后,有两种分解方式:
CaO2+H2O→Ca(OH)2↓+O2↑
(1)
CaO2+H2O→Ca(OH)2↓+H2O2
(2)

Fe2++H2O2→Fe3++OH-+·OH
(3)
·OH+RH→H2O+·R
(4)
·R+Fe3+→R++Fe2+
(5)
R++O2→ROO+→CO2+H2O
(6)
由图2可见:当CaO2的投加量从0.5倍摩尔比增加到2倍时,模拟废水中4种PAEs的去除率显著增大,其中DMP和DEP的去除率已经达到90%以上;当CaO2的投加量由2倍摩尔比增加到10倍时,模拟废水中DMP和DEP的去除率趋于平衡,BBP和DBP的去除率不断升高。这是因为:随着CaO2投加量的不断增加,纳米Fe3O4/CaO2反应体系中的H2O2含量随之增大,反应速率的增大有助于污染物的降解,但H2O2含量达到一定程度时会捕捉·OH;此外,过量的CaO2投加到该反应体系中会释放大量的热,从而导致H2O2自身的分解。因此CaO2投加量达到一定值后,再加入过量的CaO2对该反应体系中PAEs降解效果的影响不大。
2.1.1.3 纳米Fe3O4投加量对模拟废水中4种PAEs去除率的影响
设置纳米Fe3O4∶CaO2∶PAEs(摩尔比)分别为0.5∶5∶1、1∶5∶1、2∶5∶1、5∶5∶1、10∶5∶1,反应条件是:摇床转速为180 r/min、初始pH值为中性条件、反应温度为室温、反应时间为12 h,考察纳米Fe3O4投加量对模拟废水中4种PAEs去除率的影响,其试验结果见图3。

图3 纳米Fe3O4投加量对模拟废水中PAEs去除率的影响Fig.3 Effects of dosage of nano Fe3O4 on removal rate of PAEs in model wastewater
由图3可见:随着纳米Fe3O4投加量的增加,模拟废水中DMP和DEP的去除率几乎没有变化,表明这两种污染物的主要降解机理不仅有芬顿/类芬顿反应,还包括水解反应,因此受纳米Fe3O4投加量的影响不显著;模拟废水中BBP和DBP的去除率则随着纳米Fe3O4投加量的增加而显著提高,表明这两种污染物的降解机理主要是芬顿/类芬顿反应,因此加入纳米Fe3O4能显著提高BBP和DBP的去除效果。这是因为:当纳米Fe3O4/CaO2反应体系中的纳米Fe3O4的投加量较低时,铁源是限制因素,因此加入纳米Fe3O4对模拟废水中BBP和DBP降解速率的增幅较大,但随着纳米Fe3O4的投加量的增大,Fe2+催化产生的·OH会自身相互碰撞至湮灭而来不及参与目标反应就被消耗,同时Fe2+在催化H2O2产生自由基的同时自身也会被氧化成Fe3+而沉淀,导致BBP和DBP降解速率的增幅迅速趋缓[22]。
2.1.2 pH值对模拟废水中4种PAEs去除率的影响
设置纳米Fe3O4∶CaO2∶PAEs(摩尔比)为2∶5∶1,初始pH值分别为3、5、7、9和11,反应条件是:摇床转速为180 r/min、反应温度为室温、反应时间为12 h,考察pH值对模拟废水中4种PAEs去除率的影响,其试验结果见图4。
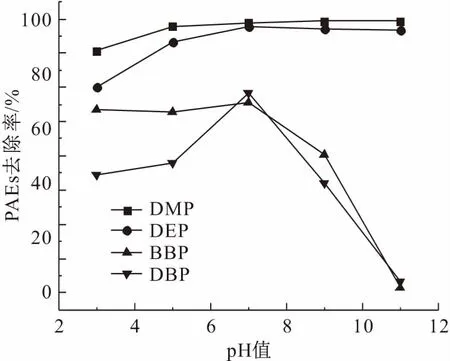
图4 pH值对模拟废水中4种PAEs去除率的影响Fig.4 Effects of pH on removal rate of the 4 kinds of PAEs in model wastewater
由图4可见,模拟废水中DMP和DEP的去除率在pH=7时均达到90%以上,而模拟废水中BBP和DBP也在pH=7时去除率达到最高,表明纳米Fe3O4/CaO2反应体系在溶液初始pH值为中性的条件下可以有效降解模拟废水中的PAEs。
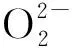
2. 2 多因素试验结果与分析
2.2.1 模型拟合方差分析及显著性检验
在单因素试验的基础上,本研究采用3因素3水平试验设计,每个因素分别取低、中、高3个水平,编码为-1、0、1,选用RSM中的Box-Behnken响应面法优化试验设计[23-24],其试验结果见表2。
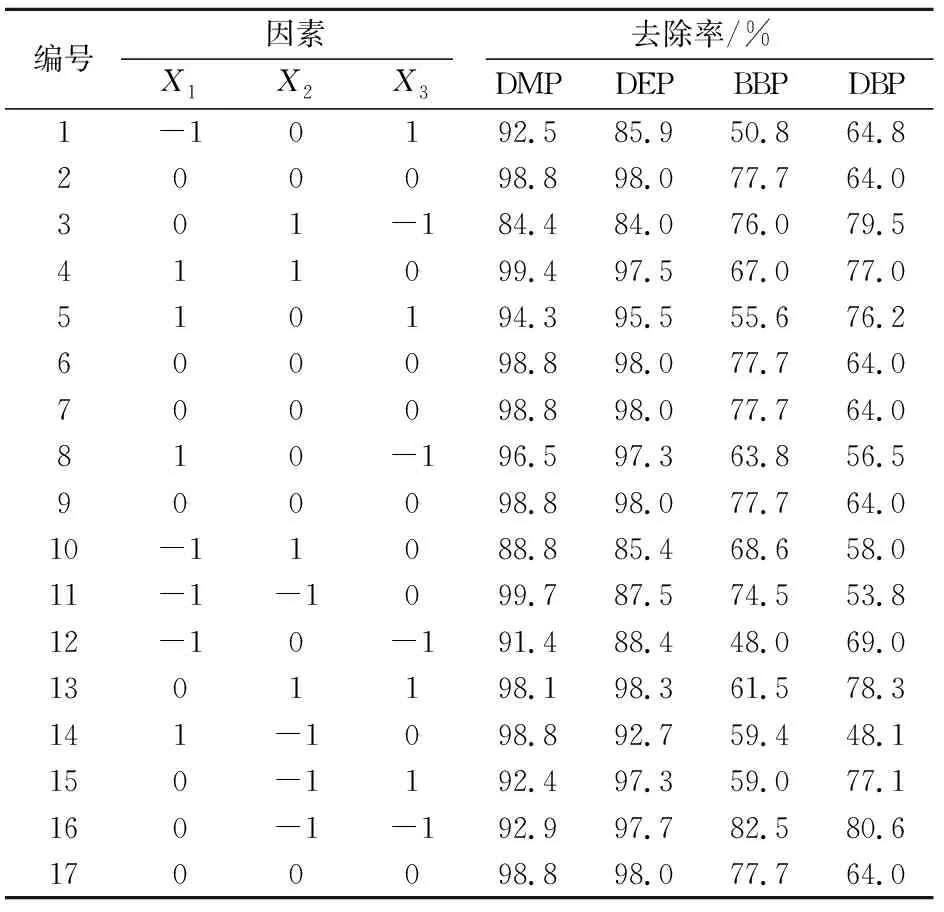
表2 Box-Behnken响应面法优化试验设计及结果Table 2 Box-Behnken design and results
本文采用Design Experts 8.0.5软件对DMP、DEP、BBP和DBP 4种PAEs的去除率数据进行统计分析,并利用二阶回归模型方程式逐步回归拟合,再对模型拟合结果进行方差分析,利用F值对每个因素进行显著性检验,p值小于0.05说明回归模型具有较好的显著性[25-26]。拟合得到如下二阶多项式回归模型:
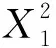
(7)
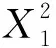
(8)
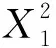
(9)
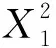
(10)
式中:Y为响应值,Y1、Y2、Y3和Y4分别为DMP、DEP、BBP和DBP的去除率;X1、X2、X3分别为纳米Fe3O4投加量(摩尔比)、CaO2投加量(摩尔比)和初始pH值。
模拟拟合结果方差分析结果显示:模型方程(7)~(10)的p值分别为0.010 1、0.035 6、0.043 9、0.025 3,说明模型拟合结果具有较好的显著性;模型决定系数R2分别为0.895 8、0.844 2、0.832 9、0.860 6,说明独立变量之间的相关性较好,表明该模型可用于实际预测。
2.2.2 响应面法分析
为了更直观地显示各影响因素之间的交互作用对模拟废水中4种PAEs去除率的影响,本文采用Design-Experts 8.0.5软件拟合得到纳米Fe3O4投加量(摩尔比)、CaO2投加量(摩尔比)和初始pH值3个影响因素对模拟废水中4种PAEs去除率的等值线图,详见图5至图8。
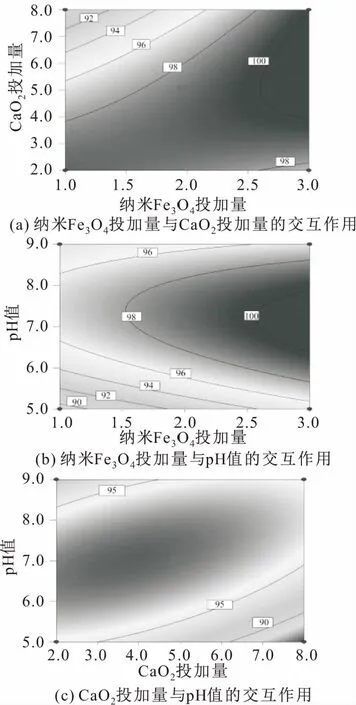
图5 不同影响因素对模拟废水中DMP去除率的等值线图Fig.5 Contour plots of different factors on DMP removal rate in model wastewater
图5(a)反映了当初始pH值取中值时,纳米Fe3O4投加量与CaO2投加量的交互作用对模拟废水中DMP去除率的影响。当纳米Fe3O4投加量较低时,模拟废水中DMP的去除率随着CaO2投加量的增加而降低;当纳米Fe3O4投加量较高时,模拟废水中DMP的去除率则与CaO2投加量呈二次方关系,但CaO2投加量的影响幅度逐渐减小。图5(b)反映了CaO2投加量取中值时,纳米Fe3O4投加量与初始pH值的交互作用对模拟废水中DMP去除率的影响。当初始pH值较低时,模拟废水中DMP的去除率随着纳米Fe3O4投加量的增加而增加,且随着初始pH值的增加,纳米Fe3O4投加量对模拟废水中DMP去除率的促进作用逐渐降低。图5(c)反映了纳米Fe3O4投加量取中值时,CaO2投加量与初始pH值的交互作用对模拟废水中DMP去除率的影响。当CaO2投加量较低时,初始pH值偏酸性或碱性时将有助于模拟废水中DMP的降解;而当CaO2投加量较高时,则初始pH值为碱性时对降解模拟废水中DMP有利。
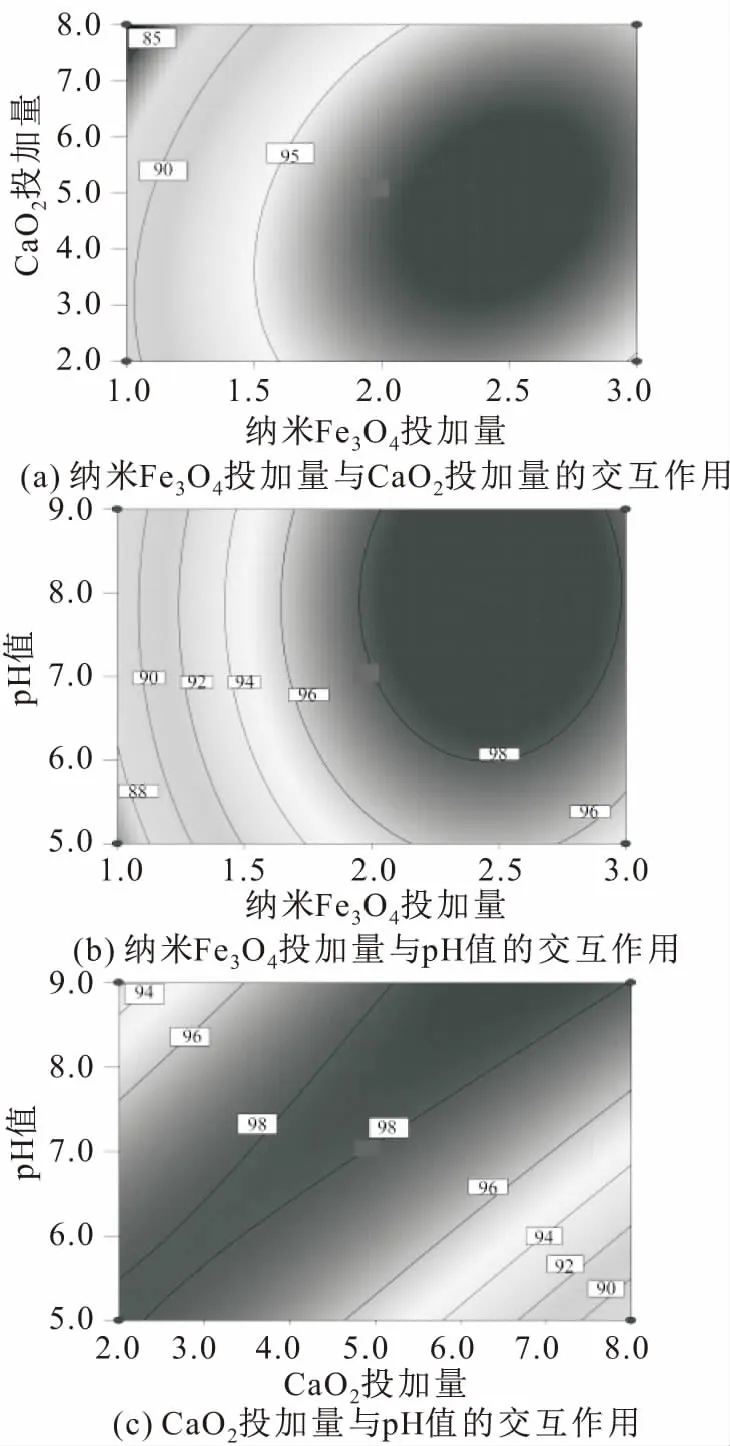
图6 不同影响因素对模拟废水中DEP去除率的等值线图Fig.6 Contour plots of different factors on DEP removal rate in model wastewater
图6(a)反映了当初始pH值取中值时,纳米Fe3O4投加量与CaO2投加量的交互作用对模拟废水中DEP去除率的影响。当CaO2投加量较大时,纳米Fe3O4投加量的增加有助于模拟废水中DEP的降解,当纳米Fe3O4投加量增加到1.5倍摩尔比时,模拟废水中DEP的去除率可达95%以上;当纳米Fe3O4投加量较低时,CaO2投加量的变化对模拟废水中DEP去除率的影响较小,当纳米Fe3O4投加量逐渐增加后,CaO2投加量的影响幅度开始变大,总体上DEP的去除率与CaO2投加量呈二次方关系。图6(b)反映了CaO2投加量取中值时,纳米Fe3O4投加量与初始pH值的交互作用对模拟废水中DEP去除率的影响。当pH值较低时,随着纳米Fe3O4投加量的增加,模拟废水中DEP的去除率先升高后略有下降;当pH值处于较高水平时,模拟废水中DEP去除率随着纳米Fe3O4投加量的增加而增加,但初始pH值对模拟废水中DEP去除率的影响幅度很小。图6(c)反映了纳米Fe3O4投加量取中值时,CaO2投加量与初始pH值的交互作用对模拟废水中DEP去除率的影响。当CaO2投加量处于较低水平时,模拟废水中DEP的去除率随着pH值的升高有所下降;当CaO2投加量处于较高水平时,模拟废水中DEP的去除率随着pH值的增加而增加,且初始pH值对DEP去除率的影响总体上很小。

图7 不同影响因素对模拟废水中BBP去除率的等值线图Fig.7 Contour plots of different factors on BBP removal rate in model wastewater
图7(a)反映了当初始pH值取中值时,纳米Fe3O4投加量与CaO2投加量的交互作用对模拟废水中BBP去除率的影响。当纳米Fe3O4投加量不变的条件下,CaO2投加量对模拟废水中BBP去除率的影响很小;当CaO2投加量不变的条件下,模拟废水中BBP的去除率随着纳米Fe3O4投加量的增加呈先上升后下降的趋势。图7(b)反映了CaO2投加量取中值时,纳米Fe3O4投加量与初始pH值的交互作用对模拟废水中BBP去除率的影响。当pH值较低时,模拟废水中BBP的去除率随着CaO2投加量的增加呈先增加后降低的趋势;当pH较高时,模拟废水中BBP的去除率随着CaO2投加量的增加而增加;当纳米Fe3O4投加量不变时,pH值对模拟废水中BBP去除率的影响很小。图7(c)反映了纳米Fe3O4投加量取中值时,CaO2投加量与初始pH值的交互作用对模拟废水中BBP去除率的影响。模拟废水中BBP的去除率较高的降解条件处于CaO2投加量与初始pH均较低或较高时,当CaO2投加量较低或较高时,模拟废水中BBP的去除率随着pH值的增加而增加,本试验范围内当CaO2投加量取中值时,pH值对模拟废水中BBP去除率的影响很小。

图8 不同影响因素对模拟废水中DBP去除率的等值线图Fig.8 Contour plots of different factors on DBPremoval rate in model wastewater
图8(a)反映了当初始pH值取中值时,纳米Fe3O4投加量与CaO2投加量的交互作用对模拟废水中DBP去除率的影响。总体上当纳米Fe3O4投加量与CaO2投加量均较高时,模拟废水中DBP的去除率较高;当CaO2投加量处于较低水平(2~6倍摩尔比)时,模拟废水中DBP的去除率随着纳米Fe3O4投加量的增加先升高后降低;当CaO2投加量处于较高低水平(6~8倍摩尔比)时,模拟废水中DBP的去除率随着纳米Fe3O4投加量的增加而增加。图8(b)反映了CaO2投加量取中值时,纳米Fe3O4投加量与初始pH值的交互作用对模拟废水中DBP去除率的影响。当初始pH值低于5.5或高于8.5且纳米Fe3O4投加量处于中间水平(1.5~2.5倍摩尔比)时,模拟废水中DBP的去除率处于较高水平,初始pH值处于中性附近,纳米Fe3O4投加量较低或较高均不利于模拟废水中DMP的降解。图8(c)反映了纳米Fe3O4投加量取中值时,CaO2投加量与初始pH值的交互作用对模拟废水中BBP去除率的影响。当初始pH值较低或较高时,CaO2投加量的增加对模拟废水中DMP的降解具有促进作用;当初始pH值在中性附近时,CaO2投加量对模拟废水中DMP降解的影响很小。
2.2.3 最佳反应条件的确定及模型验证
为了获取4种PAEs去除率最大值的优化反应条件,本文利用Design Expert 8.0.5软件的优化功能,设定优化目标为模拟废水中4种PAEs的平均去除率最高,约束条件为纳米Fe3O4投加量、CaO2投加量和初始pH值在本试验的取值范围内,得到的最优反应条件为:纳米Fe3O4∶CaO2∶PAEs为2∶5∶1、溶液初始pH值为5。在该反应条件下,模拟废水中DMP、DEP、BBP和DBP的去除率分别为94.6%、95.7%、68.2%和68.7%。
为了验证上述拟合结果的可靠性,本研究进行了3组平行试验,得到模拟废水中DMP、DEP、BBP和DBP的平均去除率分别为93.1%、94.0%、67.5%、67.8%,与预测值的偏差分别为1.5%、1.7%、0.7%、0.9%,表明模型方程具有较高的拟合精度。
3 结 论
本次试验研究表明:纳米Fe3O4/CaO2反应体系能有效降解模拟废水中DMP、DEP、BBP和DBP 4种PAEs,其中CaO2对模拟废水中DMP和DEP具有较强的降解能力,其主要降解机理可能为碱性水解,而纳米Fe3O4可以显著强化CaO2对模拟废水中BBP和DBP的降解作用,其主要降解机理可能为类芬顿反应;纳米Fe3O4/CaO2反应体系可在初始pH值为中性的条件下有效降解模拟废水中4种PAEs。此外,响应面分析结果表明:纳米Fe3O4投加量、CaO2投加量和溶液初始pH值之间的交互作用显著影响了模拟废水中4种PAEs的去除率,当纳米Fe3O4∶CaO2∶PAEs摩尔比为2∶5∶1、溶液初始pH值为5时,模拟废水中DMP、DEP、BBP和DBP的平均去除率均较高,分别为94.6%、95.7%、68.2%和68.7%,与预测值的偏差分别为1.5%、1.7%、0.7%、0.9%,表明该模型可以较好地拟合4种PAEs与各反应条件之间的关系,可用于反应条件的模拟、预测及优化。
参考文献:
[1] Matsuda K,Watanabe I,Mizukami K,et al.Dry deposition of PM2.5sulfate above a hilly forest using relaxed eddy accumulation[J].AtmosphericEnvironment,2015,107:255-261.
[2] Lovekamp-Swan T,Davis B J.Mechanisms of phthalate ester toxicity in the female reproductive system[J].EnvironmentalHealthPerspectives,2003,111(2):139-145.
[3] Martino-Andrade A J,Chahoud I.Reproductive toxicity of phthalate esters[J].MolecularNutrition&FoodResearch,2010,54(1):148-157.
[4] Caldwell J C.DEHP:Genotoxicity and potential carcinogenic mechanisms—A review[J].MutationResearch/ReviewsinMutationResearch,2012,751(2):82-157.
[5] Lottrup G,Andersson A M,Leffers H,et al.Possible impact of phthalates on infant reproductive health[J].InternationalJournalofAndrology,2006,29(1):172-180.
[6] 刘静,李亚茹,王杰,等.高级催化氧化法去除水中邻苯二甲酸酯的研究进展[J].生态环境学报,2014(5):904-910.
[7] Huang Z J,Wu P X,Lu Y H,et al.Enhancement of photocatalytic degradation of dimethyl phthalate with nano-TiO2immobilized onto hydrophobic layered double hydroxides:A mechanism study[J].JournalofHazardousMaterials,2013,246:70-78.
[8] Huang R H,Yan H H,Li L S,et al.Catalytic activity of Fe/SBA-15 for ozonation of dimethyl phthalate in aqueous solution[J].AppliedCatalysisB-Environmental,2011,106(1/2):264-271.
[9] He P J,Zheng Z,Zhang H,et al.PAEs and BPA removal in landfill leachate with Fenton process and its relationship with leachate DOM composition[J].ScienceoftheTotalEnvironment,2009,407(17):4928-4933.
[10]朱敏,张弛,康嘉玲,等.邻苯二甲酸酯的毒性及其降解研究[J].环境科学与技术,2013(S2):443-447,453.
[11]Feng X H,Zhou J,Ding S M.Photodegradation of dimethyl phthalate by Fe(III)/oxalate/H2O2system[J].AdvancesMaterialsResearch,2012,550/551/552/553:2412-2415.
[12]Dargnat C,Teil M J,Chevreuil M,et al.Phthalate removal throughout wastewater treatment plant:Case study of Marne Aval station (France)[J].ScienceoftheTotalEnvironment,2009,407(4):1235-1244.
[13]Tay K S,Rahman N A,Bin Abas M R.Fenton degradation of dialkylphthalates:Products and mechanism[J].EnvironmentalChemistryLetters,2011,9(4):539-546.
[14]Yuan B L,Li X Z,Graham N.Reaction pathways of dimethyl phthalate degradation in TiO2-UV-O2and TiO2-UV-Fe(VI) systems[J].Chemosphere,2008,72(2):197-204.
[15]Lau T K,Chu W,Graham N.The degradation of endocrine disruptor di-n-butyl phthalate by UV irradiation:A photolysis and product study[J].Chemosphere,2005,60(8):1045-1053.
[16]Wen G,Ma J,Liu Z Q,et al.Ozonation kinetics for the degradation of phthalate esters in water and the reduction of toxicity in the process of O3/H2O2[J].JournalofHazardousMaterials,2011,195:371-377.
[17]范荣桂,黄大青,方辽卫,等.高级氧化技术在纺织印染废水处理中的应用[J].安全与环境工程,2011,18(2):40-44.
[18]鲁剑,张勇,吴盟盟,等.电化学氧化法处理高氨氮废水的试验研究[J].安全与环境工程,2010,17(2):51-53.
[19]周彦波,王英秀,周振华,等.过氧化钙缓释氧剂的制备及其释氧特性研究[J].中国给水排水,2012,28(7):64-67.
[20]Wang H F,Zhao Y S,Su Y,et al.Fenton-like degradation of 2,4-dichlorophenol using calcium peroxide particles:Performance and mechanisms[J].RSCAdvances,2017,7(8):4563-4571.
[21]田依林,李明玉,马同森,等.Fenton试剂氧化水中芳香族化合物的机理[J].污染防治技术,2003,16(1):12-15.
[22]孙大贵,陶长元,刘作华,等.活性炭-Fenton组合法去除水中PAEs的研究[J].环境科学,2007,28(12):2734-2739.
[23]李海杰.低频超声耦合臭氧氧化降解水中双酚A及响应面优化研究[J].环境工程,2016,34(9):40-45.
[24]王雅辉,吕文英,邹雪刚,等.响应面法优化胡敏素对Cu2+的吸附及机理研究[J].环境科学学报,2017,37(2):624-632.
[25]Chen S S,Zeng Z,Hu N,et al.Simultaneous optimization of the ultrasound-assisted extraction for phenolic compounds content and antioxidant activity ofLyciumruthenicumMurr.fruit using response surface methodology[J].FoodChemistry,2018,242:1-8.
[26]Ruqayyah T I D,Jamal P,Alam M Z,et al.Application of response surface methodology for protein enrichment of cassava peel as animal feed by the white-rot fungusPanustigrinusM609RQY[J].FoodHydrocolloids,2014,42:298-303.

