三明治结构rGO/Fe3O4@mSiO2载体的构筑及协同抗肿瘤性能
杨永梅 嵇眀翔 杨 颖 谢安建 沈玉华*,
(1安徽大学化学化工学院,现代生物制造协同创新中心,合肥 230601)(2黄山学院化学化工学院,黄山 245041)
癌症已成为危害公众健康的重大疾病之一。多年来国内外研究者一直致力于行之有效的癌症治疗方法的探寻,使得诊治该疾病的方法得到了快速发展。现在化疗和放疗是临床上应用最广泛的方法,但其所用药物副作用大,让病人产生巨大的痛苦[1-2]。因此,近年来毒副作用有所降低的光热疗法[3]、磁热疗法[4]、免疫疗法[5]和微波疗法[6]等不断被开发出来,为癌症治疗提供了新的选择,但单一疗法仍无法得到令人满意的效果,探索多模式协同抗癌的治疗方法成了新的研究方向。另一方面,众多优异的药物载体如介孔硅[7],介孔碳[8]和金属有机框架化合物[9]等被合成出来。其中,介孔二氧化硅(mSiO2)是近年来在生物医学领域中被广泛应用的药物载体。它具有较大的比表面积、高孔容、可调孔径以及优良生物相容性等特点[10]。但是,单一的化疗效果不理想,且单纯的mSiO2无法将药物精准地运输到肿瘤部位。
氧化石墨烯(GO)是一种拥有单原子厚度的二维碳材料,不仅拥有较高的比表面积,为负载药物分子提供平台,而且具有优异的光热性能,因而可作为光热效果治疗肿瘤组织方法[11-12]中的理想材料。 但由于石墨烯片层之间有较强的范德华力作用[13],使其容易发生团聚。因此,对其表面进行修饰并与其他材料复合是防止其团聚的有效措施。另外,Fe3O4是一种典型的磁性材料,将一些药物载体材料与之复合,借用外磁场可以实现药物的靶向传输。例如Fe3O4/MoS2[14],Fe3O4@zirconium[15]以 及 Fe3O4@NH2@MOF-5[16]等复合物均利用Fe3O4的优异磁性实现了药物的靶向传输,提高了治疗效果。
鉴于此,本论文提出一种新的具有协同作用的靶向药物传输方法。如Scheme 1所示,首先对制备的Fe3O4纳米粒子进行氨基化修饰,再与GO复合,形成GO/Fe3O4复合物。然后,以十六烷基三甲基溴化铵(CTAB)作为一种致孔剂,使SiO2沿着石墨烯两侧生长,构建一种类似“三明治”结构的GO/Fe3O4@mSiO2,再将GO还原得到rGO/Fe3O4@mSiO2复合载体材料。SiO2具有大量的介孔结构,使复合材料具有较大的比表面积和孔容,利于载药。同时,复合材料中的Fe3O4作为磁靶向物质,可将药物有效运输到肿瘤部位。GO具有优异的光热性能,可在靶向定位后对肿瘤区域进行光热治疗有望实现协同抗癌治疗效果。
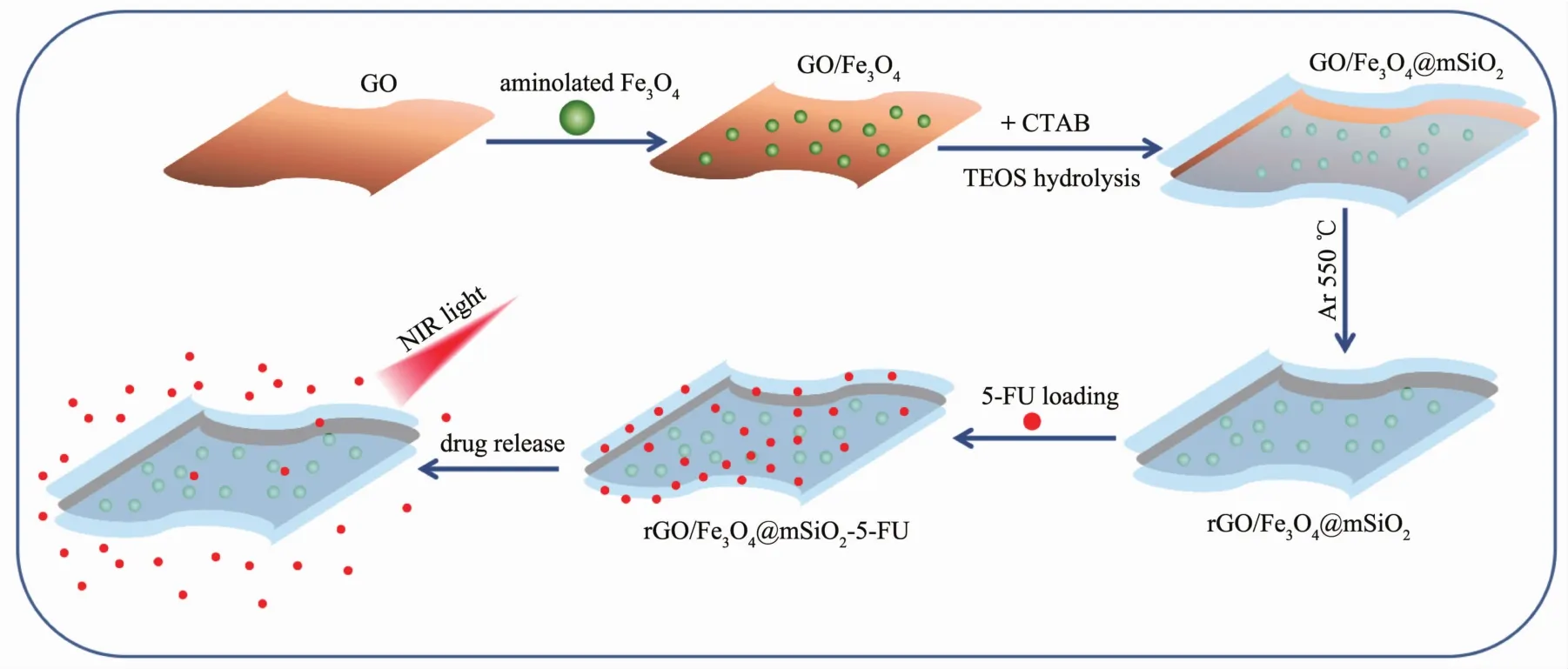
Scheme 1 Preparation,drug loading and controlled release of rGO/Fe3O4@mSiO2nanocomposites
1 实验部分
1.1 主要试剂和材料
石墨片,高锰酸钾(KMnO4),硝酸钠(NaNO3),六水合三氯化铁(FeCl3·6H2O),乙二醇(C2H6O2),乙酸钠(CH3COONa),聚乙二醇(Mr=1 500),十六烷基三甲基溴化铵(CTAB)和二甲亚砜(DMSO)购于国药试剂有限公司;3-氨丙基三乙氧基硅烷(APTES),正硅酸乙酯(TEOS)购于阿拉丁试剂(上海)有限公司;五氟尿嘧啶(5-FU),Hoechst 33342,碘化吡啶(PI),3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴盐 (MTT),胰酶(0.25% 含 EDTA,GIBCO),DMEM 高糖培养基和胎牛血清(GIBCO)购自上海生工生物工程有限公司。以上试剂均为分析纯,未经进一步纯化。实验用水为超纯水(18.0 MΩcm)。
1.2 仪器和设备
所用仪器包括紫外可见分光光度计(UV-1800,日本岛津)、荧光显微镜(DMI3000B,德国徕卡)、酶联免疫检测仪 (RT-2100C,深圳镭拓)。采用NEXUS-870 FTIR型傅里叶变换红外光谱仪,利用溴化钾压片法来检测样品结构;采用DX-2700型X射线衍射仪(Cu Kα射线作为发射源,波长为0.154 056 nm,衍射角 2θ为 5°~90°)对样品的物相进行分析,测试电压为40 kV,电流为100 mA;采用SU 1510型扫描电子显微镜(加速电压10 kV)和JEM 100SX型透射电子显微镜(加速电压200 kV),观察产物形貌与结构;采用ELSZ-2型ζ电位分析仪(日本大塚电子株式会社)对产品进行ζ电位测量;采用3H-2000BET-A型比表面测试仪器对产品进行N2吸附-脱附和孔径测定。产物的磁学性质测试在MPMS XL-7型精密SQUID磁学测量系统(美国量子设计公司)上进行。采用Fluke Ti32热红外摄像机对样品光照前后进行热红外图像采集。
1.3 rGO/Fe3O4@mSiO2纳米复合载体的制备
参照文献报道的Hummers法和溶剂热法分别制备GO纳米片[17-19]和Fe3O4纳米粒子[20],备用。将150 mg Fe3O4纳米粒子分散于100 mL无水乙醇中,缓慢滴加5 mL的APTES,超声5 min后,再磁力搅拌6 h,对其表面进行氨基化修饰,再磁铁分离。然后将修饰后的Fe3O4纳米粒子分散于75 mL去离子水中,制备浓度为2 mg·mL-1的氨基化Fe3O4纳米粒子悬浮液。配制0.25 mg·mL-1的GO溶液150 mL,加入20 mL 2 mg·mL-1氨基化的Fe3O4纳米粒子溶液,加热至40℃并搅拌2 h。然后加入1.5 g CTAB,待完全溶解后,缓慢滴加1.5 mL TEOS,40℃条件下持续搅拌24 h。然后在6 000 r·min-1下离心分离并用热乙醇(40℃)清洗2次,再用0.45 μm的水系微孔滤膜抽滤,取滤膜上的固体,纯水和乙醇清洗多次,真空干燥,得到GO/Fe3O4@mSiO2复合材料。最后在氩 (Ar)气氛下550℃煅烧3 h,得到rGO/Fe3O4@mSiO2纳米复合载体,保存备用。
1.4 药物负载及释放
抗癌药物5-FU的负载:称取5 mg制备的rGO/Fe3O4@mSiO2纳米复合载体加入到5 mL的1 mg·mL-15-FU溶液中,超声分散后,在摇床上振荡24 h,得到rGO/Fe3O4@mSiO2-5-FU悬浮液。离心分离,取上层清液稀释30倍测定吸光度。根据5-FU标准曲线,并利用公式(1)计算载药率(DLR)。

药物释放:取10 mg的rGO/Fe3O4@mSiO2-5-FU加入到50 mL pH值分别为7.4和5.0的磷酸盐缓冲液(PBS)中,振荡并在0~48 h内多次取溶液离心,取上层清液0.1 mL稀释至3 mL,测定吸光度并计算药物释放率。原溶液中每次取出溶液后均补加0.1 mL PBS,保持总体积不变,并且后面所取样品的吸光度均为其前所有吸光度数值的总和。其中光照组在药物释放8 h时光照10 min再继续相同的操作,计算并绘制出药物释放行为曲线。
1.5 细胞毒性测试
选用MTT实验来检测rGO/Fe3O4@mSiO2的生物相容性以及对HeLa细胞的杀伤能力。首先将所制备的rGO/Fe3O4@mSiO2与rGO/Fe3O4@mSiO2-5-FU复合物配制为浓度为1 mg·mL-1的悬浮液,用紫外光照10 min进行灭菌处理,然后用DMEM培养基稀释至0.1、0.01和 0.001 mg·mL-1,保存备用。 将HeLa细胞以每孔5×103个接种到96孔板,并置于含有5%(V/V)CO2的培养箱(37℃)中培养24 h。然后移去培养基,加入100 μL稀释后的复合物-培养基溶液(包括对照组),再放入培养箱中继续培养24 h。分别设置避光与光照条件,其中光照组在4 h后取出,并利用808 nm近红外光照10 min再放回。置于CO2培养箱中孵化24 h后,移去培养基,加入20 μL MTT检测液,继续孵化4 h后,去除上层液,加入100 μL DMSO溶液,持续振荡,完全溶解后使用酶联免疫检测仪进行检测490 nm处的吸光值(OD值),并用公式(2)计算细胞存活率(RCV),其中ODexp、ODbla和ODcon分别为实验组、空白组和对照组的OD值。

1.6 细胞荧光显微镜图像分析
为了进一步研究复合材料对HeLa细胞的杀伤效果,利用Hoechst 33342和PI双染色的方法观察细胞凋亡情况[21-22]。HeLa细胞按照每孔5×104个接种在6孔板上,在含5%(V/V)CO2,37℃的恒温培养箱中培养24 h。然后分别将3 mL内含1 mL rGO/Fe3O4@mSiO2与rGO/Fe3O4@mSiO2-5-FU溶液的培养基加入到6孔板中,放入培养箱中继续培养24 h。设置避光与光照条件进行对照,其中光照组在4~6 h后取出并利用808 nm近红外激光照射10 min后放回培养箱继续孵育24 h。最后取出6孔板,弃去培养基,用pH=7.4的PBS冲洗,再使用0.5 mL的Hoechst 33342(10 μg·mL-1)和 0.5 mL 的 PI(10μg·mL-1)溶液分别对其进行染色10 min,然后用PBS清洗干净,固定后在倒置荧光显微镜下观察并拍照。
2 结果与讨论
2.1 产物的形貌表征
为了解产物的形貌及尺寸,对其进行了SEM测试。图1A和B分别为GO与Fe3O4的SEM图,可以看出GO为薄片层状结构并伴有明显的褶皱,而Fe3O4为尺寸均匀的纳米微球,粒径约为200 nm。图1C显示Fe3O4纳米球均匀地分布在GO表面,表明氨基化的Fe3O4与GO成功地复合。而在图1D中可以看出,rGO/Fe3O4@mSiO2具有明显的二维平面结构,尺寸约为4 μm的片层相互堆叠,其表面已看不到Fe3O4纳米球。这可能是由于介孔SiO2覆盖于GO/Fe3O4表面上下两层,将其包裹起来形成类似“三明治”结构的复合材料。
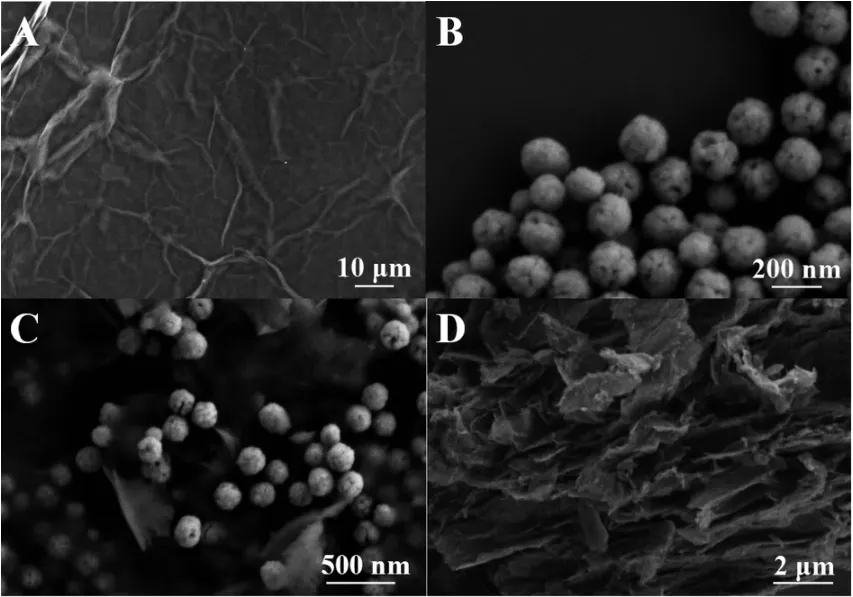
图 1 GO(A)、Fe3O4(B)、GO/Fe3O4(C)和 rGO/Fe3O4@mSiO2(D)的扫描电子显微镜(SEM)图Fig.1 SEM images of GO(A),Fe3O4(B),GO/Fe3O4(C)and rGO/Fe3O4@mSiO2(D)
2.2 产物的X射线衍射(XRD)和红外光谱(FTIR)图分析
图2A为不同样品的XRD图,从图2A-a可以看出, 物质的主要峰位在 2θ 为 30.1°、35.4°、43.1°、56.9°和 62.5°处(以△表示),分别对应 Fe3O4的(220),(311),(400),(511),(440)晶 面(PDF No.65-3107)。图2A-b在10.2°出现一个GO的特征峰(以■表示)。从图2A-c可以同时看到Fe3O4和GO的特征峰,GO的特征峰偏移至11°左右,可能是由于氨基化的Fe3O4与GO复合对其的影响。如图2A-d所示:除Fe3O4的特征峰外,在23°~26°处出现一个宽峰可能是因为rGO与SiO2的特征吸收峰在此处相互重叠而形成的,表明rGO/Fe3O4@mSiO2成功合成。为进一步证明这一结论,又对制备过程各阶段产物进行了红外光谱测试 (图2B)。从Fe3O4红外光谱图可以看出在570 cm-1处有归属于Fe3O4的Fe-O键的特征伸缩振动峰[23]。GO/Fe3O4复合物的FTIR光谱图中,在1 655 cm-1位置出现C=O振动吸收峰,这是因为GO中含有大量的羧基。而加入了表面活性剂CTAB修饰后的 GO/Fe3O4, 在 2 917、2 849 和 1 486 cm-1位置均有出峰,分别归属于CTAB分子中的-CH3和-CH2-基团的C-H伸缩振动和弯曲振动吸收峰。在GO/Fe3O4@mSiO2的FTIR图中, 约 810、965 cm-1处的吸收峰分别对应于Si-O-Si的伸缩振动吸收峰和Si-OH的振动 峰[24], 说明成功合成了GO/Fe3O4@mSiO2。同时,可以看出CTAB峰明显减弱,可能是由于其在清洗过程中被大量除去。通过Ar气氛中高温煅烧,CTAB的振动吸收峰基本消失,表明CTAB发生改变,而GO的C=O振动特征峰也随之减弱,这可能是由于在高温煅烧过程中CTAB分解产生的碳及氨作为还原剂将GO转化为rGO,生成了最终产物rGO/Fe3O4@mSiO2。
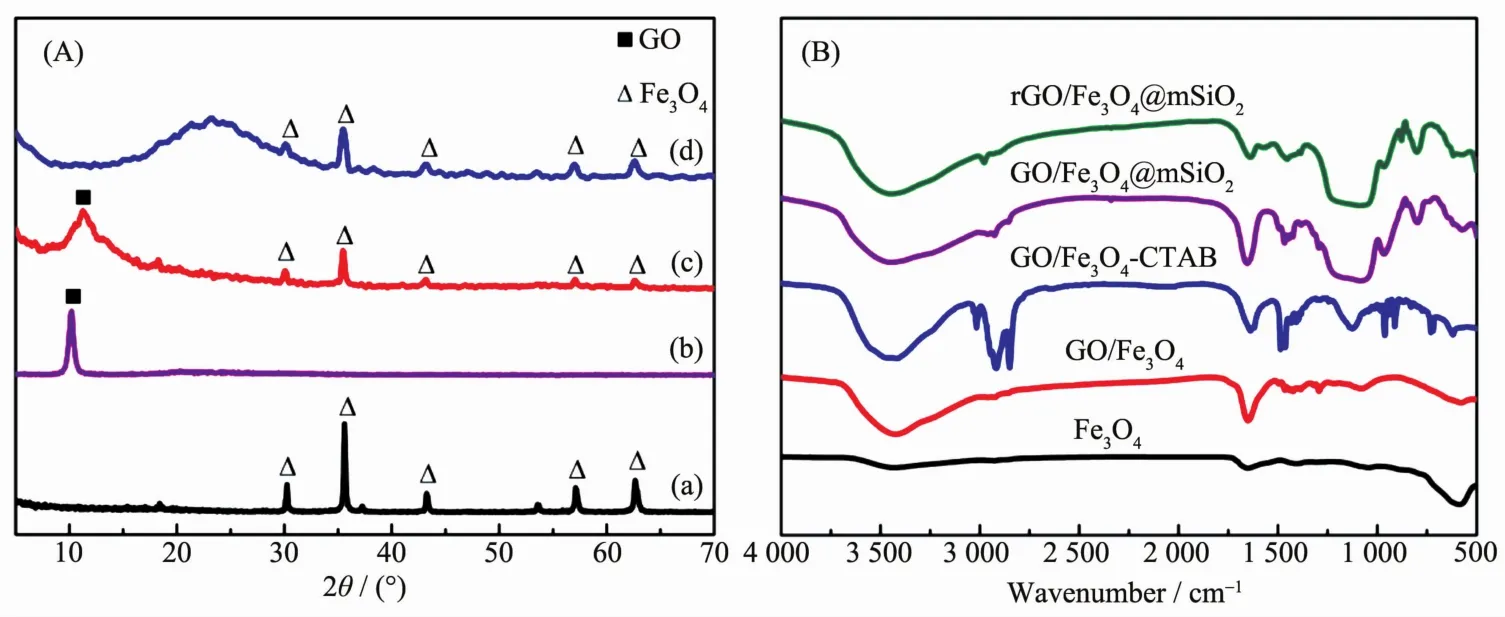
图 2 (A)Fe3O4(a)、GO(b)、GO/Fe3O4(c)和 rGO/Fe3O4@mSiO2(d)的 XRD 图;(B)样品的 FTIR 谱图Fig.2 (A)XRD patterns of Fe3O4(a),GO(b),GO/Fe3O4(c)and rGO/Fe3O4@mSiO2(d);(B)FTIR spectra of different samples
2.3 rGO/Fe3O4@mSiO2的形成机理探讨
为了探讨复合载体的形成机理,我们分别测定了各中间产物的ζ电位(图3)。Fe3O4纳米粒子ζ电位为-11.8 mV,是由于在水分散液中其表面富含羟基。利用APTES修饰后ζ电位为38.9 mV,表明Fe3O4纳米粒子表面被修饰了氨基,显正电荷,并可以较稳定地在溶液中分散。因此,经APTES修饰Fe3O4纳米粒子可通过静电引力与带负电荷(-52 mV)的GO复合,形成GO/Fe3O4复合物。由于GO负电荷较多,复合后总体显负电,电位为-13.1 mV。加入带正电荷的CTAB后,可以利用静电引力吸附在GO表面上下两层[25-27],使得GO/Fe3O4-CTAB复合物显正电(18.1 mV)。之后引入 TEOS,TEOS聚集在CTAB周围发生水解和缩聚生成SiO2,而且其异质成核过程主要发生在GO/Fe3O4表面,形成了类似“三明治”结构的GO/Fe3O4@mSiO2纳米复合材料。再经Ar气氛的煅烧后,CTAB分子碳化分解,同时GO被还原。生成的rGO/Fe3O4@mSiO2纳米复合载体经测定呈负电性(-25.7 mV)。ζ电位分析表明:产物形成的机理主要是各反应物层与层之间的静电吸附作用。
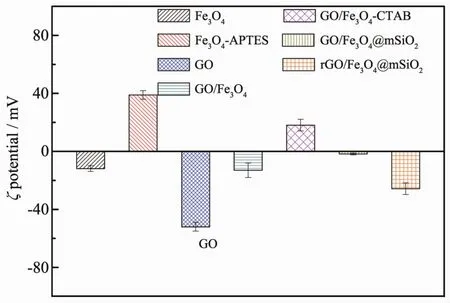
图3 不同样品的ζ电位分布图(25℃)Fig.3 ζ potential distribution of different samples(25℃)
2.4 产物的磁性和光热性能分析
为了研究所制备产物的磁学性质,测试了Fe3O4和rGO/Fe3O4@mSiO2复合物在室温下(300 K)的磁化强度随磁场变化的情况,并绘制曲线如图4A所示。Fe3O4纳米粒子的饱和磁化强度为65 emu·g-1,而rGO/Fe3O4@mSiO2复合物的饱和磁化强度则降低至32 emu·g-1。导致磁化强度降低的原因可能是由于SiO2与rGO的介入导致相同质量复合物中Fe3O4所占比重降低。低磁场放大图表明其呈现顺磁性,矫顽力约40 Oe。rGO/Fe3O4@mSiO2的磁性使其在作为药物载体时具有磁靶向特性。另外,为检测复合物光致生热性能,采用Fluke Ti32热红外摄像仪对808 nm光 照 前 后 的 去 离 子 水 、Fe3O4、GO、GO/Fe3O4、GO/Fe3O4@mSiO2以及rGO/Fe3O4@mSiO2水分散液进行热红外图像采集,光照时间为10 min。从图4B中发现相较于去离子水,Fe3O4、GO以及纳米复合物GO/Fe3O4、GO/Fe3O4@mSiO2和 rGO/Fe3O4@mSiO2水分散液温度均有升高,其中GO/Fe3O4比Fe3O4和GO都高,表明Fe3O4对GO有一定的协同光热效果[28];同时,rGO/Fe3O4@mSiO2也比 GO/Fe3O4@mSiO2水分散液升温更多,说明GO被还原后光热效果更好;因此,浓度相同的rGO/Fe3O4@mSiO2升温最高,达到18℃,可能是由于rGO更好地光热性能以及GO与Fe3O4复合的协同影响作用。同时,为考察纳米复合物循环使用情况,激光循环照射和冷却4次并分别测量其水分散液的温度,从图4B温度变化曲线可以看出4次循环后GO水分散液温度波动范围在27.5~28.9℃之间,而rGO/Fe3O4@mSiO2几乎未见温度波动,表明rGO/Fe3O4@mSiO2纳米复合物具备良好的光热稳定性。

图4 (A)Fe3O4(a)、rGO/Fe3O4@mSiO2(b)的磁滞回线;(B)样品水分散液在808 nm激光循环照射和冷却4次的温度变化曲线Fig.4 (A)Magnetization curves of Fe3O4(a)and rGO/Fe3O4@mSiO2(b);(B)Photothermal curves of aqueous dispersion of different samples under 808 nm irradiation/cooling four cycles
2.5 N2吸附等温线、孔径分布和药物的负载与释放
从rGO/Fe3O4@mSiO2的N2吸附等温线与孔径分布图(图5A)可知,该等温线为Ⅳ型吸附平衡等温线,而迟滞环属于H3型,主要对应于材料的狭缝型孔,在较高相对压力区域没有表现出吸附限制,这说明了材料以介孔为主。吸附量随着相对压力P/P0增大而缓慢增加,在相对压力P/P0达到0.4~0.5时,吸附量出现激增现象,表明从该相对压力开始,材料中的介孔孔道内发生毛细管凝聚现象,进一步证明介孔结构的存在且孔径较均匀;在相对压力达到1.0左右,吸附量达到最大。rGO/Fe3O4@mSiO2的BET比表面积和孔容分别为 217 m2·g-1和 0.047 8 cm3·g-1,孔径为3.92 nm左右。说明这种方法制备的rGO/Fe3O4@mSiO2复合材料拥有较大的比表面积与孔容,有利于药物分子的负载。
为验证rGO/Fe3O4@mSiO2药物负载能力,我们测定了负载前后5-FU溶液在266 nm处的吸光度(图5B),利用其标准曲线计算出rGO/Fe3O4@mSiO2纳米复合物对5-FU的装载量。根据计算可知,负载率为57.34%。rGO/Fe3O4@mSiO2具有如此优异的载药性能主要是由于其mSiO2和rGO均具有丰富的介孔结构以及较大的比表面积,两者复合更加增强了对药物的负载能力。为证明rGO/Fe3O4@mSiO2作为药物载体的优势,我们进一步做了药物释放实验,从图5C中可知:在pH=7.4的条件下,在0~24 h内5-FU含量不断上升,24 h后释放速度趋于平缓,最终释放量为46.6%;而在pH=5.0时,药物在前6 h内快速释放,然后也趋于平缓,最终释放量较中性条件大大提升,达到64.8%,可能是由于5-FU药物分子的N和O原子与介孔硅表面富含的羟基通过氢键结合,在中性环境下较为稳定,而在酸性环境中,H+能跟氢键受体相结合,从而氢键被破坏,最终导致药物分子更多的释放。为进一步考察光照条件对药物释放的影响,光照组在药物释放8 h后光照10 min再继续测定,实验结果表明在pH=7.4和5.0时,光照后5-FU释放速度均有大幅度提高,pH=5.0增幅更大,最终释放率也增高到约79.8%,这可能是因为光照导致材料体系温度升高,5-FU与介孔硅之间的氢键被大量破坏,作用力的减弱使药物释放率增大。实验表明在光照以及类似于肿瘤细胞所属的酸性环境下(pH=5.0),rGO/Fe3O4@mSiO2药物载体具有较高的最终释放量和较快的释放速度,可有效提高到达肿瘤部位的药物浓度,从而更有利于药物发挥抗肿瘤作用。
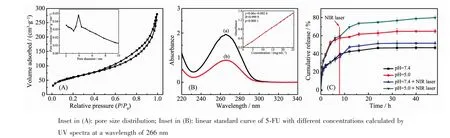
图5 (A)rGO/Fe3O4@mSiO2的N2吸附等温线;(B)5-FU被rGO/Fe3O4@mSiO2负载前 (a)、负载后 (b)的紫外吸收光谱;(C)避光与光照条件和不同pH值PBS中rGO/Fe3O4@mSiO2-5-FU释放行为曲线Fig.5 (A)N2adsorption isotherms of rGO/Fe3O4@mSiO2;(B)UV absorption spectra of the 5-FU solution before(a)and after(b)loaded on the rGO/Fe3O4@mSiO2nanocomposites;(C)Release behaviors of 5-FU from rGO/Fe3O4@mSiO2-5-FU nanocomposites in PBS with different pH values without or with NIR laser irradiation for 10 min,respectively
2.6 细胞毒性实验结果分析
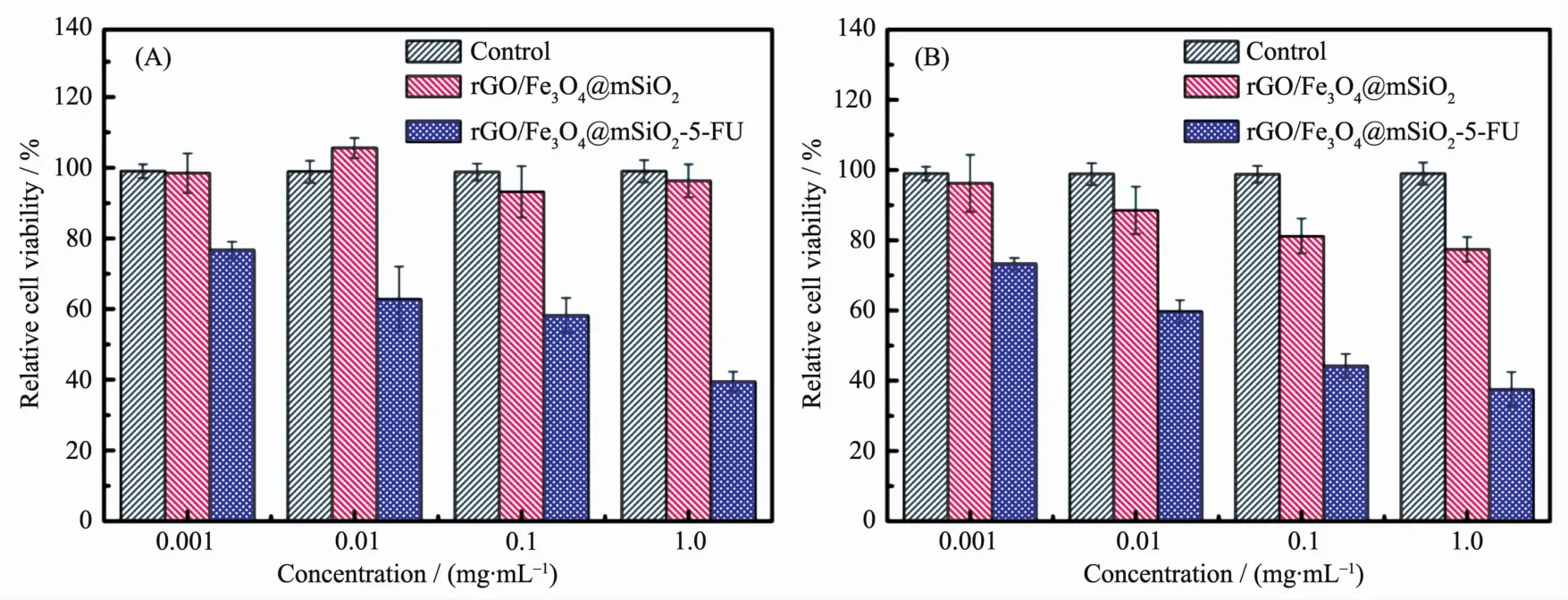
图6 不同浓度的rGO/Fe3O4@mSiO2和rGO/Fe3O4@mSiO2-5-FU在无光照 (A)和有光照(B)条件下培养的HeLa细胞存活率Fig.6 Viability of HeLa cells incubated with different concentrations of rGO/Fe3O4@mSiO2and rGO/Fe3O4@mSiO2-5-FU without(A)and with(B)irradiation
通过细胞MTT测试,研究了rGO/Fe3O4@mSiO2和rGO/Fe3O4@mSiO2-5-FU在光照与否的条件下对细胞存活率的影响,结果如图6所示。对无光照条件下的rGO/Fe3O4@mSiO2复合物(图6A)来说,细胞存活率随着材料浓度的增加没有显著的变化,平均可达95%以上,说明rGO/Fe3O4@mSiO2复合材料具有良好的生物相容性。无光照条件下的rGO/Fe3O4@mSiO2-5-FU,对细胞具有一定的杀伤效果,且在高浓度下更为显著,主要是由于rGO/Fe3O4@mSiO2-5-FU高浓度释放出的5-FU的化疗作用。而在光照条件下(图6B),细胞的存活率均有不同程度的降低,是由于rGO/Fe3O4@mSiO2的光热性能对细胞具有一定的杀伤效果。光照条件下的rGO/Fe3O4@mSiO2-5-FU,对HeLa细胞的杀伤效果则最为明显,源于rGO/Fe3O4@mSiO2-5-FU载体材料中释放出的5-FU的化疗与光照条件下材料优异的光热性能的协同抗肿瘤作用。
2.7 细胞荧光显微镜图像分析
为进一步验证rGO/Fe3O4@mSiO2作为药物载体对HeLa细胞的抑制作用,我们进行了细胞荧光成像分析。图7a为对照组,由图可以看出,HeLa细胞呈现出亮蓝色荧光(a1)且无红色荧光(a2),这说明在此条件下HeLa细胞均处于存活状态,无明显死亡现象。当在细胞中加入了rGO/Fe3O4@mSiO2时,仍无明显红色荧光(b2)出现,表明复合物具有良好的生物相容性。与之相比较,光照之后在部分区域呈现出微弱的红色荧光 (d2),说明在光照时rGO/Fe3O4@mSiO2优异的光热效应引起局部温度上升导致部分细胞坏死或凋亡。在rGO/Fe3O4@mSiO2-5-FU纳米复合物存在下培养,可以看出细胞在无光照情况下出现较弱的红色(c2),是其负载的5-FU发挥了化疗效果,而在光照条件下,出现了十分明显的亮红色荧光(e2)并拟合出紫红色荧光(e3),表明HeLa细胞大面积死亡,说明rGO/Fe3O4@mSiO2的光热和5-FU的化疗作用产生的协同效应可大幅度提升杀死癌细胞的效果。

图 7 培养基 (a)、rGO/Fe3O4@mSiO2(b,d)和 rGO/Fe3O4@mSiO2-5-FU(c,e)与HeLa细胞共孵育在无光照 (a~c)和有光照 (d,e)条件下的荧光显微镜图Fig.7 Fluorescence microscopy images of HeLa cells incubated with nothing(a),rGO/Fe3O4@mSiO2(b,d)and rGO/Fe3O4@mSiO2-5-FU(c,e)without(a~c)and with irradiation(d,e)
3 结 论
通过各层之间静电吸附作用制备了类似三明治结构的rGO/Fe3O4@mSiO2纳米复合材料,考察了其药物负载与释放能力,实验结果表明rGO/Fe3O4@mSiO2能够有效的装载抗癌药物5-FU,载药率可达57.34%,并具有较高的药物释放量;产物中Fe3O4成分的存在,使得rGO/Fe3O4@mSiO2具有优异的磁性,磁饱和强度为32 emu·g-1,可应用于磁靶向药物传输;而且,rGO/Fe3O4@mSiO2复合纳米材料具有优异光热效应,可对肿瘤细胞进行光热治疗。因此,纳米复合物rGO/Fe3O4@mSiO2是将磁靶向的Fe3O4、优异光热性能的rGO和生物相容性良好的mSiO2相结合,使其具备高效的药物装载能力以及化疗、光热疗法协同抗肿瘤作用,将在医药领域具有广阔的应用前景。
[1]Yang Y,Qi Y,Zhu M,et al.Nano Res.,2016,9(9):2531-2543
[2]Wang C,Sun W,Wright G,et al.Adv.Mater.,2016,28(40):8912-8920
[3]Liu B,Li C X,Chen G Y,et al.Adv.Sci.,2017,4:1600540
[4]Cho M J,Cervadoro A,Maricela R R,et al.J.Nanomater.,2017,7(4):72-86
[5]Solbrig C M,Saucier-Sawyer J K,Cody V,et al.Mol.Pharm.,2016,4(1):47-57
[6]Fu C H,Zhou H Q,Tan L F,et al.ACS Nano,2018,12(3):2201-2210
[7]Yu B,Zhou Y,Song M,et al.RSC Adv.,2016,6:2171-2175
[8]Sánchez Á S,García F S,Alonso A M.Carbon,2015,94:152-159
[9]Lin W,Hu Q,Yu J.ChemPlusChem,2016,81:804-810
[10]Deng G Y,Sun J,Yuan H K,et al.Nanoscale,2018,10:2866-2875
[11]Cheng R,Zou R,Ou S,et al.Polym.Chem.,2015,6(13):2401-2406
[12]Chen G Y,Meng C L,Lin K C,et al.Biomaterials,2015,40:12-22
[13]Huang C L,Huang C C,Mai F D,et al.J.Mater.Chem.B,2015,3(4):651-664
[14]Zhang Y,Chena P,Wena F F.J.Electroanal.Chem.,2016,761:14-20
[15]Kalita H,Rajput S,Prashanth Kumar B N,et al.RSC Adv.,2016,6:21285-21292
[16]Tang Z X,Li F F.J.Comput.Theor.Nanosci.,2016,13:772-776
[17]Hummers W S,Offeman R E.J.Am.Chem.Soc.,1958,80(6):1339-1339
[18]Jin Y,Wang J,Ke H,et al.Biomaterials,2013,34(20):4794-4802
[19]Zhu Y,Murali S,Cai W,et al.Adv.Mater.,2010,22(35):3906-3924
[20]Deng H,Li X,Peng Q,et al.Angew.Chem.,2005,117:2842-2845
[21]Zhao J,Huang Y,Song Y,et al.Toxicol.Lett.,2009,185(2):124-131
[22]Ji Q X,Deng J,Xing X M,et al.Carbohyd.Polym.,2010,82(4):1153-1160
[23]Lo C K,Xiao D,Choi M F.J.Mater.Chem.,2007,17:2418-2427
[24]Ma Y,Jia P,Li X,et al.J.Porous Mater.,2012,19(6):1047-1052
[25]Wang Z M,Wang W D,Coombs N,et al.ACS Nano,2010,4(12):7437-7450
[26]SONG Chun-Peng(宋春芃).Thesis for the Master of Shanghai Jiao Tong University(上海交通大学硕士论文).2012.
[27]CHEN Ya-Lin(陈亚玲),SONG Li(宋力),GUO Hu(郭 虎),et al.Chinese J.Inorg.Chem.(无机化学学报),2016,32(4):633-640
[28]ZHANG Bao-Long(张保龙).Thesis for the Master of Qingdao University of Science and Technology(青岛科技大学硕士论文).2017.

