CYP2C19*2基因多态性影响氯吡格雷药效的Meta分析
陈 娟,唐 瑞,石 萍,陈相潘,蒋学华
(1.重庆市人民医院,重庆市心血管外科学临床医学研究中心,重庆 400013;2.四川大学华西药学院,成都 610041)
氯吡格雷为无活性的前体药物,在人体内只有15%被活化为具有活性的代谢产物,发挥抗血小板药理作用[1]。不同患者对氯吡格雷的反应不同,有些患者在应用氯吡格雷时不能达到抑制血小板的良好效果,仍有急性及亚急性支架内血栓形成等主要心血管事件发生。据报道,基因多态性尤其是CYP2C19*2位点的缺失是造成氯吡格雷抵抗的重要原因[2]。
系统评价报道了CYP2C19*2基因携带者发生主要心血管事件和支架内血栓的风险显著高于非携带者[3];CYP2C19*2基因携带者发生抵抗的风险高于非携带者[4]。本研究系统评价氯吡格雷有效性和安全性指标,为临床氯吡格雷的合理使用提供参考。
1 资料与方法
1.1检索方法 计算机检索Medline、Embase、The Cochrane Library、CNKI、维普和万方数据库,检索时间均从建库至2017年6月。英文检索词为:Clopidogrel,P2Y12,Cytochrome P-450 Enzyme System,Genotype,Polymorphism,metabolizer phenotype,cardiov*和vascular;中文检索词为:氯吡格雷、波立维、基因多态性、代谢酶、CYP和细胞色素*。
1.2文献纳入与排除标准 纳入标准:(1)研究类型为队列研究。(2)研究对象为18岁以上的冠心病或急性冠脉综合征患者。(3)按照患者CYP2C19 基因型检测结果,将受试人群分为CYP2C19*2基因携带者(基因型:CYP2C19*1/CYP2C19*2、CYP2C19*2/CYP2C19*2)和CYP2C19*2基因非携带者(基因型:CYP2C19*1/CYP2C19*1)。(4)主要结局指标为主要心血管不良事件(MACE)和支架内血栓,前者包含了死亡、心肌梗死、血运重建、缺血性脑卒中和心绞痛。次要结局指标为氯吡格雷抵抗和血小板凝集率。安全性指标为出血事件。排除标准:会议摘要、综述、中英文以外其他语言、重复研究及资料不完整的文献。
1.3文献筛选、数据提取与质量评价 由2名研究者按照预先制定的标准独立筛选文献,按照预先设计的资料提取表独立提取资料,交叉复核结果。若结果不同,通过讨论达成共识。采用纽卡斯尔-渥太华量表(the Newcastle-Ottawa Scale,NOS)标准来评价纳入研究的方法学质量,≥5分的研究均可被纳入Meta分析。
1.4统计方法 采用Stata 12.0软件进行Meta分析。以相对危险度(relative risk,RR)或加权均数差(weighted mean difference,WMD)为结局指标合并统计量,结果以95%CI表示。统计学同质性的研究(P≥0.1)采用固定效应模型进行数据合并分析,反之采用随机效应模型。对存在临床异质性和方法学异质性的研究进行亚组分析。对纳入研究进行敏感性分析,若排除某个研究后结果差别较大甚至截然相反结论,说明敏感性较高,提示存在偏倚因素;反之则敏感性较低,研究结果较稳健。
2 结果
2.1检索结果 检索获得文献5 371篇,剔除重复文献331篇,阅读题目、摘要和全文,最终纳入44篇文献[5-48],受试者22 935例,各纳入研究的基本情况见表1。
2.2纳入文献质量 根据NOS量表评价标准,进行队列研究的方法学质量评价,42个研究均符合纳入排除标准,NOS得分均≥5分,结果见表1。
表1纳入Meta分析文献的基本特征
Tab.1 Main characteristics of all the studies included in the Meta-analysis

纳入研究例数/人国家男性/例(%)平均年龄/岁BMI±SD/kg·m-2疾病负担氯吡格雷[LD→MD]NOSAnutebeh Verdo Z等[5],20121 738中国1 164(67.0)70.8±9.525.8±4.2CHD+PCI300→758Tang X F等[6],2013577中国444(76.9)59.0±11.432.2±9.9ACS+PCI300→758赵清等[7],2012136中国151(55.7)59.7±8.0NRCHD6008孙硕等[8],2014478中国399(83.5)63.31±11.26NRACS+PCI759何咏聪等[9],2015146中国96(65.8)68.9±11.323.5±3.0CHD757唐晓芳等[10],2011267中国215(80.5)58.0±10.526.1±4.5CHD+PCI300→758李韶南等[11],2013462中国262(56.7)59.5±6.025.4±3.1ACS600→758李海蓬[12],2013120中国80(66.7)61.88±8.1526.48±4.53CHD+PCI300→759吴鸿谊[13],2012447中国358(80.1)63.0±10.024.8±1.6ACS300→759王辰[14],2014107中国65(60.7)67.0±10.424.4±3.5ACS+PCI300→759吴红霞[15],2011259中国202(78.0)64.4±10.7424.7±2.8CHD+PCI300→759Tousoulis D等[16],2013353希腊319(90.4)61.0±8.0NRCHD+PCI758Zhang L等[17],2013500中国329(65.8)63.9±11.725.3±3.3ACS300→758Kang Y H等[18],2013538中国449(83.5)63.35±12.0NRCHD+PCI300→758Al-Azzam S等[19],2012240约旦168(70.0)59.8±10.828.4±5.2CHD757Peng Y等[20],2013506中国417(82.4)64.9±10.5NRCHD300→759Marcucci R等[21],20121 187意大利888(74.8)69.0±32.5NRACS+PCI600→757Teixeira R等[22],201295葡萄牙79(83.5)62.0±8.5NRACS758Bonello L等[23],2012498法国406(81.0)62.0±12.027.2±4.5ACS+PCI6008Tello Montoliu A等[24],201140西班牙36(90.0)65.8±10.0NRCHD+PCI759Oh I Y等[25],20122 146韩国1 410(65.7)60.8±9.824.8±3.0CHD600/300→757Chen M等[26],2011654中国533(81.5)65.17±10.63NRACS300→757Cuisset T等[27],2011346法国281(81.2)64.0±12.027.1±4.3ACS600→75/1507Sawada T等 [28],2011100法国85(85.0)69.6±9.223.7±6.1CHD+PCI300→758Pettersen A R等[29],2011219挪威173(79.0)62.0±8.562.0±8.5CHD757Bouman H J等 [30],20111 982荷兰1 513(71.3)62.2±10.227.1±4.3CHD+PCI600→759Bonello L等[31],2010411法国321(78.1)62.9±12.227.2±4.5ACS6008Frere C等[32],2008603法国456(75.7)64.7±12.226.8±4.3ACS6008Wei Y Q等[33],2015110意大利71(64.5)65.7±11.723.2±2.9ACS300→758Sun B等[34],2014118中国22(18.6)56.2±12.125.8±3.6CHD+PCI300→759Chen Y等[35],2015336中国223(66.4)66.5±10.525.3±3.3ACS300→757Collet J P等[36],2009259法国239(92.3)40.1±5.125.7±3.8CHD757Bonello Palot N等[37],200973德国59(80.8)62.8±12.427.1±4.1CHD+PCI6007Sibbing D等[38],20092 485德国1 946(78.0)66.5±10.227.2±3.9CHD+PCI6007Giusti B等[39],2009772意大利576(74.6)NRNRCHD600→757Li S等[40],2015198中国164(82.8)57.7±9.024.8±4.1CHD758Li X等[41],2013180中国67(37.22)62.5±11.425.9±3.0CHD759Sibbing D等[42],20111 524德国1 180(77.4)67.4±10.626.9CHD+PCI6008Campo G等[43],2011300意大利231(77.0)66.0±13.027.0±4.0CHD+PCI300→758Bouman H J等[44],20111 024荷兰770(75.2)64.2±10.827.0±4.0CHD+PCI80→1006Hulot J S等[45],2011371法国314(84.6)40.3±5.525.9±4.0CHD300→757Gajos G等[46],201230波兰24(80.0)63.8±9.429.3±3.8CHD+PCI759Wu H等[47-48],2012233中国181(77.7)62.0±10.024.8±1.6ACS+PCI300→758Jeong Y H等[49],2011266韩国195(73.3)63.0±11.924.2±3.1CHD600→757
注:LD:负荷剂量(mg);MD:维持剂量(mg·kg-1);NR:未报告;CHD:冠状动脉粥样硬化性心脏病(冠心病);ACS:急性冠脉综合征;PCI:经皮冠状动脉介入治疗。
2.3Meta分析结果
2.3.1CYP2C19*2基因多态性与MACE发生风险的关系 22个队列研究[5-6,8-11,16,20-22,25-26,28,33,35-36,38-40,43,45,47-49]报道了13 708例CYP2C19*2基因携带者与非携带者的MACE发生率。纳入的22篇文献存在异质性(P=0.002,I2=52.6%)。根据服用氯吡格雷的负荷剂量将研究分为2个亚组,见图1。第1个亚组为低剂量组(氯吡格雷负荷剂量300 mg或无负荷剂量),各研究间差异不具有统计学异质性(P=0.116,I2=31.7%),采用固定效应模型合并效应量;第2个亚组为高剂量组(氯吡格雷负荷剂量为600或900 mg),各研究间不具有统计学异质性(P=0.124,I2=40.1%),采用固定效应模型合并效应量。CYP2C19*2基因携带者与非携带者相比,MACE的发生风险升高[RR=1.64,95%CI(1.48,1.82),P<0.000 1]。
对纳入文献进行敏感性分析,分别剔除每一篇文献后,剩余文献的估计效应值RR和95%CI均未发生明显变化,见图2。由图2可知,分析结果稳健可靠。

图1CYP2C19*2携带者与非携带者主要心血管不良事件发生风险的森林图
Fig.1 Forest plot of risk ratios for major adverse clinical events according to CYP2C19*2 genotype
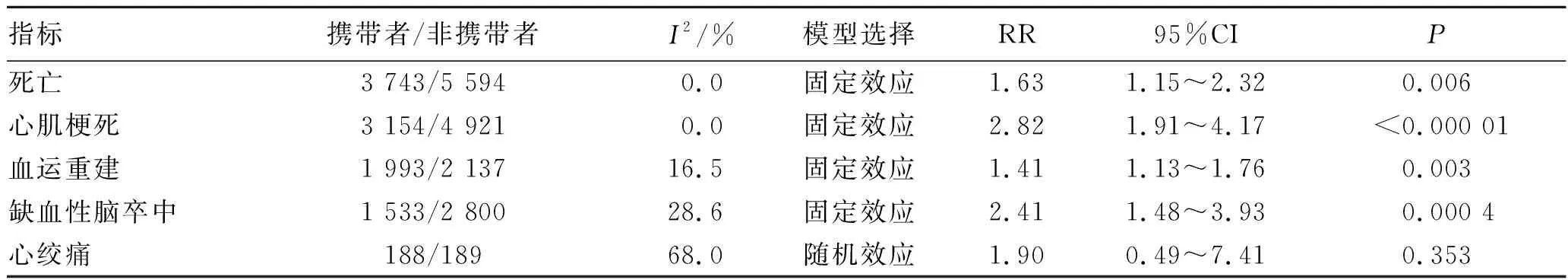
主要心血管事件包括死亡、心肌梗死、血运重建、缺血性脑卒中和心绞痛。见表2。由表2可知,这些指标是各自Meta分析的结果。结果显示,CYP2C19*2基因携带者发生死亡、心肌梗死、血运重建和缺血性脑卒中的风险更高,发生心绞痛的风险差异无统计学意义。
表2CYP2C19*2携带者与非携带者主要心血管不良事件各指标Meta分析结果
Tab.2 Results of Meta-analysis for MACE according to CYP2C19*2 genotype
指标携带者/非携带者I2/%模型选择RR95%CIP死亡3 743/5 5940.0固定效应1.631.15^2.320.006心肌梗死3 154/4 9210.0固定效应2.821.91^4.17<0.000 01血运重建1 993/2 13716.5固定效应1.411.13^1.760.003缺血性脑卒中1 533/2 80028.6固定效应2.411.48^3.930.000 4心绞痛188/18968.0随机效应1.900.49^7.410.353
2.3.2CYP2C19*2基因多态性与支架内血栓发生风险的关系 11篇文献[5,10,25,30,33,36,38-40,42-43]报道了11 781例患者CYP2C19*2基因携带者与非携带者发生支架内血栓的风险。Meta分析结果显示,各研究间不具有异质性(P=0.113,I2=35.7%),采用固定效应模型合并效应量。CYP2C19*2基因携带者与非携带者相比,支架内血栓的发生风险升高 [RR=2.17,95%CI(1.70,2.76),P<0.000 01]。
2.3.3CYP2C19*2基因多态性与氯吡格雷抵抗发生风险的关系 15篇文献[6-7,9,13,19,21,23,25,27,31,33,35,38,44,50]报道了7 127例患者CYP2C19*2基因携带者与非携带者发生氯吡格雷抵抗的风险。Meta分析结果显示,各研究间不具有异质性(P=0.201,I2=22.8%),采用固定效应模型合并效应量。CYP2C19*2基因携带者与非携带者相比,发生抵抗的风险升高 [RR=1.35,95%CI(1.28,1.43),P<0.000 01]。

图2CYP2C19*2携带者与非携带者主要心血管不良事件发生风险的敏感性分析
Fig.2 Sensitivity analysis of risk ritios on major adverse clinical events according to CYP2C19*2 genotype
2.3.4CYP2C19*2基因多态性与凝集率的关系 22篇文献[6-7,12-17,21,23-25,31-32,34-35,37,40-41,44-46,51]报道了患者服用氯吡格雷后的血小板聚集能力,共使用4种方法,5种指标测量血小板凝集率。见表3。由表3可知,这5种指标各自Meta分析的结果显示,CYP2C19*2基因携带者服用氯吡格雷后的血小板聚集能力高于非携带者,即基因携带者服用氯吡格雷后抗血小板能力更弱。
表3CYP2C19*2携带者与非携带者凝集率各指标Meta分析结果
Tab.3 Results of Meta-analysis of the platelet aggregation according to CYP2C19*2 genotype

指标患者/例I2/%模型选择WMD95%CIPMPA(LTA法)1 98422.9固定效应6.304.65^7.94<0.000 01PAR(LTA法)1 5080.0固定效应6.024.49^7.54<0.000 01PAR(TEG法)2 88640.3固定效应7.256.33^8.17<0.000 01PRI(VASP法)1 7600.0固定效应9.095.48^12.70<0.000 01PRU(VerifyNow P2Y12法)3 29041.0固定效应23.0617.89^28.23<0.000 01
注:LTA:光比浊法;TEG:血栓弹力图法;VASP:血管扩张刺激磷蛋白法;PRI:血小板反应指数;MPA:最大血小板聚集率;PAR:血小板聚集率;PRU:P2Y12 反应单位。
2.3.5CYP2C19*2基因多态性与出血事件发生风险的关系 3篇文献[5,16,18]报道了2 544例患者CYP2C19*2基因携带者与非携带者发生出血事件的风险。Meta分析结果显示,各研究间有异质性(P=0.02,I2=74%),采用随机效应模型合并效应量。CYP2C19*2基因携带者与非携带者出血事件发生率差异无统计学意义[RR=0.79,95%CI(0.44,1.39),P=0.412],即CYP2C19*2基因对氯吡格雷的安全性影响无统计学意义。
3 讨论
研究表明,有7篇文献[52-58]通过系统评价的方法,将CYP2C19*1、CYP2C19*2、CYP2C19*3、CYP2C19*4、CYP2C19*5、CYP2C19*6、CYP2C19*7、CYP2C19*8和CYP2C19*17位点分为野生型(CYP2C19*1位点)、功能性缺失型(CYP2C19*2~CYP2C19*8位点)和功能增强型(CYP2C19*17位点)3种情况进行Meta分析,结果携带功能缺失型基因的患者比携带野生型基因的患者主要心血管不良事件发生率高,携带功能增强型基因的患者比携带野生型基因的患者主要心血管不良事件发生率低。CYP2C19基因位点的突变频率是有差异的,最常见的功能缺失基因是CYP2C19*2,在高加索和非洲人种中的基因频率为15%,在亚洲人种中的基因频率为29%~35%。以上7项研究将所有频率基因笼统地分成野生型、功能性缺失型和功能增强型3类,未考虑不同突变位点频率的不同,对氯吡格雷药效影响的程度也不同。且实际临床测定患者突变基因时,考虑到成本和操作的因素,会对突变频率较高的基因进行检测。因此,进行突变频率较高的CYP2C19*2基因位点对氯吡格雷疗效影响的Meta分析,对临床实际操作和应用更有参考意义。
有3篇研究[3-4,59]进行了CYP2C19*2基因影响氯吡格雷给药后主要心血管不良事件和支架内血栓发生率的系统评价,但均未将氯吡格雷给药后的凝集率变化、发生氯吡格雷抵抗的比例作为结局指标纳入。血小板聚集是从血栓形成到粥样斑块破裂疾病进展过程中的关键因素[60],血小板功能检测结果(包括血小板聚集能力和发生氯吡格雷抵抗)也是评价氯批格雷的抗血小板疗效的指标,多数临床研究将此检测结果作为评价抗血小板药物疗效的替代终点,能更直观的反映患者的实际情况。因此,本研究分别评价了CYP2C19*2基因多态性对氯吡格雷给药后患者的凝集率、抵抗、主要心血管不良事件、支架内血栓、出血事件变化的影响。
本研究将临床上常用的主要心血管事件作为主要的结局指标,但不同研究者对主要心血管事件的定义不同,可能增大研究的异质性。不同文献对氯吡格雷抵抗的定义也有差异,增大了研究的异质性。对于次要结局指标血小板凝集能力,没有公认的测量凝集率的标准方法,现有文献一般采用比浊法、血栓弹力图法、血管扩张刺激磷蛋白法和VerifyNow P2Y12法,不同的测量方法原理不同,表示结果的指标也代表不同的意义。因此本研究分别讨论4种方法的Meta分析结果,这就造成凝集能力指标的Meta分析结果很零散、纳入的研究数量少,结果的可靠性较低。
影响氯吡格雷药效的因素除了基因多态性,还有年龄、糖尿病、高血脂、吸烟及质子泵抑制剂的使用等。本研究尽量控制这些混杂因素,只考虑了发生频率较高的功能缺失型基因CYP2C19*2基因,得到CYP2C19*2基因携带者临床有效性低于非携带者,安全性差异无统计学意义的结论。对于患有冠心病或急性冠脉综合征的CYP2C19*2基因携带者,按照常规剂量服用氯吡格雷不能达到预期的疗效。FDA提出了2种替代药物普拉格雷和替格瑞洛,但这2种药物会增加出血的风险。也有研究报道了提高CYP2C19*2基因携带者服用氯吡格雷的剂量[61],但具体增大多少剂量没有明确结论,有待于后续深入研究。

