Cu–Co–Al类水滑石的制备及其电催化还原硝酸盐研究
李 亮,貟亚锋,罗梦玉,彭婧婧,胡守波
(上海理工大学 环境与建筑学院,上海 200093)
层状复合金属氢氧化物(layered double hydroxides,LDHs)是水滑石或类水滑石化合物的统称,其结构特点是层间阴离子可与各种阴离子,包括无机离子、有机离子、同种离子、杂多酸离子以及配位化合物的阴离子进行交换。LDHs的一般化学组成可以表示为,其中M2+为二价金属阳离子(Mg2+、Co2+、Cu2+、Ni2+、Mn2+等),M3+为三价金属阳离子(Al3+、Fe3+、Co3+等),为层间可交换阴离子层间无机阴离子不同,LDHs的层间距也会有所差异。一般而言,M3+/(M2++M3+)摩尔比介于2~4之间时能得到结构完整的LDHs。通过改变M2+与M3+的比例,可在保持水滑石的特有结构基础上制备出不同类型的二元、三元类水滑石物质[2]。
类水滑石具有酸性、碱性、层间阴离子的可交换性、热稳定性等特点[3]。根据其结构特点,水滑石被广泛应用于电化学[4-5]、催化[6]、吸附[7]、医药[8]、水处理[9-10]等领域。研究者将具有催化活性的二价(Zn2+、Ni2+、Mn2+、Cu2+等)或者三价(Co3+、Fe3+、Cr3+等)金属离子替换至LDHs层板中,使其具有良好的催化性能[11]。例如铜铁具有协同催化作用,铜铁水滑石广泛应用于糠醛合成[12]、安息香异丙醚合成[13]、高氯酸盐分解[14]等领域。镁铝水滑石是高效、无毒、高性价比的环保型阻燃剂。水滑石与其他材料混用,可改善高分子材料的耐热性能、机械强度、绝缘性能、抗静电性能、抗老化温度等。
随着地表水和地下水氮污染的加重,硝酸盐作为主要含氮污染物,其快速检测与去除引起了研究者的广泛关注。目前硝酸盐的去除方法主要有化学法、电化学法、物化法、离子交换、电渗析、催化还原等。在电化学方面,有研究[15-16]表明铜电极在碱性环境下电催化还原硝酸盐具有良好的效果,并且硝酸盐的还原产物取决于外加电位。徐盼[17]的研究表明,镁铝铁三元类水滑石化合物在pH = 8左右吸附硝酸根离子的效果最好[17]。在类水滑石化合物的研究方面,王颖等[18]指出,采用水滑石作为载体的催化剂在电催化还原方面具有更高的活性,同时具有较高的选择性。鉴于其结构中阳离子的可取代性,可利用多种金属离子制备不同类型的水滑石化合物。类水滑石化合物的吸附与催化性能则往往与层间阴离子的交换性有关。其由于在催化反应中可重复利用、容易交换和分离、污染环境较小,是一种环境友好的催化剂[19]。
目前对铜钴铝类水滑石电催化还原硝酸的研究尚未见报道,而电催化法反应装置比较简单,去除硝酸盐自动化程度高,此外,电催化法还具有安全性、选择性高,无需添加其他化学药品等特点。本文通过双滴定法制备不同摩尔比的类水滑石化合物,通过X射线衍射、场发射扫描电镜对类水滑石物质结构进行表征,并利用线性伏安扫描法研究其作为阴极材料电催化还原硝酸盐的效果。
1 试验材料与方法
1.1 水滑石与涂膜电极的制备
本文利用共沉淀法制备水滑石。首先配置Co(NO3)2、Cu(NO3)2、Al(NO3)3混合溶液A和无水Na2CO3、NaOH混合溶液B;然后将溶液A和B同时滴加到一定量的去离子水中,恒温40 ℃搅拌并保持溶液pH在9~10之间;滴加完毕后继续搅拌半小时,65 ℃陈化24 h,抽滤并洗涤至中性,80 ℃干燥12 h,过100目筛即制成Cu−Co−Al三元水滑石材料。
按照质量比 10:1:2分别称取 Cu−Co−Al三元水滑石材料、乙炔黑以及聚偏氟乙烯(polyvinylidene fluoride,PVDF),将其置于玛瑙研钵中进行研磨至完全混合均匀,然后加入N−甲基吡咯烷酮(N-methylpyrrolidone,NMP)并搅拌4 h形成浆液。取厚度为0.1 mm的铜片,用无水乙醇清洗后,再使用3 000目砂纸打磨并再次清洁。将浆液均匀倒在经预处理的铜片上,并使用涂膜器进行涂膜,膜厚度为150 μm,将其在102 ℃真空条件下干燥10 h即可得到涂膜电极。
1.2 水滑石物化表征
本文分别采用德国 Bruke D8 Advance X 射线衍射仪和Sigma500型高分辨率场发射扫描电镜研究类水滑石材料的晶体结构和形貌特征。X射线衍射(XRD)测试条件为:铜靶Kα射线,波长 1.54187 Å(Å = 10−10m),电压 40 kV,电流40 mA,扫描范围为 5°~80°。
1.3 电催化性能研究
本文采用CHI电化学工作站(上海辰华,型号660E)研究硝酸盐在电极上的还原过程。以玻璃电解杯作为反应器,将制备好的涂膜电极剪切成边长为1 cm的正方形电极片,使用铂电极夹将其固定。由于电极夹与电极接触面积为0.5 cm2,故电极暴露于溶液中的实际几何面积为0.5 cm2。工作电极即为上述面积为0.5 cm2的涂膜电极,对电极为铂丝电极,参比电极为氧化汞电极,电解溶液体积为8 mL。
2 结果与讨论
2.1 材料表征
图 1为不同摩尔比的 Cu−Co−Al类水滑石XRD谱图,其中2θ为衍射角。在水滑石结构中当A2+仅为Cu2+时,合成过程发生姜−泰勒效应[20],不容易形成稳定的二元类水滑石化合物。本文通过在水滑石层板引入Co2+后,可以稳定层板结构,形成结构良好的水滑石化合物。从图 1 中可以看出,当 2θ 分别在 12°、23°、34°、38°、46°、60°附近时出现了水滑石特征衍射峰(003)、(006)、(009)、(015)、(018)、(110)的晶面,与文献[21]一致。这说明材料制备成功,得到了水滑石具有的特殊层状结构。样品 a、b、c、d 的 n(Cu2+):n(Co2+):n(Al3+)分别为1:1:2、1:1:1、1:2:1、2:1:1。样品a、d的衍射峰更为尖锐且对称性好,说明这两种配比下得到的类水滑石晶体更为完整。根据布拉格方程计算得到样品 a、b、c、d 在 2θ = 12°附近的层间距分别为 0.749 8、0.752 8、0.769 8 和 0.758 3 nm,均略小于标准的Mg−Al水滑石的层间距(0.783 7 nm)。这可能与Cu2+、Co2+半径较大有关。
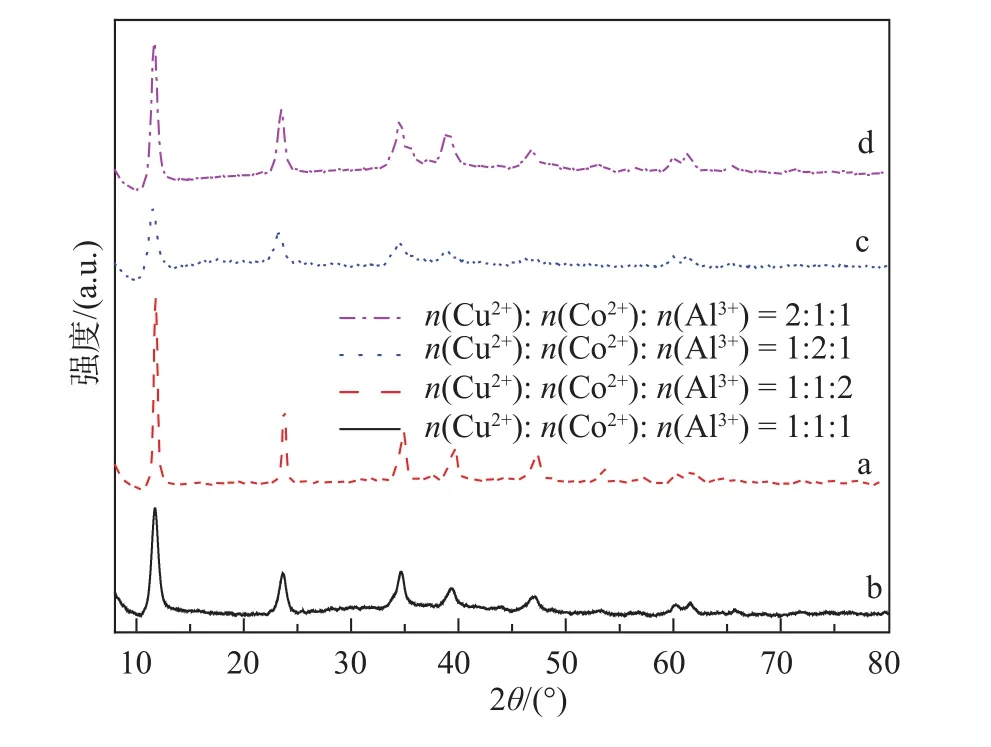
图1 Cu–Co–Al类水滑石的 XRD 谱图Fig.1 XRD patterns of Cu-Co-Al hydrotalcite-like compounds
图2为不同摩尔比的Cu−Co−Al类水滑石场发射扫描电镜(FE−SEM)图。由图中可知,四种样品均出现了明显的层状结构,属于典型的水滑石类物质,这与XRD测定结果一致。且材料尺寸多数在100 nm左右,片层厚度小于10 nm,相当于几层水滑石纳米层板的叠加纳米结构,取向比较混乱,这可能与制备方法有关。由图2(a)、(b)、(d)中可知,随着铜含量的增加层状结构更加清晰,层片面积增大,层片间的间距增加,这有利于将硝酸盐吸附到其表面,促进硝酸盐的还原。从图2(c)中可知,当钴含量增加时,片状大量聚集[22],片层之间的间距减小,同时片状面积减小,引起水滑石结构的变形,因此可能会对后续的硝酸盐吸附与电催化还原造成一定的影响。对比图2(a)~(d)四种水滑石样品可以发现,图2(d)的结构最为清晰完整,此时n(Cu2+): n(Co2+):n(Al3+)为 2:1:1。

图2 Cu–Co–Al类水滑石的 FE–SEM 图Fig.2 FE-SEM images of Cu-Co-Al hydrotalcite-like compounds
2.2 线性伏安扫描实验
图3为不同摩尔比Cu−Co−Al类水滑石涂膜电极在 1 M NaOH,1 M NaOH + 0.1 M NaNO2与 1 M NaOH + 0.1 M NaNO3溶液中的线性伏安扫描(LSV)图,其中E表示扫描电位,参比电极为汞氧化汞电极,扫速大小为20 mV·s−1。从图3中可以看出,在1 M NaOH溶液中四种涂膜电极在电位为− 0.9 V之前,电流没有发生明显变化,之后电流开始陡降,这是由于发生了析氢反应[16]。当加入 0.1 M NaNO2溶液后,四种电极从− 0.5 V左右电流发生明显变化,与 1 M NaOH溶液扫描结果有非常明显的差异。从图(a)、(b)、(c)、(d)中可以看出,它们分别在− 0.81、− 0.92、− 0.93、− 0.76 V 处出现了还原峰,可能是亚硝酸盐还原成其他物质。样品(d)峰电位绝对值最低,电催化还原亚硝酸盐活性最高,此时 n(Cu2+):n(Co2+):n(Al3+)为 2:1:1。再者 , 对 比 四 种 电 极 在 1 M NaOH + 0.1 M NaNO2溶液中的线性伏安扫描图可以发现,在0.1 M NaNO3溶液中,析氢反应电位前有两个明显的还原峰,与1 M NaOH溶液扫描结果相比,析氢电位均向负向移动,减少了对电化学还原硝酸盐的竞争。首先,在− 0.57~− 0.53 V 处发生的可能是硝酸盐还原为亚硝酸盐。其次,在− 0.92~− 0.75 V 可能是亚硝酸盐还原为氨氮[23],化学反应方程式为
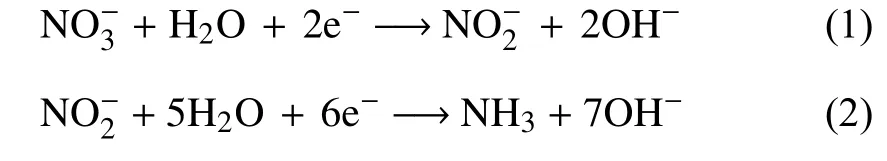
并且,硝酸盐还原的峰电流比亚硝酸盐还原的峰电流大,由此可见,作为硝酸盐还原产物的亚硝酸盐比本体溶液中亚硝酸盐在电极表面吸附量更大,更容易被还原。
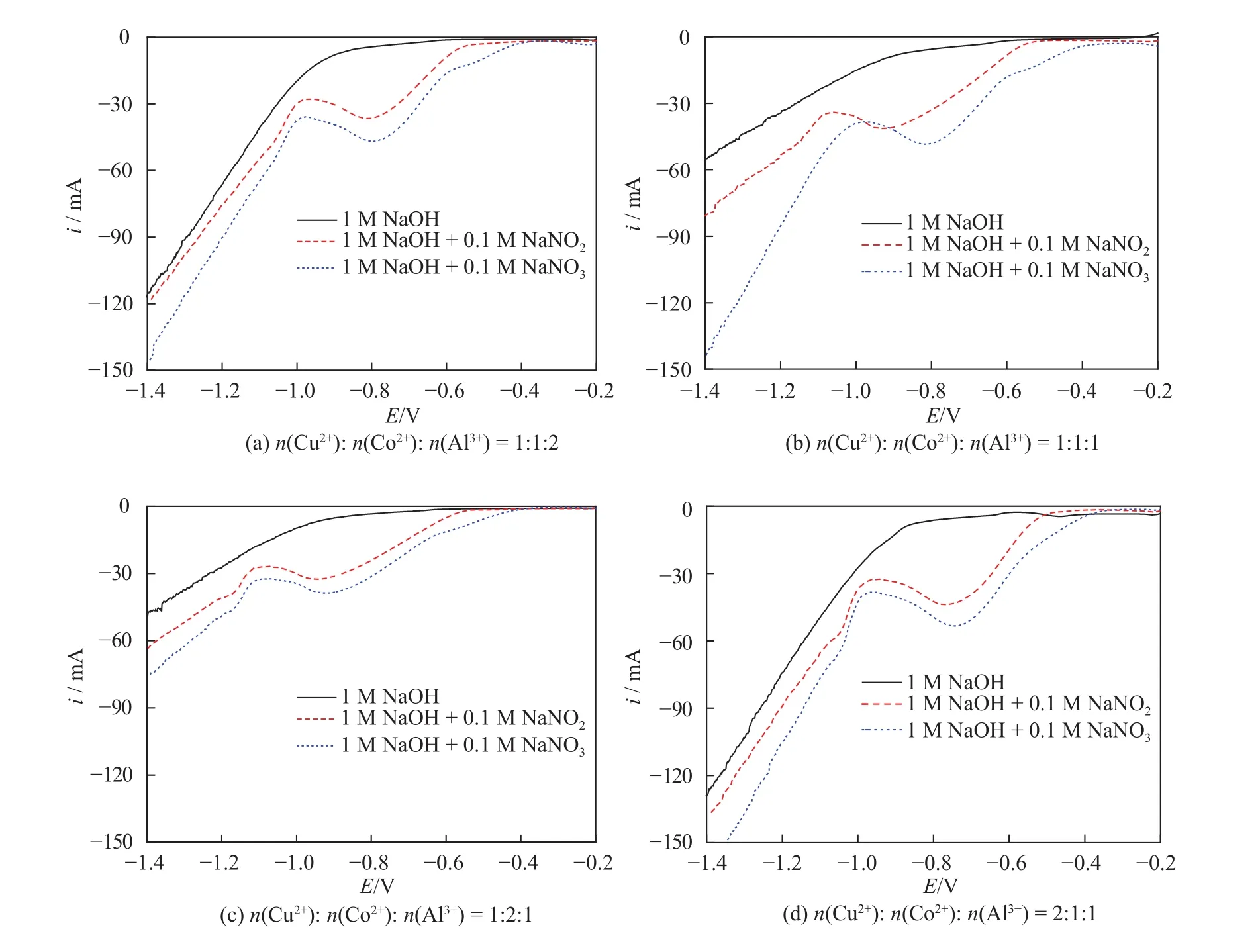
图3 不同摩尔比 Cu–Co–Al类水滑石涂膜电极的 LSV 图Fig.3 LSV diagram of the electrode coated by Cu-Co-Al hydrotalcite-like compounds with different molar ratios of n(Cu2+): n(Co2+): n(Al3+)
Reyter等[24]研究指出,纯铜电极电催化还原硝酸盐的析氢电位在− 1.4 V左右,而本研究的电极材料由于其析氢反应电位相对靠前,因此容易发生反应,从而降低析氢反应的能耗。此外,铜电极表面硝酸盐在− 1.1、− 1.3 V 还原产物分别为亚硝酸盐和氨氮,峰电流分别为6、4 mA·cm2。本研究制备的层状复合金属氢氧电极材料可在− 0.57~− 0.53 V 将硝酸盐还原为亚硝酸盐,还原峰电流在20~37 mA·cm−2;亚硝酸盐还原过程则在− 0.92~− 0.75 V 达到峰值,峰电流在 77~107 mA·cm−2,均远远大于纯铜电极。较小的还原电位和较大的还原电流表明层状复合金属氢氧电极对亚硝酸盐和硝酸盐均有较高的催化活性。对比四种摩尔比的电极材料可以发现,当 n(Cu2+):n(Co2+):n(Al3+)= 1:1:1 时,析氢反应的电位向负向移动,完成硝酸盐的电催化还原过程所需的能耗较大,其余三个析氢反应比较接近在− 1.0 V 左右。而摩尔比 n(Cu2+):n(Co2+):n(Al3+)= 2:1:1时,电催化还原硝酸盐的两个峰电流比其他三个摩尔比时的涂膜电极都大,并且还原峰的位置靠前,所需能耗较小,所以当摩尔比 n(Cu2+):n(Co2+):n(Al3+)= 2:1:1 时,电催化还原硝酸盐的效果最好。
图 4为摩尔比 n(Cu2+):n(Co2+):n(Al3+)=2:1:1类水滑石涂膜电极在不同硝酸盐浓度下的线性伏安扫描图。由图中可以发现,四种浓度下均可以观察到硝酸盐的两个还原峰。随着硝酸盐浓度增加,第一个还原峰电位从− 0.50 V逐渐移动到− 0.55 V 左右,峰电流从 12 mA·cm−2增加到43 mA·cm−2,峰电流与浓度呈正相关,线性相关系数R2为0.997 6;第二个还原峰电位从−0.72 V 逐渐移动到− 0.92 V 左右,峰电流从30 mA·cm−2增加到 144 mA·cm−2,峰电流与浓度呈正相关,线性相关系数R2为0.995 4。总体而言,随着硝酸钠浓度的增加,还原峰电流增加,并且呈现明显的分离,还原峰电位逐渐负移,表明这是一个不可逆反应。
图 5 为 n(Cu2+):n(Co2+):n(Al3+)= 2:1:1 类水滑石涂膜电极在 1 M NaOH + 0.1 M NaNO3时不同扫描速率的LSV图,其中扫描速率依次为10、20、40、60、80、100 mV·s−1,C1和 C2为两个还原峰的位置。随着扫描速率的增加,第一个还原峰 C1电位从− 0.47 V 逐渐移动到− 0.54 V左右,峰电流从18 mA·cm−2增加到56 mA·cm−2,峰电流与浓度呈正相关,线性相关系数R2为0.995 2;第二个还原峰 C2电压从− 0.69 V 逐渐移动到− 0.90 V 左右,峰电流从 70 mA·cm−2增加到 206 mA·cm−2,峰电流与浓度呈正相关,线性相关系数R2为0.990 6。由图5中可知,随着扫描速率的增加,峰电流的绝对值增加,且还原峰电流出现了左移。结合图4可以推测该反应为完全不可逆过程或准可逆过程。电极上的反应过程受扩散控制,而线性关系图不过原点,说明硝酸盐在电极表面有预吸附现象。
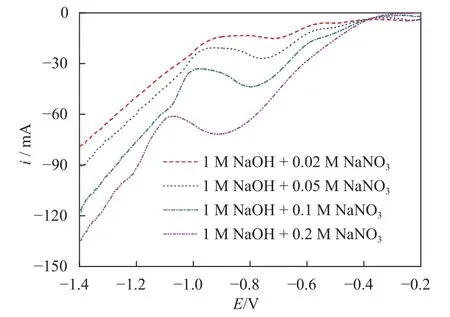
图4 n(Cu2+):n(Co2+):n(Al3+) = 2:1:1 类水滑石涂膜电极在不同硝酸盐浓度下的LSV图Fig.4 LSV diagram of the electrode coated by Cu-Co-Al hydrotalcite-like compounds at n(Cu2+):n(Co2+):n(Al3+)=2:1:1 with different nitrate concentrations

图5 n(Cu2+):n(Co2+):n(Al3+)= 2:1:1 类水滑石涂膜电极在 1 M NaOH + 0.1 M NaNO3 时不同扫描速率的LSV图 Fig.5 LSV diagram of the electrode coated by Cu-Co-Al hydrotalcite-like compounds at n(Cu2+):n(Co2+):n(Al3+) = 2:1:1 with different scan rates and in 1 M NaOH + 0.1 M NaNO3
3 结论与展望
通过共沉淀法制备不同摩尔比的Cu−Co−Al类水滑石材料,并通过表征研究材料的结构及镜貌。将所制备的材料制成涂膜电极,探究其电催化还原硝酸盐的效果,主要结论为:
(1)所制备的不同组分的 Cu−Co−Al类水滑石晶相良好,均有水滑石的特征峰晶面。在n(Cu2+):n(Co2+):n(Al3+)= 1:1:2 时特征峰尖锐,对称性较好,层状结构最稳定。场发射扫描电镜研究结果表明,不同摩尔比的Cu−Co−Al类水滑石均出现了层片状结构,且随着铜含量的增加层状结构更加清晰,层片面积增大,层片间的间距增加,有利于将硝酸盐吸附到其表面。
(2)n(Cu2+):n(Co2+):n(Al3+)= 2:1:1时,Cu−Co−Al类水滑石涂膜电极电催化还原硝酸盐的效果最好。硝酸盐的电催化还原峰电流与浓度及扫描速率呈正相关;此外,电极电位也直接影响硝酸盐还原速率与产物,电位越负,越容易生成氨氮。
(3)Cu−Co−Al类水滑石作为一种优良的电极材料,可有效吸附及电催化还原硝酸盐,可用于水体中硝酸盐的快速检测,也可用于无碳源条件下的硝酸盐电化学去除工艺过程中。

