新型PEG化GLP-1受体激动剂的合成及其降血糖活性
刘 颜,李承业,蔡星光,孙李丹,黄文龙
(1重庆医科大学药学院,重庆 400016;2中国药科大学新药研究中心,南京 210009;3嘉兴学院,嘉兴 314000)
糖尿病是一种由胰岛素分泌缺陷和/或胰岛素功能障碍所导致的慢性代谢性疾病,主要表现为高血糖[1-2]。长期代谢紊乱可导致肾、眼、神经系统及心血管等各个组织器官出现功能障碍和衰竭[3-4]。国际糖尿病联盟报告表明,糖尿病已成为危害人类健康的严重疾病之一[5]。
胰高血糖素样肽-1(glucagon-like peptide-1,GLP-1)是一种内源性肠促胰岛素激素[6],在体内发挥促进胰岛素释放、抑制胰高血糖素释放、抑制食欲和延缓胃排空等功能,还有减轻体重的效果[7]。而且其促胰岛素释放作用和抑制胰高血糖素释放作用具有血糖依赖性,因此,其低血糖风险大大降低[8-9]。但是,内源性GLP-1在血浆中会被二肽基肽酶4(dipeptidyl peptidase-4,DPP-4)等酶代谢失活,并且会被肾小球快速滤过清除,其体内半衰期只有2~3 min[10]。近年,研究人员对GLP-1的性质进行研究并开发了长效化GLP-1受体激动剂。已上市或进入临床研究的长效化GLP-1受体激动剂有艾塞那肽(Ex-4)、利西拉来(Lixisenatide)、利拉鲁肽(Liraglutide)、索玛鲁肽等(Semaglutide)。GLP-1受体激动剂同时具有稳定血糖、减轻体重的效果,成为糖尿病研究的热点[11]。
聚乙二醇(polyethylene glycol,PEG)是最常用的一种修饰剂,其毒性小、无抗原性、具有良好的两亲性和生物相容性,目前已获FDA认可。PEG化具有以下优点:增加溶解度、降低或消除免疫原性、减小水解酶降解的可能性、降低肾脏清除速率、改变药物体内分布和动力学参数、提高稳定性等。早期研究一般将相对分子质量较大的PEG缀合至多肽链来实现长效化[12-14],但相对分子质量过大会阻碍多肽与受体的相互作用,引起生物活性的直线下降[15]。因此,选择合适相对分子质量的PEG具有十分重要的意义。目前,修饰GLP-1多肽的PEG的相对分子质量均在2 000以上,低于1 000的PEG缀合鲜有报道。因此,本研究选用平均相对分子质量分别为350、550和750的单甲氧基聚乙二醇(mPEG),进行长效化GLP-1受体激动剂的设计与合成。
在前期工作中,本课题组设计并合成了一系列半胱氨酸替换的GLP-1类似物并对其进行小鼠体内降糖活性筛选,结果表明,Cys17-Gly8-GLP-1(7-36)-NH2、Cys26-Gly8-GLP-1(7-36)-NH2、Cys34-Gly8-GLP-1(7-36)-NH2和Cys37-Gly8-GLP-1(7-37)-NH2这4个GLP-1类似物的活性较好[16]。因此将这4条肽链作为化学修饰的母肽链,通过马来酰亚胺连接臂与不同相对分子质量的mPEG进行交联,设计并合成了12个衍生物,结构如图1所示。

Figure1 Structures of PEGylation GLP-1 receptor agonistsI-1-I-12
1 合成路线设计
1.1 多肽合成路线设计
采用Rink树脂作为固相载体,合成C末端为酰胺键的肽链,合成路线见路线1。其余衍生物的合成路线与其类似并采用相应的氨基酸进行耦合反应。
1.2 PEG缀合连接臂和缀合多肽的合成路线设计
3个不同长度的单甲基化PEG通过Gabriel合成法将一端的羟基变成氨基,接着与马来酰亚胺反应得到相应的马来酰亚胺PEG小分子,再与半胱氨酸改构的GLP-1类似物缀合得到目标产物。小分子合成路线如路线2所示,短链PEG-多肽缀合物的合成路线如路线3所示。
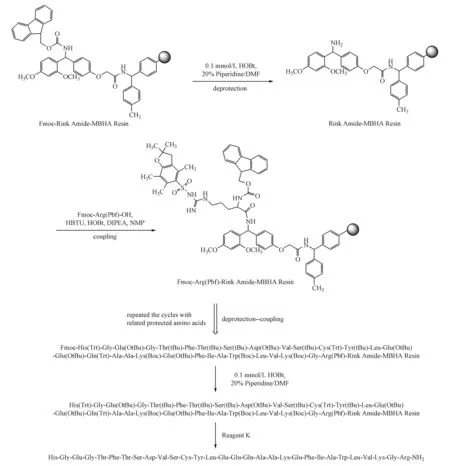
Scheme1 Synthetic route of Gly8-Cys17-GLP-1(7-36)-NH2on Fmoc-Rink Amide-MBHA Resin

Scheme2 Synthetic route of mPEG-maleimide (mPEG-MAL)

Scheme3 General synthetic route of PEG GLP-1 conjugates
2 实验部分
2.1 试剂、仪器及动物
mPEG(平均相对分子质量为350、550和750,美国Fluka-aldrich公司);制备级甲醇(美国Tedia公司);色谱纯三氟醋酸(上海阿拉丁试剂公司);其余试剂均为市售分析纯。
RY-1熔点仪(天津市新天光分析仪器技术有限公司);Bruker-ACF-300核磁共振仪(瑞士Bruker公司);C18反相柱(2.1 mm×50 mm,1.7 μm),UPLC H-Class-TQD液质联用仪(美国Waters公司);TM型血糖监测仪和血糖试纸(长沙三诺生物传感有限公司);C18反相制备柱(340 mm×28 mm,5 μm),6A制备型反相高效液相色谱仪(日本Shimadzu公司)。
昆明种小鼠,雌雄各半,质量20~30 g,由上海杰思捷实验动物有限公司提供,许可证号:SCXK(沪)2012-0006。所有动物实验均符合动物伦理委员会标准。
2.2 多肽合成
2.2.1 树脂溶胀 称取Fmoc-Rink Amide-MBHA Resin(0.182 g,0.1 mmol,取代度0.55 mmol/g),二氯甲烷溶胀30 min后,分别用甲醇和二氯甲烷冲洗干净。
2.2.2 9-笏甲氧羰基(Fmoc)的脱除 向含有树脂的反应管中加入0.1 mol/L HOBt的25%哌啶-DMF溶液7 mL,微波加热反应5min,脱保护完成后,用DMF 7 mL清洗树脂4次。
2.2.3 Fmoc保护的氨基酸的耦合 按肽序将相应氨基酸(0.5 mmol)、HOBt(81 mg,0.6 mmol)、HBTU(227.5 mg,0.6 mmol)和DIPEA(0.175 mL 1.2 mmol)溶于N-甲基吡咯烷酮(NMP)10 mL,加入盛有树脂的反应管中,氮气鼓泡,微波加热15 min。耦合完成后,用DMF 7 mL清洗树脂4次。
2.2.4 目标肽序的延长 根据目标多肽的氨基酸序列,重复上述的脱保护和耦合步骤,依次耦合相应的氨基酸,直到多肽链耦合完毕,获得缀有多肽链的树脂。
2.2.5 多肽的切割 将缀有多肽链的树脂置于多肽反应器中,加入切割剂Reagent K(TFA-苯甲硫醚-水-苯酚-乙二硫醇82.5∶5∶5∶5∶2.5),4 ℃振荡1 h后,常温振荡3 h,抽滤,收集滤液。将滤液加入5倍体积量的冰乙醚析出白色固体,冷冻离心得到相应的多肽粗品。
2.2.6 多肽的纯化 将待检测多肽用50%乙腈水溶液溶解,配制成10 mg/mL的溶液,采用制备液相进行多肽的纯化。按以下色谱条件进行纯化,色谱柱:C18反相制备柱(340 mm×28 mm,5 μm);流动相A:0.1%三氟醋酸水溶液,流动相B:0.1%三氟醋酸乙腈溶液;波长:214 nm;流速:5 mL/min。根据不同多肽性质选择不同线性梯度洗脱方法,如B 30%~90% 0~30 min。
2.3 PEG缀合连接臂合成
2.3.1 单甲氧基聚乙二醇对甲苯磺酸酯(mPEG-OTs)的合成 将平均相对分子质量为350的mPEG-OH 3.50 g(10 mmol)和三乙胺4 mL溶于二氯甲烷30 mL中,在冰浴条件下用恒压滴液漏斗向反应瓶中缓慢滴对甲苯磺酰氯7.60 g(40 mmol)的二氯甲烷20 mL溶液,滴加完毕后,恢复至室温并搅拌反应6 h,待反应完全后,减压蒸除溶剂,粗品柱色谱分离得纯品(甲醇-二氯甲烷),最终得mPEG-OTs 4.55 g,产率为90.9%。1H NMR(DMSO-d6,300 MHz)δ:7.49(2H,d,J=8.1 Hz,Ar-H),7.13(2H,d,J=8.1 Hz,Ar-H),4.13(2H,t,J=5.0 Hz,-CH2OTs),3.50(multi H,s,backbone -CH2CH2O-),3.06(3H,s,-OCH3),2.29(3H,s,Ar-CH3)。ESI-MS(m/z):561.4(n=8,[M+H]+),605.3(n=9,[M+H]+),649.3(n=10,[M+H]+),693.3(n=11,[M+H]+)。
平均相对分子质量为550的mPEG-OH 5.50 g按照上述方法,以相同比例和条件进行投料反应。反应结束后浓缩得到粗品经过柱色谱后,得到产物6.62 g,产率94.4%。1H NMR(DMSO-d6,300 MHz)δ:7.49(2H,d,J=8.1 Hz,Ar-H),7.13(2H,d,J=8.1 Hz,Ar-H),4.13(2H,t,J=5.0 Hz,-CH2OTs),3.50(multi H,s,backbone -CH2CH2O-),3.01(3H,s,-OCH3),2.29(3H,s,Ar-CH3)。ESI-MS(m/z):716.3(n=12,[M+H]+),760.4(n=13,[M+H]+),803.4(n=14,[M+H]+),847.5(n=15,[M+H]+)。
平均相对分子质量为750的mPEG-OH 7.50 g按照上述方法,以相同比例和条件进行投料反应。反应结束后浓缩得到粗品经过柱色谱后,得到产物8.11g,产率89.9%。1H NMR(DMSO-d6,300 MHz)δ:7.49(2H,d,J=8.1 Hz,Ar-H),7.13(2H,d,J=8.1 Hz,Ar-H),4.13(2H,t,J=5.0 Hz,-CH2OTs),3.50(multi H,s,backbone -CH2CH2O-),3.01(3H,s,-OCH3),2.29(3H,s,Ar-CH3)。ESI-MS(m/z):869.0(n=15,[M+H]+),913.0(n=16,[M+H]+),957.2(n=17,[M+H]+),1 001.2(n=18,[M+H]+)。
2.3.2 单甲氧基聚乙二醇邻苯二甲酰胺(mPEG-phthalimide)的合成 将mPEG350-OTs 3.01 g和邻苯二甲酰亚胺钾盐1.10 g溶于DMF 15 mL,氮气保护下升温到100 ℃反应4 h。反应结束后,减压蒸去溶剂得到黄色油状物,溶于二氯甲烷20 mL中,过滤除去不溶物,蒸除溶剂得粗品,柱色谱分离得纯品(甲醇/二氯甲烷),最终得mPEG-phthalimide 2.20 g,产率为74.3%。1H NMR(DMSO-d6,300 MHz)δ:7.84(4H,m,Ar-H),3.38(multi H,s,backbone -CH2CH2O-),3.21(3H,s,-OCH3)。ESI-MS(m/z):536.4(n=8,[M+H]+),580.3(n=9,[M+H]+),624.3(n=10,[M+H]+),668.4(n=11,[M+H]+)。
mPEG550-OTs 4.70 g按照上述方法,以相同比例和条件进行投料反应。反应结束后浓缩得到粗品经过柱色谱后,得到产物3.69 g,产率79.7%。1H NMR(DMSO-d6,300 MHz)δ:7.84(4H,m,Ar-H),3.5(multi H,s,backbone -CH2CH2O-),3.24(3H,s,-OCH3)。ESI-MS(m/z):690.4(n=12,[M+H]+),734.5(n=13,[M+H]+),778.4(n=14,[M+H]+),822.5(n=15,[M+H]+)。
mPEG750-OTs 6.81 g按照上述方法,以相同比例和条件进行投料反应。反应结束后浓缩得到粗品经过柱色谱后,得到产物4.21 g,产率62.4%。1H NMR(DMSO-d6,300 MHz)δ:7.84(4H,m,Ar-H),3.51(multi H,s,backbone -CH2CH2O-),3.24(3H,s,-OCH3)。ESI-MS(m/z):756.5(n=15,[M+H]+),800.5(n=16,[M+H]+),844.3(n=17,[M+H]+),888.4(n=18,[M+H]+)。
2.3.3 单甲氧基聚乙二醇马来酰亚胺(mPEG-maleic acid)的合成 将mPEG350-phthalimide 2.20 g和80%的水合肼5 mL溶于乙醇15 mL,升温到80 ℃回流2 h。减压蒸去溶剂得到mPEG350-NH2粗品1.32 g。将mPEG350-NH2粗品1.32 g和顺丁烯二酸酐0.45 g溶于冰醋酸,升温到120 ℃回流反应6 h。减压蒸去溶剂并经柱色谱纯化,得到产物0.74g,产率62.3%。1H NMR(DMSO-d6,300 MHz)δ:6.63(2H,s,-CH=CH-),3.56(multi H,s,backbone -CH2CH2-),3.23(3H,s,-OCH3)。ESI-MS(m/z):530.2(n=8,[M+H]+),574.2(n=9,[M+H]+),618.3(n=10,[M+H]+),662.3(n=11,[M+H]+)。
mPEG550-phthalimide 2.77 g按照上述方法,以相同比例和条件进行投料反应。反应结束后浓缩得到粗品经过柱色谱后,得到产物0.95 g,产率60.1%。1H NMR(DMSO-d6,300 MHz)δ:6.63(2H,s,-CH=CH-),3.57(multi H,s,backbone -CH2CH2-),3.23(3H,s,-OCH3)。ESI-MS(m/z):618.3(n=10,[M+H]+),622.3(n=11,[M+H]+),706.4(n=12,[M+H]+),750.4(n=13,[M+H]+)。
mPEG750-phthalimide 4.21 g按照上述方法,以相同比例和条件进行投料反应。反应结束后浓缩得到粗品经过柱色谱后,得到产物1.05 g,产率55.8%。1H NMR(DMSO-d6,300 MHz)δ:6.63(2H,s,-CH=CH-),3.56(multi H,s,backbone -CH2CH2-),3.23(3H,s,-OCH3)。ESI-MS(m/z):706.3(n=12,[M+H]+),750.3(n=13,[M+H]+),794.3(n=14,[M+H]+),828.4(n=15,[M+H]+)。
2.4 PEG-多肽缀合物的合成
将PEG马来酰亚胺小分子溶于DMSO,配成约10 mg/mL的溶液,将合成的多肽链溶解于DMSO,两溶液混合后,加入DIEPA 20 μL,室温下搅拌反应过夜,液质监测反应情况。色谱条件为:C18反相柱(2.1 mm×50 mm,1.7 μm);流动相A:0.1%甲酸水溶液,流动相B:0.1%甲酸乙腈溶液,流动相梯度:流动相B 10%~90%,2 min,B 90%~90%,3 min;流速为0.3 mL/min;紫外检测波长为214 nm。反应监测结束后,反应液使用含有1%三氟乙酸的乙腈溶液稀释后进入制备液相色谱进行纯化,色谱条件为:C18反相柱(340 mm×28 mm,5 μm);流动相A:0.1%三氟醋酸水溶液,流动相B:0.1%三氟醋酸乙腈溶液;流动相梯度:流动相B 40%~80%,30 min;80%~85%,10 min;85%~95%,10 min;95%~40%,10 min;流速为5 mL/min,检测波长为214 nm。收集溶液,旋干乙腈,冻干即得纯品。所有PEG-多肽缀合物均按上述方法进行缀合和纯化。合成的12个目标化合物的熔点、外观和ESI-MS质谱数据见表1。
Table1 MS data of PEGylation GLP-1 receptor agonistsI-1-I-12

Compd.mp/℃AppearanceESI-MS,m/znMolecular weightCalcd.Found I-1191-195White solid567856783 719.93 763.93 807.93 851.93 719.93 763.93 807.93 851.9[M+3H]3+ 1 240.9[M+3H]3+ 1 258.6[M+3H]3+ 1 270.3[M+3H]3+ 1 285.0[M+4H]4+930.9[M+4H]4+942.0[M+4H]4+952.9[M+4H]4+963.9[M+3H]3+ 1 240.6[M+3H]3+ 1 255.3[M+3H]3+ 1 270.3[M+3H]3+ 1 285.0[M+4H]4+930.8[M+4H]4+941.9[M+4H]4+952.9[M+4H]4+963.8 I-2198-202White solid910111291011123 895.93 939.93 983.94 027.93 895.93 939.93 983.94 027.9[M+3H]3+ 1 299.6[M+3H]3+ 1 314.3[M+3H]3+ 1 328.9[M+3H]3+ 1 343.8[M+4H]4+974.9[M+4H]4+985.9[M+4H]4+996.9[M+4H]4+ 1 007.9[M+3H]3+ 1 299.6[M+3H]3+ 1 314.3[M+3H]3+ 1 328.9[M+3H]3+ 1 343.7[M+4H]4+974.8[M+4H]4+985.7[M+4H]4+996.7[M+4H]4+ 1 008.0 I-3134-140White solid16171819161718194 227.94 271.94 315.94 359.94 226.94 270.94 314.94 358.9[M+4H]4+ 1 058.0[M+4H]4+ 1 068.9[M+4H]4+ 1 080.0[M+4H]4+ 1 090.9[M+5H]5+846.4[M+5H]5+855.2[M+5H]5+863.9[M+5H]5+872.8[M+4H]4+ 1 057.9[M+4H]4+ 1 068.5[M+4H]4+ 1 079.8[M+4H]4+ 1 090.8[M+5H]5+846.2[M+5H]5+855.2[M+5H]5+863.9[M+5H]5+872.7 I-4203-207White solid6789789103 741.83 785.83 829.83 873.83 772.83 816.83 860.83 904.8[M+2H]2+ 1 871.9[M+2H]2+ 1 893.9[M+2H]2+ 1 915.9[M+2H]2+ 1 937.9[M+3H]3+ 1 258.6[M+3H]3+ 1 273.2[M+3H]3+ 1 287.9[M+3H]3+ 1 302.6[M+2H]2+ 1 871.3[M+2H]2+ 1 893.5[M+2H]2+ 1 916.1[M+2H]2+ 1 938.1[M+3H]3+ 1 258.5[M+3H]3+ 1 272.8[M+3H]3+ 1 288.0[M+3H]3+ 1 302.6 I-5212-215White solid89101191011123 832.83 876.83 920.83 964.83 860.83 904.83 948.83 992.8[M+2H]2+ 1 917.4[M+2H]2+ 1 939.4[M+2H]2+ 1 961.4[M+2H]2+ 1 982.4[M+3H]3+ 1 287.9[M+3H]3+ 1 302.6[M+3H]3+ 1 317.2[M+3H]3+ 1 331.9[M+2H]2+ 1 917.1[M+2H]2+ 1 939.1[M+2H]2+ 1 961.9[M+2H]2+ 1 983.0[M+3H]3+ 1 287.9[M+3H]3+ 1 302.4[M+3H]3+ 1 316.5[M+3H]3+ 1 331.9
(Continued)

Compd.mp/℃AppearanceESI-MS,m/znmolecular weightCalcd.Found I-6233-237White solid17181920171819204 230.84 274.84 318.84 362.84 229.84 273.84 317.84 361.8[M+3H]3+ 1 411.3[M+3H]3+ 1 425.9[M+3H]3+ 1 440.6[M+3H]3+ 1 455.3[M+4H]4+ 1 058.4[M+4H]4+ 1 069.4[M+4H]4+ 1 080.4[M+4H]4+ 1 091.4[M+3H]3+ 1 411.8[M+3H]3+ 1 425.5[M+3H]3+ 1 439.6[M+3H]3+ 1 455.3[M+4H]4+ 1 058.4[M+4H]4+ 1 069.3[M+4H]4+ 1 080.6[M+4H]4+ 1 091.7 I-7184-189White solid678956783 741.83 785.83 829.83 873.83 689.83 733.83 777.83 821.8[M+2H]2+ 1 871.5[M+2H]2+ 1 893.9[M+2H]2+ 1 917.9[M+2H]2+ 1 938.7[M+3H]3+ 1 230.9[M+3H]3+ 1 245.6[M+3H]3+ 1 260.3[M+3H]3+ 1 274.9[M+2H]2+ 1 871.5[M+2H]2+ 1 893.4[M+2H]2+ 1 916.9[M+2H]2+ 1 938.3[M+3H]3+ 1 230.8[M+3H]3+ 1 245.5[M+3H]3+ 1 260.0[M+3H]3+ 1 274.0 I-8194-199White solid8910118910113 805.83 849.83 893.83 937.83 791.83 835.83 879.83 923.8[M+2H]2+ 1 903.8[M+2H]2+ 1 925.9[M+2H]2+ 1 947.9[M+2H]2+ 1 969.9[M+3H]3+ 1 264.9[M+3H]3+ 1 279.6[M+3H]3+ 1 294.2[M+3H]3+ 1 308.9[M+2H]2+ 1 903.8[M+2H]2+ 1 925.9[M+2H]2+ 1 947.7[M+2H]2+ 1 970.1[M+3H]3+ 1 264.3[M+3H]3+ 1 279.6[M+3H]3+ 1 294.0[M+3H]3+ 1 308.7 I-9203-207White solid9101112101112133 828.83 872.83 916.83 960.83 870.83 914.83 958.84 002.8[M+2H]2+ 1 915.4[M+2H]2+ 1 937.4[M+2H]2+ 1 959.4[M+2H]2+ 1 981.4[M+3H]3+ 1 291.3[M+3H]3+ 1 305.9[M+3H]3+ 1 320.6[M+3H]3+ 1 335.2[M+2H]2+ 1 915.0[M+2H]2+ 1 937.2[M+2H]2+ 1 958.9[M+2H]2+ 1 981.2[M+3H]3+ 1 291.3[M+3H]3+ 1 305.9[M+3H]3+ 1 320.5[M+3H]3+ 1 335.6 I-10164-166White solid678956783 858.03 902.03 946.03 990.03 825.03 859.03 903.03 947.0[M+3H]3+ 1 287.0[M+3H]3+ 1 301.7[M+3H]3+ 1 316.3[M+3H]3+ 1 331.0[M+4H]4+957.2[M+4H]4+965.8[M+4H]4+976.8[M+4H]4+987.8[M+3H]3+ 1 287.3[M+3H]3+ 1 301.8[M+3H]3+ 1 316.8[M+3H]3+ 1 331.0[M+4H]4+957.3[M+4H]4+965.7[M+4H]4+976.4[M+4H]4+987.9 I-11240-242White solid78910789103 876.03 920.03 964.04 008.03 832.03 876.03 920.03 964.0[M+3H]3+ 1 293.0[M+3H]3+ 1 307.7[M+3H]3+ 1 322.3[M+3H]3+ 1 337.0[M+4H]4+959.0[M+4H]4+970.0[M+4H]4+981.0[M+4H]4+992.0[M+3H]3+ 1 293.6[M+3H]3+ 1 307.6[M+3H]3+ 1 322.6[M+3H]3+ 1 336.7[M+4H]4+958.9[M+4H]4+970.1[M+4H]4+980.9[M+4H]4+991.8 I-12232-236White solid10111213111213144 008.04 052.04 096.04 140.04 074.04 118.04 162.04 206.0[M+4H]4+ 1 003.0[M+4H]4+ 1 014.0[M+4H]4+ 1 025.0[M+4H]4+ 1 036.0[M+5H]5+815.8[M+5H]5+824.6[M+5H]5+833.4[M+5H]5+842.2[M+4H]4+ 1 003.0[M+4H]4+ 1 014.3[M+4H]4+ 1 025.2[M+4H]4+ 1 036.3[M+5H]5+815.8[M+5H]5+824.7[M+5H]5+833.7[M+5H]5+842.3
nrepresents the number of back bone “CH2CH2O” units in a PEG monomer
3 降糖活性评价
3.1 受体激动活性研究
GLP-1衍生物的受体激动活性是其发挥多种生理作用的前提,因而优先对已合成的GLP-1衍生物的受体激动活性进行研究。实验室前期通过质粒转染,构建了高度表达GLP-1受体的HEK293细胞[17],该细胞株可在GLP-1衍生物的作用下,产生大量cAMP。本研究以Ex-4和Gly8-GLP-1(7-36)-NH2为对照,通过试剂盒测定衍生物刺激细胞后生成的cAMP量,评估衍生物的受体激动活性。
3.2 正常小鼠单次给药单次给糖实验
为了初步评估衍生物的体内降糖活性,以Ex-4和Liraglutide组为阳性对照,进行单次给药单次给糖实验,即在小鼠给糖前30 min腹腔给药,检测从给药至给糖后2 h期间其血糖变化,评估化合物的降糖活性。
3.3 正常小鼠单次给药多次给糖实验
为了进一步探索衍生物的体内长效化降糖活性,以Ex-4和Liraglutide组为阳性对照,进行单次给糖后进行多次腹腔糖耐量实验,每隔3小时腹腔注射葡萄糖并测定给糖后的血糖,一共给糖3次,从而评估衍生物的降糖活性和长效化时间。
4 结果与讨论
4.1 受体激动活性研究
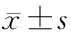
修饰不会导致GLP-1生物活性的丧失。此外,4条母肽链进行不同长度的PEG小分子修饰后,随着PEG相对分子质量的增加,衍生物的受体激动活性呈现轻微的下降趋势,原因可能是PEG侧链在一定程度上影响了GLP-1与受体的相互作用。另外,肽链C端缀合PEG的衍生物激动活性略优于接近N端PEG化衍生物,尽管不同缀合位置对总体受体激动活性影响不大。
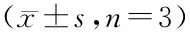

Compd. EC50/(pmol/L)Compd. EC50/(pmol/L)Ex-41.8±0.8Gly8-GLP-1(7-36)-NH25.6±0.9* I-15.8±1.3* I-76.3±1.7* I-28.0±1.1* I-88.7±1.2* I-310.8±1.0* I-911.6±1.7* I-47.4±0.9* I-102.4±1.5 I-59.1±1.4* I-116.6±0.8* I-612.6±2.4* I-129.2±1.1*
*P<0.05vsEx-4 group
4.2 正常小鼠单次给药单次给糖实验
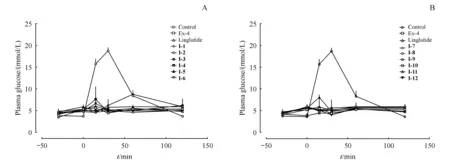
由图2可知,给药后所有衍生物在腹腔糖耐量期间均具有较好的降糖活性,效果与阳性对照药相当。
4.3 正常小鼠单次给药多次给糖实验
由图3可知,给药后衍生物在第1轮腹腔糖耐量期间均具有较好的降糖活性,效果与阳性对照药相当,第2次给糖后,降糖效果均呈现轻微下降趋势,但15 min后的血糖均在10 mmol/L以下。在第3次糖耐量期间,各个衍生物的长效化活性呈现明显差异,其中优选化合物I-12降糖活性的下降程度最小,与阳性对照药Ex-4和Liraglutide相当。



5 结 论
早期研究中缀合GLP-1多肽链的PEG的相对分子质量均在2 000以上,低于1 000的PEG修饰鲜有报道。本研究选用平均相对分子质量为350、550和750的mPEG分别缀合到GLP-1肽链上,设计并合成了12个目标化合物,所有化合物的结构和纯度经质谱和液相色谱分析确证。所有多肽链均通过微波促进Fmoc/tBu正交保护策略固相方法合成,经反相制备高效液相系统纯化得到肽链纯品,PEG侧链则通过马来酰亚胺基团作为连接臂,与肽链中的巯基反应得到目标化合物。本研究对化合物进行初步活性评价,受体激动活性研究结果表明,大部分衍生物的受体激动活性都得到了保持,说明短链PEG修饰不会导致GLP-1生物活性丧失。4条母肽链进行不同长度的PEG小分子修饰后,随着PEG相对分子质量的增加,衍生物的受体激动活性呈现轻微的下降趋势,原因可能是PEG侧链在一定程度上影响了GLP-1与受体的相互作用。单次给药单次给糖实验表明,所有衍生物均具有较好的降糖活性,效果与阳性对照相当。单次给药多次给糖实验表明,优选化合物I-12的降糖活性维持时间最长,与阳性对照药Ex-4和Liraglutide相当,具有成为GLP-1类似物新药分子的潜力。将相对分子质量较小的PEG结构与修饰过的GLP-1多肽链缀合这一思路也为今后GLP-1受体激动剂的长效化设计与研发提供方向。

