基于改进模糊连接度的CT图像肝脏血管三维分割方法
张 睿 吴薇薇 周著黄* 姜 涛 吴水才
1(北京工业大学生命科学与生物工程学院,北京 100124)2(首都医科大学生物医学工程学院,北京 100069)
引言
肝癌是我国常见的恶性肿瘤之一,发病率居第5位,病死率高居第3位[1]。肝癌局部热消融治疗(包括射频消融和微波消融等)已成为继手术切除、肝移植后的第三大根治性手段[2],它是在医学影像引导下,将消融针(射频电极/微波天线)插入肿瘤内作为热源,将肿瘤组织加热到较高温度,使肿瘤原位凝固性坏死。基于医学影像的消融针穿刺路径规划和穿刺导航是肝肿瘤热消融治疗的关键,而肝脏血管的三维分割又是其重要环节。笔者主要针对CT影像中肝血管的三维分割开展研究。
医学图像三维分割方法主要包括阈值法、区域生长、水平集、图论方法(如图割等)、模糊连接度和机器学习等[3]。其中,模糊连接度是一类重要的分割方法,但将其直接应用于CT图像肝血管三维分割时,却难以达到较好的效果,且存在参数敏感和较为耗时等问题。为此,本研究改进传统模糊连接度算法,使其可适用于CT图像肝血管的三维分割任务。研究思路是针对CT图像进行肝血管增强处理,再将血管增强响应引入模糊亲和度函数,并使用Otsu多阈值算法代替置信连接度对模糊场景进行初始化。
血管增强算法以Sato等[4]和Frangi等[5]的算法最为典型。此后Li[6]、Erdt[7]、Zhou[8]、Xiao[9]、Yang[10]、Zeng[11]等的研究中也提出了各自的血管增强策略,但将这些算法应用于CT图像肝血管增强任务时,肝血管增强效果欠佳。不适宜增强拓扑结构复杂的血管和结点;即使在理想的血管结构中,增强效果也仅在血管中心显著,而沿血流切向迅速衰减;此外对灰度不均的血管增强效果不一,影响后续肝血管分割。Jerman等针对以上问题,对血管增强算法性能进行了大幅优化[12],但将该算法应用于肝血管增强时,可能出现肝脏轮廓、肝实质和噪声的误增强现象。因此,本研究还针对此问题,改进了Jerman血管增强算法。
1 方法
本研究提出的肝血管分割算法流程如图1所示,内含3个关键步骤:预处理、肝血管增强、肝血管分割。算法的初始输入为原始腹部增强CT图像IOri和肝脏掩膜IMask。IMask能获得肝脏感兴趣区域,大幅降低运算量,其获取可参照本课题组先前发表的肝脏快速三维分割等方法[13]。
1.1 预处理
首先将IOri与IMask进行逻辑与运算,结果记作IROI。为增强血管结构对比度,同时抑制对肝脏轮廓的误增强,本研究对IROI进行自适应S型非线性灰度映射,得到结果ISg。S型非线性灰度映射为
(1)
式中,β和α分别表示待增强血管结构的中心灰度值和灰度范围,其值由K均值聚类算法自适应获得。将IROI肝区内部结构进行聚类数目为5的K均值聚类,按聚类中心灰度由低到高分别表示背景区域、肝肿瘤等病变区域、肝实质区域、低灰度血管与肝实质混合区域和高灰度血管区域。从中提取第4类区域均值m1与第5类区域均值m2,β和α计算为
(2)
此外,新型血管增强算法是需针对各向同性图像进行,故对ISg进行各向同性插值采样,采用sinc插值算法,得到结果IIso。预处理效果如图2所示。
1.2 肝血管增强
1.2.1血管增强算法原理
基于Hessian矩阵的多尺度血管增强算法,是目前研究最多的血管增强算法,适用于区分医学影像中的滴状、管状和平面状结构。其算法原理概述为令Iinput(x)为待增强的灰度图像,矢量矩阵x=[x1,x2,…,xD]表示D维灰度图像体素的空间坐标。可求取Iinput(x)在位置x、尺度空间σ下的D阶Hessian矩阵元素,即

图1 本研究提出的肝血管分割算法流程(以3Dircadb数据集的第1例CT图像为例)Fig.1 Flow chart of the proposed liver vesselness segmentation method (No. 1 of 3Dircadb dataset)
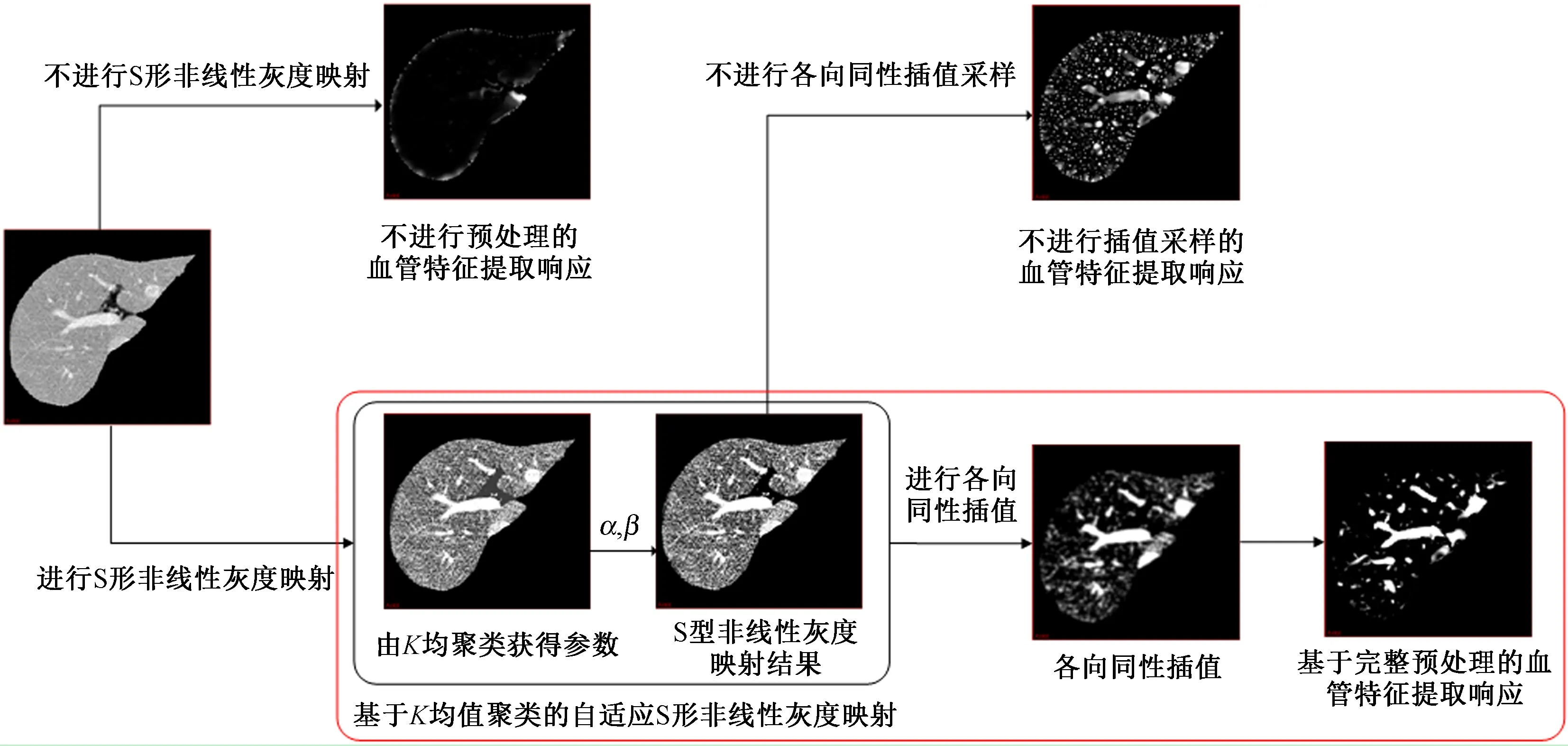
图2 预处理流程(以3Dircadb数据集的第1例CT图像为例)Fig.2 Flow chart of preprocessing (No. 1 of 3Dircadb dataset)
(3)
式中,i,j=1,2,…,D,G(x,σ)是D维高斯运算,*代表卷积运算,σ∈[σmin,σmax],σmin和σmax对应待增强血管结构的最小尺寸和最大尺寸。

结合多尺度策略,令响应υp获取各个尺度空间σ下、位置x处增强响应υk的极大值作为血管增强算法的最终响应υp=sup{υk[eigH(x,σ)]:σmin≤σ≤σmax}。
1.2.2Jerman血管增强算法
在三维增强CT图像中,理想的血管结构对应的Hessian矩阵特征值满足λ2≈λ3∧|λ2,3|≫|λ1|。据此,Jerman等构造了新型血管增强响应函数,大幅改进了血管增强算法性能[12]。为便于计算,Jerman等定义:若图像中血管灰度高于背景时,需对Hessian矩阵特征值求取相反数。
增强CT图像中,血管边缘或低阶血管区域的λ2与λ3量度较低(|λ3|>|λ2|→Low),不匹配理想的血管结构所对应的Hessian矩阵特征值关系,致使传统血管增强算法响应出现显著衰减。为弥补这一缺陷,Jerman等对量度较低的特征值λ3进行分段补偿(见式(4)),得到优化的特征值λρ。为了标准化多尺度血管增强响应,λ3需分别在各个尺度空间下进行优化。
(4)
式中,τ是介于0~1之间的阈值系数,文献[12]中该参数的优选值是0.6。

图3 血管特征提取算法效果比较(以3Dircadb数据集的第1例CT图像为例)。(a)Frangi算法;(b)Sato算法;(c)Erdt算法;(d)Jerman算法;(e)本研究算法Fig.3 Comparison of our vesselness filter with traditional ones (No. 1 of 3Dircadb dataset).(a)Frangi′s vesselness; (b) Sato′s vesselness; (c) Erdt′s vesselness; (d) Jerman′s vesslenss; (e) Our vesselness
此外,传统血管增强算法会抑制滴状结构,在血管结点处(|λ1|≈|λ2|≈|λ3|→High)增强效果不佳。据此,Jerman等针对λ2≥λρ/2>0的椭球型结构进行补偿,得到其最终的血管增强响应,即
(5)
1.2.3改进的Jerman血管增强算法
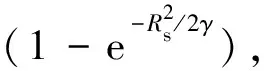
(6)

综上,本研究改进的新型血管增强算法1流程为
输入:预处理后的CT图像IIso
输出:血管增强图像IVesselness
1) 设置待增强的血管尺度范围σmin←1,σmax←4,阈值τ←0.6,多尺度策略步进次数v←5,噪声抑制项系数γ=30
2)forσ←σmindo
3) 在当前尺度σ下,计算图像体素在空间位置x对应的Hessian矩阵元素,构建Hessian矩阵Hij(x,y,z,σ),并进行特征值分解,获得Hessian矩阵特征值λi
4) 对特征值λi进行排序,令λ1>λ2>λ3,求取各特征值的相反数
5) 计算当前尺度下,λ3的分段补偿特征值λρ(σ)
6) 计算当前尺度下的分段血管增强响应υours
7) 计算下一尺度σ←σnext的Hessian矩阵元素和血管增强响应,直到σ=σmax
8)endfor
9) 计算各尺度响应υours的极大值,作为最终的血管增强响应υp
图3定性比较本研究优化的血管增强算法与传统血管增强算法,可以看出本研究优化后的血管增强算法既保证对血管结构的完整增强,又在很大程度上抑制了非血管区域的误增强。
1.3 肝血管分割
模糊性是CT等医学影像具有的特性之一,Zadeh等创立模糊集合理论[16],Rosenfeld等将“连接度”这一思路融入其中[17],随后Udupa等提出借助模糊连接度进行图像分割的理论框架[18-19]。至此,模糊连接度分割算法在各类医学图像分割中得到了广泛的关注与应用。
1.3.1模糊连接度分割算法
模糊连接度分割算法的理论核心在于3种模糊关系的处理,即模糊邻近关系、模糊亲和度和模糊连接度。这里主要介绍模糊亲和度。
模糊亲和度用以表示在整个场景C中体素对(c,d)的局部相似度,记作μκ(c,d)∈[0,1],其计算方法为
μκ(c,d)=μα(c,d)[ω1h1(f(c),f(d))+
ω2h2(f(c),f(d))]
(7)
其中,h1与h2的计算方式为
(8)
(9)
式中:f(·)是当前位置体素的灰度;m与s分别是分割前景感兴趣区域内体素的灰度均值与灰度标准差;ω1与ω2是权重参数,满足ω1+ω2=1,参考Pednekar等[20]自适应权重选取,使图像中各体素合理地求取不同的ω1和ω2值,避免整幅图像中采用固定的权重参数计算。
自适应权重的计算方式为
(10)
1.3.2基于置信连接度的模糊连接度分割算法
在模糊连接度分割算法中,需要统计分割前景感兴趣区域内的灰度均值与标准差。这里,划定感兴趣区域需要一定程度的人工交互;此外,模糊连接度算法分割需要多个初始种子点,且对种子点的位置敏感。为解决上述缺陷,产生了借助置信连接度算法进行初始化的模糊连接度分割算法[21]。
合适地选取种子点,能够使置信连接度算法的结果更加精确。由于血管狭长结构的特殊性,种子点(集)能否均匀地分布在各支血管中,直接影响着血管系统最终分割的完整性。针对肝血管的种子点选取,通常在5 mm×5 mm×3 mm的局部区域内进行(尽可能确保区域内有且只有一条血管结构通过)[11,15],先利用局部极值自动选取候选种子点(集),再通过经验阈值进行优选,确定最终的种子点(集)。
在5 mm×5 mm×3 mm的子区域内筛选种子点(集)虽较好满足了分割的完整性,但耗时较长,且置信连接度算法对种子点的经验阈值、乘法因子、迭代次数、迭代半径等参数均较为敏感,导致最终模糊连接度的分割结果易出现过分割或欠分割现象,图4给出了乘法因子l对模糊连接度分割结果的影响,其中红色结构是模糊连接分割算法的结果,绿色结构是专家手工勾勒的肝血管结构,可以看出,l稍加改变就会对血管的分割结果造成明显影响。

图4 乘法因子对模糊连接分割算法结果的影响(以3Dircadb数据集的第8例CT图像为例)。(a)l=1.0;(b)l=1.2;(c)l=1.4Fig.4 Impact of the multiplication factor on liver vessel segmentation by using the fuzzy connectedness based on confidence connectedness (No. 8 of 3Dircadb dataset). (a) l=1.0; (b) l=1.2; (c) l=1.4
1.3.3改进的模糊连接度分割算法
本研究对模糊连接度分割算法的核心优化在于利用改进的血管增强响应υp代替增强CT图像IOri的灰度值,作为模糊亲和度函数的输入,即将式(7)改写为
μκ(c,d)=μα(c,d)(ω1h1(υp(c),υp(d))+
ω2h2(υp(c),υp(d)))
(11)
图5中比较了图像IOri、ISg和IVesselness分别作为模糊亲和度函数输入的结果。可以看出,直接将增强CT图像IOri的灰度代入模糊亲和度函数中(见式(7)),几乎无法分割出肝血管;将对比度增强后的图像ISg的灰度代入模糊亲和度函数中,能够获得效果不佳的血管结构,其血管表面不平滑,且血管内部存在孔洞现象;而将血管增强响应υp代入模糊亲和度函数中(见式(11)),能够获得更为理想的血管结构。

图5 不同模糊亲和函数输入的模糊连接分割算法结果比较(以3Dircadb数据集的第1例CT图像为例)。(a)原始CT的模糊连接分割;(b)S形非线性灰度映射的模糊连接分割;(c)血管增强响应的模糊连接分割;(d)金标准Fig.5 Comparison of liver vessel segmentation by using fuzzy connectedness with different fuzzy affinity functions (No. 1 of 3Dircadb dataset). (a) Fuzzy connectedness of original CT; (b) Fuzzy connectedness of sigmoid; (c) Fuzzy connectedness of vesselness; (d) Gold standard
本研究针对置信连接度算法的参数敏感性和运行耗时问题进行改进,由Otsu多阈值算法代替置信连接度算法统计感兴趣区域信息。Otsu多阈值算法无须选取种子点(集),仅需设置唯一参数阈值数目N。经多次试验,N值优选为2。首先,对血管增强图像IVesselness进行Otsu多阈值算法处理,得到图像IOtsu;再将图像IVesselness与IOtsu进行逻辑与运算,得到前景感兴趣区域图像IvesMask;统计图像IvesMask内的灰度均值与灰度标准差,作为模糊连接度分割算法的初始化输入参数。最后,借助一个种子点二值化模糊场景,得到本研究的肝血管分割结果。
在研究中,种子点的选取策略为:将图像IVesselness细分为5 mm×5 mm×3 mm的区域,筛选出灰度均值最大的区域Rsub,将该区域中灰度极大值点作为种子点。综上,本研究提出的改进模糊连接度血管分割算法为
输入:血管增强图像IVesselness;一个种子点Pseed
输出:血管分割结果ISeg
1) 参数初始化设置,令Otsu多阈值算法阈值数N←2,模糊连接度分割算法阈值T←0.05
2) 对图像Ivesselness进行Otsu多阈值分割算法,获得结果IOtsu
3) 将Ivesselness与IOtsu进行逻辑与运算,得到前景感兴趣区域IvesMask,统计IvesMask中的灰度均值m与灰度标准差s
4) 将m与s代入模糊亲和度函数中,计算模糊场景
5) 将Ivesselness细分为5 mm×5 mm×5 mm子区域,寻找灰度均值最大的子区域Rsub,将该区域内灰度极大值点作为血管结构种子点Pseed
6) 结合种子点Pseed,对模糊场景进行二值化分割
2 实验
实验数据选取公开CT图像数据集3Dircadb(来源: http://www.ircad.fr/research/3dircadb)由法国消化系统癌症治疗研究所(Research Institute against Digestive Cancer)提供。内含20例对比度增强三维CT图像(男女各10例),每例数据的像素尺寸为0.56~0.86 mm,层厚为1~4 mm,切片数为64~502层,单层分辨率为512像素×512像素。数据集内含放射学专家逐层手工勾勒的肝血管轮廓,为本研究中肝血管分割的金标准。本研究实验选取全部20例CT数据。
为了定量分析血管增强与血管分割算法,本研究采用以下评估参数进行算法性能比较(见式(12)~(15))。对于血管增强算法,首先采用局部血管响应强度进行定量对比,再通过对比度噪声比(contrast-to-noise ratio, CNR)进行全局血管增强响应性能比较。CNR的计算方式为
(12)
式中,μvessel和μbackground分别表示血管区域和背景区域的灰度均值,σvessel和σbackground分别表示血管区域和背景区域的灰度标准差。
本研究血管增强算法的参数选择如表1所示。
表1血管增强算法参数选择(最优参数依据文献[12,15]得到)
Tab.1Parametersettingsforvesselnessalgorithms(Theoptimalparameterswereobtainedfromliteratures[12,15])

方法最优参数Frangi[5]α=0.5, β=0.5, γ=30, σmin=1, σmax=4, ν=5Sato[4]α1=0.3, α2=2, σmin=1, σmax=4, ν=5Erdt[7]σmin=1, σmax=4, ν=5Jerman[12]σmin=1, σmax=4, ν=5, τ=0.6Oursσmin=1, σmax=4, ν=5, γ=30, τ=0.6
对于肝血管分割算法的评估,采用准确性、敏感性和特异性,即

(13)

(14)
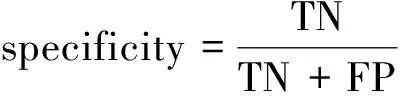
(15)
式中,TP和TN分别是正确分割为血管和背景的体素数量,FP和FN分别是错误分割为血管和背景的体素数量。
3 结果
首先定量比较血管增强算法的局部血管增强响应值。在各个血管增强算法的局部结果上标定统一线段(line1),遍历该线段对应体素的灰度响应强度,绘制成图6。理想的血管增强响应满足血管外响应强度为极小值,而血管内响应强度快速上升至极大值。从图6中明显看出,传统血管增强算法对于血管中心增强效果显著,但向血管边界拓展时增强效果迅速衰减;而Jerman算法与本研究改进的增强算法的显著增强区域更接近血管的实际尺寸。

图6 局部血管特征提取算发响应强度比较。(a)Frangi算法;(b)Sato算法;(c)Erdt算法;(d)Jerman算法;(e)本算法;(f)金标准;(g)Line 1的灰度分布Fig.6 Comparison of local vascular enhancement response of different vesselness filters. (a)Frangi′s vesselness; (b)Sato′s vesselness; (c)Erdt′s vesselness; (d)Jerman′s vesselness; (e)Our vesselness; (f)Gold standard; (g)The intensity distribution at the marker of Line 1
同时,对血管增强算法的对比度噪声比进行分析,结果见图7。可以看出,本研究的血管增强算法的对比度噪声比显著优于传统的Frangi、Sato和Erdt血管增强算法,满足置信区间0.95的显著性分析(P≪0.01),且略高于Jerman血管增强算法。这说明,本研究改进的血管增强算法在保留Jerman算法血管增强性能的前提下,更好地抑制了肝区内的背景噪声。

图7 不同血管特征提取算法结果的对比度噪声比Fig.7 Contrast to noise ratio of different vesselness filters
针对本研究血管分割算法的性能评估是与传统分割算法进行定量比较的,这里,传统分割算法包括基于置信连接度的传统模糊连接度分割算法[21]、基于置信连接度的区域生长算法、阈值水平集算法[22]和测地线轮廓水平集算法[23]。各算法分割的肝血管结果见图8。各算法分割结果对应的准确性、敏感性和特异性如表2所示。结果表明:本研究改进的模糊连接度分割算法的准确性与敏感性均显著优于基于置信连接度的传统模糊连接度分割算法,满足置信区间0.95的显著性分析(P≪0.01)。
最后,以血管增强算法结果IVesselness为输入,定量比较了分割算法的耗时,结果见表3。可以看出,借助Otsu多阈值算法代替置信连接度算法,能够大幅降低分割流程初始化的执行时间。
表2血管分割结果评估结果
Tab.2Evaluationoftheproposedlivervesselsegmentationmethod
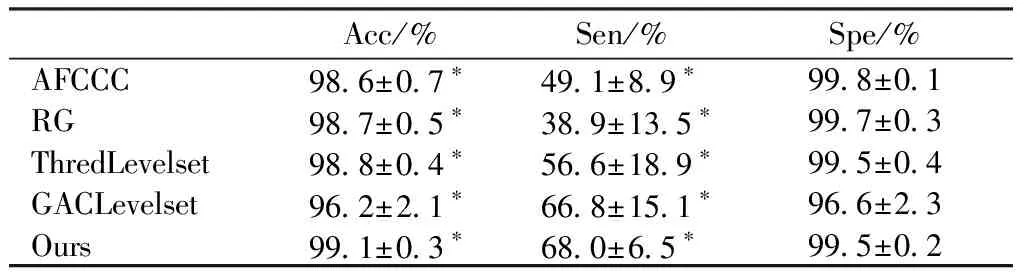
Acc/%Sen/%Spe/%AFCCC98.6±0.7∗49.1±8.9∗99.8±0.1RG98.7±0.5∗38.9±13.5∗99.7±0.3ThredLevelset98.8±0.4∗56.6±18.9∗99.5±0.4GACLevelset96.2±2.1∗66.8±15.1∗96.6±2.3Ours99.1±0.3∗68.0±6.5∗99.5±0.2
注:Acc-准确性; Sen-敏感性; Spe-特异性; AFCCC-基于置信连接度的模糊连接分割算法; RG-基于置信连接度的区域生长算法; ThredLevelset-阈值水平集算法; GACLevelset-测地线轮廓水平集算法; *满足置信区间0.95的显著性分析
Nate: Acc-accuracy; Sen-sensitivity; Spe-specificity; AFCCC-adaptive fuzzy connectedness based on confidence connectedness; RG-region growing based on confidence connectedness; ThredLevelset-Threshold level set segmentation; GACLevelset-Geodesic active contours segmentation; * A significant analysis that satisfies the confidence interval of 0.95

图8 不同算法的血管分割结果。AFCCC-基于置信连接度的模糊连接分割算法; RG-基于置信连接度的区域生长算法; ThredLevelset-阈值水平集算法; GACLevelset-测地线轮廓水平集算法 (以3Dircadb数据集的第8、14、16、17、18例CT图像为例)Fig.8 The segmentation results of liver vessels with different methods. AFCCC-adaptive fuzzy connectedness based on confidence connectedness; RG-region growing based on confidence connectedness; ThredLevelset-Threshold level set segmentation; GACLevelset-Geodesic active contours segmentation (No. 8, 14, 16, 17, and 18 of 3Dircadb dataset)

OursAFCCCRGThredLevelsetGACLevelset21.4±7.5190.7±214.7164.8±204.2192.5±104.1 182.4±124.5
4 讨论
本研究提出了一种针对肝血管的改进血管增强算法,并将该算法的响应引入模糊亲和度函数,经由基于Otsu多阈值算法的模糊连接度分割算法完成对肝血管结构的三维自动分割。经定量比较发现,本研究提出的血管增强算法和模糊连接度分割算法的性能都更加优异,本研究的算法具有以下优势:
1) 本研究改进的血管增强响应更加均匀,无论在同一根血管内部或是在不同血管分支中,且显著增强区域更接近血管的实际尺寸。
2) 本研究改进的血管增强算法能更好地抑制肝内部背景与噪声,为后续分割任务奠定基础。
3) 将均匀的血管增强响应引入模糊亲和度函数中,能够缓解模糊连接度分割算法因灰度层次过多导致的无法分割或分割残缺的现象,并降低了模糊分割算法对于种子点位置的敏感性。
4) 利用Otsu多阈值算法代替置信连接度算法作为模糊连接度分割的初始化,降低了模糊连接度算法因置信连接度参数敏感而出现显著的过分割或欠分割问题,也减少了置信连接度算法初始化的耗时。
5) 相比基于置信连接度的传统模糊连接度分割算法[21]、区域生长算法和水平集分割算法[22-23],本研究提出的肝血管三维分割方法能获得更高的分割精度。
基于模糊连接度算法的肝血管分割存在一定程度的孔洞现象[18,21],本研究发现,这种孔洞现象可能是由于待分割的前景区域内局部灰度差异显著造成的。基于增强CT图像IOri和对比度增强图像ISg的模糊连接度分割结果中都存在明显的孔洞现象,但这种现象在结合本研究血管增强算法的模糊连接度分割结果中却有明显改善,说明灰度值一致性高的血管增强响应缓解了模糊连接度分割算法的孔洞问题。血管内部的孔洞虽然可以通过孔洞填补算法进行修复,但增加了处理流程的运算量,且一旦孔洞现象出现在血管边缘,即使采用孔洞填补算法也难以弥补,因此从孔洞出现的根源处优化算法更具意义。

表4 种子点位置的敏感性分析Tab.4 Sensitivity analysis of the seed points location in segmentation processing
此外,由于本研究提出的模糊连接度分割算法还需借助一个种子点引导分割,因此这里有必要探讨种子点的敏感性问题。这里随机选取4组数据,将种子点人为选取在高阶血管、低阶血管和末梢血管中,分别对分割结果的准确性、敏感性和特异性进行定量评估,评估结果列于表4中,且将1组数据的分割结果绘成图9。可以看出,结合增强算法的模糊连接度分割几乎不受种子点位置的影响。

图9 血管分割流程中种子点敏感性分析。(a)~(c)种子点分别选在血管增强响应结果的主血管、分支血管和末梢血管中;(d)~(f)对应种子点的三维肝脏血管分割结果Fig.9 Sensitivity analysis of the seed position in liver vessel segmentation. (a)~(c) The seeds were selected in high-scale, low-scale and peripheral vessels; (d)~(f) The corresponding three-dimensional liver vessels segmentation results
本研究提出的分割算法还存在以下不足:对于某些对比度极低且尺寸远大于4 mm的血管结构分割并不完整 (见图10),其原因可能在于这一尺寸的血管结构远超出血管增强算法的尺度范围,在今后工作中将继续完善。本研究另一不足是实验数据量有限(20例),未来研究中,需采用更多的数据进一步验证本研究方法的性能。

图10 本研究血管分割方法的不足。(a)原始CT图像;(b)本研究算法分割结果与金标准的比较Fig.10 The drawback of our vessel segmentation method. (a) Original CT image; (b) Segmentation by the propose method (red) and the gold standard (green)
5 结论
本研究提出一种基于改进模糊连接度的CT图像肝血管三维分割算法,利用改进的血管增强算法响应代替增强CT图像灰度作为模糊连接度分割的输入,使用Otsu多阈值算法代替置信连接度对模糊连接度进行初始化,自动分割出完整的肝血管结构。实验结果表明:相比基于置信连接度的传统模糊连接度分割算法、区域生长算法和水平集分割算法,本研究的肝血管分割算法能够取得更高的分割精度和分割效率。在今后的工作中,可提取多种有效的血管特性,将其量化后结合血管特征响应一同融入模糊亲和度函数,有望获得更理想的血管分割结果。

