基于反冲洗铁泥制备的磁性吸附剂除砷及再生
曾辉平,尹灿,盛加宝,李冬,张杰,3
(1.北京工业大学 建筑工程学院,北京,100124;2.北京市市政工程设计研究总院有限公司,北京,100082;3.哈尔滨工业大学 环境学院,黑龙江 哈尔滨,150090)
砷是一种有毒、致癌的化学元素,长期饮用含砷水会引起皮肤、肝脏、膀胱、肾、肺等人体器官的病变[1]。世界卫生组织(WHO)给出的饮用水标准最大砷质量浓度限值为10 μg/L[2]。但有报道称,世界上超过20个国家和地区的地下水存在砷含量超标问题[3]。为保证人体健康,饮用水中砷的质量浓度必须严格控制,为此,混凝沉淀[4]、离子交换[5]、吸附[6]、膜过滤[7-8]、电化学[9]等众多的除砷技术应运而生。其中,吸附法以其高效的吸附性能、使用条件限制小、运行过程中无需额外投加药剂、操作简单等优点成为各大除砷技术中最有发展前景的方法[3]。在过去几十年的研究中,研究者们开发各种各样的除砷吸附剂并研究吸附性能,但是这些吸附剂往往使用纯化学药剂制备,有的成本很高,所以,人们开始致力于一些废弃材料的研究[10-12],一方面利用废弃物的吸附潜能以节约成本,另一方面可以为废弃物资源化提供一种新的途径。曾辉平等[13]指出,除铁锰水厂生物滤池产生的反冲洗含铁废弃污泥是一种很好的吸附剂,最大砷吸附量能达40.37 mg/g。但由于这种材料粒径小,导致其在吸附后很难从处理过后的水中分离出来,所以,在工程应用中具有局限性,OCINSKI等[14]也得到过类似的研究结果。鉴于此种反冲洗铁泥中有较高的铁含量,本研究采用溶剂热法将其成功制备成一种带有磁性的粉末吸附剂(magnetic powder adsorbent,MPA),可以用简单的磁装置收集,从而解决原材料细小粉末态吸附剂使用后与水分离困难的问题。另外,当吸附剂达到吸附饱和以后,为了保证高效的吸附能力需要更换新的吸附介质[15]。吸附介质的频繁更换以及大量废弃吸附剂的处理都会增加成本,因而,吸附剂能否再生和重复利用也是评估吸附剂性能的一个重要方面。所以,本文还系统研究磁性吸附剂的再生过程,以便为这种新型的磁性吸附剂找到再生的最佳条件,明确吸附剂的再生过程中性能变化,以期望制备的磁性吸附剂能够最大限度地开发利用价值,避免资源浪费。
1 材料与方法
1.1 主要仪器与主要试剂
原材料:除铁除锰水厂(进水总 Fe2+质量浓度为14.9 mg/L,Mn2+质量浓度为0.8~1.0 mg/L)稳定运行阶段生物滤池的反冲洗废水经自然风干、用研钵研磨后过直径为0.150 mm筛,得到反冲洗铁泥粉末。
主要试剂:砷测定过程中使用的硼氢化钾;氢氧化钠和硫脲均为优级纯;盐酸为分析纯。其他使用药剂如Na2HAsO4·7H2O、无水乙酸钠和乙二醇等均为分析纯,药品购自天津福晨化学试剂有限公司。
主要仪器:100 mL聚四氟乙烯内衬高压反应釜;DHG-9070A电热鼓风干燥箱(上海一恒科学仪器有限公司);THZ-82恒温振荡器(金坛市杰瑞尔电器有限公司);AFS-8230原子荧光分光光度计(北京吉天仪器有限公司);pHSJ-3F实验室pH计(上海仪电科学仪器股份有限公司);BRUCKER D8 X射线衍射仪(德国布鲁克公司);Versalab振动样品磁强计(美国Quantum Design公司);Nicolet IS10傅里叶转换红外线光谱分析仪(美国尼高力公司);电子分析天平,等。
1.2 磁性吸附剂的制备
将2 g反冲洗泥、10.8 g无水乙酸钠溶于60 mL乙二醇中,搅拌30 min后,将形成的悬浊液转入100 mL聚四氟乙烯内衬高压反应釜中,拧紧釜体,密封。随后,将反应釜放入烘箱,将烘箱升温至180℃恒温保持10 h。待反应釜自然冷却至室温,取出底部黑色沉淀,分别用无水乙醇和去离子水交替清洗,用磁铁分离,此过程重复5~8次。将所得产物置于干燥箱中,于60℃下干燥6 h,得到磁性粉末吸附剂MPA,制备流程如图1所示。
1.3 除砷实验
1.3.1 等温吸附实验
称取0.02 g MPA置于一系列250 mL具塞玻璃瓶中,加入100 mL初始质量浓度范围为0.1~40 mg/L的As(Ⅴ)溶液,利用盐酸和氢氧化钠调节pH至7.0±0.1。温度分别设置为25,35和45℃,以100 r/min的转速恒温振荡24 h,测定As(Ⅴ)的剩余质量浓度。吸附结束后再次测定溶液pH。
1.3.2 等电点测定实验
MPA吸附砷前后的等电点采用酸碱趋势法测定[14,16]。在一系列容量为 250 mL锥形瓶中加入100 mL浓度为0.1 mol/L的硝酸钠溶液和0.05 g MPA,调节pH至4~11,在25℃下以100 r/min的转速在恒温震荡箱中震荡吸附24 h至pH稳定,计算吸附前后pH的差值ΔpH。作初始pH和ΔpH的关系图,ΔpH=0时得到MPA的等电点pHpzc1,在此情况下吸附质不释放任何H+和OH-。同理,用吸附砷后的MPA重复以上步骤得到等电点pHpzc2。

图1 MPA制备流程Fig.1 Preparation flow chart of MPA
1.3.3 不同pH和离子强度下除砷影响实验
在一系列容量为250 mL锥形瓶中加入100 mL初始质量浓度为0.5 mg/L的As(Ⅴ)溶液,吸附剂投加量为0.2 g/L,溶液pH在3~10范围内,硝酸钠浓度离子分别采用1,5,10,50和100 mmol/L,在25℃条件下以100 r/min震荡吸附24 h后测定溶液剩余As(Ⅴ)质量浓度。
1.4 再生实验
1.4.1 再生前后吸附动力学实验
称取0.8 g MPA置于容量为1 L的聚乙烯瓶中,加入800 mL质量浓度为1 mg/L的As(Ⅴ)溶液,在25℃下以130 r/min的转速恒温振荡。自反应开始至24 h,以一系列不同的时间间隔取水样,每次1 mL,测定砷质量浓度。同理使用一次再生材料(MPA-1)、二次再生材料(MPA-2)以及三次再生材料(MPA-3)测定动力学。
1.4.2 不同氢氧化钠质量分数和脱附时间下的再生实验
将达到吸附饱和的 MPA进行再生。解吸再生过程吸附剂投加量为10 g/L,采用0.1%,0.5%,1%和2%这4种质量分数的氢氧化钠再生液,在25℃下以130 r/min的转速恒温震荡脱附7 h,每间隔一定时间取水样,测定砷质量浓度,计算脱附量。
1.4.3 不同温度下的再生实验
采用质量分数为 1%的氢氧化钠再生液,脱附温度在15~75℃范围内以10℃为间隔,每个温度下在以130 r/min的转速恒温震荡。震荡脱附3 h后取水样,测定水中砷质量浓度,计算脱附量。
1.5 固体废物的砷浸出实验
将5.7 mL 冰醋酸溶入去离子水中,定容至1 L,保持溶液pH为2.88±0.05,获得提取剂。按液固比为20∶1 L/kg加入提取剂和吸附剂,盖紧瓶盖后进行回旋震荡,调节转速为40~120 r/min,于25℃下震荡18 h取样,测砷质量浓度。
1.6 砷的测定与分析方法
实验所涉及的砷质量浓度均使用原子荧光光谱法测定。取10 mL上清液过0.45 µm滤膜后置于容量为100 mL容量瓶中,加入5 mL稀盐酸和10 mL硫脲定容至100 mL,用原子荧光光度计(AFS)测砷质量浓度。为增加准确性,测定2个平行样质量浓度取平均值,As(Ⅴ)的吸附量和脱附量计算公式如下。
吸附量:
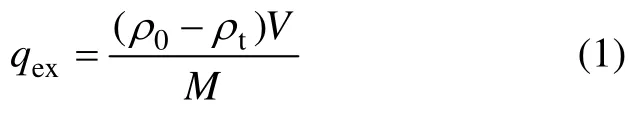
脱附量:

式中:qex和qet分别为单位吸附剂的吸附和脱附砷的质量分数,mg/g;ρ0为加入的待去除As(Ⅴ)的初始质量浓度,mg/L;ρt为 t时刻溶液中的As(Ⅴ)的质量浓度,mg/L;V为参加反应溶液的体积,L;M为在吸附过程中吸附剂MPA的质量,g。
2 结果与讨论
2.1 MPA表征
图2所示为MPA的X线衍射测定结果。将图谱中出现的特征衍射峰与各矿物标准 XRD图谱进行比对,可得MPA的主要磁性成分为磁赤铁矿即γ-Fe2O3。本实验原材料为取自除铁锰水厂生物滤池的反冲洗铁泥,其主要成分为无定形的羟基氧化铁并掺杂着其他水处理过程中截留去除的杂质[13],推测磁性物质形成过程如下:在溶剂热反应过程中,羟基氧化铁作为铁源,反应釜中形成的高温、高压密闭环境使乙二醇作为还原剂还原部分三价铁,同时在醋酸钠造成的碱性环境下二价铁与未反应的三价铁生成磁铁矿,在后续干燥过程中磁铁矿在氧化条件下经次生作用生成磁赤铁矿。反应式如下:

图2 MPA的XRD衍射图谱Fig.2 XRD pattern of MPA

在室温下测得MPA的磁滞回线如图3所示。MPA的磁滞回线呈现典型的“S”形,其饱和磁化强度为16.95 A·m2/kg。实验制备的磁性吸附剂材料在悬浮状态下短时间内不会完全沉降,但在外加磁场的作用下,磁性材料 MPA能够迅速地富集,水样变澄清,磁分离效果很好。
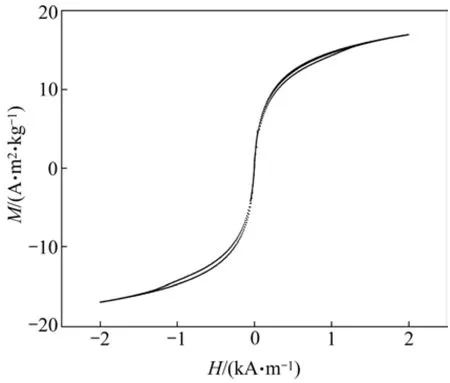
图3 MPA的饱和磁滞回线Fig.3 Hysteresis loops of MPA
2.2 MPA除砷性能
不同的初始砷质量浓度下往往吸附剂的吸附容量会有很大差别。吸附等温实验是计算吸附材料最大吸附容量的一种重要实验手段。实验将25℃下MPA对As(Ⅴ)的等温吸附测试结果用Langmuir模型(式(3))和Freundlich模型(式(4))进行拟合,得到曲线如图4所示,相关参数见表1。
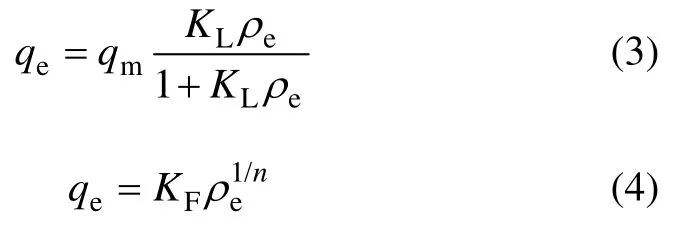
式中:qe为平衡吸附量,mg/g;ρe为平衡质量浓度,mg/L;qm为最大吸附量,mg/g;KL和 KF分别为Langmuir和Freundlich吸附常数。

图4 25℃时Langmuir和Freundlich方程拟合MPA的吸附等温线Fig.4 Langmuir and Freundlich Isothermal adsorption simulation at 25℃
Langmuir模型为单分子层理论吸附模型,而Freundlich模型经常用来描述不均匀表面的吸附,常为多层吸附[17]。从表1中得到的R2看,MPA对As(Ⅴ)的吸附过程与 Langmuir模型的拟合程度更高,说明As(Ⅴ)在MPA上的吸附与单层吸附理论更为契合。拟合得到 25℃下 MPA最大吸附量为 8.694 mg/g。对MPA在35℃和45℃下同样进行等温吸附实验,计算得到的 As(Ⅴ)最大吸附量为 10.005 mg/g和 13.400 mg/g,该结果表明温度升高对As(Ⅴ)的吸附有促进作用。另外,对吸附后的溶液 pH进行测定发现,吸附后溶液pH上升0.3~0.8。
2.3 MPA除砷机制探究
2.3.1 砷吸附前后MPA等电点的变化
在溶液为某一特定 pH时,会使得吸附剂解离出阴离子或阳离子的程度或趋势相当,吸附剂表面呈电中性,此时溶液的pH即为该物质的等电点pHpzc[18]。吸附前后等电点的变化是表征离子在吸附剂表面吸附类型的重要参数。图5所示为根据吸附砷前后的MPA得到的 pH-ΔpH曲线。未吸附砷前 MPA的等电点pHpzc1为 7.68。用吸附砷后的 MPA测试得到的 pHΔpH曲线与ΔpH=0轴的交点明显向左偏移,等电点pHpzc2降低为 7.18。阴离子的专性吸附会使吸附剂表面带上更多的负电荷,不同于静电吸附,这种专性吸附会导致吸附剂等电点的降低[19],故判断 As(Ⅴ)在MPA 上发生专性吸附。

表1 MPA的吸附等温线拟合参数Table 1 Isotherm parameters for arsenic adsorption on the MPA
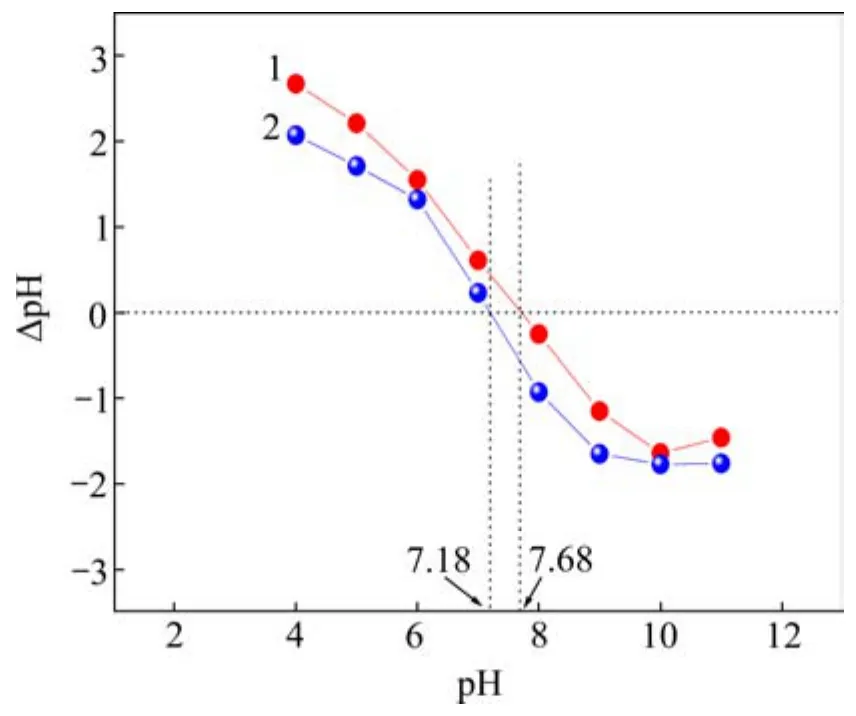
图5 吸附砷前后MPA的pH-ΔpH曲线Fig.5 Relationship between ΔpH and initial pH for determination of pHpzc before and after As(Ⅴ)adsorption
2.3.2 不同pH和离子强度下除砷效果及MPA的FTIR表征
不同pH和离子强度条件下MPA的除砷效果如图6所示。离子强度改变对吸附行为的影响可以用来判断被吸附离子在吸附剂表面的吸附络合物类型,从而提供砷吸附机理的信息。一般认为,形成外层络合物在宏观上表现为离子强度的增加会使砷吸附量减少,这是因为溶液中存在的其他离子可以通过同样的静电引力作用在吸附剂表面形成外层络合物,与砷竞争导致吸附量下降;而内层络合作用可以在各种表面上进行,不受制于吸附剂表面带有的电荷,形成的内层络合物表现为吸附量对离子强度并没有依赖性,反而可能由于溶液中的离子补偿了因专性吸附导致的表面电荷空缺而使吸附容量增大[19]。从图6可以看出:除少量异常外,当硝酸钠浓度从 1 mmol/L升高到100 mmol/L时,As(Ⅴ)的吸附容量均呈逐渐升高趋势。这表明As(Ⅴ)在MPA表面形成内层络合物,内层络合物以共价键或离子键结合,相比于外层络合物更加稳定。这与 MPA吸附砷前后等电点的偏移呈现的结果相一致。
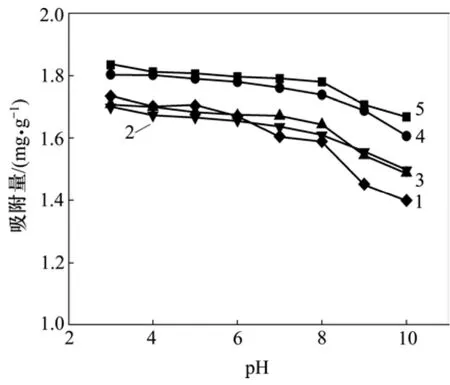
图6 不同pH下硝酸钠浓度对MPA除砷的影响Fig.6 Influence of NaNO3 concentrations on MPA’s arsenic removal efferent under different pH
另外,在等温吸附实验中发现,吸附砷后的溶液pH均有一定程度升高。PECINI等[20]认为,砷酸盐能够取代金属氧化物表面的—OH或水分子,以配体交换的方式形成内层复合物。所以,为进一步明确MPA的除砷机理,对吸附砷前后的MPA 进行FTIR表征(如图7所示),并分析其官能团组成和成键结构。从图7可以看到:吸附砷前的MPA在波长3 386.37 cm-1处的峰为羟基的伸缩振动峰,在1 628.64 cm-1处的峰为羟基的弯曲振动峰,波长452.21 cm-1处的峰为FeOOH的吸收峰,1 400.62 cm-1处的峰为羧基的振动峰。显然,溶剂热法制备的以磁赤铁矿为主的 MPA存在有多种表面羟基,它们是能发生离子交换的重要结构,且有一些未转化的 FeOOH也能发挥吸附效能。吸附砷后,3 386.37 cm-1和1 628.64 cm-1处振动峰的降低,且1 400.62 cm-1处的羧基振动峰减弱,此外,在波长876.04 cm-1处显现出微弱的As—O键伸缩振动峰,这是吸附过程中含羟基结构与 As(Ⅴ)结合在 MPA表面形成砷酸铁所致[21-22]。由此判断 MPA同大部分金属氧化物一样,其表面的—OH2或—OH与 As(Ⅴ)进行离子交换并络合形成Fe—O—As键,发生专性吸附,吸附后溶液 pH升高与—OH被砷酸盐取代进入溶液中有关。
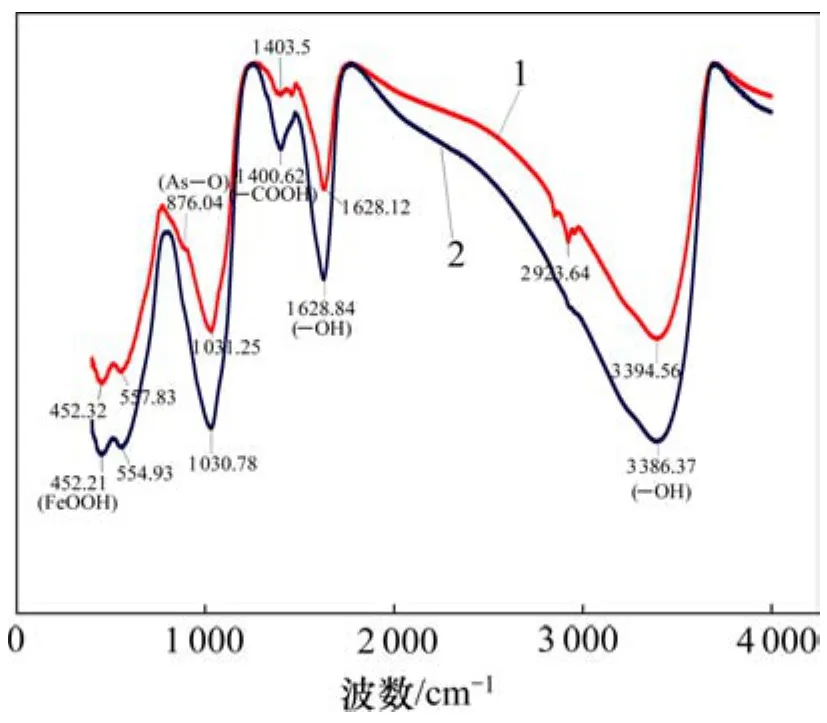
图7 吸附砷前后MPA的FTIR表征图Fig.7 FTIR characterization diagram of MPA before and after As(Ⅴ)adsorption
2.4 MPA再生性能
在除砷性能测试中发现,砷在极碱性环境中会与氢氧根离子发生竞争而不能与 MPA顺利发生吸附反应。利用此原理,本文使用的再生液选用不同质量分数的氢氧化钠溶液,用来对吸附到 MPA上的砷进行解吸,并探讨和研究其过程。
2.4.1 不同氢氧化钠质量分数下 MPA的砷解吸及再吸附效果
图8所示为不同再生液质量分数下MPA解吸砷的量及再吸附效果。从图8(a)可以看出:砷的脱附量随着时间的延长逐渐增大,到7 h时4种再生条件下的砷解吸量均已达到平衡,而且在脱附时间为 0.5 h时已经有很大一部分砷被脱附下来,随后的脱附量随时间缓慢变化直至达到平衡。其原因可能是再生开始时吸附于 MPA表面的砷很快被脱除,但分布于孔隙中的砷需要经过缓慢迁移才能进入再生液。但是不难发现,砷的脱附量与使用的氢氧化钠再生液质量分数有很大的关系。质量分数为0.1%,0.5%,1.0%和2%的氢氧化钠再生液达到的砷脱附量分别为 0.409,0.504,0.607和0.618 mg/g,即再生液质量分数越高,解吸下来的砷越多。但氢氧化钠质量分数为1%和2%时达到的脱附量已经非常接近,说明此时再增加氢氧化钠的质量分数对砷的脱附不会再有很大的影响。CHEN等[15]在实验中也得到相似的结论:随着氢氧化钠升高到一定浓度后,砷的脱附效率趋于稳定,再增加氢氧化钠的浓度不会得到更高的砷脱附率。另一方面,并非所有的被吸附的砷都能被解吸下来,氢氧化钠质量分数为0.1%,0.5%,1.0%和2.0%时的解吸率分别为56.08%,69.15%,83.34%和84.81%。
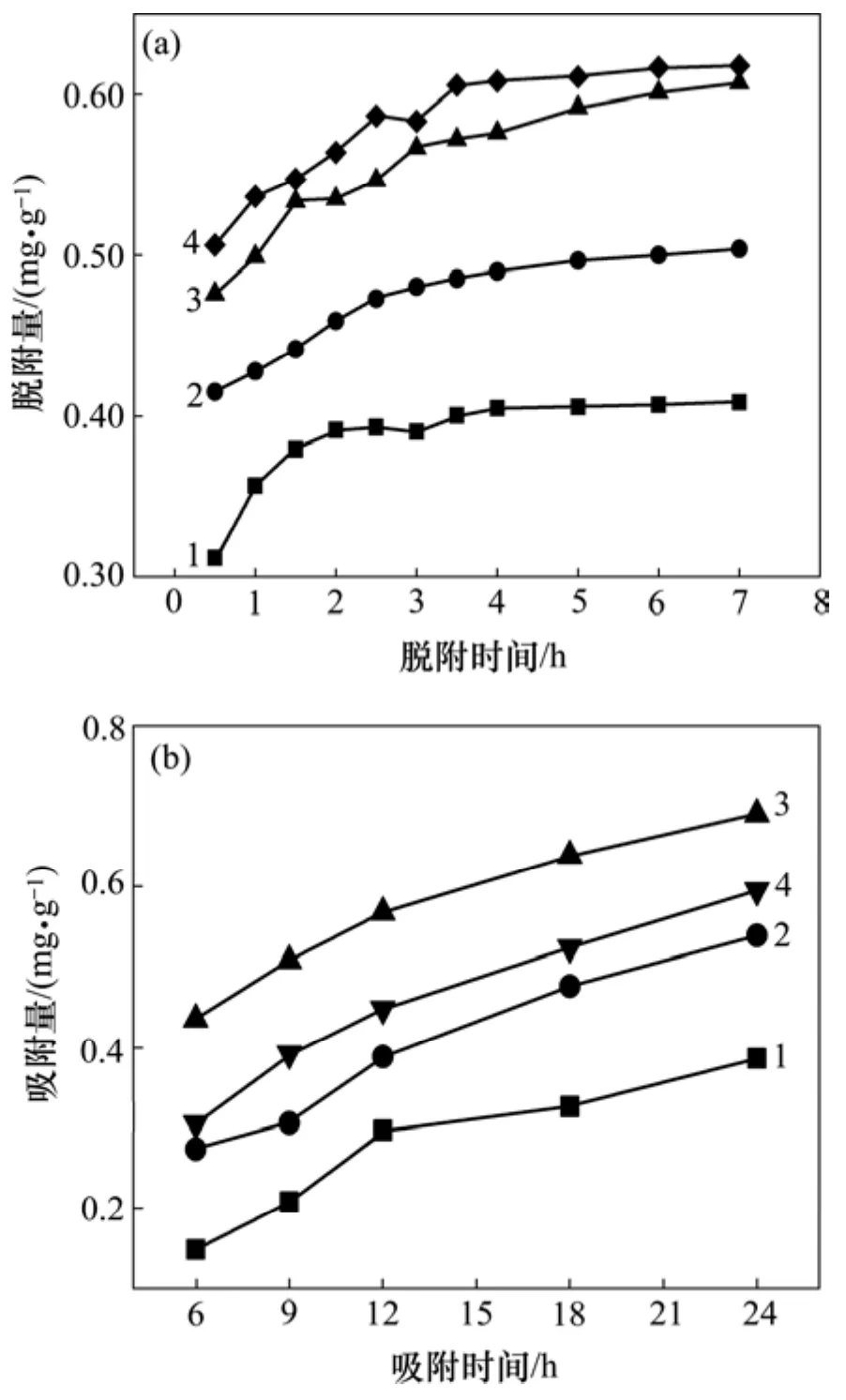
图8 脱附和吸附特征Fig.8 Characteristics of desorption and adsorption
用 4种不同质量分数的氢氧化钠再生后的 MPA再次进行吸附实验,在不同的吸附时间下吸附量如图8(b)所示。从图8(b)可以看出:氢氧化钠质量分数的第 2次吸附效果从好变差依次为 1.0%,2.0%,0.5%和0.1%,且在6,12和24 h的吸附时间下均得到一致的结果。这可能是由于随着再生液质量分数从0.1%增长到1.0%,解吸下来的砷逐渐变多,故吸附剂上空出的砷吸附位点变多,所以,吸附效果呈现出氢氧化钠质量分数从1.0%到0.5%再到0.1%依次变差。但再生液质量分数升高到2.0%,推测更强的碱性环境可能改变了 MPA的表面结构性质,不利于发生吸附,而且空的吸附位点并没有显著增多,导致其吸附效果并没有很大提升。故再生液中氢氧化钠的质量分数对MPA的再生性能有重要的影响,在当前实验条件下,质量分数为1.0%的氢氧化钠再生效果最佳。
2.4.2 不同温度下砷的解吸
因为氢氧化钠质量分数在 1.0%时脱附效果较好且再增加质量分数脱附效果并未有显著增强,所以,选用质量分数为1.0%的氢氧化钠作为再生液。在一系列温度下进行脱附实验研究,结果如图9所示。从图9可见:脱附量随温度的升高存在一个先升高后降低的变化过程,最佳脱附温度为55℃左右。升高温度有利于吸附的砷从吸附剂上脱附下来[19],所以,在15~55℃内脱附量逐渐增加。但从温度对吸附效果的影响实验结果来看,随着温度升高,吸附过程的推动力也增加,脱附下来的砷会很快又被吸附到 MPA表面,因而在65℃和75℃时脱附量反而下降。

图9 不同温度下As(Ⅴ)的脱附量Fig.9 As(Ⅴ)desorption at different temperatures
2.4.3 再生次数对吸附动力学的影响
为了更好地研究MPA再生后的吸附性能的变化,使用原材料MPA和经质量分数为1%的氢氧化钠再生液、1次再生材料MPA-1,2次再生材料MPA-2及3次再生材料MPA-3分别进行吸附动力学研究,结果如图10所示。再生后的MPA在吸附前期(前6 h)反应速率更快,这很可能是由于再生过程改变了 MPA内部孔道结构,使一些吸附位点裸露出来,从而使 MPA的结构更有利于吸附。但再生材料在24 h时的吸附容量呈现下降趋势。对4个周期的动力学使用准一级动力学(式(5))和准二级动力学(式(6))进行拟合,拟合得到的参数见表2。
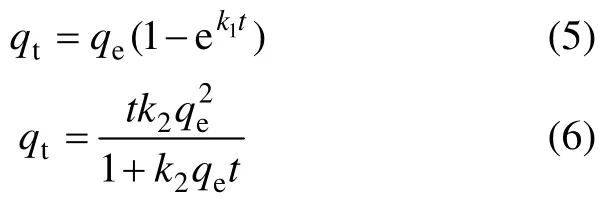
式中:t为反应时间,h;qt为在t时刻MPA吸附砷的量,mg/g;qe为吸附平衡时MPA吸附砷的量,mg/g;k1和k2分别为准一级和准二级动力学方程的速率常数。

图10 MPA再生前后吸附动力学曲线Fig.10 Adsorption kinetic curve of MPA before and after regeneration
研究发现,这4种材料对As(Ⅴ)的吸附过程均与准二级动力学模型拟合更好,说明再生前后的 MPA对 As(Ⅴ)的整个吸附过程中化学吸附起关键性作用[16]。由准二级动力学模型计算的理论平衡吸附量qe发现再生后的吸附容量会逐渐降低,这与实际实验中所观察到的结果一致。正如2.4.1节论证,再生液的处理并不能使吸附到 MPA上的砷完全脱附下来,仍有一部分吸附位点被砷占据,所以,再生次数的增加会导致砷的饱和吸附量越来越低。3次再生后吸附量能够保持初始吸附量的71.1%。
2.5 砷浸出试验
MPA多次使用后必然会耗尽吸附性能。水处理中废弃吸附剂通常会被作为固体废物进行填埋处理,为模拟使用后的 MPA固体废弃物中的砷在填埋场环境中的迁移,参考 TCLP(toxicity characteristic leaching procedure)方法进行砷浸出实验。不同振荡频率下MPA吸附废物中的As(Ⅴ)浸出实验结果如图11所示。

表2 动力学模型拟合参数Table 2 Parameters of kinetic models

图11 不同振荡频率下MPA固体废弃物的砷浸出质量浓度Fig.11 As(Ⅴ)mass concentration leached from MPA waste at different rotating speeds
显然,转速提高会增大固体颗粒相互之间以及与水分子之间推动力,促进离子脱落,故浸出的砷质量深度也相应略有升高。根据危险废物浸出毒性鉴别标准(GB 5085.3—2007),浸出液中危害成分砷的质量深度不得超过5 mg/L,但由图11知,在所有转速下浸出的砷质量深度均远远低于此限值。因此,As(Ⅴ)离子在MPA上的结合很牢固,耗尽吸附性能的MPA可以直接进行填埋处理而对环境影响不大。
3 结论
1)以铁泥为原料,乙二醇为溶剂、通过添加无水乙酸钠在高压反应釜中进行溶剂热反应制备磁性粉末吸附剂MPA,MPA对As(Ⅴ)的吸附过程与Langmuir单分子层等温吸附模型更为契合,25,35和45℃时拟合得到的最大吸附量分别为8.694,10.005和13.400 mg/g。
2)MPA吸附砷后的零电点降低,从 7.68降为7.18。随着离子强度的增加,砷的去除率升高。
3)使用质量分数为0.1%,0.5%,1.0%和2.0%的氢氧化钠溶液作为再生液对砷进行解吸再生,质量分数 1.0%时效果最佳,超过 1.0%后解吸率并不会有明显增加且会降低再生材料的再吸附效果。在15~75℃范围内的解吸实验中,55℃时的解吸率最高。
4)MPA经3次再生后仍具有较强的吸附能力,仍能够保持初始吸附量的 71.1%,再生材料对砷的吸附速率变快但最终吸附量逐渐下降。在模拟垃圾填埋场环境下,吸附在 MPA上的 As(Ⅴ)不易溶出,对环境影响不大。

