岷江流域全氟化合物的污染特征及排放通量
方淑红,李 成,卞玉霞,王 迪,郝云庆,印红玲,孙 静
岷江流域全氟化合物的污染特征及排放通量
方淑红*,李 成,卞玉霞,王 迪,郝云庆,印红玲,孙 静
(成都信息工程大学资源环境学院,四川 成都 610225)
采用超高效液相色谱串联质谱分析了四川省岷江流域水体中13种全氟化合物(PFASs)的浓度水平.结果表明,岷江流域水相中PFASs的浓度为1.54~30.2ng/L,平均值为(11.2±8.0) ng/L,浓度最高点出现在乐山下游(30.2ng/L).其中,岷江流域水相中最主要的PFASs为全氟丁烷羧酸(PFBA),浓度为0.16~28.4ng/L,占总全氟化合物的54.0%~94.1%(都江堰除外).岷江流域沉积物中PFASs浓度最高点在宜宾三江(岷江、金沙江和长江)汇合处(47.5ng/g dw),最低值在都江堰(0.334ng/g dw).其中,主要的PFASs是全氟己烷羧酸(PFHxA) (4.44%~66.9%)和全氟辛烷羧酸(PFOA) (1.52%~77.5%).岷江流域PFASs的年排放通量为1.443t/a,排放通量最高的为PFBA(1.037t/a),占总排放通量的71.9%.
全氟化合物;岷江;污染特征;排放通量
全氟有机化合物(PFASs)是化合物分子中的碳原子所连接的氢原子全部被氟原子取代的一类有机化合物的统称.由于其特殊的化学特性,因而被广泛应用于纺织、造纸、包装、农药、地毯、皮革、地板打磨、洗发香波和灭火泡沫等工业和民用领域[1].目前,PFASs几乎在所有的环境介质和生物体中均有检出[2-7].研究表明,PFASs可以沿食物链发生生物富集[8-9],并且对生物体有一定的毒性作用[10],因此,引发了国际上学术界和公众的广泛关注.全氟辛烷磺酸(PFOS)及其盐类和全氟辛基磺酰氟(PFOSF)被列入新增的POPs名单中.我国也制定出相应的措施,要求到2020年基本淘汰PFOS/F.
PFASs在环境中的迁移方式之一是水体传输,并且水体是PFASs在环境中的一个汇.虽然PFASs已被管控,但是由于沉积物是PFASs的蓄积库,随着时间的推移,会向水相分配,给水体带来二次污染.因此,研究PFASs在水环境中的浓度水平和分布,对了解PFASs的污染特征非常重要.
目前,我国对于环境中PFASs的调查研究主要集中在东部及南部地区的流域,如珠江、长江中下游、淮河、海河、辽河等水体[11-14],而对西南地区水体中PFASs的污染现状则鲜有报道.岷江作为四川境内的主要河流之一,是四川省成都平原最重要的水资源.而针对岷江流域中PFASs污染特征的研究仍处于空白阶段.因此,本研究选取岷江流域作为研究对象,分析水相及沉积物中PFASs的污染水平及分布特征,估算岷江每年向长江输出的PFASs通量,为科学管控PFASs提供基础数据.
1 材料与方法
1.1 样品采集
岷江流域从都江堰市被都江堰引水工程分为内外江,外江为干流,经过新津、彭山、乐山市,到宜宾汇入长江.都江堰以上为岷江上游,而岷江上游为松潘、茂县、汶川等地,少有工业污染,因此,本研究从都江堰开始采样(即岷江中下游),沿途有新津、彭山、乐山和宜宾.样品采集于2016年10月,具体采样位置见图1.采样前采样工具(均为不锈钢材质)和聚丙烯样品瓶均用甲醇和超纯水进行清洗并干燥.采集水样为表层水,每个点位采集1.5L,保存于聚丙烯瓶中.每个点位采集表层沉积物200g,保存于铝箔纸中,运回实验室,冷冻干燥后,研磨过100目筛子,-4℃保存.
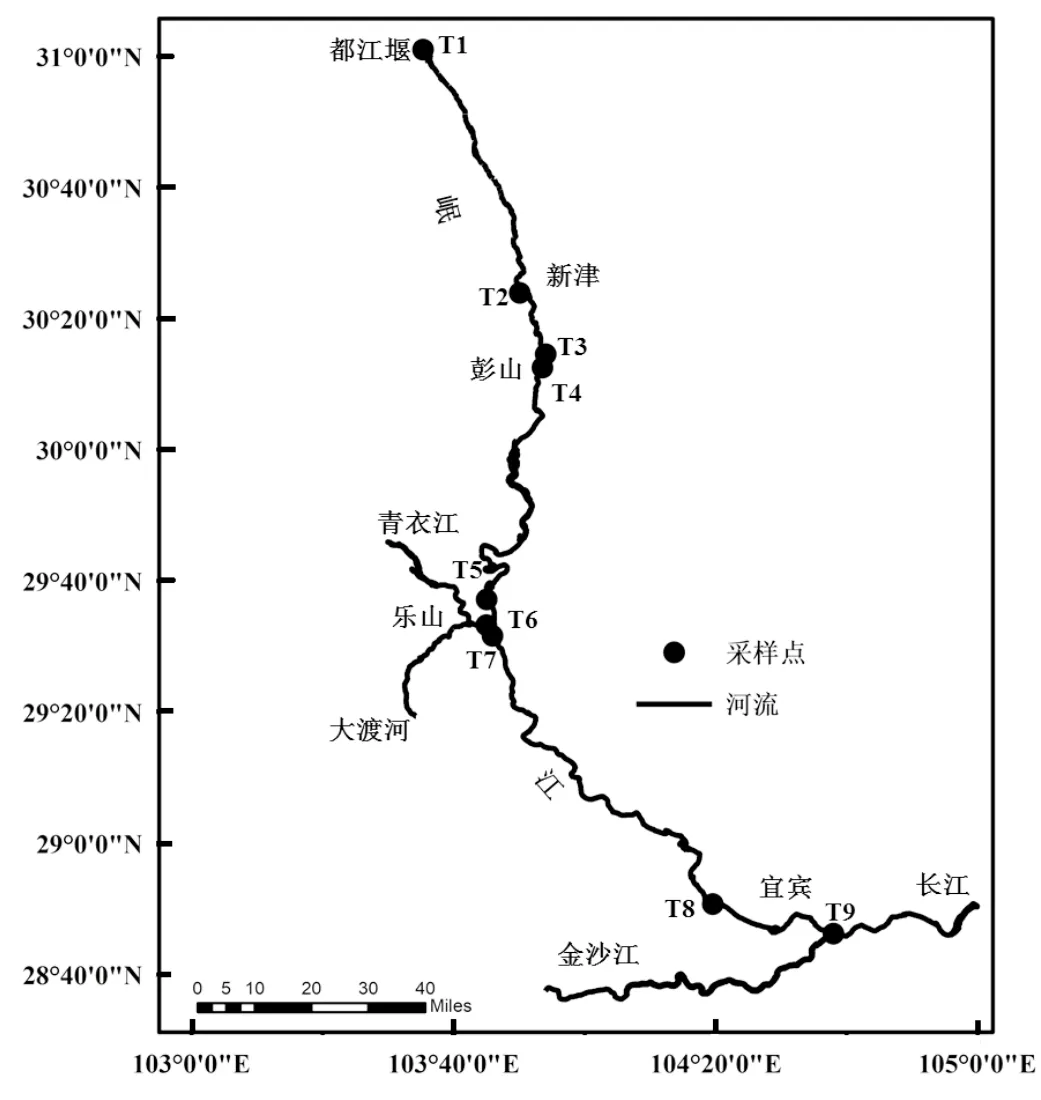
图1 岷江中下游采样点位分布
1.2 标准样品与试剂
本研究中的标准样品为高纯度混合标准品PFAC-MXB(Wellington公司),含有全氟羧酸类和全氟磺酸类化合物.其中,羧酸类包括:全氟丁烷羧酸 (PFBA),全氟戊烷羧酸(PFPeA),全氟己烷羧酸(PFHxA),全氟庚烷羧酸(PFHpA),全氟辛烷羧酸(PFOA),全氟壬烷羧酸 (PFNA),全氟癸烷羧酸(PFDA),全氟十一烷羧酸 (PFUnDA),全氟十二烷羧酸(PFDoDA).磺酸类包括:全氟丁烷磺酸(PFBS),全氟己烷磺酸(PFHxS)、全氟辛烷磺酸(PFOS)和全氟癸烷磺酸(PFDS).PFAC-MXA为高纯度混合碳同位素标记品:13C4-PFBA,13C2-PFHxA,13C4-PFOA,13C5-PFNA,13C2-PFDA,13C2-PFUnA,13C2-PFDoA,18O2-PFHxS和13C4-PFOS.
本研究使用的主要实验试剂包括甲醇(分析纯/99.5%、色谱纯/99.8%,成都市科隆化工试剂厂)、氨水(25%,成都市科隆化工试剂厂)、Milli-Q超纯水.
1.3 样品前处理方法
水样和沉积物预处理参照Chen等[15]的方法.所有水样处理前,均需0.45μm的尼龙滤膜进行过滤,去除悬浮颗粒物.将过滤后的水样用Cleanert PEP固相萃取柱(500mg/6mL,天津博纳艾杰尔科技有限公司)富集并纯化,每个点位2~3个平行样.具体操作如下:分别用10mL甲醇和10mL超纯水对固相萃取柱进行活化.活化完成后,取500mL过滤后水样(加入2ng内标)以1滴/s的速度过萃取柱.萃取完成后平衡1h,然后用5mL 20%的甲醇/H2O溶液去除杂质,最后用10mL甲醇溶液洗脱目标化合物至15mL离心管中.洗脱液氮吹近干,用0.6mL甲醇和0.4mL H2O复溶,过0.22μm尼龙针头过滤器,转移至样品瓶中,于-18℃下保存,等待上机测样.
沉积物处理步骤如下:准确称取约5.0g沉积物(每个点位2~3个平行样品),置于50mL PP材质的离心管中,加入2ng内标,涡旋混合均匀,放置过夜.加入5mL甲醇,超声萃取15min,4000r/min下离心5min,上清液转移到新的15mL PP离心管中.重复上述萃取步骤3次.萃取液合并,氮吹至1mL左右,用Milli-Q水稀释至100mL,过Cleanert PEP固相萃取柱富集纯化.洗脱液氮吹近干,用0.6mL甲醇和0.4mL H2O复溶,过0.22μm尼龙针头过滤器,转移至样品瓶中,于-18℃下保存待分析.
1.4 仪器分析方法
本研究采用安捷伦超高效液相色谱-三重四级杆串联质谱仪(1290-6470),C18色谱柱(Zorbax SB-C18, 2.1mm´50mm,1.8μm)对目标化合物进行定性和定量分析,柱温维持在35℃.仪器进样量为5μL,在水(5mmol/L的醋酸铵,A相)和甲醇(B相)二元流动相的作用下进行分离,流速为0.4mL/min,流动相梯度如下:0.00~0.10min,A相比例为90%;0.10~ 6.00min,A相比例由90%降为5.00%;6.00~8.00min,A相比例为5.00%,保持2min.质谱条件为:采用电喷雾离子源,负离子模式(ESI),多反应离子监测(MRM)模式分析;雾化气压力0.24MPa;电喷雾电压3000V;干燥气温度250℃.
1.5 质量保证和质量控制
为了避免污染,样品在采集过程中和前处理过程中都避免接触和使用玻璃以及聚四氟乙烯容器.前处理过程中,每12个样品设置2个方法空白;为了监测仪器的污染状态,在测样过程中,每20个样品设置1个溶剂空白.
本研究的方法检出限(MDLs)定义如下:1)对于没有在空白样品中检测出的PFASs,其MDLs值为3倍信噪比时的浓度;2)对于在空白样品中检测到的PFASs,其MDLs值为空白样品中浓度的均值加上3倍的标准偏差.如表1所示,水样的方法检出限为0.12~112pg/L,沉积物方法检出限为0.004~0.212ng/g dw.
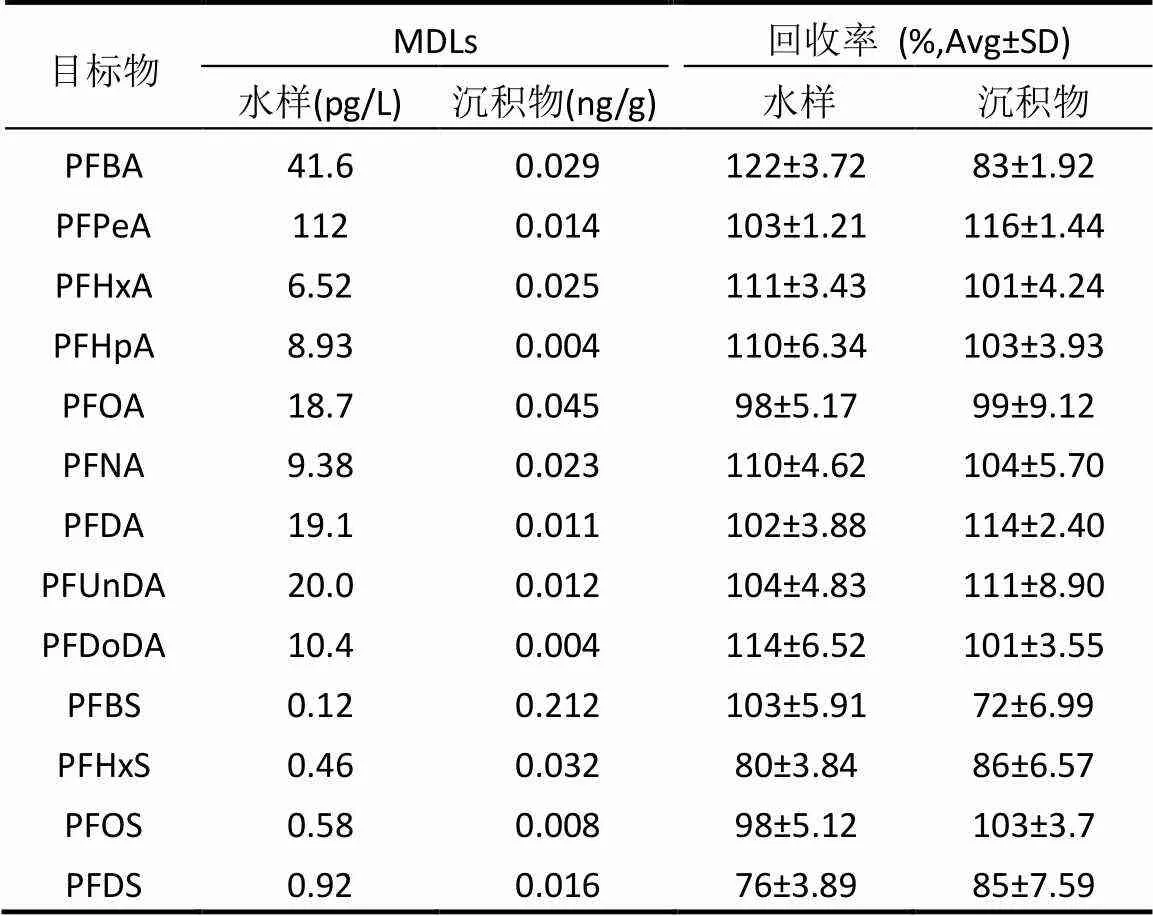
表1 PFASs在水和沉积物中方法检出限及回收率
本研究分别在沉积物中进行了5ng/g、水中为5ng/L的回收率实验.表1分别列出了PFASs在水和沉积物中的回收率(各5个平行样品),结果显示,水样中PFASs的回收率为76%~122%,沉积物回收率为72~116%,回收率结果较好,无需对结果进行校正.
1.6 数据分析
2 结果与讨论
2.1 岷江流域水相中PFASs的污染特征
PFASs在岷江流域水相中的浓度为1.54~ 30.2ng/L,平均值为(11.2±8.0) ng/L(图2).其中浓度最高的采样点位于乐山下游,为30.2ng/L,然后依次为乐山市区(14.7ng/L)>新津(14.5ng/L)>宜宾市区(12.1ng/L)>宜宾上游(11.3ng/L)>乐山上游(7.25ng/L)>彭山市区(5.26ng/L)>彭山上游(4.57ng/L)>都江堰(1.54ng/L).都江堰PFASs浓度最低,是由于岷江流域流经龙池国家森林公园到达都江堰,在此之前为岷江上游,几乎没有工业污染,人为活动对该流域水体带来的影响较小.而乐山、新津、宜宾3个城市,PFASs浓度水平较高,且下游地区高于上游地区,说明城市生活和工业污染是岷江水体中PFASs的主要来源.乐山、新津和宜宾均有不同大小的工业园区,其中涉及到纺织、电子厂、食品加工厂等,而PFASs被广泛应用于纺织材料、电子产品、防火材料和汽车等产品中.乐山地区最典型,在下游地区的浓度(30.2ng/L)要显明显高于上游地区(11.3ng/L).周珍等[16]和Sun等[17]的研究结果显示污水处理厂进水和出水中PFASs浓度变化不大,说明现有的污水处理工艺对PFASs去除效果并不明显.因此,工业废水或者生活废水中的PFASs会进入地表水,从而导致岷江在新津、乐山和宜宾河段中的PFASs浓度较高.
13种PFASs在岷江水样中均有检出,说明PFASs在岷江流域的广泛存在.其中PFBA、PFHxA、PFOA和PFDA的检出率为100%,其次为PFHpA (89%)和PFBS(89%),长碳链的PFUnDA、PFDoDA和PFDS的检出率较低,分别为22%、11%和22%,说明水相中较常见的PFASs为中短碳链的化合物(C<10),而长碳链的PFASs在水相中并不常见.如图3所示,在岷江流域水相中,最主要的PFASs为PFBA,浓度为0.16~28.4ng/L,除都江堰外(11.9%),均占总全氟化合物的50%以上(54.0%~94.1%).其次为PFOA,浓度为0.07~0.98ng/L,比例为0.47%~ 40.0%.除都江堰外,其它点位PFASs的污染特征较为相似(图3),说明其它地区水体中PFAS的污染来源相近.而都江堰最主要的PFASs是PFOA为(0.54±0.22) ng/L,占∑PFASs的40.0%.现有的研究结果表明,8:2PFOH可以在大气中发生迁移并且能够降解为PFOA[18-19].这可以解释都江堰虽然远离工业区,而水体中却仍检测出一定浓度的PFOA.
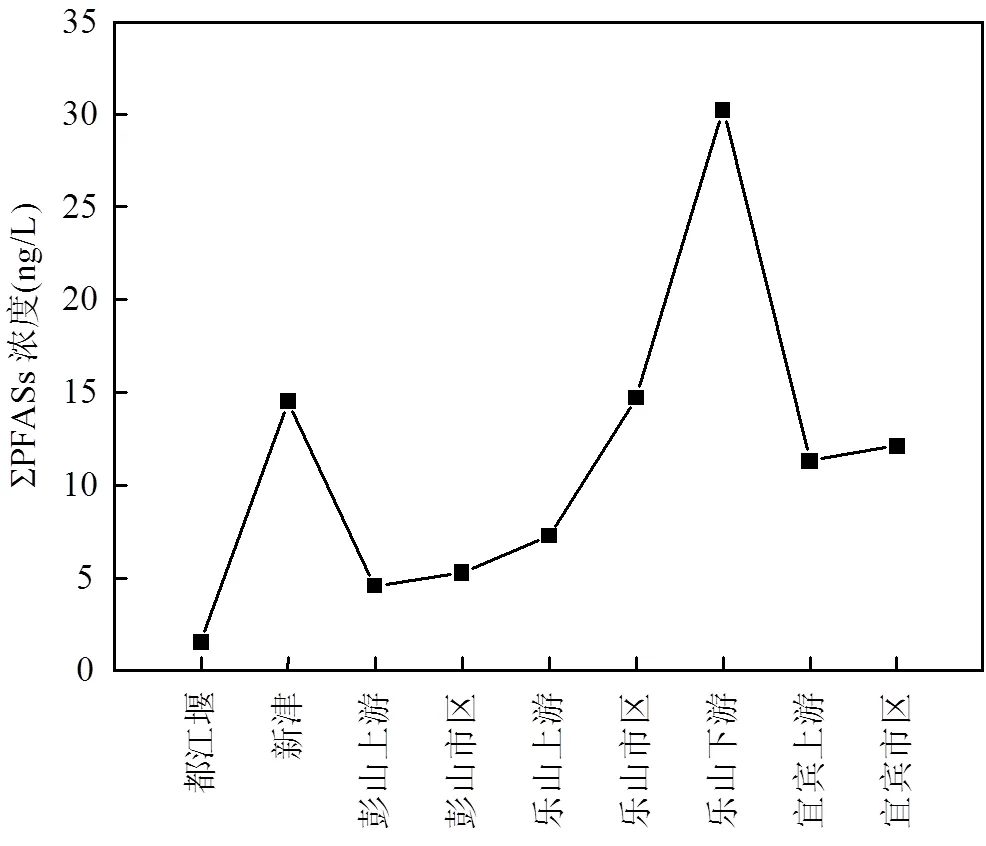
图2 岷江流域水相中PFASs的浓度水平
汉江武汉段水体中[16]∑PFASs浓度为4.11~ 4.77ng/L,以PFBS和PFHxS 为主,其次是PFBA.拉萨河表层水中∑PFASs浓度为0.006~1.724ng/L,主要污染物为PFBA, 其次为PFPeA[20].大运河∑PFASs浓度范围为7.4~153.5ng/ L(平均40.5ng/L),南方河段大部分以PFOA为主,而北方河段PFOA主导性降低,短碳链的PFASs的比例升高[21].双台子河口(辽东湾)短链的PFBA 和PFPeA 是水体样品中的主要污染物,浓度分别介于8.17~82.03ng/L和17.58~ 105.77ng/L[22].钱塘江(杭州段)∑PFASs的浓度水平为0.98~122ng/L,主要污染物为PFOA、PFHxA、PFBA及PFHpA,而长链的化合物如PFUnDA、PFDoDA、PFTrDA、PFTeDA 等均未在样品中检出[23].加拿大瑞瑟鲁特湖中PFASs的浓度水平为0.112ng/L,主要污染物为短碳链的PFHxA和PFHxS[24].欧洲莱茵河表层水中PFASs浓度为0.35~621ng/L,PFBA和PFBS是主要污染物[25].通过比较可以看出,岷江流域中PFASs的浓度水平高于汉江、拉萨河及加拿大瑞瑟鲁特湖,低于双台子河口、钱塘江、大运河及莱茵河.短碳链的PFASs在不同流域水体中占主导因子,说明近年来PFASs的生产和使用正在从长碳链向短碳链转变.由于长碳链的PFASs具有较强的生物富集能力及生物毒性[9-10],美国国家环保署已于2010年宣布,到2015年逐步消除PFOA及长碳链的PFCAs[26].另外,我国也将短碳链的PFASs及C6调聚物作为PFOA(C8)替代品,应用于油墨、灭火剂、半导体材料灭火剂等领域,从而导致近年来短碳链PFASs在环境中呈现出较高的浓度和比例.
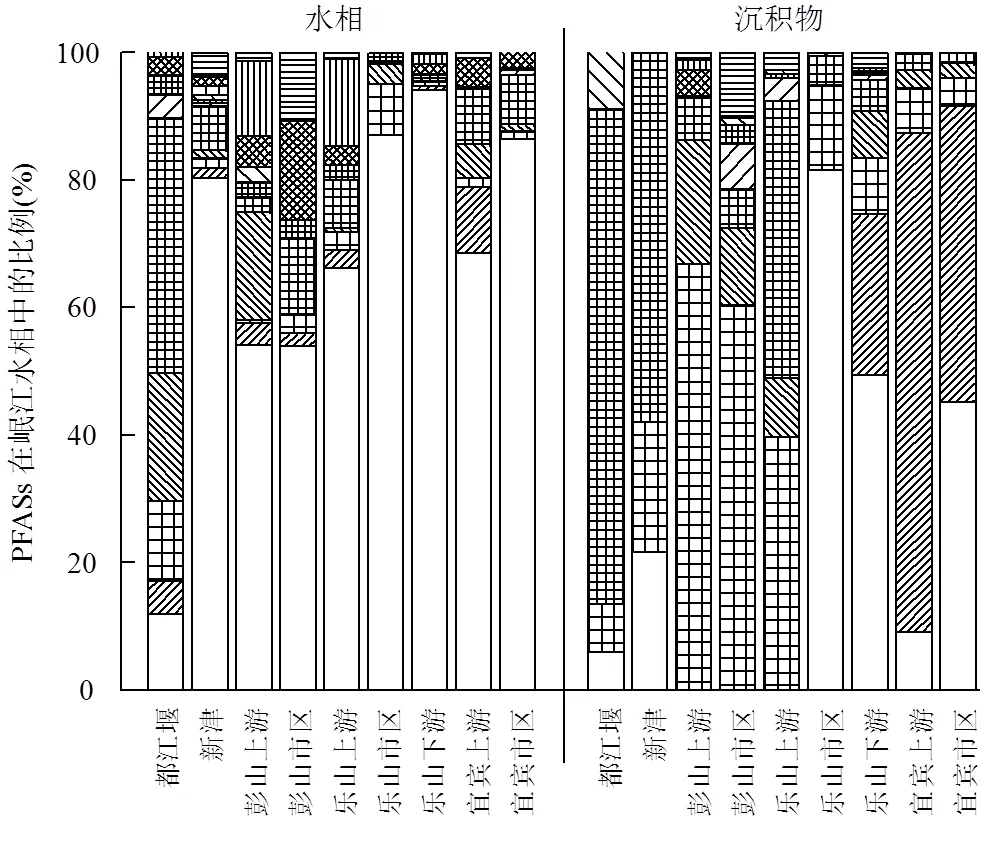
图3 岷江水相及沉积物中PFASs的比例特征

2.2 岷江流域沉积物中PFASs的污染特征
如图4所示,沉积物中∑PFASs的浓度范围在0.334~47.5ng/g dw之间,平均浓度为(13.2±14.4) ng/g dw.除PFDS和PFDoDA外,其它11种PFASs在岷江流域均有不同程度的检出.其中,检出频率最高的是PFHxA和PFOA,在所有样品中均被检出;其次为PFHpA(78%)和PFNA(78%).另外几种短碳链的PFASs的检出频率,如PFBA(67%)、PFPeA (33%)和PFBS(22%),相较于水相中的检出率均有所降低(PFBA:100%;PFPeA:78%;PFBS: 89%).这是由于PFASs的碳链越短,其ow值越小[27],因而不容易向有机质中分配,从而导致沉积物中检出频率低于水相.
岷江流域沉积物中主要的PFASs是PFHxA,占总PFASs的4.44%~66.9%;其次为PFOA,占总PFASs的1.52%~77.5% (图3).值得关注的是,虽然PFBA和PFPeA的检出频率并不高,但是在乐山及宜宾河段呈现出较高的浓度,且市区浓度明显高于上游浓度.其中PFBA在乐山上游未检出,市区和下游的浓度分别为11.7ng/g dw(占比81.5%)和8.87ng/g dw(占比49.3%);在宜宾上游为2.17ng/g dw(占比9.03%),市区为21.4ng/g dw(占比45.1%).这说明乐山和宜宾市区有PFBA的污染源,如涂料和油漆助剂、化妆品助剂等通过大气或者水体进入岷江.
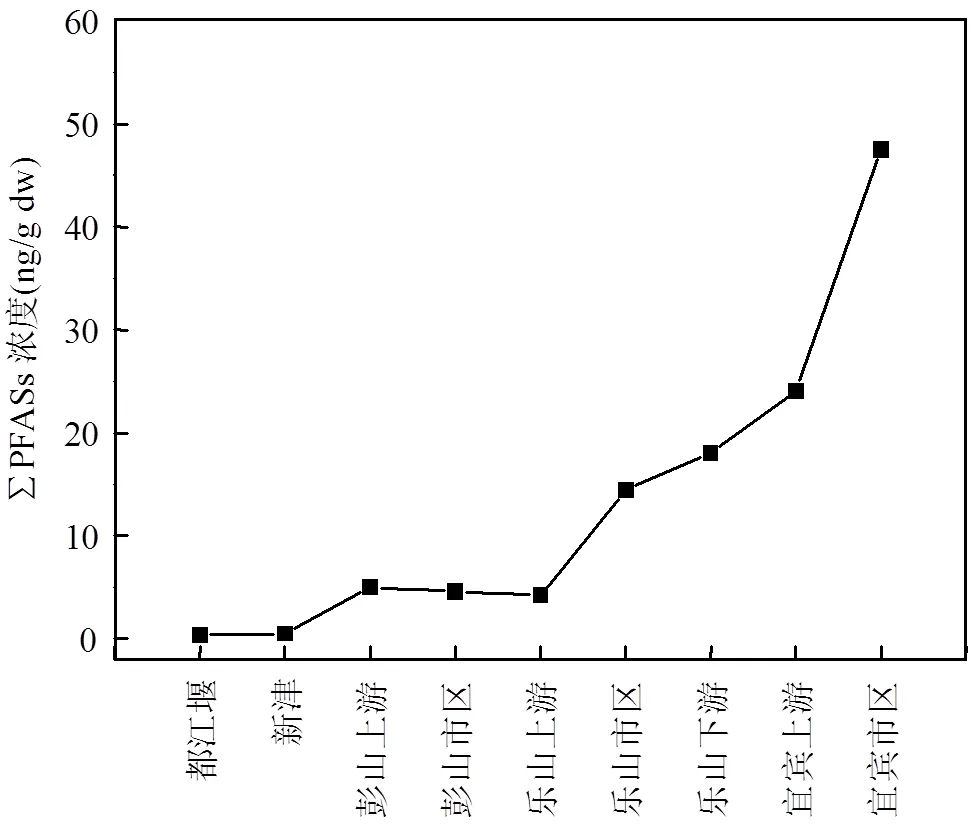
图4 岷江流域沉积物中PFASs的浓度水平(ng/g dw)
从空间分布来看,沉积物中∑PFASs浓度最高的为岷江在宜宾市区的三江汇合处,浓度为47.5ng/g dw,约是宜宾上游地区(24.0ng/g dw)的2倍.这表明城市污染源是岷江流域水体中PFASs的主要来源.乐山下游(18.0ng/g dw)和乐山市区(14.4ng/g dw)的浓度仅次于宜宾河段,都江堰地区的浓度最低,仅为0.334ng/g dw.总体来说,PFASs在底泥中的浓度从上游河段至下游呈现出升高趋势,这和PFASs在水相中的空间分布有一定差异.主要原因有以下两点:(1)当地污染源影响.乐山、宜宾下游地区城市发达,城市生活及工业污染源较多,导致下游地区污染物浓度升高.(2) PFASs是一类有机污染物,在水体中容易从水相向沉积物有机质中分配.杨耿等[28]的研究结果表明,岷江上游沉积物有机质含量较低(0.02~ 0.81%),而下游河段沉积物中有机质含量较高(0.14~ 2.03%),即PFASs在下游河段更易向沉积物中分配.因此,城市生活和工业污染源以及下游河段沉积物中有机质含量较高,是导致下游地区沉积物中PFASs浓度升高的主要原因.
Zhao等[29]调查研究了天津海河中PFASs的污染特征,PFASs的总浓度为0.52~16.3ng/g,其中PFOS和PFOA是主要的污染物.Chen等[15]的研究发现,辽河沉积物中PFASs的总浓度为0.54~2.34ng/g,其中PFHxA和PFOA是主要的污染物.黄河沉积物中[30]PFASs的总浓度为8.19~17.4ng/g(平均浓度11.6ng/g),长碳链的PFASs是主要污染物.加拿大瑞瑟鲁特湖沉积物中PFASs浓度为0.064ng/g, 主要污染物为PFOA[24].法国塞纳河支流沉积物中PFASs浓度为8.4ng/g dw,PFOS为主要污染物[31].通过比较可以看出,不同流域沉积物中PFASs的浓度水平和污染特征存在较大差异,岷江流域沉积物中PFASs的浓度高于海河、辽河流域及瑞瑟鲁特湖,和黄河流域、塞纳河支流相当.
2.3 岷江流域PFASs的年排放通量
宜宾市区采样点位于岷江与长江、金沙江汇合处,采样点到长江无点源污染,因此,本文选取宜宾三江汇合处宜宾河段来估算岷江向长江输出的PFASs的通量,可以反映出岷江流域PFASs的年输出量.本研究采用Pan等[32]估算长江PFASs排放通量的计算公式,具体如下:
water=water×water(1)
sediment=sediment×sediment(2)
total=water+sediment(3)
式中:water为污染物在水相中的浓度,t/m3;water为岷江流域的年径流量,m3;sediment为污染物在沉积物中的浓度,t/t dw;sediment为岷江流域的年输沙量,t.水利部长江水利委员会在2017年长江泥沙公告中[33]的数据显示,岷江流域2016年径流量(water) 7.72×1010m3,2016年输沙量(sediment)为1.07×1010t (干重).
如表2所示,岷江流域PFASs的通量为1.443t/a,其中溶解态的(水相)排放通量为0.9347t/a,占总排放通量的64.8%;通过沉积物输出的通量为0.5083t/a,占总排放通量的35.2%.其中,排放通量最高的是PFBA,为1.037t/a,占总排放通量的71.9%,然后依次为PFPeA(0.2364t/a,16.4%)、PFOA(0.0803t/a, 5.57%)、PFHxA(0.0334t/a,2.31%)、PFBS(0.0233t/a, 1.61%)、PFHpA(0.0217t/a,1.50%)、PFNA(0.0064t/a, 0.44%)、PFDA(0.0039t/a,0.27%)和PFOS(0.0004t/a, 0.03%).Pan等[32]的研究结果显示,长江每年PFASs的排放通量为20.7t/a.本研究中岷江流域PFASs年通量仅占长江流域的6.96%.虽然岷江流域PFASs浓度水平并不低,如长江水相中PFASs浓度为18.9~ 21.6ng/L,沉积物为0.33~0.46ng/g dw;印度恒河PFASs浓度为<0.04~3.91ng/L.但是由于岷江年径流量和输沙量较低,所以岷江流域PFASs通量远低于长江(20.7t/a)、印度恒河(69t/a)、及欧洲河流(18.82t/a)[32,34-35].虽然岷江流域PFASs的排放通量低于其它流域,但是由于PFASs难以降解,可以随河流发生长距离迁移,因此,仍需加强对岷江流域PFASs的管控.另外, PFASs本地源的排放量、当地降水量、河流径流量及泥沙量在不同采样时间均存在一定差异,从而导致PFASs排放通量的估算存在一定的不确定度,因此,应加强对岷江流域中PFASs的监测分析,以便更全面准确的掌握岷江流域向长江流域排放的PFASs通量.
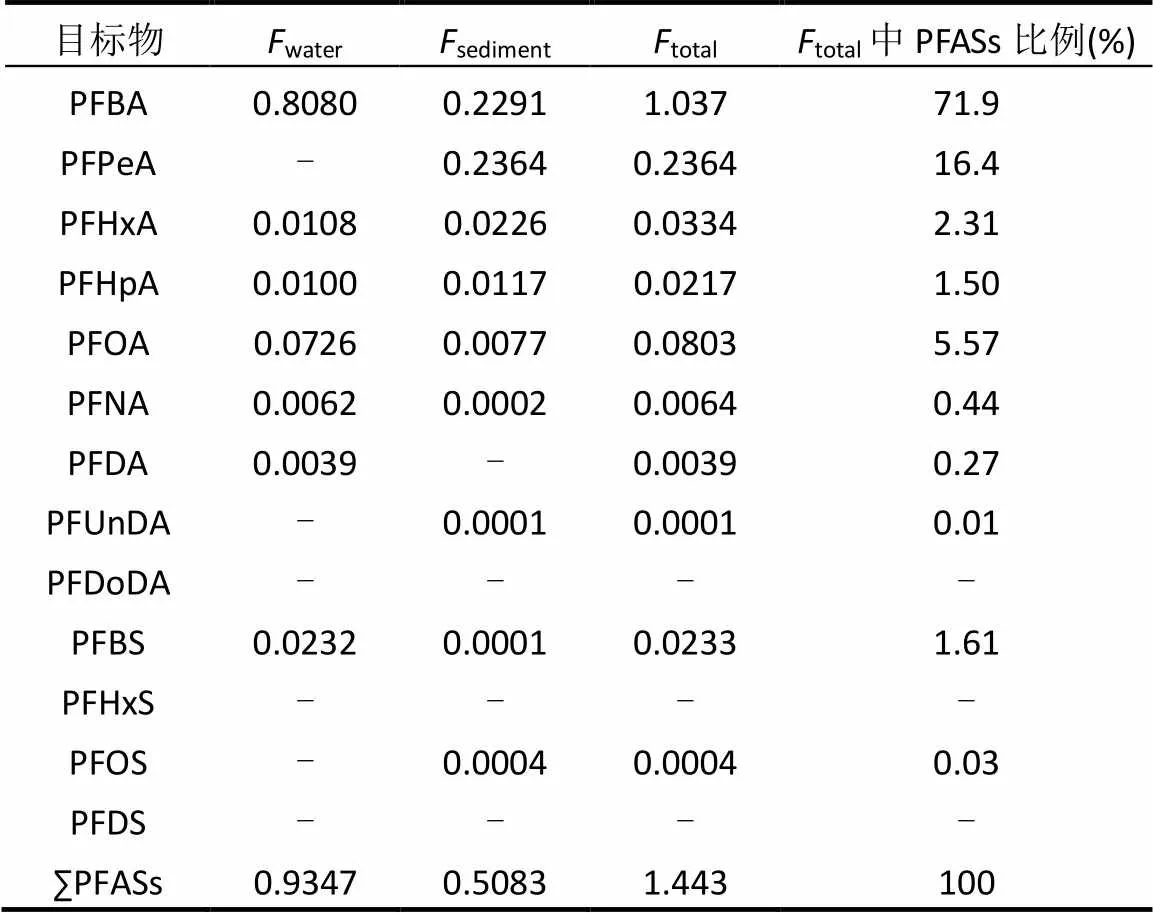
表2 岷江流域向长江年输出PFASs通量的估算(t/a)
注:-:在宜宾市区水相或沉积物中未检出.
3 结论
3.1 岷江流域水相中PFASs的浓度为1.54~ 30.2ng/L,平均值为(11.2±8.0) ng/L,浓度最高点出现在乐山下游,为30.2ng/L,最低点为都江堰.其中,岷江流域水相中最主要的PFASs为PFBA,浓度为0.16~ 28.4ng/L,占总PFASs的50%以上(54.0%~94.1%,都江堰除外).
3.2 岷江流域沉积物中PFASs浓度最高点在宜宾三江汇合处(47.5ng/g dw),最低处为都江堰(0.334ng/ g dw).主要的PFASs是PFHxA(4.44%~66.9%)和PFOA(1.52%~77.5%).
3.3 岷江流域PFASs的年排放通量为1.443t/a,排放通量最高的为PFBA(1.037t/a),占总排放通量的71.9%.
[1] Prevedouros K, Cousins I, Buck R, et al. Sources, fate and transport of perfluorocarboxylates [J]. Environmental Science & Technology, 2006,40(1):32-44.
[2] Yu N, Wang X, Zhang B, et al. Distribution of perfluorooctane sulfonate isomers and predicted risk of thyroid hormonal perturbation in drinking water [J]. Water Research, 2015,76:171-180.
[3] Chen H, Yao Y M, Zhao Z, et al. Multimedia distribution and transfer of per- and polyfluoroalkyl substances (PFASs) surrounding two fluorochemical manufacturing facilities in Fuxin, China [J]. Environmental Science & Technology, 2018,52(15):8263-8271.
[4] Tian Y, Yao Y, Chang S, et al. Occurrence and phase distribution of neutral and ionizable per- and polyfluoroalkyl substances (PFASs) in the atmosphere and plant leaves around landfills: A case study in Tianjin, China [J]. Environmental Science & Technology, 2018,52(3): 1301-1310.
[5] Song X, Vestergren R, Shi Y, et al. Emissions, transport, and fate of emerging per- and polyfluoroalkyl substances from one of the major fluoropolymer manufacturing facilities in China [J]. Environmental Science & Technology, 2018,52(17):9694-9703.
[6] Yeung L W Y, Dassuncao C, Mabury S, et al. Vertical profiles, sources, and transport of PFASs in the Arctic Ocean [J]. Environmental Science & Technology, 2017,51(12):6735-6744.
[7] Poothong S, Thomsen C, Padilla-Sanchez J A, et al. Distribution of novel and well-known poly- and perfluoroalkyl substances (PFASs) in human serum, plasma, and whole blood [J]. Environmental Science & Technology, 2017,51(22):13388-13396.
[8] Martin J W, Mabury S A, Solomon K R, et al. Bioconcentration and tissue distribution of perfluorinated acids in rainbow trout (Oncorhynchus mykiss) [J]. Environmental Toxicology and Chemistry, 2003,22(1):196-204.
[9] Fang S H, Chen X W, Zhao S Y, et al. Trophic magnification and isomer fractionation of perfluoroalkyl substances in the food web of Taihu Lake, China [J]. Environmental Science & Technology, 2014, 48(4):2173-2182.
[10] Eriksen K T, Raaschou-Nielsen O, Sorensen M, et al. Genotoxic potential of the perfluorinated chemicals PFOA, PFOS, PFBS, PFNA and PFHxA in human HepG2cells [J]. Mutation Research, 2010, 700(1/2):39-43.
[11] So M K, Miyake Y, Yeung W Y, et al. Perfluorinated compounds in the Pearl River and Yangtze River of China [J]. Chemosphere, 2007, 68(11):2085-2095.
[12] Li F S, Sun H W, Hao Z N, et al. Perfluorinated compounds in Haihe River and Dagu Drainage Canal in Tianjin, China [J]. Chemosphere, 2011,84:265-271.
[13] Yang L P, Zhu L Y, Liu Z T. Occurrence and partition of perfluorinated compounds in water and sediment from Liao River and Taihu Lake, China [J]. Chemosphere, 2011,83:806-814.
[14] Yu N Y, Shi W, Zhang B B, et al. Occurrence of perfluoroalkyl acids including perfluorooctane sulfonate isomers in Huai River Basin and Taihu Lake in Jiangsu Province, China [J]. Environmental Science & Technology, 2013,47(2):710-717.
[15] Chen X W, Zhu L Y, Pan X Y, et al. Isomeric specific partitioning behaviors of perfluoroalkyl substances in water dissolved phase, suspended particulate matters and sediments in Liao River Basin and Taihu Lake, China [J]. Water Research, 2015,80:235-244.
[16] 周 珍,胡宇宁,史亚利,等.武汉地区水环境中全氟化合物污染水平及其分布特征 [J]. 生态毒理学报, 2017,12(3):425-433. Zhou Z, Hu Y N, Shi Y L, et al. Occurrence and distribution of per- and polufluoroalkyl substances in waste water and surface water samples in Wuhan [J]. Asian Journal of Ecotoxicology, 2017, 12(3):425-433.
[17] Sun H W, Li F S, Zhang T, et al. Perfluorinated compounds in surface waters and WWTPs in Shenyang, China: mass flows and source analysis [J]. Water Research, 2011,45(15):4483-4490.
[18] Liu J X, Avendaño M S. Microbial degradation of polyfluoroalkyl chemicals in the environment: A review [J]. Environment International, 2013,61:98-114.
[19] Ellis D A, Martin J W, De Silva A O, et al. Degradation of fluorotelomer alcohols: A likely atmospheric source of perfluorinated carboxylic acids [J]. Environmental Science & Technology, 2004, 38(12):3316-3321.
[20] 孙殿超,龚 平,王小萍,等.拉萨河全氟化合物的时空分布特征研究 [J]. 中国环境科学, 2018,38(11):4298-4306. Sun D C, Gong P, Wang X P, et al. Special distribution and seasonal variation of perfluoroalkyls substances in Lhasa River Basin, China [J]. China Environmental Science, 2018, 38(11):4298-4306.
[21] 朴海涛,陈 舒,焦杏春,等.大运河丰水期水体中全氟化合物的分布 [J]. 中国环境科学, 2016,36(10):3040-3047. Piao H T, Shu C, Jiao X C, et al. Geographical distribution of perfluorinated compounds in waters along the Grand Canal during wet season [J]. China Environmental Science, 2016, 36(10):3040-3047.
[22] 魏立娥,邵秘华,张 晶,等.双台子河口水体全氟化合物的污染水平分析 [J]. 环境科学学报, 2016,36(5):1723-1729. Wei L E, Shao M H, Zhang J, et al. The pollution analysis of perfluorinated compounds in water of the Shuangtaizi estuary [J]. Acta Scientiae Circumstantiae, 2016,36(5):1723-1729.
[23] 张 明,唐访良,俞雅雲,等.钱塘江(杭州段)表层水中全氟化合物的残留水平及分布特征 [J]. 环境科学, 2015,36(12):4471-4478.Zhang M, Tang F L, Yu Y Y, et al. Residue concentration and distribution characteristics of perfluorinated compounds in surface water from Qiantang River in Hangzhou section [J]. Environmental Science, 2015,36(12):4471-4478.
[24] Lescord G L, Kidd K A, De Silva A O, et al. Perfluorinated and Polyfluorinated Compounds in Lake Food Webs from the Canadian High Arctic [J]. Environmental Science & Technology, 2015.
[25] Möller A, Ahrens L, Surm R, et al. Distribution and sources of polyfluoroalkyl substances (PFAS) in the River Rhine watershed [J]. Environmental Pollution, 2010,158(10):3243-3250.
[26] US-EPA PFOA Stewardship Program. http://www.epa.gov/oppt/pfoa/ pubs/stewardship/pfoastewardshipbasics.html [Z]. 2010.
[27] Higgins C P, Luthy R G. Sorption of perfluorinated surfactants on sediments [J]. Environmental Science & Technology, 2006,40(23): 7251-7256.
[28] 杨 耿,秦延文,韩超南,等.岷江干流表层沉积物中磷形态空间分布特征 [J]. 环境科学, 2018,39(5):2165-2173.Yang G, Qin Y W, Han C N, et al. Distribution of phosphorus fractions in surface sediments of Minjiang Mainstreams [J]. Environmental Science, 2018,39(5):2165-2173.
[29] Zhao X, Xia X, Zhang S, et al. Spatial and vertical variations of perfluoroalkyl substances in sediments of the Haihe River, China [J]. Journal of Environmental Sciences, 2014,26(8):1557-1566.
[30] Zhao P, Xia X, Dong J, et al. Short- and long-chain perfluoroalkyl substances in the water, suspended particulate matter, and surface sediment of a turbid river [J]. Science of The Total Environment, 2016,568:57-65.
[31] Labadie P, Chevreuil M. Partitioning behaviour of perfluorinated alkyl contaminants between water, sediment and fish in the Urge River (nearby Paris, France) [J]. Environmental Pollution, 2011,159(2): 391-397.
[32] Pan C G, Ying G G, Zhao J L, et al. Spatiotemporal distribution and mass loadings of perfluoroalkyl substances in the Yangtze River of China [J]. Science of The Total Environment, 2014,493:580-587.
[33] 水利部长江水利委员会.长江泥沙公报 [Z]. 2017. Changjiang Water Resources Commission of the ministry of water resources. Changjiang sediment bulletin [Z]. 2017.
[34] McLachlan M S, Holmström K E, Reth M, et al. Riverine discharge of perfluorinated carboxylates from the European continent [J]. Environmental Science & Technology, 2007,41(21):7260-7265.
[35] Yeung L W Y, Yamashita N, Taniyasu S, et al. A survey of perfluorinated compounds in surface water and biota including dolphins from the Ganges River and in other waterbodies in India [J]. Chemosphere, 2009,76(1):55-62.
Pollution characteristics and flux of perfluoroalkyl substances in Minjiang River.
FANG Shu-hong*, LI Cheng, BIAN Yu-xia, Wang Di, HAO Yun-qing, YIN Hong-ling, SUN Jing
(College of Resources and Environment, Chengdu University of Information Technology, Chengdu 610225, China)., 2019,39(7):2983~2989
Thirteen kinds of perfluoroalkyl and polyfluoroalkyl substances (PFASs) were analyzed in water and sediment samples collected from Minjiang River by ultra-performance liquid chromatography tandem mass spectrometry (UPLC-MS/MS). PFASs in water phase were in the range of 1.54~30.2ng/L, with mean value of (11.2±8.0) ng/L, and the greatest value appeared at the down stream of Leshan city (30.2ng/L). In addition, perfluorobutanoic acid (PFBA) was the predominant PFASs in water phase, with the concentrations of 0.16~28.4ng/L and concentration profile of 54.0%~94.1% (except Dujiang yian). PFAS concentrations in sediment displayed the highest level (47.5ng/g dw) at Yibin city, near the confluence of Minjiang River, Jinsha River and Yangtze River, while the lowest one was at Dujiang Yan (0.334ng/g dw). Furthermore, the main PFASs in sediment were perfluorohexanoate (PFHxA) (4.44%~66.9%) and perfluroroocantanoic acid (PFOA) (1.52%~77.5%). Estimated flux of PFASs in Minjiang River was 1.443tons/year, and PFBA displayed the greatest mass loading (1.037tons/year), accounting for 71.9% of total flux.
perfluoroalkyl substances;Minjiang River;pollution characteristics;estimated flux
X522
A
1000-6923(2019)07-2983-07
方淑红(1986-),女,山东济宁人,讲师,博士,研究方向为环境化学.发表论文17篇.
2018-11-19
国家自然科学基金资助项目(21607018,41601422);四川省教育厅科研基金资助项目(2017Z055);成都信息工程大学引进人才科研启动项目资助项目(KYTZ201605);成都信息工程大学中青年学术带头人科研基金资助项目(J201714)
* 责任作者, 讲师, fsh@cuit.edu.cn

