水钠锰矿的制备及其对Cd2+的吸附性能试验研究
李胜英,苏志恒,蒋鹏杰,陈慧文,张艺嘉,冯建海
(河池学院 化学与生物工程学院,广西 宜州 546300)
水钠锰矿是环境中常见的氧化锰矿物,具有层状结构。六方水钠锰矿因具有电荷零点低、呈混合价态存在、颗粒细小、比表面积大等特性,在重金属离子吸附与氧化还原、有机污染物氧化和催化降解等环境治理方面有重要作用[1-2],可用于吸附废水中的重金属离子[3-7]。通常,水钠锰矿可用KMnO4和MnCl2在碱性条件下制备[8-11],也可用氧化羟锰矿(Mn(OH)2)为原料制备[12-13],或用KMnO4在回流条件下被浓盐酸还原制备[14-16]。试验研究了以高锰酸钾为锰源,采用反相乳液法制备水钠锰矿,并将所制备的水钠锰矿用于从水体中吸附去除Cd2+。
1 试验部分
1.1 主要试剂与仪器
主要试剂:环己烷、司班80、吐温80、丙酮、氨水、盐酸、氢氧化钠、高锰酸钾、硫酸镉,均为分析纯,购自广东汕头西陇化工有限公司。
主要仪器:SHZ-D(Ⅲ)型循环真空泵(上海予正仪器设备有限公司),DHG-9245A电热鼓风干燥箱(上海凯朗越仪器设备厂),DF-101S集热式恒温加热磁力搅拌器(河南省予华仪器有限公司),pHS-3C(数显)型pH计(上海智光仪器仪表有限公司),D-UPT-Ⅱ-10L纯水仪(成都越纯科技有限公司),ZWY-1102C恒温培养振荡器(上海智诚分析仪器制造有限公司),SG2型坩埚电阻炉(江苏省东台市电器厂),电子分析天平(上海越平科学仪器有限公司),GGX-800型原子吸收光谱仪(北京海光仪器公司)。
1.2 水钠锰矿的制备
取一定量司班80和吐温80加入到25 mL环己烷中,用浓氨水调溶液pH至11,在35 ℃恒温水浴中搅拌30 min,加入10 mL浓度为0.5 mol/L的高锰酸钾溶液,搅拌2.5 h。经破乳、抽滤、烘干、煅烧后得到水钠锰矿样品。
1.3 水钠锰矿的表征
对于水钠锰矿样品,采用X射线粉末衍射分析仪(Rigaku D/max 2500v/pc型,日本理学公司)分析晶型,采用场发射环境扫描电镜(SEM)(FEI Quanta 200 FEG型,荷兰飞利浦公司)分析形貌,采用傅里叶变换红外光谱仪(Nicolet6700型,美国赛默飞世尔公司)分析官能团及共价键结构,采用差热分析仪(上海将来实验设备有限公司)测定失重情况,采用能谱仪(OXFORD INCA 250型,英国Oxford Instruments公司)进行表面元素分析。
1.4 水钠锰矿对Cd2+的吸附
称取0.10 g水钠锰矿于锥形瓶中,与200 mL一定浓度Cd2+溶液混合放在恒温摇床中振荡吸附,吸附平衡后,测定吸附后溶液中Cd2+质量浓度,计算吸附量。计算公式为
(1)
式中:q—Cd2+吸附量,mg/g;ρ0—Cd2+初始质量浓度,mg/L;ρ1—吸附后Cd2+质量浓度,mg/L;V—溶液总体积,L;m—吸附剂质量,g。
2 试验结果与讨论
2.1 水钠锰矿的SEM表征
所制备的水钠锰矿高倍率扫描电子显微照片如图1所示。可以看出,所制备的水钠锰矿粒子呈规则片状,分散较均匀,但有一定程度团聚。

图1 水钠锰矿不同倍率下的SEM照片
2.2 水钠锰矿的红外光谱分析
水钠锰矿的红外光谱分析结果如图2所示。可以看出:3 400 cm-1处和1 648 cm-1处的吸收峰分别为游离—OH的伸缩振动吸收峰和弯曲振动谱带;828 cm-1处的吸收峰归属于水钠锰矿八面体空穴处—OH的弯曲振动吸收峰;而1 008 cm-1处的吸收峰归属于层间Mn3+—OH的弯曲振动吸收峰;423、472、528 cm-1吸收峰为空穴处Mn—O的红外吸收峰[15]。

图2 水钠锰矿的红外光谱分析结果
2.3 水钠锰矿的XRD分析
水钠锰矿的XRD分析结果如图3所示。与水钠锰矿标准谱线PDF#86-0666对比看出,所制备的水钠锰矿的谱线与标准谱线基本相同。因此,可以认为所制备的物质为水钠锰矿,且基本没有杂质,纯度较高。

图3 水钠锰矿XRD图谱
2.4 水钠锰矿的能谱分析
表1和图4分别为水钠锰矿的主要成分和能谱分析结果。可以看出:水钠锰矿中含有少量C杂质,这应是煅烧过程中,有少量表面活性剂未被烧尽所致;Au是测定时为使样品具有较良好的导电性加入的。

表1 水钠锰矿主要成分 %

图4 水钠锰矿的能谱分析结果
2.5 水钠锰矿的热重分析
图5为水钠锰矿的DTG-TG曲线。可知:在100~250 ℃范围内,有明显的失重峰,这是化合物失去表面吸附水及层间水所致;在400 ℃处有一小峰,是样品中含有的少量碳燃烧所致;在700 ℃处有一明显峰,是水钠锰矿晶型结构发生变化所致。

图5 水钠锰矿DTG-TG曲线
2.6 水钠锰矿对水体中Cd2+的吸附
2.6.1 吸附时间对水钠锰矿吸附Cd2+的影响
在相同初始Cd2+质量浓度(60、75、90、115 mg/L),相同温度(分别为298、313、328 K)条件下,吸附时间对水钠锰矿吸附Cd2+的影响试验结果如图6所示。

温度:a—298 K;b—313 K;c—328 K。
由图6看出:不同温度下,水钠锰矿对Cd2+的吸附速率都较大,在吸附120 min后基本都达到平衡;而在313 K条件下的Cd2+吸附效果较298、328 K条件下更好,Cd2+初始质量浓度为60 mg/L时,水钠锰矿对Cd2+的平衡吸附量最大,达123.99 mg/g。
2.6.2 溶液pH对水钠锰矿吸附Cd2+的影响
在初始Cd2+初始质量浓度为60 mg/L、298 K条件下,溶液pH对水钠锰矿吸附Cd2+的影响试验结果如图7所示。
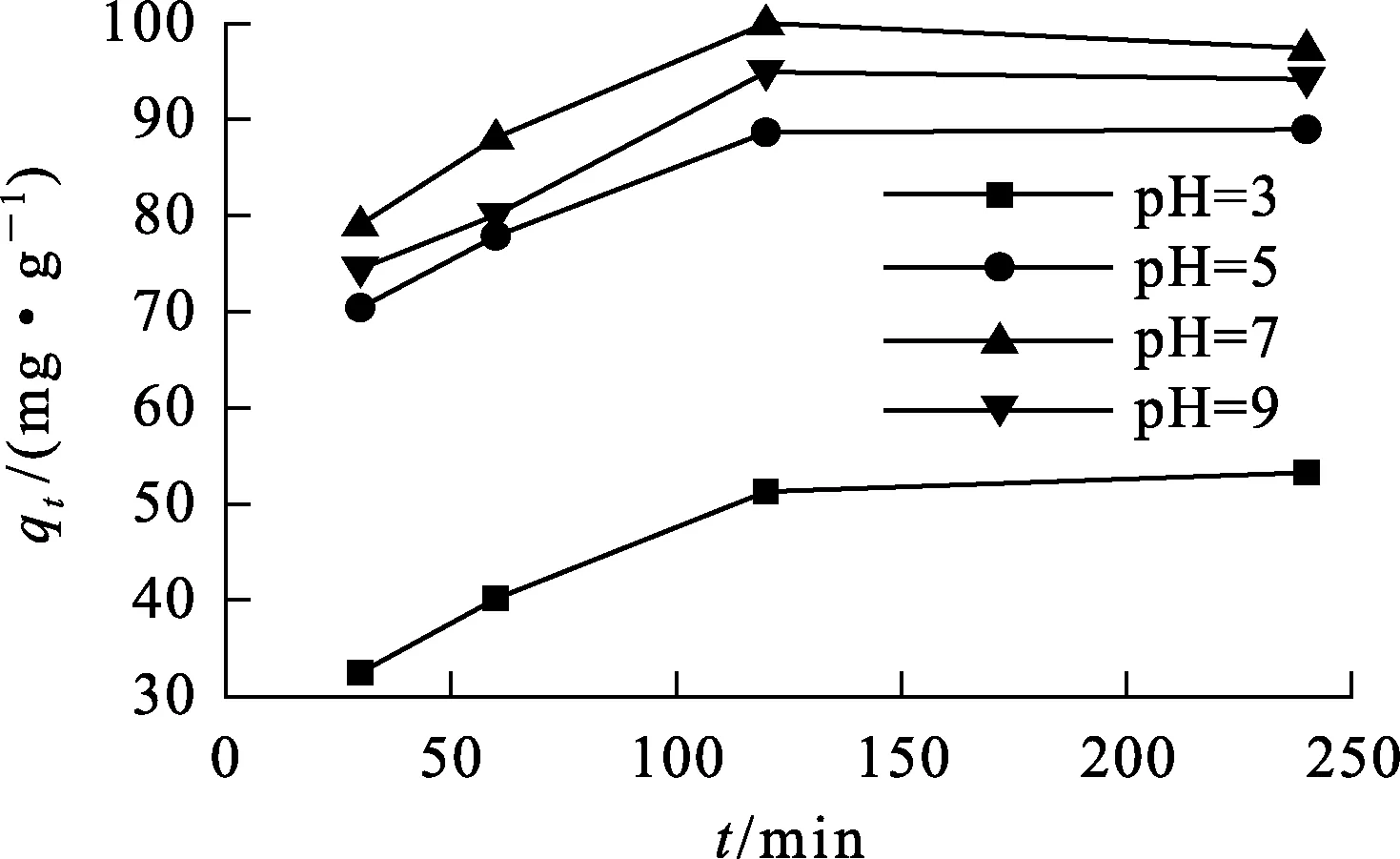
图7 溶液pH对水钠锰矿吸附Cd2+的影响
由图7看出:溶液pH=3时,水钠锰矿对Cd2+的吸附效果相对较差;pH=5、7、9时,吸附量接近,吸附效果较好。这说明,在酸性条件下,水钠锰矿对Cd2+的吸附效果较差;接近中性条件下,吸附效果较好。
2.7 水钠锰矿吸附Cd2+的等温线
采用Langmuir和Freundlich等温吸附方程考察水钠锰矿对Cd2+的吸附行为,方程见式(2)(3),相关参数见表2。
(2)
(3)
式中:ρe—Cd2+平衡质量浓度,mg/L;qe—平衡吸附量,mg/g;qm—饱和吸附量,mg/g;b、kF、n,均为常数。
由表2看出:298、313、328 K条件下,Langmuir等温吸附方程的相关系数R2(分别为0.995 7、0.996 3、0.969 1)比Freundlich等温吸附方程的相关系数R2(分别为0.825 6、-0.088、-0.460 8)大,说明前者拟合结果比后者拟合结果更好,因此认为,Langmuir等温吸附方程能更好地描述Cd2+在水钠锰矿上的吸附过程。

表2 Langmuir和Freundlich等温吸附模型相关参数
2.8 水钠锰矿吸附Cd2+的动力学
采用准一级和准二级动力学模型对试验数据进行拟合,298 K条件下水钠锰矿吸附Cd2+的动力学参数见表3。
准一级动力学方程,
ln(qe-qt)=lnqe-k1t;
(4)
准二级动力学方程,
(5)
式中:qt—为吸附t时间时吸附量,mg/g;qe—吸附平衡时吸附量,mg/g;k1—准一级动力学系数;k2—准二级动力学系数;t—吸附时间,min。

表3 298 K条件下水钠锰矿吸附Cd2+的动力学参数
由表3看出:准一级动力学方程的相关系数R2(0.731 4、-0.203 6、0.399 4、-0.219 5)小于准二级动力学方程的相关系数R2(0.999 2、0.999 1、0.999 3、0.999 2);且由准一级动力学方程拟合所得的吸附平衡时吸附量qe更小,其拟合值与实际值相差较大,说明拟合失真;而由准二级动力学方程拟合得到的qe与试验所得qe相近,说明准二级动力学方程能较好反映水钠锰矿对Cd2+的吸附动力学过程,水钠锰矿对Cd2+的吸附过程以化学吸附为主。
3 结论
采用反相乳液法可制备水钠锰矿,用所制备的水钠锰矿从水体中吸附去除Cd2+有较好结果。所制备的水钠锰矿呈片状,纯度较高,仅含少量杂质;用此水钠锰矿从水体中吸附Cd2+,吸附平衡时间为120 min,40 ℃条件下吸附量最大,约为120 mg/g;溶液呈中性时更有利于吸附;吸附行为符合Langmuir 等温吸附方程与准二级动力学吸附模型,吸附过程以化学吸附为主。

