中成药处方药、 非处方药说明书规范性分析
王新芳, 魏 琴, 罗永皎, 武 雪, 王新刚, 张鸿燕
(兰州大学第二医院, 甘肃 兰州730030)
药品说明书是药品生产企业提供的包含药理学、 毒理学、 药效学、 医学等有关药品安全性、 有效性的重要科学数据和结论, 是医护人员用以指导临床正确使用药品的技术性资料, 也是有关部门鉴定医疗责任的重要法律依据。中成药是指基于中医药理论指导下以中药材为药物原料,根据处方、 生产工艺及药物质量标准生产的药物制剂[1],是我国传统药物类型, 分为处方药及非处方药, 但目前市场流通该类药品中普遍存在说明书不规范的现象, 而这对各类人群参考用药十分重要[2]。 本研究对兰州大学第二医院所使用的162 份处方药、 34 份非处方药说明书进行整理分析, 以期为中成药说明书进一步规范和完善提供参考,并为提高医院用药安全和服务质量提供依据。
1 资料与方法
1.1 来源 收集兰州大学第二医院2017 年6 月之前使用的, 均为相应指导原则颁布后修订的196 份口服中成药说明书, 其中处方药162 份, 非处方药34 份。 以国家食品药品监督管理局颁布的《中药、 天然药物处方药说明书撰写指导原则》[3]( 《指导原则》 ) 《中药、 天然药物处方药说明书格式》[4]( 《说明书格式》 ) 《中成药非处方药说明书规范细则》[5](《规范细则》 ) 为标准, 对所收集说明书进行分类汇总。
1.2 统计学分析 采用Microsoft Office Excel 2007 软件,统计本研究所纳入中成药说明书的核准日期、 修订日期、成分、 性状、 规格、 用法用量、 不良反应、 禁忌、 注意事项、 药物相互作用、 药理毒理、 临床实验、 贮藏、 包装、特殊人群用药等项目, 分析其完整性以及规范性。
2 结果
2.1 处方药说明书调查 162 份处方药品说明书中, 核准日期、 规格、 禁忌、 孕妇及哺乳期妇女用药、 儿童用药、老年人用药、 药物相互作用、 药理毒理、 临床试验等项目存在缺失现象, 成分、 性状、 规格、 用法用量、 禁忌、 注意事项、 贮藏、 包装、 特殊人群用药等项目存在不规范现象, 见表1。
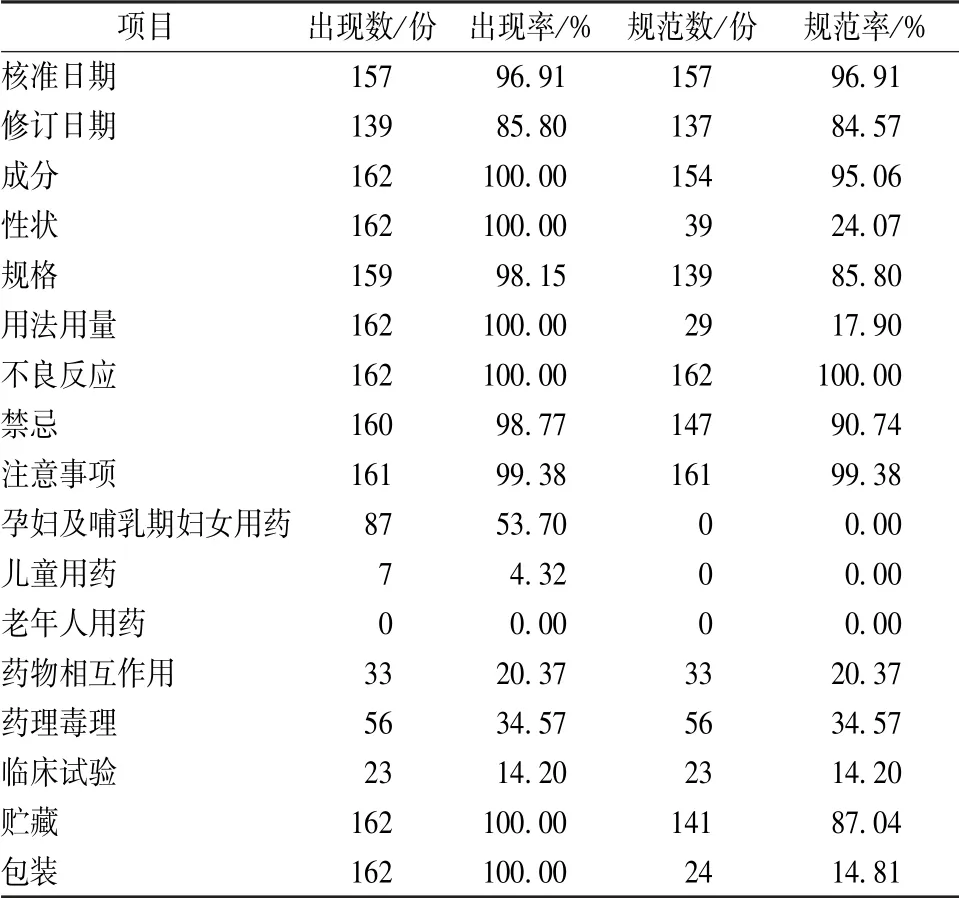
表1 处方药说明书调查数据
2.2 非处方药说明书调查 34 份非处方药说明书缺项现象并不严重, 但有一些核准日期、 成分、 性状、 规格、 用法用量、 禁忌、 注意事项、 包装等项目存在不规范现象,见表2。
3 讨论
3.1 核准、 修订日期 《说明书格式》 规定, 核准、 修改日期应印制在说明书首页左上角, 后者位于前者下方,进行过多次修改的, 仅列最后1 次修改日期; 未进行修改的, 可不列修改日期, 而本研究162 份处方药说明书中5份未列出核准日期, 2 份列出多个修订日期, 规范率分别为96.91%、 84.57%。 另外, 《规范细则》 未要求印制核准日期, 而本研究34 份非处方药说明书中有1 份左上角包含核准日期, 规范率为97.06%。

表2 非处方药说明书调查数据
3.2 成分 《指导原则》 规定, 应列出处方中的全部成分, 并未提到口服药需列出辅料, 而本研究162 份处方药说明书中7 份含有辅料, 1 份药味列举不全, 规范率为95.06%。 《规范细则》 规定, 除《中药品种保护条例》 第十三条规定的情形外(中药一级保护品种), 必须列出全部处方组成和辅料, 而本研究34 份非处方药说明书中乌灵胶囊、 六味地黄丸未列出辅料, 经查阅国家食品药品监督管理总局“中药保护品种库” 发现, 前者为中药二级保护品种, 后者为非保护品种, 均非中药一级保护品种, 故不符合要求, 规范率为94.12%。
3.3 性状 《指导原则》 和《规范细则》 均规定, 应包括药品外观、 气、 味等, 但本研究发现大部分药品缺少外观颜色、 气味等项, 而本研究162 份处方药说明书中仅39份列举齐全, 规范率为24.07%; 34 份非处方药说明书中仅13 份符合要求, 规范率为38.24%。
3.4 规格 《指导原则》 规格表示方法一般按《中国药典》 要求规范书写, 单位为国际单位(g、 mg、 mL 等),而本研究162 份处方药说明书中20 份规格项的单位为汉字(为非处方药标准), 3 份无规格项, 规范率为85.80%; 个别规格项包含药材净质量, 如脑心清片每片质量0.41 g(含柿叶提取物50 mg); 部分只列出药材净含有量, 如愈风宁心滴丸, 每丸含葛根0.417 g。 另外, 具体表述也不统一。 《规范细则》 要求数字以阿拉伯数字表示, 计量单位必须以汉字表示, 每1 份说明书只能写1 种规格, 而本研究34 份非处方药说明书中3 份规格为国际单位, 1 份无规格项, 规范率为88.24%。
3.5 用法用量 《指导原则》 规定, 计量单位应为g、mg、 mL 等国际计量单位, 而本研究162 份处方药说明书中仅29 份使用国际计量单位, 规范率为17.90%。 《规范细则》 规定, 数字以阿拉伯数字表示, 所有质量或容量单位以汉字表示, 而本研究34 份非处方药说明书中5 份单位用国际单位表示, 规范率为85.33%。
3.6 禁忌 《指导原则》 规定, 应当列出该药品不能应用的各种情况, 如禁止应用该药品的人群、 疾病等情况;尚不清楚有无禁忌的, 应在该项下以“尚不明确” 来表述, 而本研究162 份处方药说明书中2 份缺少此项, 5 份出现慎用字眼(注意事项内容), 8 份包含忌食辛辣刺激性食物(注意事项内容), 规范率为90.74%。 《规范细则》 规定, 应列出禁止应用该药品的人群或疾病等情况, [禁忌]内容应采用加重字体印刷, 而本研究34 份非处方药说明书中5 份未加重字体, 1 份包含注意事项内容, 规范率为82.35%。
3.7 注意事项 《指导原则》 并未严格规定必须列出该项目, 但尚不清楚有无注意事项的, 可在该项下以“尚不明确” 来表述, 而本研究162 份处方药说明书中1 份缺少此项, 规范率为99.38%。 《规范细则》 规定, 该项必须注明“对本品过敏者禁用, 过敏体质者慎用” “本品性状发生改变时禁止使用” “如正在使用其他药品, 使用本品前请咨询医师或药师” “请将本品放在儿童不能接触的地方”; 对于是否适用于孕妇、 哺乳期妇女、 儿童、 老人等特殊人群尚不明确的, 必须注明“应在医师指导下使用”,[注意事项] 内容应采用加重字体印刷, 而本研究34 份非处方药说明书中仅6 份内容齐全, 10 份未包括哺乳期妇女用药说明, 14 份未包括老年患者用药说明, 4 份未加重字体, 规范率仅为17.64%。
3.8 特殊人群用药 《指导原则》 《规范细则》 对特殊人群用药规定类似, 但处方药此项内容可单独列出, 其余都应在注意事项中列出, 而本研究162 份处方药说明书中73份含孕妇用药信息, 其中仅5 份含哺乳期妇女用药项, 儿童、 老年患者用药信息数分别为13、 1 份, 但由于《指导原则》 中并未严格规定必须包括此类项目, 故规范率无法计算。 另外, 非处方药此类要求见注意事项。
3.9 药理毒理、 临床试验 该2 项内容仅为《指导原则》规定, 而本研究162 份处方药说明书中55 份含药理毒理项, 其中11 份为“药理作用”, 其余44 份并未包括毒理内容, 23 份含临床试验项(其中21 份同时包含药理毒理项), 两者出现率分别为33.95%、 14.20%。
3.10 贮藏 《指导原则》 《规范细则》 对贮藏项要求相同, 均按药品标准书写, 有特殊要求的应注明相应温度,而本研究162 份处方药说明书中21 项有特殊储存要求的未标温度, 如密闭、 置阴凉干燥处, 34 份非处方药说明书均符合规定, 规范率分别为87.04%、 100%。
3.11 包装 《指导原则》 《规范细则》 对包装项要求相同, 前者要求应先表述直接接触药品的包装材料和容器,再表述包装规格, 而本研究162 份处方药说明书中25 份含药品规格, 如10 g×6 袋/盒, 规范率为15.43%; 34 份非处方药说明书中10 份该项完整, 规范率为29.41%。
3.12 汇总分析 本研究162 份处方药、 34 份非处方药说明书中除[有效期]、 [执行标准]、 [批准文号]、 [生产企业] 等规范完整以外, 其他项目均存在不完整、 不规范现象, 尤其是处方药说明书中用法用量项的规范率非常低。用法用量是说明书核心内容, 也是指导医生处方、 药师调配、 患者正确服药的重要依据[6], “数次” “适量” 等字眼不仅非常不利于患者明确使用药品, 也为医生处方判断带来很大困扰。
同时, 特殊人群用药内容也严重缺失。 首先, 随着我国人口老龄化发展, 老年人占总人口比例逐渐增大, 药品使用比例也相应升高[7]; 其次, 《2016 年儿童用药安全调查报告白皮书》 指出, 我国儿童药物不良反应发生率为12.5%, 为成人的2 倍, 其中新生儿高达24.4%, 为成人的4 倍[8]; 最后, 由于二胎政策的全面放开, 药物咨询工作中妊娠期用药咨询所占的比例也越来越高, 但某些中药因其独特的功效和毒性作用, 并不适合妊娠期妇女使用[9]。 特殊人群由于年龄阶段及身体机能特殊性, 其用药应区别于普通成人, 但中成药说明书中特殊人群用药信息严重不完整, 给此类人群安全用药带来了极大隐患, 故药品研发企业应积极对特殊人群的用药进行相关研究, 并制定具体规定以便于特定人群参考。
另外, 患者用药时经常会存在多种药物同时服用的情况, 但中成药说明书中基本没有药物相互作用的提示, 这也给联合用药带来了很大风险。 因此, 药品研发企业应查阅资料或通过相关研究, 提供尽可能详细的联合用药信息。
4 结语
药品说明书是临床合理用药的主要参考依据, 更是裁定医疗事故中用药合理性的法定文件。 本研究调查分析发现, 我国口服中成药品说明书中各项内容完整、 规范的屈指可数, 无论是格式还是内容均存在不少问题, 尤其是不良反应、 注意事项、 特殊人群用药、 药物相互作用等与临床用药的安全性息息相关的内容更是严重不规范。 因此,国家药监部门应遵照《中成药非处方药说明书规范细则》《中药、 天然药物处方药说明书撰写指导原则》 《中药、 天然药物处方药说明书内容书写要求》 等相关规定进行规范化管理, 严格按照规定审核新进中成药说明书, 为临床合理用药提供可靠的参考依据。

