氟比洛芬微生物计数方法适用性研究
北京市药品检验所 中药成分分析与生物评价北京市重点实验室(102206)江志杰 张光华
北京茗泽中和药物研究有限公司(102629)李斐菲 郭青苇
氟比洛芬又称苯氟布洛芬、氟联苯丙酸,是一种强效苯丙酸类解热抗炎镇痛药,能抑制前列腺素合成环氧合酶而起到止痛、抗炎及解热作用。它为白色或类白色结晶性粉末,在甲醇、乙醇、丙酮或乙醚中易溶,在乙腈中溶解,在水中几乎不溶[1]。它是一种新型的非甾体类镇痛抗炎药,品种有片剂、滴眼药、缓释胶囊剂等[2]。药品一旦受到微生物污染,将造成药品变质,主要成分分解而失效,也可能分解产生毒素,造成机体反应,引起疾病甚至威胁生命[3],而原料的微生物污染情况直接影响到最终产品的质量。微生物检查作为药品安全性的重要指标[4],微生物计数法用来测定原辅料或药品受污染的程度,评价产品的一般卫生质量及安全性[5]。按照《中国药典》2015年版四部通则1107非无菌药品微生物限度标准的规定,应对产品进行需氧菌总数、霉菌和酵母菌总数的测定。中国药典2005年版开始引入微生物检查方法验证试验,通过方法适用性试验研究来考察其抑菌性的大小,制定适合产品的微生物学检查方法[7],以保证选用方法准确、可靠。本文按照《中国药典》2015年版的操作要求及指导原则,对氟比洛芬微生物计数方法进行适用性研究,以确定适宜、有效的检查方法。
1 仪器与材料
1.1 仪器设备 SPX-100B-Z生化培养箱(上海博讯实业有限公司医疗设备厂);DNP-9082电热恒温培养箱(TAMATO科学株式会社);XS1.DTXD-0.36脉动真空灭菌器(山东新华医疗器械股份有限公司);SW-CJ-1FD超净工作台(苏净集团苏州安泰空气技术公司);JM-B2002电子天平(诸暨市超泽衡器设备有限公司)。
1.2 样品 氟比洛芬(批号分别为2131701、2131702、2131703),由永光制药有限公司生产。
1.3 试剂与培养基 蛋黄卵磷脂(批号:20180304)和组氨酸盐酸盐(批号:20180304)来源于北京奥博星生物技术有限责任公司;聚山梨酯80(批号:1306211)、磷酸氢二钾(批号:1405061)和磷酸二氢钾(批号:1303011)来源于西陇化工股份有限公司;pH7.0氯化钠-蛋白胨缓冲液(批号:20171208)来源于青岛高科园海博生物技术有限公司;沙氏葡萄糖琼脂培养基(批号:20170123)、沙氏葡萄糖液体培养基(批号:20170711)、胰酪大豆胨琼脂培养基(批号:20170920)和胰酪大豆胨液体培养基(批号:20170810)来源于青岛高科园海博生物技术有限公司,均在验证合格的灭菌程序下灭菌,培养基适用性试验均符合药典要求。
pH7.6无菌磷酸盐缓冲液:照中国药典2015年版通则8004配制,过滤,分装,灭菌。
缓冲液A:聚山梨脂80 30g、蛋黄卵磷脂3g、组氨酸盐酸盐1g、蛋白胨1g、氯化钠4.3g、磷酸二氢钾3.6g、磷酸氢二钠7.2g、纯化水1000ml,121度消毒15分钟。注意:先将蛋黄卵磷脂加到聚山梨酯80中,研磨,混合,然后加入培养基或是混合液体中,煮沸,待完全溶解后分装,消完毒后,带厚手套,将底下的沉淀慢慢摇均匀,也可以放置一周后,摇匀使用。
1.4 菌种 金黄色葡萄球菌 [CMCC (B)26003]、铜绿假单胞菌 [CMCC (B)10104]、大肠埃希菌 [CMCC(B)44102]、白色念珠菌 [CMCC(F)98001]、黑曲霉 [CMCC(F)98003]均购自中国食品药品检定研究院,菌株传代数均为第3代。
1.5 试验环境 符合《中国药典》2015年版的要求,在环境洁净度D级下的局部洁净度B级的单向流空气区域内进行;微生物限度室、洁净工作台及生物安全柜洁净度经监测符合相关要求;每次试验洁净工作台沉降菌监测记录均符合规定。
2 方法
2.1 菌液的制备 接种金黄色葡萄球菌、大肠埃希菌和铜绿假单胞菌的新鲜培养物至10ml胰酪胨大豆肉汤培养基中,33℃培养24h;接种白色念珠菌的新鲜培养物至10ml沙氏葡萄糖液体培养基中,23℃培养24h。上述培养物用0.9%无菌氯化钠溶液制成适宜浓度的菌悬液。
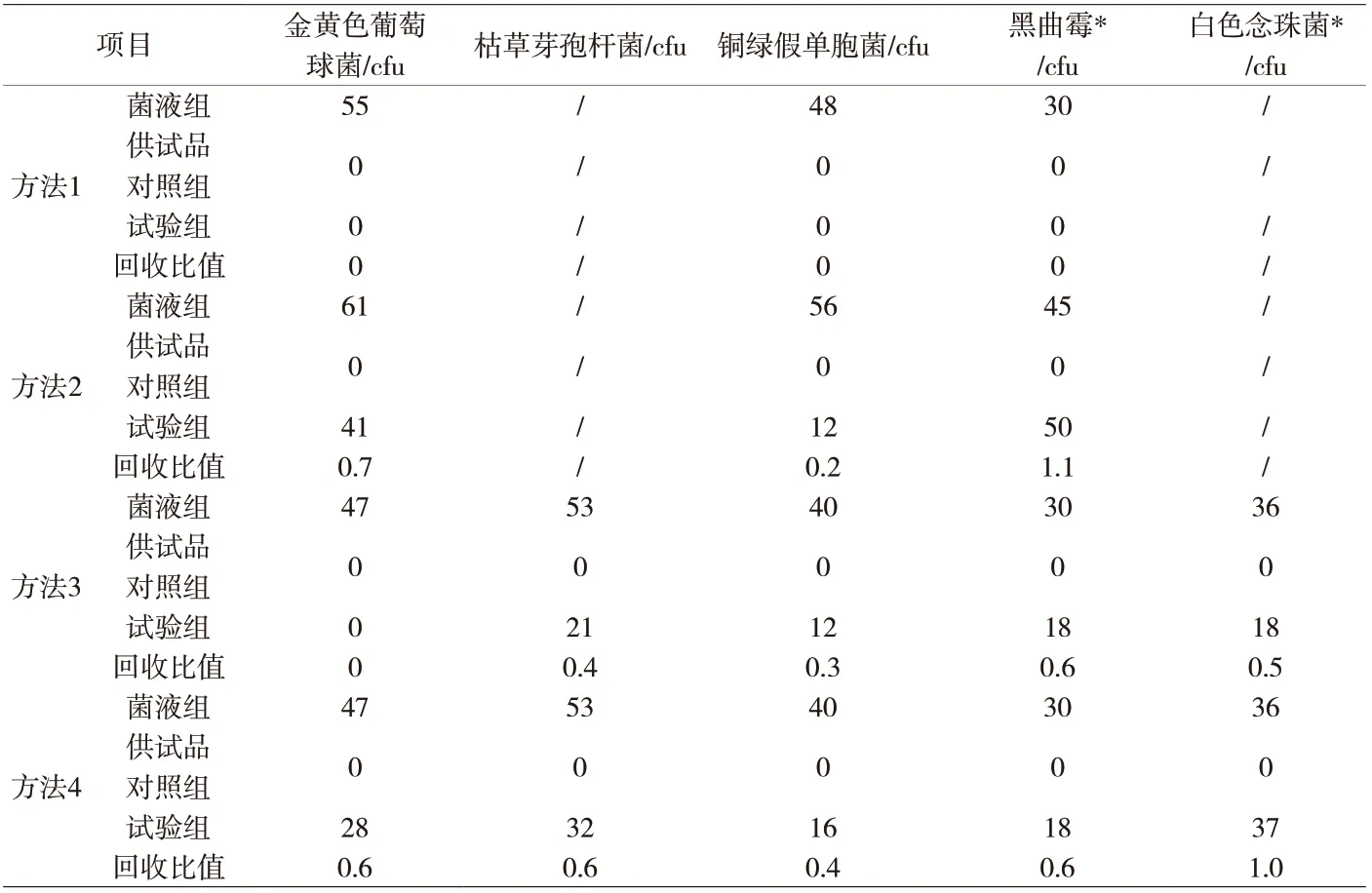
附表1 不同方法的预实验结果
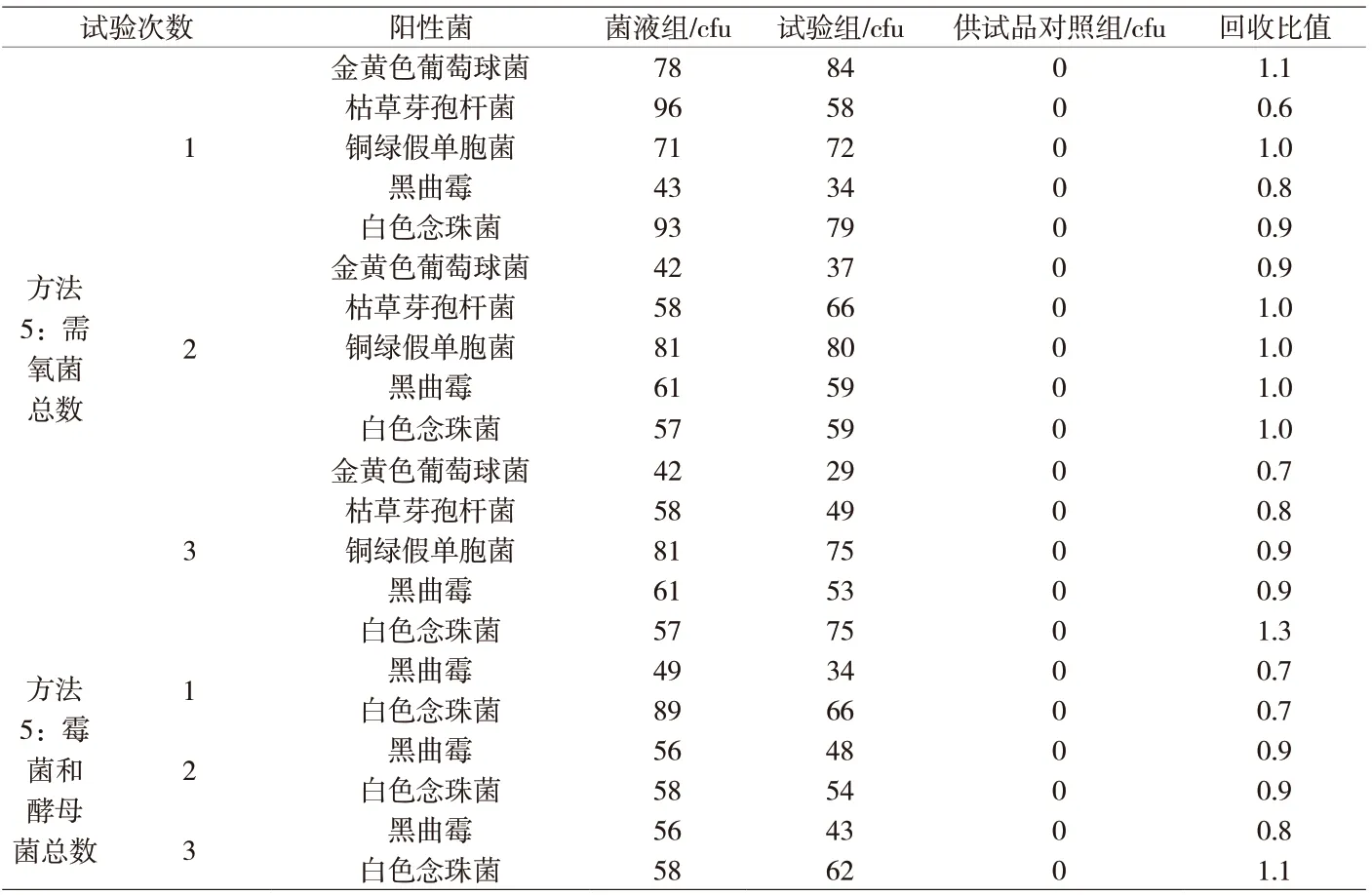
附表2 氟比洛芬微生物计数方法适用性回收比值
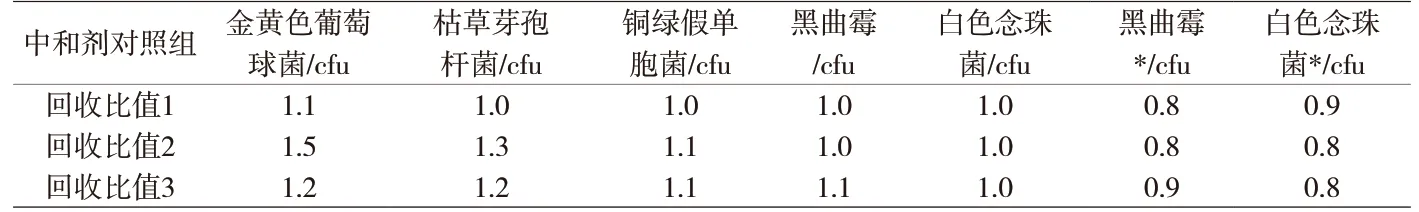
附表3 中和剂对照组的回收比值
接种黑曲霉的新鲜培养物至沙氏葡萄糖琼脂斜面培养基中,25℃培养7d,加入3ml含0.05%聚山梨酯80的0.9%无菌氯化钠溶液,将孢子洗脱。过滤菌丝吸出孢子悬液至无菌试管内,用含0.05%聚山梨酯80的0.9%无菌氯化钠溶液制成适宜浓度的孢子悬液。
2.2 微生物计数法用供试液的制备 供试液①:取本品5g,加含3%聚山梨脂80 pH7.0无菌氯化钠-蛋白胨缓冲液至1000ml,振摇至供试品分散均匀,制成1∶200的供试液。
供试液②:取本品5g,加含3%聚山梨脂80 pH7.6无菌磷酸盐缓冲液至1000ml,振摇至供试品分散均匀,制成1∶200的供试液。
供试液③:取本品5g,加缓冲液A至1000ml,振摇至供试品分散均匀,制成1∶200的供试液。
2.3 需氧菌总数、霉菌和酵母菌总数计数方法适用性试验
2.3.1 菌液对照组 方法1、方法2、方法4和5:取pH7.0无菌氯化钠-蛋白胨缓冲液10ml,加入制备好的试验菌液0.1ml(细菌、酵母菌小于1000cfu,霉菌小于600cfu),混匀,使每1ml稀释液中含菌量小于100cfu,分别取此菌液1ml注皿,测定其每毫升的活菌数,结果为 A。方法3:取pH7.0无菌氯化钠-蛋白胨缓冲液20ml,加入制备好的试验菌液0.1ml(细菌、酵母菌小于1000cfu,霉菌小于600cfu),混匀,使每2ml稀释液中含菌量小于100cfu,分别取此菌液2ml注皿,测定其每毫升的活菌数,结果为A。
2.3.2 供试品对照组 方法1、方法2、方法4和5:分别取取供试液①、供试液②、供试液③10ml,加入稀释液0.1ml,取1ml注皿,分别测定供试品本底的需氧菌总数和霉菌和酵母菌总数,测定结果为B。方法3:取供试液③20ml,加入稀释液0.1ml,取2ml注皿,分别测定供试品本底的需氧菌总数、霉菌和酵母菌总数,测定结果为B。
2.3.3 试验组 方法1、方法2、方法4和5:取供试液①、供试液②、供试液③10ml各五只试管,分别加入制备好金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、白念珠菌和黑曲霉试验菌菌悬液0.1ml,混匀,取1ml注皿,测定需氧菌总数、霉菌和酵母菌总数,测定结果为C。方法3:取供试液③20ml各五只试管,分别加入制备好金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、白念珠菌和黑曲霉试验菌菌悬液0.1ml,混匀,取2ml注皿,测定需氧菌总数、霉菌和酵母菌总数,测定结果为C。
2.3.4 中和剂对照组 方法5:取供试液③10ml各五只试管,分别加入制备好金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、白念珠菌和黑曲霉试验菌菌悬液0.1ml,混匀,取1ml注皿,测定需氧菌总数、霉菌和酵母菌总数,测定结果为D。上述所加菌液的体积均未不超过供试液体积的1%。已注入供试液的平皿,细菌计数倾注胰酪胨大豆琼脂培养基,而方法5是倾注含3%聚山梨酯80、0.3%卵磷脂的胰酪胨大豆琼脂培养基,待凝固后,置33℃培养3d,逐日观察结果;霉菌和酵母菌计数倾注沙氏葡萄糖琼脂培养基,待凝固后,置25℃培养5d,逐日观察结果。
2.3.5 比值计算 试验菌的比值=(菌落数C-菌落数B)/菌落数A;中和剂对照组的比值=菌落数D/菌落数A。
3 结果与分析
3.1 微生物计数方法适用性预实验结果 从附表1预实验结果可以看出,方法1中的金黄色葡萄球菌、铜绿假单胞菌、黑曲霉的回收率均为0,说明氟比洛芬的抑菌作用很强,通过分析发现,供试液①pH值为6.0左右,偏酸性,因此后面的试验均采用了碱性的磷酸缓冲液作为稀释液,考虑到样品为非水溶性的粉末状,为了分散均匀,稀释液中添加了一定量的聚山梨酯80;方法2中的铜绿假单胞菌的回收率为0.2,方法3中的金黄色葡萄球菌的回收率为0,可能是供试液量增加导致的,均不符合药典要求;方法4结果显示,除铜绿假单胞菌的回收比值为0.4,其余试验菌株的回收比值均大于0.5,因此考虑在培养基中添加一定量的卵磷脂和聚山梨酯80。
3.2 微生物计数方法适用性结果 氟比洛芬的需氧菌总数、霉菌和酵母菌总数采用平皿法进行方法适用性试验结果见附表2。在3次独立的需氧菌计数方法平行试验中,金黄色葡萄球菌的回收比值分别为1.1、0.9、0.7,枯草芽孢杆菌的回收比值分别为0.6、1.0、0.8,铜绿假单胞菌的回收比值分别为1.0、1.0、0.9,黑曲霉的回收比值分别为0.8、1.0、0.9,白色念珠菌的回收比值分别为0.9、1.0、1.3,5株需氧菌的回收比值均符合药典规定,因此,可照此方法测定氟比洛芬的需氧菌总数。在3次独立的霉菌和酵母菌计数方法平行试验中,黑曲霉的回收比值分别为0.7、0.9、0.8,白色念珠菌的回收比值分别为0.7、0.9、1.1,2株真菌的回收比值均符合药典规定,因此,可照此方法测定氟比洛芬的霉菌和酵母菌总数。
3.3 中和剂对微生物有无毒性结果 为考察缓冲液A和培养基中添加一定量的卵磷脂和聚山梨酯80对微生物有无毒性,设置了中和剂对照组,从附表3中的结果来看,中和剂对照组的菌落数与菌液对照组的菌落数比值均在0.8~1.5之间,符合药典要求的0.5~2.0范围内。
4 讨论
随着《中国药典》2015年版的实施,对原料及辅料的微生物限度控制也越来越严格[6]。而原料的微生物检验方法适用性验证也应符合《中国药典》2015年版四部[7]通则1106的要求,若回收比值为0.5~2.0,方法可用于样品的需氧菌总数、霉菌和酵母菌总数的计数检查。产品存在抑菌性时,中国药典2015年版强调的方法学适用性试验更显重要性,只有采用适宜方法去除抑菌活性,才有可能检出药品中污染的微生物,避免检验结果假阴性,从而保证微生物限度检查方法的科学性,以有效控制药品质量[8]。已有许多文献报道,通过各种手段消除供试品的抑菌作用,找到合理的科学的检测方法。平皿法是非无菌制剂微生物计数的传统方法,具有简单方便,成本低,结果准确的优点,是优先考虑的方法[4]。预实验发现氟比洛芬的抑菌性比较强,而薄膜过滤法能直接彻底消除抑菌作用、计数结果准确度高,但是不适用于非完全溶解的供试品。Tween-80 和卵磷脂常作为季铵化合物、对羟基苯甲酸等化合物的中和剂,可能会保护微生物细胞膜起到中和作用。聚山梨酯80是一种表面活性剂,可作为乳化剂和中和剂等,用于药品的微生物限度检查时供试液的制备,使供试液分散系统更具相容性。因此,选用卵磷脂和聚山梨酯80作为中和剂,采用培养基稀释法,最低稀释级取1∶200的供试液1ml 注皿,才可以消除其抑菌作用。最终确定的方法为:取本品10g,加缓冲液A至2000ml,振摇至供试品分散均匀,制成1∶200的供试液。需氧菌总数测定,取1∶200的供试液1ml,注皿,平行2份,注入3%聚山梨酯80和0.3%蛋黄卵磷脂的胰酪大豆琼脂培养基,依法检查(中国药典2015年版通则1105平皿法);霉菌和酵母菌总数测定,取1∶200的供试液1ml,注皿,平行20份,依法检查(中国药典2015年版通则1105平皿法)。

