水液相环境下α-丙氨酸两性离子的手性对映体转变机理
徐锐英,马宏源,姜春旭,潘宇,李冰,佟华,王佐成
(1.白城师范学院传媒学院,吉林 白城 137000;2.白城师范学院物理学院,吉林 白城 137000;3.白城师范学院机械工程学院,吉林 白城 137000)
α-丙氨酸(α-alanine,α-Ala)是蛋白质的重要成分,是结构最简单的手性氨基酸。根据光学活性的不同可分为左旋-丙氨酸(L-α-Ala)和右旋-丙氨酸(D-α-Ala),根据构型的不同可分为S-型(S-α-Ala)和R-型(R-α-Ala)两种异构体。L-α-Ala可促进葡萄糖代谢,治疗低血糖,D-α-Ala具有抑菌作用,还可用于手性制药。已有研究[1-2]表明,通常生命体内有微量的D-α-Ala存在,其部分来源于L-α-Ala的手性转变,体内过量的D-α-Ala可引起帕金森和衰老症等疾病。
研究α-Ala的手性转变对于解释生命体内右旋-丙氨酸的存在以及研究复杂的氨基酸手性转变均具有重要意义,为此学者们对α-Ala分子的旋光异构做了大量的工作。文献[3-7]的研究发现:以氨基氮作为质子迁移桥梁是中性α-Ala分子手性转变的优势通道,裸反应的决速步骤能垒266.1 kJ/mol,在2个水分子簇的催化作用下,决速步骤能垒被降至138.6 kJ/mol。文献[8]的研究表明:小尺寸的扶手椅型SWBNNT对中性α-Ala分子手性转变具有催化作用,使决速步骤能垒降至201.1 kJ/mol。文献[9-10]的理论研究表明,在水分子簇的催化及溶剂效应的作用下,氨基与羧基间具有分子内内单氢键和双氢键的中性α-Ala分子旋光异构决速步骤的能垒分别是109.61和113.37 kJ/mol,说明生命体内水液相环境下氨基与羧基间具有分子内内单氢键和双氢键的α-Ala分子可以缓慢地旋光异构。文献[11]的理论研究表明,甲醇溶剂环境下两种稳定构象的中性α-Ala分子手性转变决速步的能垒分别为109.8和111.0 kJ/mol,与文献[9-10]的研究相比较可知,甲醇溶剂与水溶剂对中性α-Ala分子的消旋作用基本相同。已有研究[12]表明,甘氨酸在水液相中最稳定的构象是两性的,亦即生命体内水液相环境下的甘氨酸绝大多数以两性离子的形式存在。本研究表明,水液相下α-Ala的最稳定构象也是两性的,因此生命体内大量的α-Ala是以两性离子的形式存在。文献[13]通过实验研究,得到了295 K和60 K温度下两性的α-Ala离子手性对映体的结构特性,说明了两性的α-Ala离子可能旋光异构,但没有在理论上给予解释。以往针对α-Ala手性转变机理的研究[4-12]也都是针对中性的分子,文献[14-17]只是考察了水分子诱导甘氨酸等分子的质子迁移的机理,目前,对水溶剂中水分子对α-Ala两性离子手性转变的影响鲜见报道,基于此本工作对水液相环境下α-Ala两性离子的手性对映体转变机理进行了研究。
1 研究与计算方法
考虑到反应过程中各个驻点体系存在氢键和范德华等弱作用及水的溶剂效应,使用色散校正密度泛函的WB97X-D[18]和自洽反应场理论的SMD模型[19]方法,在6-31++G(d, p)基组水平对标题反应各个驻点的几何构型进行全优化。为验证过渡态[20]确是连接我们期望的极小点,对过渡态进行IRC(内禀反应坐标)[21]计算。为获得相对可信的反应过程势能面并兼顾计算资源,采用多体微扰论的MP2[22]方法和高角动量基组,在SMD/MP2/6-311++g(3df, 2pd)水平计算各驻点体系的单点能,用Gtotal=Gtc+ESP计算总吉布斯自由能(其中Gtc和ESP分别为吉布斯自由能热校正和单点能)。水分子可以在α-Ala的前面、后面、右侧和上部与α-Ala通过氢键作用形成络合物,分别记作S-Ala·H2O(f)、S-Ala·H2O(b)、S-Ala·H2O(r)和S-Ala·H2O(u),2个水分子簇与α-Ala络合记作S-Ala·2H2O,其它驻点分子与水分子(簇)络合物的标记形式相似,计算工作由Gaussian09[23]程序完成。
2 结果与讨论
水液相环境下α-丙氨酸两性离子的手性对映体构象见图1,根据质子迁移是否有水分子作媒介,其手性转变过程可分为单体异构和水分子(簇)做质子转移媒介的异构两种情形,下面分别进行讨论。
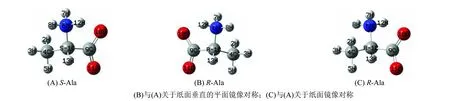
图1 水液相环境下α-丙氨酸两性离子的稳定构象Fig.1 The stable conformations of α-alanine zwitterion in water/liquid phase environment
2.1 单体S-Ala的手性对映体转变
水液相环境下S-Ala的手性对映转变反应历程见图2,反应过程的吉布斯自由能势能面见图3。
第1基元反应,反应物S-Ala经过渡态TS1,实现了α-氢13H从α-碳1C向羰基氧11O的迁移,异构成第一中间体INT1。从S-Ala到TS1过程,1C—13H键长从0.109 2 nm拉伸至0.152 0 nm,骨架二面角6N—1C—9C—10O从-6.46°变为-37.53°,C—H键的大幅拉伸断裂再加上C—C键的内旋转需要较多的能量,TS1产生了247.9 kJ/mol的能垒。
第2基元反应,INT1经过渡态TS2,实现了7H从氨基氮6N向α-碳1C的迁移,异构成第2中间体R-INT2,至此S-Ala实现了手性转变。从INT1经过渡态TS2,6N—7H键长从0.102 2 nm拉伸至0.121 2 nm,N—H键的小幅拉伸断裂所需能量不会很高;二面角6N—1C—4C—9C从172.23°变为-145.73°,使α-碳从sp2杂化向sp3杂化(从空配向满配)过渡又会释放一些能量。因此TS2产生的能垒不是十分高,能垒是144.0 kJ/mol。从势能面可以看出TS2的稳定性不及TS1,原因是TS2的偶极矩8.551 D小于TS1的偶极矩11.622 D,极性水溶剂的作用使TS1变得相对稳定些。TS2产生的内禀能垒低于TS1的内禀能垒,原因是INT1处在势能面较高的位置。
第3基元反应,R-INT2经过渡态R-TS3m或R-TS3n,实现了13H从羧基外侧向内侧的旋转,异构成第3中间体R-INT3。从R-INT2到R-TS3m,二面角13H—11O—9C—10O从-178.90°变为-90.21°,9C—11O键长从0.134 2 nm拉伸至0.137 6 nm,碳-氧键9C—11O的内旋转和小幅拉伸所需能量不高,R-TS3m产生的能垒是32.0 kJ/mol。相似的过渡态R-TS3n产生的能垒是32.8 kJ/mol,不再赘述。
第4基元反应,R-INT3经过渡态R-TS4,实现了13H在羧基内的迁移,异构成第4中间体R-INT4。从R-INT3到R-TS4,11O—13H键长从0.097 1 nm拉伸至0.129 3 nm,O—H键的拉伸断裂所需能量不是很高,但R-TS4的11O—13H—10O键角是107.28°,11O—13H—10O的氢键极弱,R-TS4的四元环结构不稳定,因此R-TS4产生的能垒又不是很低,是137.1 kJ/mol。
第5基元反应,R-INT4经过渡态R-TS5,实现了氨基的8H和12H从右侧向左侧的翻转,异构成第5中间体R-INT5。从R-INT4到R-TS5,二面角8H—6N—1C—12H从-117.03°变为173.98°,非骨架形变所需能量不高,R-TS5产生的能垒是20.3 kJ/mol。
第6基元反应是R-INT5经与第3基元相似的羧羟基旋转的过渡态R-TS6m和R-TS6n,异构成中间体R-INT6。R-TS6m和R-TS6n产生的能垒分别是42.1和41.0 kJ/mol,不再赘述。
第7基元反应,R-INT6经过渡态R-TS7,实现了质子13H从羰基氧10O向氨基氮6N的迁移,异构成产物P_R-Ala。从R-INT6到R-TS7过程,10O—13H键长从0.099 7 nm拉伸至0.118 5 nm,一个O—H键的小幅拉伸需要的能量不多,又10O—13H—6N的键角是146.36°,10O—13H—6N是中等强度的氢键,五元环过渡态R-TS7比较稳定,因此R-TS7产生的能垒很低,只有2.3 kJ/mol。结构分析表明,P_R-Ala和S-Ala的构象镜像对称,说明至此S-Ala实现了手性对映体转变。
从图3可以看出,水液相下,单体S-Ala实现手性对映体转变要经过7个基元反应,总反应活化能是281.6 kJ/mol。决速步骤是第一基元反应,决速步内禀能垒是247.9 kJ/mol。由于正负反应能垒低于40.0 kJ/mol时,反应物和产物可同时存在[24],所以R-INT4、R-INT5、R-INT6和P_R-Ala是同时以产物形式存在,只是P_R-Ala的分布最高,并且是S-Ala的手性对映体。决速步内禀能垒247.9 kJ/mol已经远远大于质子迁移的极限能垒167.0 kJ/mol[24],说明水液相下,单体S-Ala不能实现手性对映体转变。
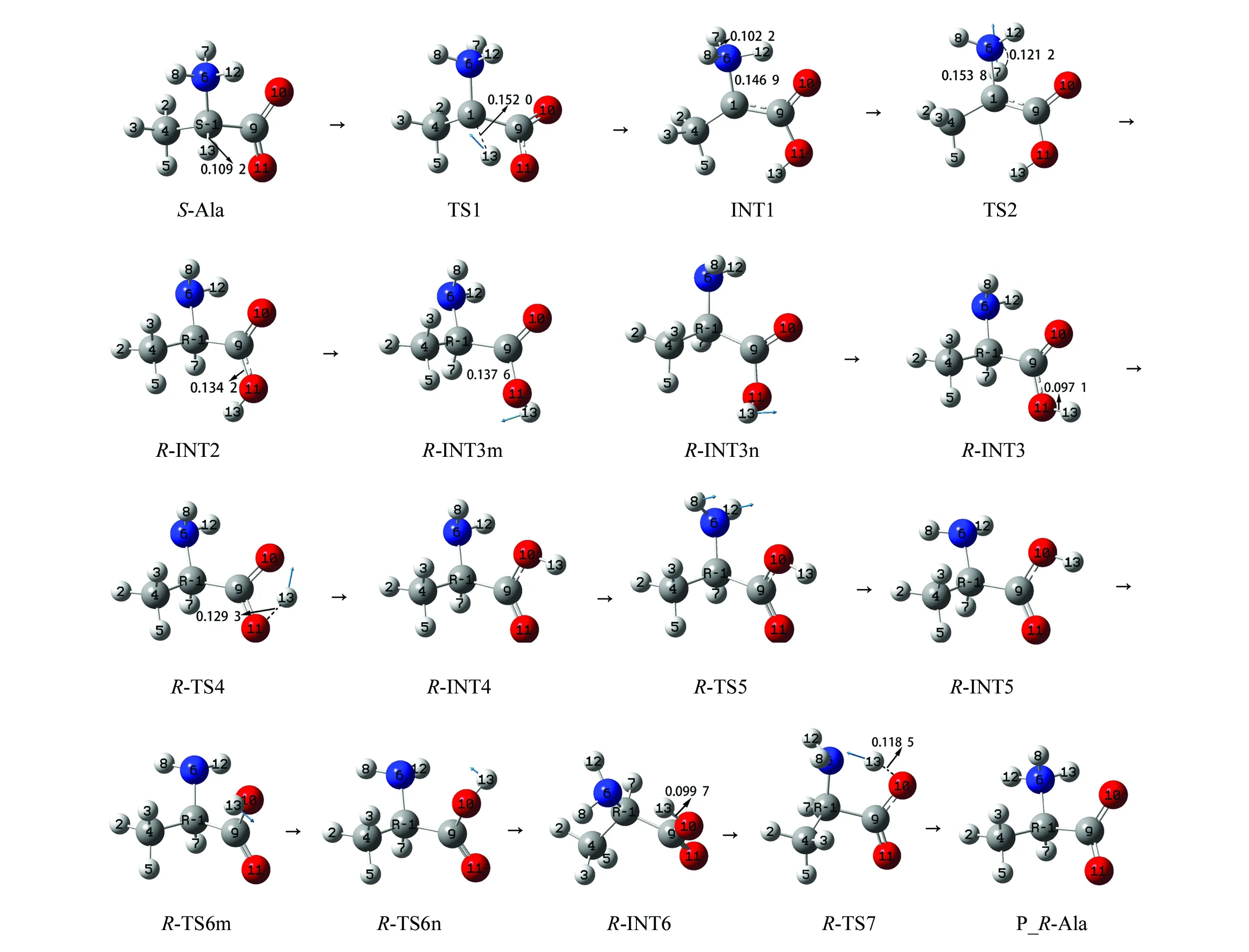
图2 水液相环境下单体S-Ala的手性对映体转变历程及驻点构型Fig.2 Reaction process of chiral enantiomer transition and stationary point structures of monomer S-Ala in water/liquid phase environment
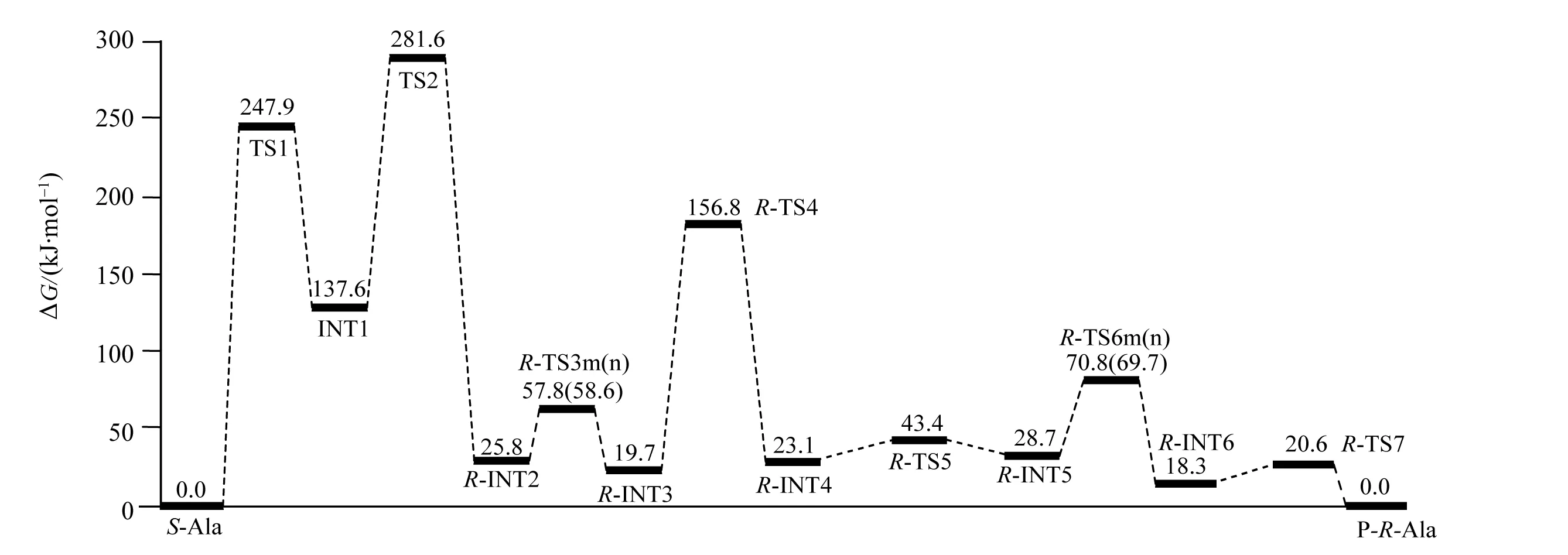
图3 水液相环境下单体S-Ala的手性对映体转变反应势能面Fig.3 Potential energy surfaces of chiral enantiomer transition of monomer S-Ala in water/liquid phase environment
2.2 水分子(簇)作质子迁移媒介S-Ala的手性对映转变
考虑水分子的影响时,对于非质子迁移的基元反应过程,水分子的影响极小[25-26],只讨论水分子(簇)作质子迁移媒介的各个基元反应。水分子(簇)作质子迁移媒介时,除了水分子(簇)催化单体S-Ala手性对映体转变的第1、2、4、7基元反应可以使S-Ala实现手性对映转变的反应通道,还增加了水分子簇在INT1的里侧(纸面里)做质子转移媒介,只经过一步反应就将从α-碳迁移到羧基的质子在纸面里直接传递到α-碳,使S-Ala实现手性对映体转变的更有捷径的路径,此新路径命名为n通道。下面对这两个通道的水分子(簇)作质子迁移媒介的各个基元反应分别进行讨论。
2.2.1 水分子(簇)催化单体S-Ala手性对映体转变通道的质子迁移过程 水分子(簇)催化单体S-Ala手性对映体转变的第1、2、4、7基元反应历程见图4,反应过程的吉布斯自由能势能面见图5。
第1基元反应,计算表明,1个水分子对此基元的催化作用远小于2个和3个水分子簇,这里只讨论2个和3个水分子簇的情况。
2个水分子簇做质子迁移媒介时,首先2个水分子簇在S-Ala的前面与α-氢12H和羰基氧10O氢键作用,形成底物络合物S-Ala·2H2O(f)。然后S-Ala·2H2O(f)经过渡态TS1·2H2O(f)异构成第1中间体络合物INT1·2H2O(f),此基元反应是2个水分子簇做质子迁移媒介,实现了α-氢从α-碳向羰基氧10O的净迁移。从S-Ala·2H2O(f)到TS1·2H2O(f)过程,键长1C—12H、14O—19H和17O—16H从0.109 1、0.098 1和0.098 8 nm分别拉伸至0.142 3、0.168 7和0.170 3 nm断裂,活性中心骨架二面角6N—1C—4C—9C变化较小。1个C—H键较大幅度的断裂需要一定的能量,2个O—H键的断裂也需要一些能量,这导致TS1·2H2O(f)会产生较高的能垒。但结构分析表明,过渡态TS1·2H2O(f)的八元环存在3条较强的氢键,TS1·2H2O(f)比较稳定;IRC计算表明,TS1·2H2O(f)是协同非同步晚期过渡态,从S-Ala·2H2O(f)到TS1·2H2O(f)过程是2个O—H键依次断裂成键后C—H才断裂,这又降低了从S-Ala·2H2O(f)越过TS1·2H2O(f)所需的能量。因此TS1·2H2O(f)产生的能垒不是很高,是146.1 kJ/mol,远低于单体TS1产生的247.9 kJ/mol的能垒,说明2个水分子簇对此基元反应有极好的催化作用。
3个水分子簇与2个水分子簇做质子迁移媒介时的机理基本相同,不再赘述,TS1·3H2O(f)产生的能垒是141.8 kJ/mol。在误差允许的范围内可以认为其与TS1·2H2O(f)产生的能垒146.1 kJ/mol相等,原因是TS1·3H2O(f)的九元环的4条氢键稍强于TS1·2H2O(f)的八元环的3条氢键,但TS1·3H2O(f)的九元环结构较TS1·2H2O(f)的八元环结构偏离平面程度大,降低了TS1·3H2O(f)的稳定性,因此他们产生的能垒相差不明显。
第2基元反应,同上只讨论2个和3个水分子簇的情况。
2个水分子簇做质子迁移媒介时,首先2个水分子簇在INT1的后面与质子化氨基上的15H和手性碳1C氢键作用,形成络合物INT1·2H2O(b)。然后INT1·2H2O(b)经过渡态TS2·2H2O(b)异构成第2中间体络合物R-INT2·2H2O(b),此时S-Ala·2H2O实现了手性转变。此基元反应是2个水分子簇做质子迁移媒介,实现了质子从质子化氨基在纸面里向α-碳的净迁移。从INT1·2H2O(b)到TS2·2H2O(b)过程,键长6N—15H和18O—17H基本没变,14O—13H从0.098 5 nm拉伸至0.123 4 nm断裂。1个O—H键的小幅拉伸断裂需要的能量不高,TS2·2H2O(b)产生的能垒是22.9 kJ/mol。这比2.1节TS2产生的能垒大幅降低,说明2个水分子簇对此基元反应有极好的催化作用。
3个水分子簇与2个水分子簇做质子迁移媒介时的机理基本相同,TS2·3H2O(b)产生的能垒是18.8 kJ/mol,其与TS2·2H2O(b)产生的能垒差别不是很大。
第4基元反应,计算表明,2个水分子簇的催化作用好于1个水分子很多,比3个水分子簇的催化作用也好写,故这里只讨论2个水分子簇的情况。
首先2个水分子簇在R-INT3的右侧,水分子簇与羧基氢键作用,形成络合物R-INT3·2H2O(r)。
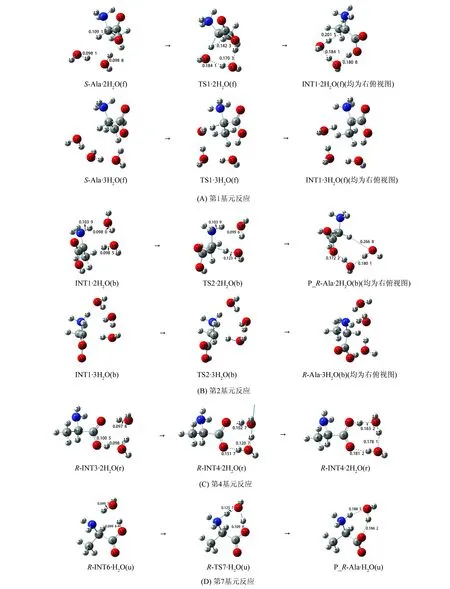
图4 水分子簇做质子转移媒介的第1、2、4、7基元反应历程及驻点结构Fig.4 Process of elementary reaction 1, 2, 4, 7 and stationary point structures with water molecules clusters as proton transfer carrier
然后R-INT3·2H2O(r)经过渡态R-TS4·2H2O(r)异构成第4中间体络合物R-INT4·2H2O(r),此基元是2个水分子簇做质子迁移媒介,R-INT3实现了质子在羧基内的净迁移。从R-INT3·2H2O(r)到R-TS4·2H2O(r)过程,键10O—12H、14O—15H和19O—16H的键长从0.100 5、0.098 3和0.097 8 nm分别拉伸至0.151 7、0.120 7和0.102 7 nm断裂。IRC计算表明,R-TS4·2H2O(r)是协同非同步过渡态,在R-TS4·2H2O(r)只是10O—12H和14O—15H断裂,过渡态之后之后19O—16H才断裂。2个O—H键的断裂需要一些能量。又结构分析表明,R-TS4·2H2O(r)的八元环结构基本在同一平面,八元环结构的3条氢键也较强,这导致R-TS4·2H2O(r)产生的能垒又不会太高,是35.5 kJ/mol。该能垒远低于单体TS4产生的能垒137.1 kJ/mol,说明2个水分子簇对此基元反应有极好的催化作用。
第7基元反应,计算表明,水分子(簇)对此基元反应起了阻碍作用,为节省篇幅,这里仅讨论1个水分子的作用。
首先1个水分子在R-INT6的上部,水分子与氨基和羧羟基氢键作用,形成络合物R-INT6·H2O(u)。
然后R-INT6·H2O(u)经过渡态R-TS7·H2O(u)异构成产物络合物P_R-Ala·H2O(u)。此基元是1个水分子做质子迁移媒介,实现了质子从羧基向氨基的净迁移。从R-INT6·H2O(u)到R-TS7·H2O(u),键10O—12H和14O—15H的键长从0.099 6和0.099 7 nm分别拉伸至0.109 9和0.125 7 nm断裂。2个O—H键的小幅拉伸所需能量不会很高,并且氨基氮具有较好的获得质子的能力,因此R-TS7·H2O(u)产生的能垒较小,仅有8.7 kJ/mol。但此能垒高于单体的R-TS7产生的能垒2.3 kJ/mol,说明水分子对此基元起了负催化作用。原因之一是从R-INT6·H2O(u)到R-TS7·H2O(u)过程比从R-INT6到R-TS7过程多1个化学键的断裂;原因之二是结构分析表明,R-TS7·H2O(u)的7圆环结构远小于R-TS7的五圆环结构的共面程度。
2.2.2 n通道上水分子簇作质子迁移媒介的第2基元反应 同于前面的第1基元反应,只讨论2个和3个水分子簇的情况,反应历程见图6,反应过程的吉布斯自由能势能面见图5的n曲线。
2个水分子簇做质子迁移媒介时,首先2个水分子簇在INT1的后面与α-碳1C和羧羟基氢16H氢键作用,形成络合物n_INT1·2H2O(b)。然后n_INT1·2H2O(b)经过渡态n_TS2·2H2O(b)异构成产物络合物n_P_R-Ala·2H2O(b)。此基元反应是2个水分子簇做质子迁移媒介,实现了质子从质子化氨基向α-碳1C的净迁移。从n_INT1·2H2O(b)到n_TS2·2H2O(b)过程,键10O—16H、17O—19H和14O—12H的键长从0.098 3、0.097 9和0.098 6 nm分别拉伸至0.099 5、0.099 7和0.119 3 nm,只是14O—12H明显拉伸断裂,活性中心骨架二面角6N—1C—4C—9C从-153.70°变为-124.41°。1个O—H键小幅度的断裂和骨架不大的形变需要的能量不高,n_TS2·2H2O(b)产生的能垒只有16.8 kJ/mol。n_TS2·2H2O(b)靠近n_INT1·2H2O(b),是早期过渡态,此基元反应是协同非同步过程。结构分析表明,n_P_R-Ala·2H2O(b)和S-Ala·2H2O(f)镜像对称,因此在此通道S-Ala·2H2O只经2步反应就实现了手性对映体转变。计算表明n_P_R-Ala和S-Ala也镜像对称,亦即n_P_R-Ala·2H2O(b)脱水后得到了S-Ala手性对映体n_P_R-Ala。
3个水分子簇与2个水分子簇做质子迁移媒介时的机理基本相同,不再赘述。n_TS2·3H2O(b)产生的能垒是10.3 kJ/mol,与n_TS2·2H2O(b)产生的能垒相比较明显减小,说明3个水分子簇比2个水分子簇对此基元反应的催化作用好些。
综合图3和图5可以看出,水分子簇的催化使水液相下S-Ala的手性对映体转变可以在两个通道进行,决速步能垒和总活化能均来自第1基元反应,决速步能垒和总活化能是146.1 kJ/mol(2个水分子簇催化)和141.8 kJ/mol(3个水分子簇催化)。新通道n的第2能垒低于原来通道3、4和5基元的能垒,n通道具有优势。由于正负反应能垒低于40.0 kJ/mol时,反应物和产物可同时存在[24],水分子簇的催化使水液相下S-Ala手性转变的产物是R-INT2、R-INT3、R-INT4、R-INT5、R-INT6和P_R-Ala同时存在,只是P_R-Ala的分布最高,并且是S-Ala的手性对映体。
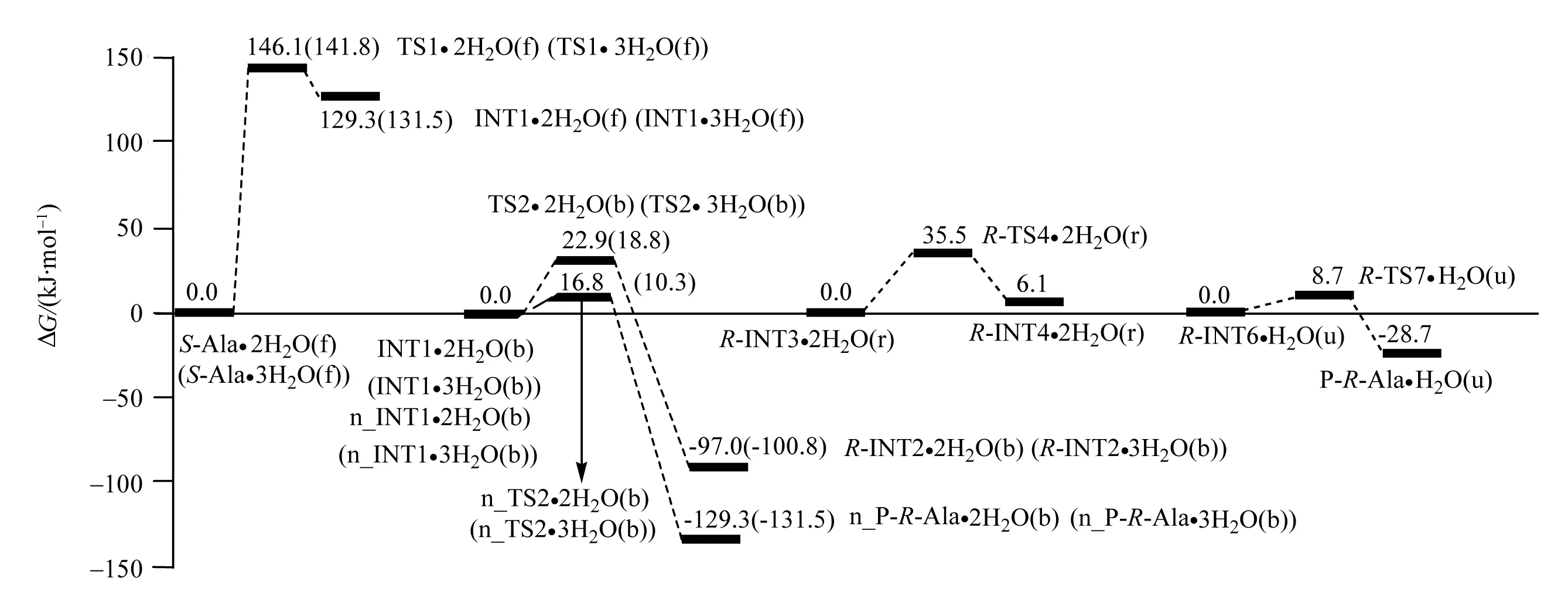
图5 水分子(簇)做媒介S-Ala手性对映体转变过程中氢迁移反应的势能面Fig.5 Potential energy surfaces of hydroge transfer reaction in chiral enantiomer transition of S-Ala with water molecules(clusters) as transfer carrier
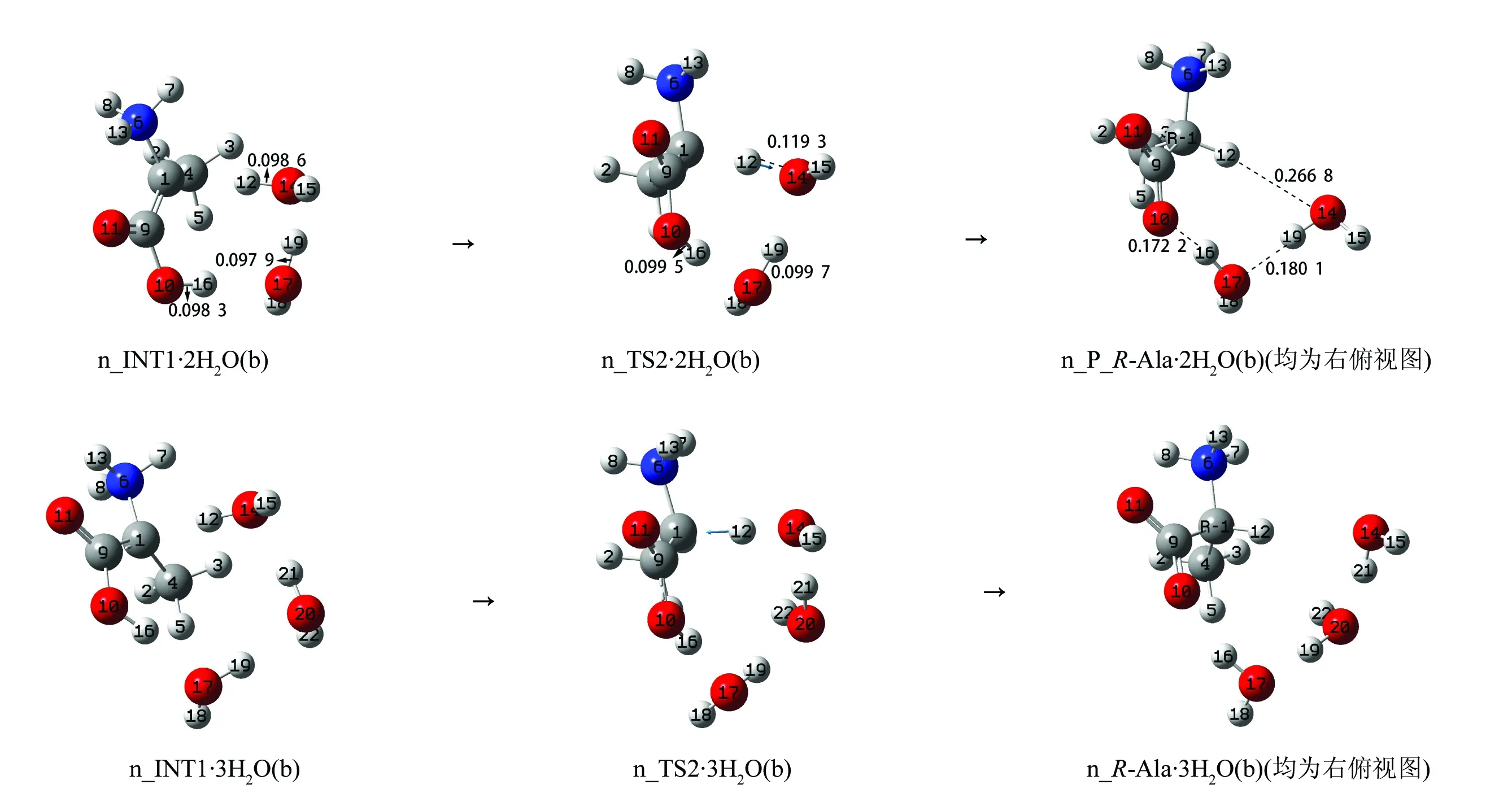
图6 n通道上水分子簇做质子转移媒介的第2基元反应历程及驻点结构Fig.6 Process of elementary reaction 2 and stationary point structures with water molecules clusters as proton transfer carrier in channel n
3 结 论
在SMD/MP2/6-311++g(3df, 2pd)//SMD/WB97X-D/6-31++G(d, p)双水平,对水液相环境下α-丙氨酸两性离子的手性对映体转变及水分子(簇)的催化进行研究得到如下结论:
水液相下单体S-Ala实现手性对映体转变只有一个通道,总反应的活化能是281.6 kJ/mol,决速步骤是第一基元反应,决速步内禀能垒是247.9 kJ/mol。产物同时以R-INT4、R-INT5、R-INT6和P_R-Ala四种构象共存,其中P_R-Ala是S-Ala的手性对映体,分布最高。
水液相下水分子(簇)催化的S-Ala的手性对映体转变可以在两个通道进行,水分子(簇)对水液相下S-Ala手性对映体转变过程的质子迁移反应有正催化也有负催化。水分子(簇)对总反应具有正催化作用,使决速步能垒和总活化能降到146.1 kJ/mol(2个水分子簇催化)和141.8 kJ/mol(3个水分子簇催化),在新通道n上的手性对映体转变具有优势。S-Ala手性转变的产物是R-INT2、R-INT3、R-INT4、R-INT5、R-INT6和P_R-Ala同时存在,其中P_R-Ala的分布最高。
结果表明:水液相下S-Ala两性离子可以在水分子簇的催化作用下缓慢实现手性对映体转变。

