川芎嗪涂膜剂的制备及其体外经皮渗透特性研究
王颖 何亚楠 车逸豪 袁仕梦 赵海荣 巫秀美 杨志斌


中图分类号R969;R541
文献标志码A
文章编号1001-0408(2020)02-0160-05
DOI
10.6039/{.issn.1 001-0408.2020.02.07
摘 要 目的:初步优选川芎嗪涂膜剂的制备工艺,并研究其体外经皮渗透特性。方法:采用单因素试验,以聚乙烯醇(PVA-124)、无水乙醇、甘油、吐温80、氮酮的用量为因素,采用改良的评分标准对涂膜剂基质的成膜时间、成膜性、延展性、均匀度和有无气泡等指标进行评价,优选川芎嗪涂膜剂基质处方。在优选基质处方的基础上制备备不同载药量川芎嗪(300、250、200、150、100、50 mg/mL)的涂膜剂,并考察其最大载药量。采用高效液相色谱法测定川芎嗪含量,并进行方法学考察。取离体大鼠背部皮肤,对高、中、低载药量(100、75、50 mg/mL)川芎嗪涂膜剂进行体外经皮渗透试验,分别于第15、30、45、60、75、90、120、150、180 min时取样测定,并计算川芎嗪的渗透速率。结果:PVA-124、无水乙醇、甘油、吐温80、氮酮的用量分别为2.5 9、7.0 mL、1.97mL、0.07 mL、0.28 mL(以50 mL处方量计)时的川芎嗪涂膜剂基质处方为最优;川芎嗪的最大载药量为100 mg/mL。川芎嗪含量测定方法的线性范围为3.125-100 μg/mL,其专属性、精密度、重复性、回收率、稳定性考察均符合要求(RSD均小于2%);高、中、低载药量川芎嗪涂膜剂的渗透速率分别为608.42、384.19、158.20 μg/(cm2.h)。结论:按优选处方制备的川芎嗪涂膜剂成膜时间短、质量稳定可靠,载药量可达100 mg/mL;75 mg/mL载药量的涂膜剂即可达到川芎嗪有效治疗血药浓度的渗透速率范围。
关键词 川芎嗪;涂膜剂;处方优化;大鼠;经皮渗透试验;渗透速率
近年来,我国心脑血管疾病发病率高且呈上升趋势,截至2017年我国心脑血管病患者人数已达到2.9亿,多数患者需长期服药[1-2]。中医药在临床用于心脑血管疾病的治疗已有较多实践及报道,开发中药成分类心脑血管疾病治疗的新型制剂具有重要意义。川芎嗪,又名四甲基吡嗪(Tetramethylpyrazine,TMPZ),是从中药川芎中提取的一种活性生物碱,具有活血化淤的功能[3],是治疗心脑血管疾病的有效成分[4]。已上市的川芎嗪制剂主要包括口服制剂和注射剂等,但易引起胃部不适及累积性中毒等不良反应[5]。为改善上述问题,国内外研究者研制开发了川芎嗪的体外透皮吸收剂型,如贴剂、凝胶剂和软膏剂等外用制剂,并取得了一定进展[6-8],但尚未见到有关川芎嗪涂膜剂的制备及对其透皮吸收规律的研究。涂膜剂是将药物溶解或分散于含成膜材料的溶剂中,涂抹后可逐渐释放药物从而起治疗作用的一种新型外用剂型,具有无首关效应、生物半衰期长、药物毒副作用小等优点,并可提高患者服药依从性[9-12]。基于此,本研究拟制备一种川芎嗪涂膜剂并优选其制备方法,同时研究其透皮吸收特性,旨在为该剂型的后续开发奠定基础。
1 材料
1.1 仪器
TPY-2型药物透皮扩散试验仪(上海黄海药检仪器有限公司);BSA124S型微量电子天平[赛多利斯科学仪器(北京)有限公司];TCL-16M型台式高速冷冻离心机(湖南湘立科学仪器有限公司);DHG-9240型电热鼓风干燥箱(上海一恒科学仪器有限公司);VORTEX-5型涡旋混合器(海门市其林贝尔仪器制造有限公司);1260Infrnity型高效液相色谱仪(美国Agilent公司);SK8200H型超声波清洗器(上海科导超声仪器有限公司);HWS24型电热恒温水浴锅(上海一恒科技有限公司);DZG-303A型超纯水机(上海艾柯仪器有限公司)。
1.2 药品与试剂
川芎嗪原料药(深圳市丽晶生化科技有限公司,批号:11032-118,纯度:≥99%);川芎嗪对照品(中国食品药品检定研究院,批号:110817-201608,纯度:≥98%);0.9%氯化钠注射液(昆明南疆制药有限公司,批号:C150120L;作为生理盐水使用);薇婷脱毛膏[利洁时家化(中国)有限公司,批号:J20140017];乙腈(色谱纯,北京百灵威科技有限责任公司,批号:17115012,色谱纯);聚乙烯醇124(PVA-124,西陇化工股份有限公司,批号:151024);无水乙醇(天津市福晨化学试剂厂,批号:20161008);甘油(浙江遂昌惠康药业有限公司,批號:20141230);吐温80(上海索莱宝生物科技有限公司,批号:626N047);氮酮(湖北科捷制药有限公司,批号:161201);乙腈(北京百灵威科技有限责任公司,批号:17115012,色谱纯);其他试剂均为国产分析纯,水为超纯水。
1.3 动物
健康成年SD大鼠,清洁级,雄性,体质量180~220g,购于湖南斯莱克景达实验动物有限公司,动物生产许可证号:SCXK(湘)2016-0002。大鼠在大理大学实验动物中心适应性饲养1~2周后,用于后续实验。饲养条件:清洁级,室温16~22℃,相对湿度70%,12 h明暗交替照明,动物自由进食、饮水。动物处置方法均符合中国伦理委员会有关动物研究指导原则要求。
2 方法与结果
2.1 川芎嗪涂膜剂制备方法的优化
2.1.1 涂膜剂基质的制备参照文献方法[13],按处方量称取成膜材料PVA-124适量,加水密封浸润24 h,于90℃水浴下溶胀至凝胶状,取出放凉;边搅拌边向PVA-124凝胶溶液中依次加入处方量的无水乙醇、甘油、吐温80、氮酮,搅拌使之分散均匀,最后加水至足量,得黏稠状涂膜剂基质。
2.1.2 涂膜剂基质的评价方法取“2.1.1”项下涂膜剂基质1 mL均匀涂抹于3 cmx3 cm的玻璃板上,以成膜时间、成膜性、延展性、均匀度以及有无气泡等作为指标进行评价[14],评分标准见表1。由于成膜时间(a)和成膜性(b)是评价涂膜剂的重要指标,故设定其权重为0.3;延展性(c)、均匀度(d)、有无气泡(e)均由直接观察得到,存在一定主观性,故设定其权重为0.2。按公式计算综合评分(y):y=0.3×(a+b)+0.2×(c+d+e)。
2.1.3 单因素试验优化基质处方根据前期预试验考察结果,对基质影响最大的5个因素分别为PVA-124用量(A)、无水乙醇用量(B)、甘油用量(C)、吐温80用量(D)和氮酮用量(E)。对上述因素分别进行考察及处方优化:(I)PVA-124用量:在基质处方的其他成分基本不变的情况下,设置PVA-124用量分别为1.5、2.0、2.5、3.0g(基质处方量均以50 mL计,以下同);(2)无水乙醇用量:在基质处方的其他成分基本不变的情况下,设置无水乙醇体积分数分别为6.0、6.5、7.0、7.5、8.0、8.5 mL;(3)甘油用量:在基质处方的其他成分基本不变的情况下,设置甘油用量分别为1.77、1.97、2.17、2.37 mL;(4)吐温80用量:在基质处方的其他成分基本不变的情况下,设置吐温80用量分别为0.05、0.07、0.09、0.11 mL;(5)氮酮用量:在基质处方的其他成分基本不变的情况下,设置氮酮用量分别为0.26、0.28、0.30、0.32 mL。
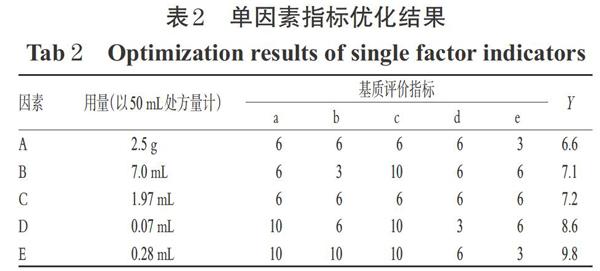
根据上述不同因素水平和“2.1.1”项下方法分别制备涂膜剂基质(处方中不足部分以水补足)。对所制备的涂膜剂基质样品采用“2.1.2”项下评分标准进行评价。结果显示,PVA-124、无水乙醇、甘油、吐温80、氮酮的用量分别为2.5 g、7.O mL、1.97 mL、0.07 mL、0.28 mL时,相应的基质综合评分最高,详见表2。
2.1.4 涂膜剂载药量的考察在“2.1.3”项下优选的基质处方基础上制备含不同载药量川芎嗪(300、250、200、150、100、50 mg/mL)的涂膜剂,再按“2.1.2”项下的评分标准优选川芎嗪涂膜剂的载药量。结果显示,当载药量≤100 mg/mL时,所制备的川芎嗪涂膜剂体系分散均匀,成膜完整连续,易于涂布,成膜时间在5 min以内,且不会出现药物析出等现象,故将100 mg/mL设定为该涂膜剂的最大载药量。
2.1.5 川芎嗪涂膜剂的制备按基质处方工艺和载药量考察结果,称取PVA-124 5.Og,加入水80 mL密封浸润24 h后,于90℃水浴下溶胀至凝胶状,取出放凉;边搅拌边向PVA-124凝胶溶液中加入川芎嗪10 g,再依次缓慢加入无水乙醇溶液14 mL、甘油4 mL、吐温80 0.15mL、氮酮0.55 mL,搅拌使之分散均匀,最后加水至100mL,即得黏稠状的川芎嗪涂膜剂(载药量100 mg/mL)。同法制备载药量为75、50 mg/mL的川芎嗪涂膜剂,用于后续试验。
2.2 川芎嗪含量测定方法的建立
2.2.1 色谱条件色谱柱:Symmetry-C18(250 mmx4.6mm,5μm);流动相:水(A)-乙腈(B),梯度洗脱(0~20min, 5%B→41%B);流速:1.0 mL/min;柱温:35℃;检测波长:280 nm;进样量:5μL。
2.2.2 线性关系考察精密称取川芎嗪对照品10 mg,加生理盐水溶解并定容至50 mL,制得200 μg/mL的对照品母液。取上述对照品母液适量,以生理盐水稀释制成质量浓度分别为100、50、25、12.5、6.25、3.125 μg/mL的系列对照品溶液。取上述系列对照品溶液各适量,按“2.2.1”项下色谱条件分别进样检测,平行操作3次。以峰面积为纵坐标(y)、质量浓度为横坐标(x)进行线性回归,得标准曲线y=7.398 9x-2.286 2(r=0.999 9)。结果表明,川芎嗪质量浓度在3.125~100 μg/mL范围内线性关系良好。
2.2.3 专属性试验取未给药大鼠的背部皮肤,加生理盐水适量研磨后制成空白皮肤匀浆液后备用;取空白涂膜剂基质,加生理盐水适量稀释后备用;取体外经皮渗透试验3h时的接收液冻干样品,加适量生理盐水溶解后备用;取川芎嗪原料药,加适量空白皮肤匀浆液溶解后备用;取川芎嗪原料药,加适量生理盐水溶解后备用。取上述溶液各适量,按“2.2.1”项下色谱条件分别进样检测,记录色谱图。结果显示,各色谱峰分离良好,无杂质峰干扰,表明涂膜剂基质和空白皮肤匀浆液对川芎嗪的含量测定无干扰,详见图1。
2.2.4 精密度试验取“2.1.5”项下制备的川芎嗪涂膜剂(载药量50 mg/mL),用生理盐水稀释制成低、中、高質量浓度(6.25、25、100 μg/mL)的溶液,于同日内的3个不同时间点,按“2.2.1',项下色谱条件进样测定,每个浓度均重复测定6次。结果,川芎嗪峰面积RSD分别为0.49%、0.65%、0.42%(n=6),表明该方法精密度良好。2.2.5重复性试验取体外经皮渗透试验中川芎嗪涂膜剂(载药量50 mg/mL)在90 min时的取样液各适量,共6份,按“2.2.1”项下色谱条件进样测定,并按标准曲线法计算含量。结果,取样液中川芎嗪含量为24.71 μg/mL,RSD为1.12%(n==6),表明该方法重复性良好。
2.2.6 稳定性试验精密吸取体外经皮渗透试验中川芎嗪涂膜剂(载药量50 mg/mL)在90 min时的接收液适量,分别在室温下放置0、4、8、12、16、24 h时,按“2.2.1”项下色谱条件进样测定,结果,川芎嗪峰面积RSD为0.61%(n=6);另取上述样品接收液适量,于-80℃分别冻融1、2、3、4、5、6次,同法进样测定,结果,川芎嗪峰面积RSD为1.98%(n=6)。结果表明,样品接收液在室温下放置24h或冻融6次的条件下稳定性均较良好。2.2.7加样回收率试验精密吸取体外经皮渗透试验中川芎嗪涂膜剂(载药量50 mg/mL)在90 min时的接收液(已知含川芎嗪24.71 μg/mL),共5份,每份1 mL,分别加入“2.2.2”项下25 μg/mL的对照品溶液1 mL,混匀,按“2.2.1”项下色谱条件进样测定并计算加样回收率。结果,川芎嗪平均加样回收率为101.6%,RSD为1.91%(n==5),表明本方法准确度较好。
2.3 川芎嗪涂膜剂体外经皮渗透特性考察
2.3.1 离体鼠皮制备参照文献方法[16]进行离体鼠皮制备。以脱毛膏对大鼠背部皮肤进行脱毛处理,次日将大鼠断颈处死,分离已脱毛的背部皮肤,仔细剥离皮下脂肪层和结缔组织,用生理盐水冲洗干净并浸泡,4℃保存备用。
2.3.2 体外经皮渗透试验取“2.3.1”项下制备的离体鼠皮,置于药物透皮扩散试验仪的直立式扩散池(扩散杯面积为2.54 cm2)中,角质层面向供给室,真皮层面向接收室。使皮肤与扩散液(生理盐水7 mL)结合紧密、无气泡,设置温度为(37±0.5)℃、接收池搅拌子转速为300 r/min[l6]。试验设置川芎嗪涂膜剂高、中、低剂量组,于离体表皮层皮肤涂抹“2.1.5”项下制备的高、中、低载药量(100、75、50 mg/mL)的川芎嗪涂膜剂各300 μL,进行经皮渗透试验,平行测定3次。分别于第15、30、45、60、75、90、120、150、180 min时吸取接收液样品各1 mL,同时补加等容等温的新鲜扩散液。取样液于-80℃冷冻保存,室温解冻后备测。
2.3.3 数据处理与统计取“2.3.2”项下各时间点的取样液,根据“2.2”项下方法测定川芎嗪含量,并按照以下公式计算川芎嗪的单位面积累积渗透量(Qn)[17]:Qn=(
)/A0式中,A为有效经皮吸收面积(2.54cm2),V为扩散液总体积(7 mL),K为取样液体积(1mL),Cn为第n次取样时样品接收液中的药物浓度,Ci为第i次(i≤n-l)取样时接收液中的药物浓度。以Qn为纵坐标、时间(t)为横坐标作经皮渗透曲线图,并在O~180 min的时间范围内以Qn对t进行线性回归,所得斜率即为药物的渗透速率(J)。
对3种不同载药量的川芎嗪涂膜剂的经皮渗透曲线进行比较(如图2所示),结果显示,高、中、低载药量的川芎嗪涂膜剂的J值分别为608.42、384.19、158.20μg/(cm2·h)。这表明在载药量50~100 mg/mL的范围内,川芎嗪体外渗透速率随载药量的增加而增大。
3 讨论
在药物透皮吸收研究中,实验用离体皮肤的性质及状态对药物的经皮渗透行为影响較大。最理想的皮肤材料是利用人体皮肤进行实验研究,但人体皮肤难以获得。因此,基于与人体皮肤接近程度及可及性考虑[18-19],本试验选择大鼠皮肤为模型进行制剂的经皮渗透特性研究。
涂膜剂制备工艺的好坏直接影响到涂膜剂的稳定性及其质量。除成膜时间为量化指标外,成膜性、均匀度等性能均是依靠主观来定性评价,因此本课题组对传统评分标准进行了改良,将成膜时间、成膜性等分别量化计分,并作为评价涂膜剂的重要指标,设定其权重为0.3;而对于存在一定主观性的延展性、均匀度、有无气泡等观察指标,则将权重设定为0.2,提高了该涂膜剂评价标准的准确性。
本实验通过单因素考察初步探索了川芎嗪涂膜剂的处方,后续将进一步通过正交设计或响应面法等对制备工艺进行优化。现工艺中涂膜剂的最大载药量为100 mg/mL。本研究分别考察了高、中、低(100、75、50mg/mL)3种载药量川芎嗪涂膜剂的体外透皮特性,结果显示,在透皮扩散面积为2.54 cm2的情况下,75 mg/mL载药量的涂膜剂渗透速率为384.19 μg/(cm2.h),已达到文献报道的川芎嗪有效治疗血药浓度的渗透速率范围即157.17~488.085 μg/(cm2.h)[20],可作为后续川芎嗪涂膜剂有效载药量进一步优化筛选的参考依据。
综上,本研究设计并制备了川芎嗪涂膜剂并初步考察了其体外释放特性,其制备工艺简便,所得75 mg/mL载药量的涂膜剂的体外渗透速率可达到川芎嗪有效血药浓度的渗透速率范围。但体外试验结果无法完全反映体内生物环境的影响,因此后续需进一步评价川芎嗪涂膜剂的体内有效性和安全性,并进行质量研究,以期为该制剂的开发和应用提供更多的理论依据。
参考文献
[1]刘星言,何志巍,李彩虹,等.川芎嗪醇质体贴剂的制备及体内外评价[J].中国现代医学杂志,2012,22(18):23-27.
[2]马丽媛,吴亚哲,王文,等.《中国心血管病报告2017》要点解读[J]中国心血管杂志,2018,23(1):3-6.
[3]王巧凤.川芎嗪注射液治疗急性脑血栓形成42例疗效观察[J].实用医技杂志.2003,10(1):29.
[4]王利胜,袁爱贤,韩坚,等.HPLC法测定川芎嗪在小鼠血浆、脑、肝中的含量[J].中国药房,2008,19(9):654-656.
[5]张廷伟.盐酸川芎嗪的药理作用及其临床应用[J].医药导报,2006,25(11):1179-1181.
[6]胡晓飞,刘善新,毕建云,等.川芎嗪透皮吸收研究进展[J].辽宁中医药大学学报,2014,16(8):162-164.
[7]侯惠民,杞晓红,王浩.含有川芎嗪的组合物以及川芎嗪透皮贴剂及其制备方法:中国,1415296A[P].2003-05-07.
[8]王丽.磷酸川芎嗪制剂研究进展[J].科学技术创新,2018(27):46-47.
[9]任佳佳.马黄涂膜剂的制备及透皮吸收研究[D].济南:山东中医药大学,2016.
[10]
VITORINO C, JOAO SOUSA, PAIS A. Overcoming theskin permeation barrier: challenges and opportunities[J].Curr Pharm Design,2015,21(20):1-2.
[11] AHADA,AQILM,ALl A. Investigation of antihyperten-sive activity of carbopol valsartan transdermal gel contai-ning 1,8-cineole[J]. Int t,Biol Macromol, 2014, 64: 144-149.
[12]
KIM JH, KO JA, KIM JT, et al. Preparation of a capsai-cin-loaded nanoemulsion for improving skin penetra-tion[J]. JAgric Food Chem,20 14, 62(3):725-732.
[13]张枝雪,黄茜,李玥,等.膜翅目昆虫提取物Ento-Ⅱ涂膜剂的镇痛及活血化瘀作用研究[J].中草药,2018,49(9):2108-2113.
[14]谢玲,钟晓红,刘东波,等,紫珠止血涂膜剂成膜材料及附加剂的优选[J].中国实验方剂学杂志,2012,18(5):27-29.
[15]张援,许实波,李向阳,等.不同接受液和动物皮肤对格列美脲体外经皮渗透行为的影响[J].中山大学学报(自然科学版),2004,43(5):86-90.
[16]肖学成,熊驰,彭秀菊,等.HPLC测定他克莫司软膏體外透皮吸收[J].中国现代应用药学,2014,31(7):839-843.
[17]崔颖,张韻慧,郭鹏.四元单纯形网格法优化磷酸川芎嗪微乳处方[J].中成药,2009,31(1):43-46.
[18]刘建芳,吕慧英,侯艳宁.涂膜剂的研究进展[J].中国医院药学杂志,2010,30(4):325-327.
[19]赵培,于莹莹,王晓冬.乌头总碱贴片对不同动物皮肤经皮渗透性比较[J].哈尔滨商业大学学报(自然科学版),2007,23(6):27-29、67.
[20]
QI X,ACKERMANN C,SUN D,et al.Physicochemicalcharacterization and percutaneous delivery of 2,3,5,6-te-tramethylpyrazine[J]t Int,Pharm,2003,253 (1/2):177- 183.
(收稿日期:2019-07-02 修回日期:2019-12-08)
(编辑:段思怡)
△基金项目:国家自然科学基金资助项目( No.81703742);云南省科技计划青年项目(No.2016FD074);国家地方联合工程研究中心创新能力建设项目(No.云发改高技[2015]395);云南省科技创新平台建设计戈0项目(No.2015DG030)
*硕士研究生。研究方向:药物新剂型。电话:0872-2214251。E-mail: wy15754632309@126.com
# 通信作者:助理研究员,博士研究生。研究方向:药物新剂型。电话:0872-22142510 E-mail: 79204431@163.com

