吡啶在有机合成中的应用
王 磊,刘中付,肖陆飞
(1.滁州职业技术学院 食品与环境工程系,安徽 滁州239000;2.滁州市生态环境局,安徽 滁州239000)
吡啶,又名氮杂苯,分子式C5H5N,是一种具有共轭结构的六元杂环化合物。在常温常压下为无色或者微黄色液体,具有刺激性的臭味,易燃、易爆、有毒。熔点-41.6℃,沸点115.3℃,密度0.98 g/cm3。目前,文献报道的制备吡啶的方法主要有两种,一是从煤炼焦油中提取吡啶,二是通过化学合成法得到吡啶,如醛或酮和氨的反应、1,5-二羰基化合物和氨的反应、醇和氨的反应、不饱和烃的氨氧化合、烷基吡啶脱烷基等。吡啶是一种重要的化工中间体,广泛应用于农药、医药、兽药、染料、香料、表面活性剂、缓蚀剂、饲料、食品添加剂、太阳能电池等领域,其中多数领域涉及有机合成,如它可作为有机反应的溶剂、原料、催化剂和缚酸剂等。鉴于此,本文研究了吡啶在有机合成中的重要应用。
1 作为有机反应的溶剂
绝大多数有机反应都是在溶剂中发生的,溶剂的性质对于有机反应的速率和产率有着重要影响。在有机合成反应中,溶剂除了起到传热和传质作用,还决定了化学反应的历程。因此,溶剂常被作为有机反应的一个重要影响因素而广泛研究,如溶剂的极性、毒性、沸点、价格等性质,从而选择最合适的溶剂。吡啶由于环中氮原子的吸电子诱导效应,使得其具有较强的极性,不仅能与水以任意比互溶,还能溶解大多数的极性和非极性有机化合物,甚至能溶解某些盐类,因此,吡啶是一个很好的溶剂,可作为有机合成反应的溶剂。
乙酸异戊酯是实验室和工业上常用的一种有机溶剂,在调味、制革、胶片及纺织等领域有着重要应用。文献[1]以吡啶为溶剂,以异戊醇和冰醋酸为原料,回流反应1 h,收率达到84.4%,比以苯为溶剂大大节省了反应的时间,提高了反应的收率,这是因为吡啶的沸点比苯高,提高了反应所需的温度。该方法中由于吡啶和水互溶,有利于后期产品的分离提纯,是较理想的合成方法。6-乙硫基-3-庚烯-2-酮是重要的医药、农药中间体,由乙酰乙酸钠和乙硫丁醛在吡啶存在下缩合生成[2],反应温度为室温,反应条件温和,转化率可达95%,适合工业化生产。此外,由于吡啶环上的N原子吸电子作用,吡啶是一个标准的缺π-电子杂环,具有抗氧化能力,因此更适宜于用作氧化反应的溶剂,如将异佛尔酮催化氧化制酮代异佛尔酮[3],以吡啶为溶剂,较胺类溶剂有更好的转化率和选择性。
然而由于吡啶的毒性及强烈的刺激性气味,限制了它只作为溶剂在有机反应中的应用。在多数有机反应中,吡啶除了具备溶剂的作用外,往往同时还兼有缚酸剂和催化剂的作用。
2 作为缚酸剂
由于吡啶环氮原子上有一对共用电子对,使得其可接受质子而显碱性,与强酸作用可形成稳定的盐,同样与路易斯酸反应也可成盐,因此可常用于有机反应中的缚酸剂,加速有机反应的进行。以吡啶为缚酸剂,多用于磺酰胺、酰胺、羧酸酯、磺酸酯、磷酸酯等的合成反应。
2.1 合成磺酰胺
文献[4]将邻硝基苯胺溶于干燥吡啶中,缓慢加入对甲苯磺酰氯,反应得到N(2-硝基苯基)-4-甲基苯磺酰胺,该物质可用来制备具有肿瘤细胞抑制作用的苯磺酰胺类组蛋白去乙酰化酶抑制剂。文献[5]报道了2-氨基-5,8-二甲氧基[1-2,4]三唑并[1,5-c]嘧啶和2-氟-6-三氟甲基苯磺酰氯进行反应,用干燥的吡啶来吸收反应生成的氯化氢,得到其磺酰胺缩合物中间体,继续与2,2-二氟乙醇反应得到除草剂五氟磺草胺。
2.2 合成碳酰胺
2,3-二氯-5-甲基吡啶是重要的农药和医药中间体,文献[6]报道了合成2,3-二氯-5-甲基吡啶的方法,在合成中间体N-苄基-N-(1-丙烯基)-氯乙酰胺时,使用吡啶作缚酸剂,产率可达到84%,比起碳酸钾和碳酸氢钾作缚酸剂效果要好很多,这可能是因为反应体系对无机缚酸剂溶解效果差的原因。文献[7]以自制的阳离子单酯表面活性剂氯化2-羟基-3-硬脂酰氧基丙基三甲基铵和硬脂酰氯为原料,用吡啶作为缚酸剂,成功制备出阳离子双酯表面活性剂氯化2,3-二(硬脂酰氧基)丙基三甲基铵,该表面活性剂结构上因为带有双酯,具有很好的生物降解性,是一种新型环保表面活性剂。
2.3 合成羧酸酯
薄荷基甲酸薄荷酯是一种重要的精细化工产品,因为具有较好的凉感,广泛用于牙膏中。薄荷基甲酸薄荷酯是由无水吡啶为缚酸剂,薄荷基甲酰氯和L-薄荷醇反应制备而成[8],实验考察了吡啶对反应收率的影响,发现当吡啶用量是L-薄荷醇用量的6倍时,产品收率最高。
2.4 合成磺酸酯
六对甲苯磺酸甘露醇酯是一种具有良好生物活性的药物,文献[9]以甘露醇为原料与对甲苯磺酰氯在吡啶中进行反应,反应温度为0~10℃,反应4 h,产率可达85.4%。该反应中吡啶作为缚酸剂与反应生成的氯化氢结合成稳定的盐,避免了氯化氢对不稳定反应物的副作用,加速了反应的进行。蚊蝇醚对粉虱、介壳虫等具有明显的灭杀效果,且毒性低,安全性好。
文献[10]以1-(4-苯氧基苯氧基)-2-丙醇和对甲苯磺酰氯反应,加入吡啶作为缚酸剂,合成了中间体1-(4-苯氧基苯氧基)-2-对甲苯磺酸丙酯,再与2-吡啶酸钠反应得到蚊蝇醚。酮康唑是第一个口服有效的咪唑类广谱抗真菌药,中间体1在甲苯中,以对甲苯磺酰氯为酰化试剂,吡啶为缚酸剂合成了产物2[11-12],其合成路线如图1,该物质为制备酮康唑的重要中间体。
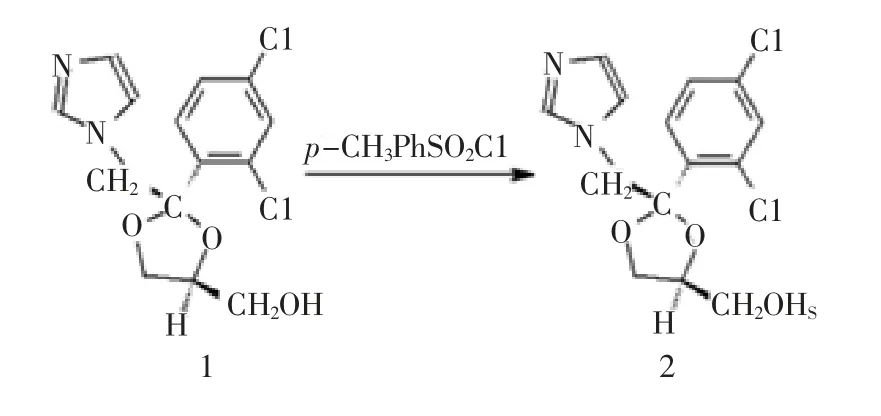
图1 酮康唑中间体2的反应方程式
2.5 合成磷酸酯
硫代磷酸三(4-取代基苯)酯是重要的精细化工产品,是合成异氰酸酯盐工业、染料工业的重要原料,还广泛应用于阻燃增塑剂、照相乳剂助剂、涂料、胆碱酯酶抑制剂中。文献[13]以对氨基酚和三氯硫磷为反应物,以丙酮为溶剂,合成了硫代磷酸三(4-氨基苯)酯,考察了缚酸剂N,N-二甲基苯胺、三乙胺、吡啶、氢氧化钠、碳酸钠等对反应收率的影响,实验表明三乙胺和吡啶对反应收率的影响要优于氢氧化钠和碳酸钠。然而由于吡啶有难闻的臭味,且单独使用吡啶作为缚酸剂的效果并不好,在三乙胺中加入少量的吡啶(2%左右)作为复合缚酸剂,反应收率比使用单一缚酸剂要高。
3 作为有机合成的催化剂
在一些有机反应中加入少量吡啶可以改变反应的速率和选择性,如加速固体光气分解成活性中间体、催化醛或酮与活泼α-氢原子的化合物反应、催化酸酐酯化反应、催化卤原子的取代反应、迈克尔加成等。
3.1 固体光气的引发剂
光气是非常好的羰基化试剂,在有机合成反应中起着重要作用,然而光气是剧毒性气体,危险性大且操作起来不方便。为实现光气反应过程中的绿色化,常用固体光气代替光气进行相关反应。固体光气又名三光气,化学名为双(三氯甲基)碳酸酯,可以和醇、醛、胺、酰胺、羧酸、酚、羟胺等多种化合物反应,在有机合成领域具有广阔的应用前景。在胺类引发剂的作用下,1分子固体光气可生成3分子的活性中间体,可在较温和的条件下与亲核试剂进行反应[14]。文献[15]以间甲基苯甲酸和二乙胺为原料,固体光气为酰氯化试剂,用少量吡啶引发固体光气,一锅法合成驱蚊剂N,N-二乙基间甲基苯甲酰胺(DETA),具体反应过程如图2,可知吡啶在该反应中既是固体光气的引发剂,也是酰化反应的缚酸剂。
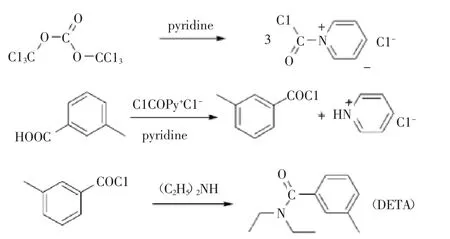
图2 吡啶引发固体光气合成DETA
3.2 Knoevenagel缩合反应
醛或酮在弱碱催化下,与具有活泼α-氢原子的化合物缩合得到α,β-不饱和羰基化合物的反应称为Knoevenagel反应,吡啶是常用的催化剂。文献[16-17]用苯甲醛和丙二酸为原料,吡啶为催化剂,经Knoenenagel缩合生成肉桂酸。该反应中,丙二酸中亚甲基上活泼氢在吡啶作用下形成碳负离子,进攻苯甲醛上的羰基碳,脱去吡啶和羧基后得到肉桂酸,反应机理如图3。类似的,α-氯代酮与β-酮酸酯在吡啶催化剂作用下可以生成呋喃衍生物[18]。
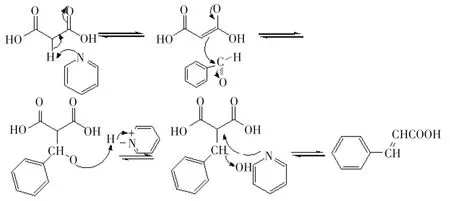
图3 吡啶催化合成肉桂酸
3.3 酸酐酯化反应
酸酐和醇的酯化反应要比相应的酸和醇的酯化反应更容易,酸酐的羧基碳受到羰基氧和另一羧基影响,更容易被亲核试剂进攻,且其离去基团为羧基,比羧酸成酯时的离去基团羟基更容易离去。反应中通常加入少量酸性或碱性催化剂来加速反应,如浓硫酸、高氯酸、氯化锌、吡啶、无水乙醇钠、乙酸钠等。乙酰水杨酸是目前国内外使用最多的解热镇痛抗炎药物,由于原料水杨酸中的酚羟基酯化反应较困难,多由水杨酸和乙酸酐反应而成。文献[19]以吡啶作为该反应的催化剂,用量为水杨酸的5%,在80℃反应30 min,产品纯化后的收率就可达到80%以上,可知吡啶是该反应的优良催化剂,这可能是因为一方面吡啶能和乙酸酐作用形成活性络合物,另一方面反应中生成的乙酸能和吡啶形成稳定的盐。
邻苯二甲酸丁苄酯是聚氯乙烯、聚醋酸乙烯、聚氨酯等多种合成材料的优良增塑剂,需求量逐年递增,其合成技术备受关注。近年来采用相转移催化新技术制备邻苯二甲酸丁苄酯的技术越发得到重视。文献[20]报道了先以邻苯二甲酸酐和正丁醇反应生成单酯,然后在氢氧化钠溶液中和苄氯反应,并加入适量的相转移催化剂制备邻苯二甲酸丁苄酯。研究发现在氢氧化钠溶液中加入少量吡啶,可提高反应的产率,同时可减少相转移催化剂的用量。这可能是因为吡啶能和苄氯作用形成N-苄基吡啶盐,如图4,它不仅增大了苄氯在水中的溶解度,并且由于吡啶环是一个良好的离去基团,所以N-苄基吡啶盐比苄氯更容易与邻苯二甲酸单丁酯负离子反应,从而提高产率。
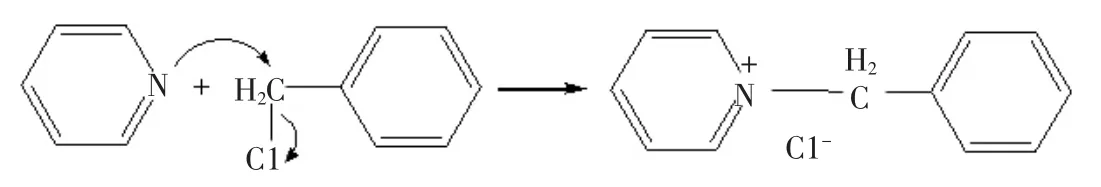
图4 吡啶和苄氯形成N-苄基吡啶盐
3.4 卤代反应
在亲核取代反应中,有时候由于亲核试剂的亲核性较弱,影响到反应的速率,这个时候可加入少量吡啶,使它先和较弱的亲核物质反应,结合成较强的活性中间体,或者将较弱的亲核试剂转化为较强的亲核试剂,从而加速反应的进行。如吡啶可以催化苯和溴素的反应生成溴苯[21],反应机理是吡啶和溴素先生成N-溴代吡啶,然后苯和N-溴代吡啶进行亲核取代反应得到溴苯,并释放出吡啶。
在有机分子中引入氟原子,使其具有独特的物理、化学性能和生物活性,可广泛应用在材料、工业助剂和药物等方面。章凯丽[22]以3-氨基苯甲酸为起始原料,在氟化氢吡啶试剂中一锅法合成了重要的化工中间体3-氟苯甲酸。该反应中吡啶首先进攻氟化氢生成亲核活性更强的氟负离子,然后再和重氮盐进行亲核取代反应。吡啶催化氟化氢的反应机理如图5。
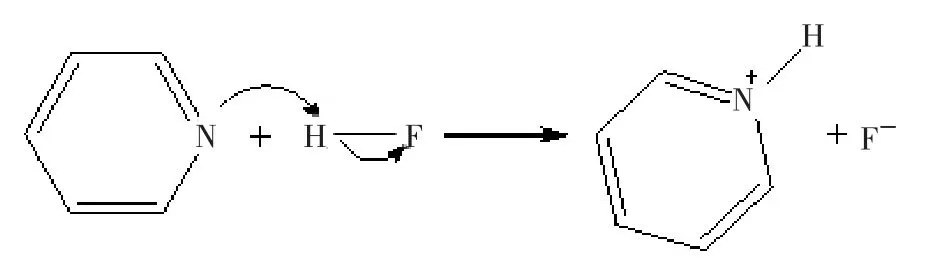
图5 吡啶催化氟化氢变成亲核活性更强的氟负离子
液溴是有机合成中常用的一种溴化剂,但由于液溴具有较高的挥发性和强烈的刺激性,加上液溴化学活性高,反应不易控制,近年来多使用它的替代物作为溴化剂。将吡啶、HBr和Br2在一起制成三溴吡啶 盐,它是一种优良的溴化剂,比起液溴反应要温和很多,常用于烯烃的溴加成反应和活泼α-氢原子的取代反应。王东林[23]以2,4-戊二酮和三溴吡啶盐为原料合成了3-溴-2,4-戊二酮,该物质是合成医药和农药的重要有机中间体,其反应式如图6。
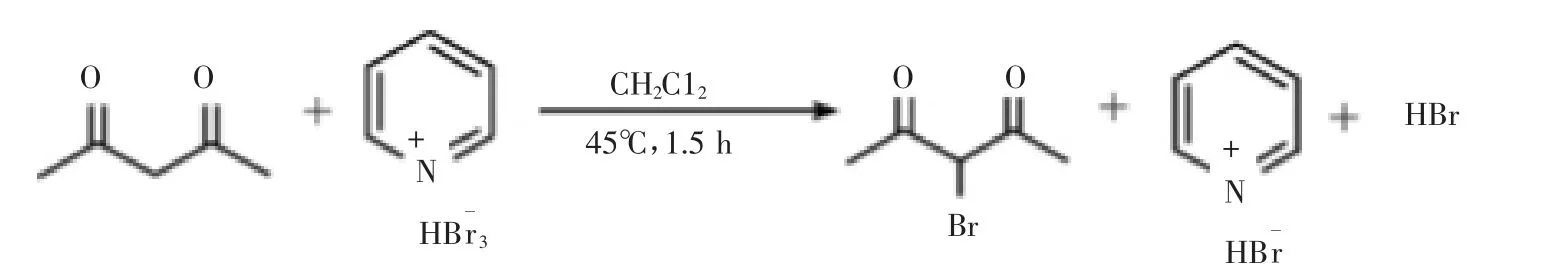
图6 3-溴-2,4-戊二酮的合成
4 作为有机反应的原料
由于吡啶环上氮原子的各向异性,环上各个位置有不同的电子云密度,邻对位电子云密度最低,氮原子上最高。吡啶环上可以发生亲电取代和亲核取代反应,但由于氮原子的吸电子作用,亲电取代反应较难发生,一般发生在氮原子的间位。亲核取代反应较容易发生,一般发生在邻对位。利用吡啶的化学性质以它为原料可以合成出更多的有机物。
4.1 吡啶环上直接取代反应
吡啶和氨基钠在甲苯或者二甲苯中反应,生成2-氨基吡啶,这是吡啶环上的第一个亲核取代反应,即著名的Chichibabin氨基化反应。吡啶环上可发生溴代反应,文献[24]以吡啶为原料,在浓硫酸的作用下,和Br2直接取代生成3-溴吡啶,该物质是一种重要有机合成中间体,在医药、农药等方面有着广泛的用途。研究发现,随着浓硫酸量的增加,反应收率有所提高,这可能是因为吡啶和浓硫酸先反应生成活性中间物N-吡啶磺酸,然后再在3位上进行溴代反应。吡啶环上的磺化反应很难发生,在硫酸汞催化作用下,也可得到较好的收率[25]。吡啶环上的烃基化反应是合成吡啶衍生物的常用方法之一,由于吡啶2位碳上的氢具有一定的酸性,在强碱性亲核试剂的进攻下,能生成2-烷基吡啶。常见的亲核试剂如烷基锂、格利雅试剂等[26]。
4.2 制备吡啶N-氧化物
由于吡啶环上2,4,6位电子云密度较低,吡啶环上的亲电取代反应较难发生。若吡啶环上有供电子基团时,可活化吡啶环上2,4,6位的亲电取代反应。吡啶N-氧化物上的氧负离子就是一个强的供电子基团,由于吡啶N-氧化物制备比较简单、价格低廉,被广泛地应用在活化和功能化吡啶方面,是一类重要的吡啶衍生物。同时吡啶N-氧化物也很容易被还原剂如PCl3还原成吡啶,这在制备各种不同位置取代基的吡啶发挥着重要作用。如吡啶环上很难发生硝化反应,即便是在酸性催化剂的作用下,也只有少量的发生在3位上。但吡啶N-氧化物可以让硝化反应变的很容易,且硝化反应发生在4位上,反应过程如图7。目前吡啶N-氧化物的制备主要是以吡啶为原料,通过氧化剂如过氧化氢[27]、过氧酸[28]等将其氧化而得。
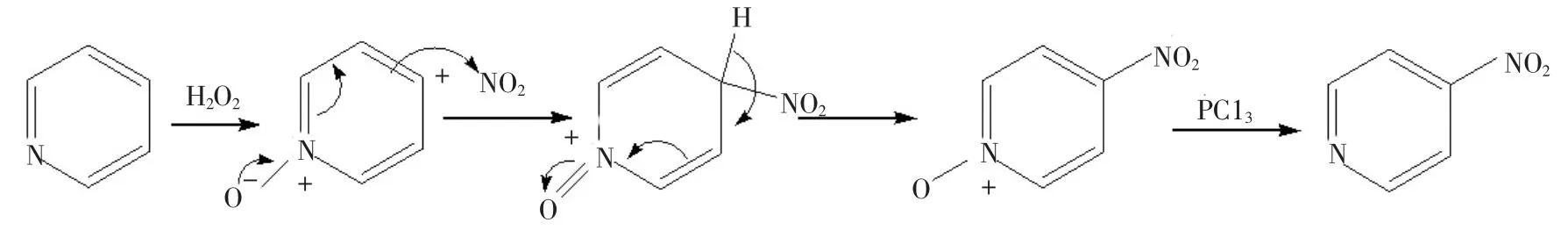
图7 4-硝基吡啶的合成
4.3 制备4-二甲氨基吡啶
如前所述,吡啶是酰化反应的良好催化剂,但若是空间位阻较大的醇类进行酰化反应时,吡啶的催化效果就不是很理想了。而让4-二甲氨基吡啶(DMAP)代替吡啶作为酰化反应的催化剂时,反应速率明显提高,说明DMAP作催化剂对酰化反应进行有着极强的催化作用。近年来,人们对于DMAP作为酰化催化剂的研究较多,证明了它是一种高效的酰化催化剂,在医药、农药、染料、香料、功能材料等领域发挥着重要作用[29-31]。目前,工业上合成DMAP方法主要是以吡啶和SOCl2为原料,反应生成双吡啶盐,再与DMF亲核取代反应而成,具体反应过程如图8。
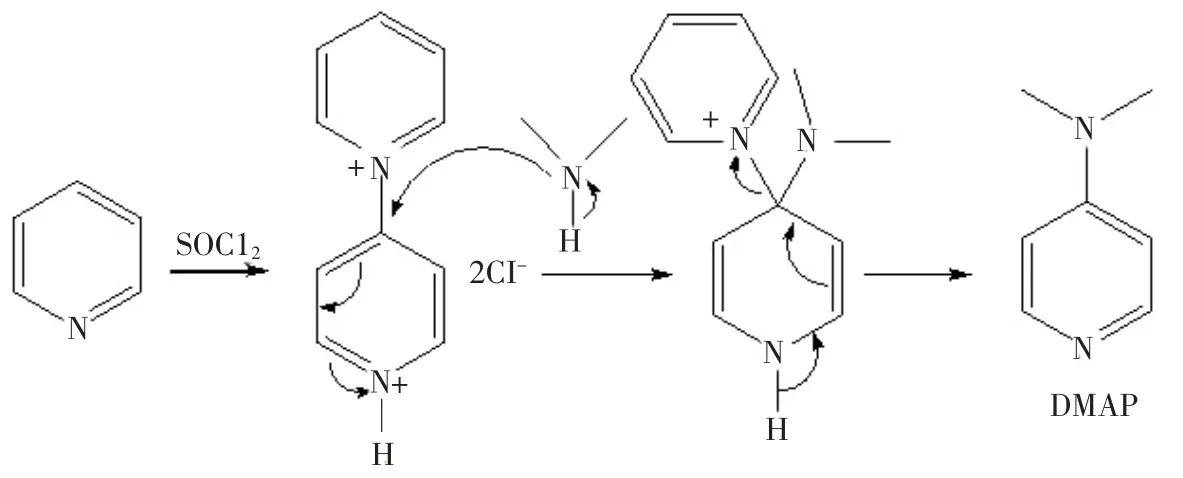
图8 以吡啶为原料合成DMAP
4.4 合成金属配合物
由于吡啶环上的电子是非定域的,且氮原子上含有可提供的孤对电子,因此吡啶可以作为配体和多种金属离子形成稳定的配合物。吡啶类配合物具有优良的特性,在分子器件、分子识别、光学材料、选择性催化、抗癌药物等方面有着广泛应用。吡啶和铁、镍、钴形成的配合物可以活化分子氢,使多烯烃进行选择性的氢化反应[32],且氢化反应的条件温和、选择性高、生成的单烯烃收率高。乙酸镍吡啶叔丁基过氧化氢配合物[33]在较温和的条件下催化分子氧将一系列烷基苯和苄醇类化合物氧化为相应的羰基化合物,表现出很高的选择性。李邦玉[34]提出了与金属配位的吡啶环上α位C-H键将被活化,原因是吡啶配位到金属原子上后,环上电子云密度会进一步降低,α位更易发生亲核取代反应。张金菊[35]以GeCl4为原料,以吡啶和水杨酸为配体,合成了吡啶水杨酸锗配合物,该配合物具有较好的抗癌活性。陈英[36]以Cu2+、吡啶和环烷酸为原料,当三者摩尔比为1∶4∶2时,成功合成了Cu2+、吡啶、环烷酸三元配合物,该配合物可用于炼油污水中环烷酸含量的测定。牛效迪[37]在酞菁钴的衍生物即对称的四取代烷基苯氧基酞菁钴的基础上,采用溶剂热的方法合成了与吡啶形成的轴向配合物,研究了其光谱性质,发现酞菁钴吡啶轴向配合物可以改变酞菁染料薄膜的光记录性能。然而,单一吡啶作为配体形成的配合物结构和功能有限,为合成出结构新颖、功能独特的吡啶配合物,使用吡啶衍生物或者吡啶类化合物代替吡啶作为配体已成为近年来的研究热点[38],也将是未来该领域的发展方向。
4.5 其他合成
作为有机反应的原料,吡啶还可以制备离子液体如吡啶丁烷磺酸硫酸氢盐[39],它可以高效催化光皮树果实油与甲醇酯交换制备生物柴油。吡啶为原料合成的单吡啶表面活性剂[40]及双吡啶表面活性剂[41]抑菌效果显著,如枯草杆菌、大肠杆菌、葡萄球菌等。吡啶还是合成吡虫啉[42-43]、盐酸右哌甲酯[44]、帕司烟肼[45]等农药和医药的重要原料和中间体。
5 结论
综上所述,吡啶在有机合成中发挥着重要作用。但由于吡啶具有毒性和特殊气味,限制了它在有机反应溶剂、缚酸剂及催化剂方面的单独使用,因此,研究复合型的吡啶溶剂、缚酸剂及催化剂在未来将具有重要的价值和意义。而作为反应的原料和中间体,特别是近年来,吡啶类药物和吡啶类配合物备受化学工作者关注,其广阔的应用前景亟待更多的人们去发现和研究。

