微生态制剂对重症急性胰腺炎病人的炎症指标、降钙素原、尿胰蛋白酶原激活肽水平及肠道菌群的影响研究
代宇,叶勇,林影,陈曙蓓
重症急性胰腺炎(SAP)是一种起病急、进展快、病情重的外科常见急腹症,常表现为全身性炎症反应、胰腺坏死,严重者还可能出现多器官功能障碍[1]。SAP病人肠道黏膜屏障功能障碍是引起肠道菌群失调和菌群移位,导致胰腺及其他脏器感染的主要原因,因此,控制病人肠道屏障功能损伤,是阻止病情发展,改善病人预后的关键环节[2-3]。微生态制剂是一种利用正常微生物或促微生物生长物质制成的活的微生物制剂,可有效刺激机体正常菌群生长繁殖,抑制致病菌过度生长,对肠道屏障功能具有一定的保护作用。研究发现,降钙素原(PCT)、尿胰蛋白酶原激活肽(TAP)与SAP病情发展密切相关[4]。基于此,本研究回顾性分析了微生态制剂治疗SAP病人的临床疗效,及对炎症指标、PCT、TAP水平及肠道菌群的影响,以为临床治疗提供参考。
1 资料与方法
1.1 一般资料 回顾性分析2016年10月至2018年8月在内江市第二人民医院就诊的SAP病人112例,根据治疗方案不同,分为对照组(给予肠内营养治疗)和研究组(在肠内营养基础上给予微生态制剂治疗)。纳入标准:符合《中国急性胰腺炎诊治指南(2013,上海)》[5]中SAP的诊断标准,经CT、MRI检查确诊,且发病至入院时间≤48 h。排除标准:(1)SAP并发症需要手术者;(2)近1个月内接受益生菌或抗生素治疗者;(3)合并严重心、肝、肾等功能障碍者;(4)合并血液病、糖尿病、高脂血症及其他感染性疾病者。病人或其近亲属知情同意,本研究符合《世界医学协会赫尔辛基宣言》相关要求。
研究组60例,男38例,女22例;年龄范围为23~64岁,年龄(42.96±5.51)岁;发病至入院时间范围为4~45 h,发病至入院时间(15.64±3.02)h;Ranson评分范围为3~5分,Ranson评分(4.25±0.48)分;Balthazar CT评分范围为3~4分,Balthazar CT评分(3.40±0.81)分;其中,胆源性31例,酒精性18例,饮食性8例,其他3例。对照组52例,男33例,女19例;年龄范围为22~65岁,年龄(43.08±5.67)岁;发病至入院时间范围为3~46 h,发病至入院时间(16.10±3.14)h;Ranson评分范围为3~5分,Ranson评分(4.19±0.53)分;Balthazar CT评分范围为3~4分,Balthazar CT评分(3.51±0.76)分;其中,胆源性28例,酒精性14例,饮食性6例,其他4例。两组病人性别、年龄、发病至入院时间、Ranson评分、Balthazar CT评分及病因等一般资料比较,差异无统计学意义(P>0.05)。
1.2 方法 病人入院后均给予监护、禁食、吸氧、胃肠减压、解痉镇痛、静脉滴注补充血容量、抗感染等常规基础治疗。对照组37例病人入院48 h后给予肠内营养治疗,15例病人入院72 h病情平稳后给予肠内营养治疗,在内镜监视下经鼻置入肠营养管,再经空肠营养管缓慢滴注生理盐水500 mL,再给予百普素(无锡纽迪希亚制药有限公司,15%为氨基酸形式、85%为短肽形式,每袋125 g,提供能量为500 Kcal;生产批号H20170170),起始滴注速度为50 mL/h,根据病人肠道耐受情况调节滴注速度至120 mL/h,输液总量由前期500 mL逐步增加至1 500 mL。研究组43例病人入院48 h后给予肠内营养联合微生态制剂治疗,17例病人入院72 h病情平稳后给予肠内营养联合微生态制剂治疗,每日在肠内营养管中注入双歧三联活菌胶囊(贝飞达,晋城海斯制药有限公司生产)210 mg。包含长型双歧杆、嗜酸乳杆菌、粪肠球菌,活菌数量>1×109/100 g每克含长型双歧杆菌≥1.0×106CFU,嗜酸乳杆菌≥1.0×106CFU,粪肠球菌≥1.0×106CFU。辅料为:淀粉、预胶化淀粉、乳糖、硬脂酸镁每克含长型双歧杆菌≥1.0×106CFU,嗜酸乳杆菌≥1.0×106CFU,粪肠球菌≥1.0×106CFU。辅料为:淀粉、预胶化淀粉、乳糖、硬脂酸镁每克含长型双歧杆菌≥1.0×106CFU,嗜酸乳杆菌≥1.0×106CFU,粪肠球菌≥1.0×106CFU;生产批号H20150807),每次420 mg,2次/日。两组病人疗程均为7 d,可根据病人实际情况适量延长疗程。
1.3 观察指标 比较两组病人治疗1个疗程后临床疗效、两组病人治疗前后APACHEⅡ评分[6],血清炎性因子、PCT、TAP水平及肠道菌群情况。(1)临床治疗有效评价:临床有效标准,一是主要临床症状如腹胀、腹部疼痛、恶心、呕吐、高热等基本消失;二是临床指征如腹肌紧张、上腹部压痛及腹部反跳痛等基本消失;三是实验室指标如肝肾功能生化指标、血常规白细胞、血淀粉酶、尿淀粉酶等检测值恢复正常。7 d之内达到上述标准则为显效,7~10 d之内达到上述标准为有效,超过10 d未达到上述标准为无效(无效病人根据病情情况继续给予贝飞达治疗,治疗后均达到有效),有效率=(显效例数+有效例数)/总例数×100%。(2)炎性因子包括:血清肿瘤坏死因子α(TNF-α)、白介素6(IL-6)、白介素8(IL-8),炎性因子水平均采用酶联免疫吸附实验法(ELISA)测定。(3)PCT、TAP水平,均采用ELISA法测定。(4)肠道菌群情况,采集病人肠道排泄物进行细菌培养,分别接种于双歧杆菌、乳杆菌、肠杆菌、肠球菌4种选择性培养基中,前两种放入厌氧气袋中密封后放入37℃的培养箱中培养48 h,后两种直接放入37℃的培养箱中培养24 h,均采用平板活菌计数法计算细菌总数。
1.4 统计学方法 采用SPSS20.0进行数据分析,计量资料采用t检验进行比较,计数资料采用χ2检验进行比较,P<0.05为差异有统计学意义。
2 结果
2.1 两组病人临床疗效比较 研究组临床治疗有效率明显高于对照组,差异有统计学意义(P<0.05)。见表1。
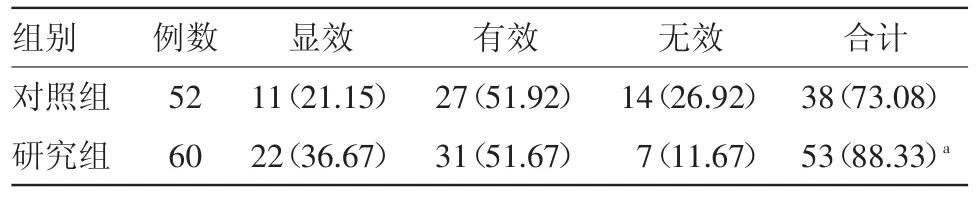
表1 重症急性胰腺炎112例临床疗效比较/例(%)
2.2 两组病人治疗前后APACHEⅡ评分比较 治疗前,研究组和对照组APACHEⅡ评分分别为(13.14±5.08)分和(13.36±5.27)分;两组比较差异无统计学意义(t=0.225,P=0.822);治疗后,研究组和对照组APACHEⅡ评分分别为(7.25±3.49)分和(8.92±3.60)分,两组比较差异有统计学意义(t=2.489,P=0.014)。同组病人治疗前后APACHEⅡ评分比较,差异有统计学意义(P<0.05)。
2.3 两组病人治疗前后炎性因子比较 治疗前,两组病人血清TNF-α、IL-6、IL-8水平比较,差异无统计学意义(P>0.05);治疗后,研究组血清TNF-α、IL-6、IL-8水平明显低于对照组,差异有统计学意义(P<0.05)。见表2。
2.4 两组病人治疗前后PCT、TAP水平比较 治疗前,两组病人血清PCT、TAP水平比较,差异无统计学意义;治疗后,研究组血清PCT、TAP水平比较明显低于对照组,差异有统计学意义(P<0.05)。见表3。
表2 重症急性胰腺炎112例治疗前后炎性因子比较/(ng/L,±s)
注:TNF-α为血清肿瘤坏死因子α、IL-6为白介素6、IL-8为白介素8。与同组治疗前比较,a t=12.371,c t=21.944,e t=20.901,b t=19.029,d t=30.083,f t=26.421,均P<0.001
组别对照组研究组t值P值TNF-αIL-6例数52 60 IL-8治疗后62.08±7.80e 57.19±7.43f 3.394 0.001治疗前61.47±5.29 60.61±5.35 0.853 0.396治疗后49.10±4.90a 42.87±4.85b 6.747 0.000治疗前75.68±6.71 76.07±6.65 0.308 0.758治疗后48.57±5.86c 43.64±5.05d 4.783 0.000治疗前93.97±7.76 95.06±8.25 0.717 0.475
表3 重症急性胰腺炎112例治疗前后PCT、TAP水平比较/±s
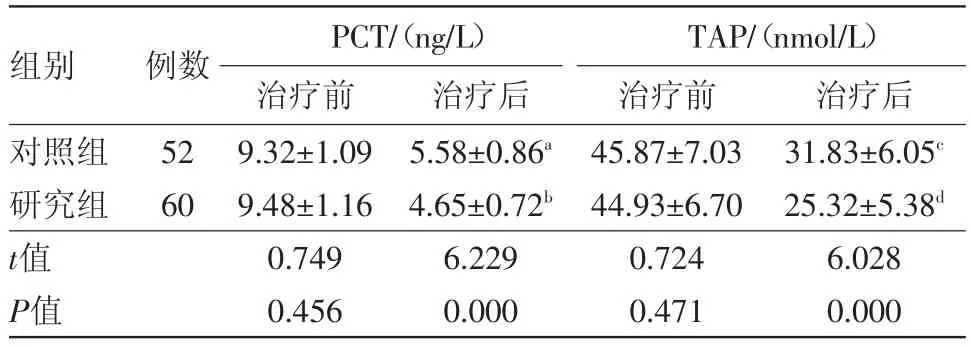
表3 重症急性胰腺炎112例治疗前后PCT、TAP水平比较/±s
注:PCT为降钙素原、TAP为尿胰蛋白酶原激活肽。与同组治疗前比较,a t=19.425,b t=27.403,c t=10.916,d t=11.678,均P<0.001
治疗后31.83±6.05c 25.32±5.38d 6.028 0.000组别对照组研究组t值P值例数52 60 PCT/(ng/L)TAP/(nmol/L)治疗前9.32±1.09 9.48±1.16 0.749 0.456治疗后5.58±0.86a 4.65±0.72b 6.229 0.000治疗前45.87±7.03 44.93±6.70 0.724 0.471
2.5 两组病人治疗前后肠道菌群计数比较 治疗前,两组病人肠道菌群计数比较,差异无统计学意义;治疗后,研究组病人肠道双歧杆菌、乳杆菌计数明显高于对照组(P<0.05),肠杆菌、肠球菌计数明显低于对照组(P<0.05)。见表4。
表4 重症急性胰腺炎112例治疗前后肠道菌群计数比较/(ln/g,±s)
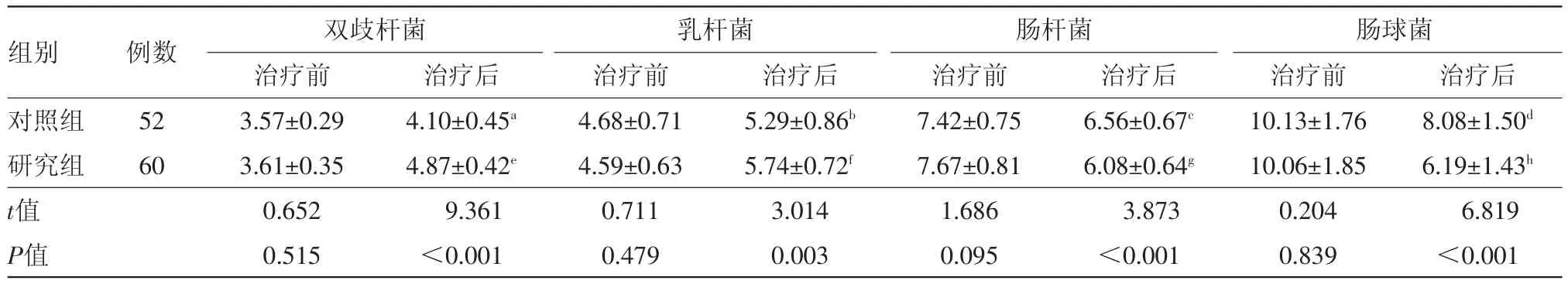
表4 重症急性胰腺炎112例治疗前后肠道菌群计数比较/(ln/g,±s)
注:与同组治疗前比较,a t=7.139,b t=3.944,c t=6.166,d t=6.392,e t=17.852,f t=9.311,g t=11.930,h t=12.820,均P<0.001
组别对照组研究组t值P值双歧杆菌 乳杆菌例数52 60肠杆菌 肠球菌治疗后8.08±1.50d 6.19±1.43h 6.819<0.001治疗前3.57±0.29 3.61±0.35 0.652 0.515治疗后4.10±0.45a 4.87±0.42e 9.361<0.001治疗前4.68±0.71 4.59±0.63 0.711 0.479治疗后5.29±0.86b 5.74±0.72f 3.014 0.003治疗前7.42±0.75 7.67±0.81 1.686 0.095治疗后6.56±0.67c 6.08±0.64g 3.873<0.001治疗前10.13±1.76 10.06±1.85 0.204 0.839
3 讨论
重症急性胰腺炎是消化内科常见的急危重症,病人由于炎症反应、细胞因子过度生成、肠菌群失调、肠黏膜细胞过度凋亡及肠动力紊乱等原因,造成肠道黏膜屏障功能障碍。肠道黏膜是重要的消化吸收场所,也是人体关键的免疫和代谢器官,正常生理状态下,肠道内各菌种相互制约,维持肠内微生态平衡,胃肠道黏膜可有效发挥屏障功能,阻挡肠道菌群及其有害产物通过血液循环进入腹腔其他脏器[7]。当肠道菌群失调,有益菌群数量减少,潜在致病菌大量生长繁殖,肠道屏障功能受损,肠道黏膜通透性增强,引起肠道菌群移位及肠源性感染,最后发展为多器官功能障碍综合征,严重威胁病人生命健康[8-9]。因此,调节肠道菌群、修复肠道屏障功能障碍是治疗SAP的重要突破口,对提高临床治疗有效率具有重大意义。
大量研究发现,微生态制剂对机体肠道菌群具有很好的调节作用。本研究选用的微生态制剂贝飞达,又称双歧杆菌三联活菌肠溶胶囊,包含长型双歧杆菌、嗜酸乳杆菌、粪肠球菌三种活菌,口服后可迅速、完全达到肠道,并定植于肠道不同部位。粪肠球菌为需氧菌,分布于肠道上部,繁殖速度最快,可产生细菌素等抑菌物质,并抑制大肠杆菌和沙门氏菌等病原菌的生长,还能抑制肠道内产尿素酶细菌和腐败菌的繁殖改善肠道微环境;嗜酸乳杆菌为兼性厌氧菌,分布于肠道中部,可分解糖类产生乳酸,提高肠道酸度,抑制肠道致病菌繁殖;长型双歧杆菌为厌氧菌,分布于肠道下部,可维护肠道正常细菌菌群平衡,抑制病原菌的生长,还可刺激肠道的免疫系统、淋巴组织,产生分泌性抗体[10-11]。三种菌群联合使用可有效抑制致病菌生长,重新建立宿主肠道菌群的微生态平衡。本研究中,病人临床治疗有效率可达到88.33%,治疗后APACHEⅡ评分明显降低,且病人肠道益生菌双歧杆菌、乳杆菌计数明显升高,肠道致病菌肠杆菌、肠球菌计数明显下降,表明病人肠道菌群结构改善,肠道黏膜屏障功能明显加强。
本研究结果还显示,采用微生态制剂治疗的SAP病人,血清中炎性因子TNF-α、IL-6、IL-8水平明显降低。TNF-α是启动炎性反应的关键因子,由单核细胞、巨噬细胞等产生,可刺激氧自由基和一氧化氮生产,促使白细胞趋化、黏附,增强血管内皮细胞通透性,从而加剧SAP病人胰腺坏死及肠道病理生理改变[12-13];IL-6由单核细胞、巨噬细胞、T细胞和B细胞产生,可参与机体多项急性相反应,并正反馈于TNF-α释放而形成恶性循环,研究发现,IL-6与SAP的发生发展密切相关,其作用机制可能与改变胞内G细胞活性,参与中性多核白细胞功能上调有关[14];IL-8由巨噬细胞、上皮细胞产生的趋化性细胞因子,可诱导调节炎症细胞增殖,引起机体局部炎症反应[15]。微生物制剂可调控抗炎和促炎细胞因子的产生,从而提高肠道免疫功能,降低机体炎症反应。
PCT是一种甲状腺C细胞合成分泌的多肽,稳定性较好,正常生理状态下,在机体内可维持较低的浓度水平,当机体受到炎性因子和细菌内毒素刺激时,可诱导产生大量的PCT[16-17]。TAP为胰蛋白酶原激活的降解产物,被激活水解后可进入血液循环、腹腔、尿液中,胰蛋白酶原被激活为SAP重要的发病机制,故血清中TAP的水平可直接反映胰腺炎的严重程度[18-19]。因此,PCT和TAP水平的动态变化均可作为胰腺细胞损伤和坏死程度的监测指标,可用于SAP和早期诊断和预后评估。本研究中,微生态制剂治疗的SAP病人PCT、TAP水平较治疗前明显降低,表明微生态制剂治疗可有效控制病情发展,改善病人预后。
综上所述,微生态制剂治疗SAP病人疗效确切,可明显降低病人炎性因子和PCT、TAP水平,调节肠道菌群微生态平衡,值得临床应用。

