NiFe2O4@LiMn2O4 正极材料的制备及其电化学性能研究①
梁力勃, 卢德娟, 梁晶晶, 熊美玉, 陈彦辛, 赖飞燕
(1.贺州学院 材料与化学工程学院,广西 贺州542899; 2.广西贺州市桂东电子科技有限责任公司,广西 贺州542899)
尖晶石型锰酸锂(LiMn2O4)材料因具有工作电压高、安全性能好、价格低廉和环境友好等优点[1-3],而成为目前锂离子电池正极材料的研究热点之一。 但是,LiMn2O4材料存在倍率和循环性能差等问题,特别是在高温条件下,这一缺陷的存在使得LiMn2O4材料在商业化应用中受到限制[4-5]。
针对LiMn2O4材料存在的上述问题,对其进行改性的方法主要有体相掺杂和表面包覆。 体相掺杂主要是在锰酸锂材料中掺入阴离子、阳离子或阴阳混合离子,如Li+、F-或Al3+/F-等[6-7]。 表面包覆是在锰酸锂颗粒表面包覆一层不与电解液反应的材料,该材料一般为金属/非金属氧化物、磷酸盐、碳材料、氟化物或金属单质等[8-10]。 通过在锰酸锂颗粒表面包覆一层保护材料,能有效抑制锰酸锂材料中Mn 的溶解,减少锰酸锂材料的歧化反应,提高锰酸锂材料的循环性能。 但是这些材料的电子或离子电导率低[11-13],会导致锰酸锂材料的首次充放电效率和放电比容量下降。
铁酸镍(NiFe2O4)材料为反尖晶石结构,具有与锰酸锂材料相似的晶体结构;另外,NiFe2O4材料中的四面体和八面体结构主要是由O2-堆积而成,这种结构的存在有利于提高材料的电子和离子电导率[14-16]。正是因为NiFe2O4材料具有上述优点,NiFe2O4材料在各个领域的应用非常广泛,如:超级电容器,锂离子电池负极,催化剂等。 本文主要针对锰酸锂材料存在的问题,将NiFe2O4材料包覆于锰酸锂材料表面,既能起到保护锰酸锂基体材料不被电解液腐蚀,又能提高包覆层电子和离子的传输速率,降低电极的极化作用。
1 实 验
采用溶胶-凝胶法,以Ni(NO3)2·6H2O(99.9%,分析纯)和Fe(NO3)3·9H2O(99.9%,分析纯)为原料,按摩尔比1 ∶2.02 加入到去离子水中,机械搅拌0.5 h,充分溶解后加入LiMn2O4材料(中信大锰矿业有限责任公司),继续搅拌2 h。 逐滴加入质量浓度为15%的氨水到混合溶液中,调节溶液pH 值至9,继续搅拌0.5 h,抽滤,洗涤,于80 ℃鼓风干燥箱中干燥,得到前驱体材料。 将前驱体材料置于600 ℃管式炉中,在空气条件下烧结3 h,制备得到NiFe2O4包覆LiMn2O4复合正极材料。 并将未包覆的LiMn2O4材料、NiFe2O4包覆量质量比为0.5%,1%和2%的LiMn2O4正极材料分别标记为LMO,0.5NLMO,1NLMO 和2NLMO。
使用X-射线衍射仪测试复合材料晶体结构,使用场发射扫描电镜测试复合材料颗粒表面形貌,并结合能谱测试仪对1NLMO 样品进行元素含量和分布测试。 使用透射电子显微镜测试NiFe2O4包覆层与LiMn2O4材料之间的连接情况。
将活性物质、导电碳(Super-P)和聚偏氟乙烯(PVDF)按质量比为85 ∶10 ∶5进行混合,以N-甲基吡咯烷酮(NMP)为溶剂,充分混合,涂覆到铝箔上,100 ℃真空干燥12 h,压片,制备直径12 mm 的正极片。 以锂片为负极,Celgard 2400 为隔膜,1 mol/L LiPF6(EC ∶DMC 体积比为1 ∶1)为电解液,在惰性气氛手套箱中组装成R2025 扣式电池。 用武汉蓝电测试仪(Land CT2001A)测试材料在恒电流条件下的电化学性能、材料循环伏安和交流阻抗。
2 实验结果与讨论
2.1 物相分析
图1 为铁酸镍和不同质量百分比铁酸镍包覆锰酸锂样品的XRD 图。 经Jade5.0 软件分析可知,图1(a)中可以看到铁酸镍的衍射峰与JDPSC №54-0964 卡片的峰值相对应,属Fd-3m 空间群的立方尖晶石结构,说明采用同包覆材料的制备方法和条件能制备出纯度较高的铁酸镍材料。 从图1(b)中可以看到,所有铁酸镍包覆锰酸锂样品不存在任何杂质峰,说明合成的材料中没有产生新的物质,且锰酸锂材料的晶体结构也未受到铁酸镍包覆材料的影响。 另外,也可能是因为铁酸镍包覆量较少,未达到XRD 衍射仪的检测限。

图1 样品XRD 图
2.2 形貌分析
图2 为不同质量百分比铁酸镍包覆锰酸锂样品的SEM 图。 从图2 中看到,锰酸锂颗粒为八面体结构,表面光滑平整,棱角清晰。 经铁酸镍包覆后的锰酸锂样品,从SEM 图中并不能观察到材料颗粒表面和颗粒大小有明显的变化,颗粒仍保持八面体结构;但是颗粒的棱角变得较为平滑,说明NiFe2O4材料可能已经包覆在LiMn2O4颗粒的表面上了。
为了进一步观测NiFe2O4材料在LiMn2O4颗粒表面的形貌结构,对LMO 和1NLMO 两个样品分别进行了TEM测试,结果如图3 所示。从图3 中看到,TEM测试结果和SEM 测试结果相一致,锰酸锂颗粒表面光滑,无杂质,具有较好的晶体结构;NiFe2O4包覆层以薄膜结构包覆在LiMn2O4颗粒表面,该薄膜层均匀致密地包覆在LiMn2O4颗粒表面,厚度约为14 nm。 该致密包覆层有利于电池在充放电过程中,抑制锰酸锂颗粒与电解液的直接接触,减缓电解液对锰酸锂材料的侵蚀作用。 而铁酸镍具有高的离子和电子电导率[14,17],作为包覆层不仅有利于保护锰酸锂基体材料不被电解液腐蚀,而且有利于提高材料的电化学性能。

图2 样品SEM 图

图3 样品TEM 图
2.3 电化学性能分析
图4 是样品在25 ℃、0.1C 和3.0~4.3 V 条件下的首次充放电曲线。 从图4 看到,4 个样品的首次充放电曲线形状基本上保持一致,在约3.9 V 和约4.1 V 处均出现了一对充放电平台。 在约3.9 V 的充放电平台为Li+在锰酸锂晶体结构中Li—Li 八面体的嵌入/脱出,约4.1 V 的充放电平台为Li+在Li—Li 四面体中的嵌入/脱出。
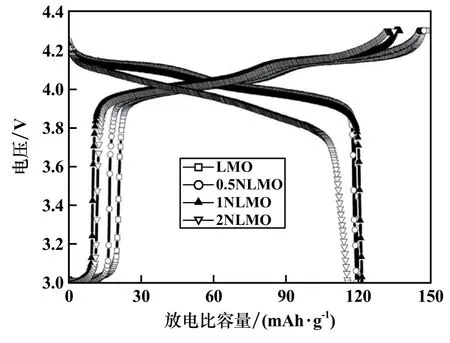
图4 样品首次充放电曲线
各样品的首次放电比容量和充放电效率见表1。结果表明,经过铁酸镍的包覆,复合材料的充放电机制并没有发生改变;具有高离子和电子电导率的铁酸镍作为包覆材料能有效提高复合材料的充放电效率。1NLMO 样品的首次放电比容量较LMO 高,但低于LiMn2O4材料的理论比容量(148 mAh/g),这主要是因为LiMn2O4材料中的Li+在首次嵌/脱过程中会有所损失。
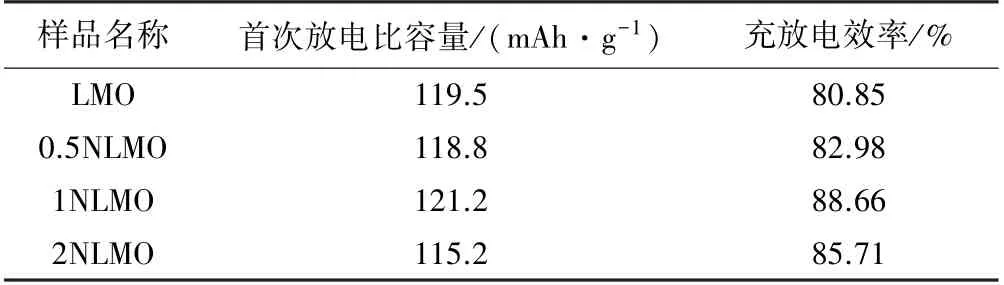
表1 样品首次放电比容量和充放电效率
图5 为样品在25 ℃、1C 和3.0 ~4.3 V 条件下循环400 圈的循环寿命图,各样品首次放电比容量和充放电效率见表2。 铁酸镍包覆后的样品均具有较高的放电比容量和容量保持率,说明具有高的离子和电子电导率的铁酸镍能有效保护锰酸锂基体材料在充放电过程中不被电解液腐蚀,抑制Mn 的溶解,从而达到提高材料循环性能的目的。

图5 样品循环性能图

表2 1C 倍率下循环400 圈样品首次放电比容量和容量保持率
图6 是样品在25 ℃,3.0 ~4.3 V,0.1C-10C-0.1C倍率条件下的放电曲线图,各样品放电比容量见表3。从图6 和表3 中看到,4 个样品的放电比容量都随着倍率增大而减小。 当NiFe2O4包覆量为1%时,1NLMO样品具有较好的倍率性能,0.5NLMO 样品次之,2NLMO 样品最差。 适量的铁酸镍包覆能有效保护锰酸锂基体材料不被电解液腐蚀,减少锰的溶解;铁酸镍具有一定的离子和电子电导率,包覆在锰酸锂颗粒表面能在一定程度上提高离子和电子的传输速率,从而达到提高样品电化学性能的目的。
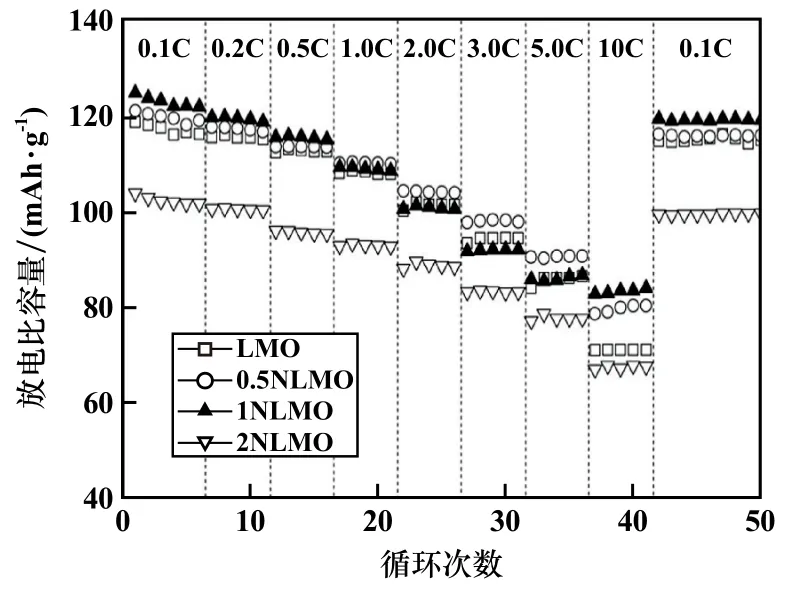
图6 样品倍率性能图

表3 样品在不同倍率下的放电比容量
3 结 论
采用溶胶-凝胶法制备的NiFe2O4@LiMn2O4复合正极材料具有良好的电化学性能。 分析结果表明,NiFe2O4包覆后的锰酸锂样品具有与未包覆锰酸锂相同的Fd-3m 空间群立方尖晶石结构,形貌结构为八面体结构;当NiFe2O4包覆量为1%时,NiFe2O4包覆层均匀致密地包覆在LiMn2O4颗粒表面,厚度约14 nm,该包覆层具有一定的离子和电子电导率,能有效抑制LiMn2O4与电解液的直接接触,减弱了Mn 离子和电解液间发生的副反应,减少Mn 的溶解,有利于提高LiMn2O4结构的稳定性,提高电池材料的循环和倍率等性能。 样品1NLMO 首次放电比容量(0.1C)为121.2 mAh/g,10C 倍率放电条件下放电比容量为84.8 mAh/g;1C 循环400周后容量保持率为90.64%。

