PD-1/PD-L1抑制剂治疗非小细胞肺癌的疗效及预后观察
吕厚宽,庄文辉,黄一桂,许玫莎
海口市第三人民医院1药剂科,2呼吸科,海口571100
2015年,中国新发肺癌73.3万例,死亡61.0万例,发病率和病死率均居所有恶性肿瘤之首[1]。多数患者被确诊时已属于晚期,手术效果较差,治疗以放射治疗和药物化疗为主,疗效不甚理想[2]。随着肿瘤基础研究的深入,越来越多关于肿瘤增殖、免疫耐受及免疫逃逸的机制被阐明,新的免疫治疗靶点被发现[3]。程序性死亡受体-1(programmed cell death 1,PDCD1,也称PD-1)广泛表达于活化的免疫细胞表面,参与自身免疫耐受,而其配体程序性死亡受体配体-1(programmed cell death 1 ligand 1,PDCD1LG1,也称PD-L1)是一种负性免疫共刺激分子,高表达于多种肿瘤细胞表面,如非小细胞肺癌(non-small cell lung cancer,NSCLC)、黑色素瘤及卵巢癌等[4],与肿瘤细胞的免疫逃逸密切相关。本研究应用纳武利尤单抗(nivolumab)对43例一线化疗无效或复发的晚期NSCLC患者进行治疗和随访,以期为临床更好的治疗提供参考,现报道如下。
1 对象与方法
1.1 研究对象
选择2018年1—12月海口市第三人民医院诊治的86例晚期NSCLC患者作为研究对象。纳入标准:①经病理检查或细胞学检查确诊为NSCLC;②TNM分期[6]为ⅢB~Ⅳ期;③经过铂类化疗药物为主的治疗后疾病进展或复发。排除标准:①因任何原因要求退出研究者;②合并其他系统原发肿瘤;③美国东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)[5]评分≥2分。将86例NSCLC患者分为对照组(43例)和研究组(43例),两组患者年龄、性别、病理类型、TNM分期、ECOG评分等基线特征比较,差异均无统计学意义(P>0.05),具有可比性。本研究经医院伦理委员会审批通过。
1.2 治疗方案
对照组采用多西他赛治疗,每次剂量为75 mg/m2静脉滴注1 h,每3周用药1次。研究组采用纳武利尤单抗治疗,每次剂量为3 mg/kg静脉滴注1 h,每2周用药1次,直到患者出现不耐受或疾病进展。所有患者出现不良反应时均给予相应的对症治疗。
1.3 评价标准
疗效评价标准参考实体瘤疗效评价标准(1.1版)[7],所有患者均在治疗9周首次进行疗效评价,然后每6周评价1次,其中病灶完全消失为完全缓解(CR),病灶最大直径减少超过30%为部分缓解(PR),病灶最大直径增加超过20%或出现新的病灶为疾病进展(PD),病情稳定(SD)指病灶缓解未达到PR而疾病进展未达到PD。总有效率=(CR+PR)例数/总例数×100%。患者不良反应参考WHO抗癌药物不良反应标准[8],由责任医师和护士在用药期间负责严密观察和报告。
1.4 随访方法
随访从患者接受治疗开始,随访终点为患者死亡,患者出院后每2周进行1次电话或门诊随访。最终随访0.6~13.1个月,截止时间为2019年4月20日。
1.5 统计学方法
采用SPSS 22.0软件对数据进行统计分析,计数资料以例数及率(%)表示,组间比较采用χ2检验;等级资料的比较采用Mann-WhitneyU检验;采用Kaplan-Meier法绘制生存曲线,以Log-rank进行分析。以P<0.05为差异有统计学意义。
2 结果
2.1 疗效的比较
对照组总有效率为9.30%(4/43),与研究组的20.93%(9/43)比较,差异无统计学意义(χ2=2.266,P=0.132)。但研究组患者的疗效明显优于对照组,差异有统计学意义(U=168.000,P<0.01)。(表1)
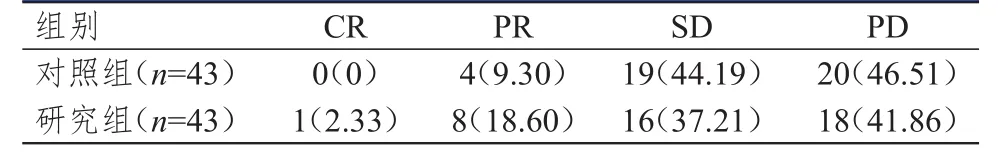
表1 两组患者的疗效[ n(%)]
2.2 不良反应的比较
研究组患者脱发、贫血、肌肉疼痛及中性粒细胞减少不良反应发生率均明显低于对照组,差异均有统计学意义(P<0.01)。其中研究组患者肌肉疼痛和中性粒细胞减少发生率均为0。(表2)
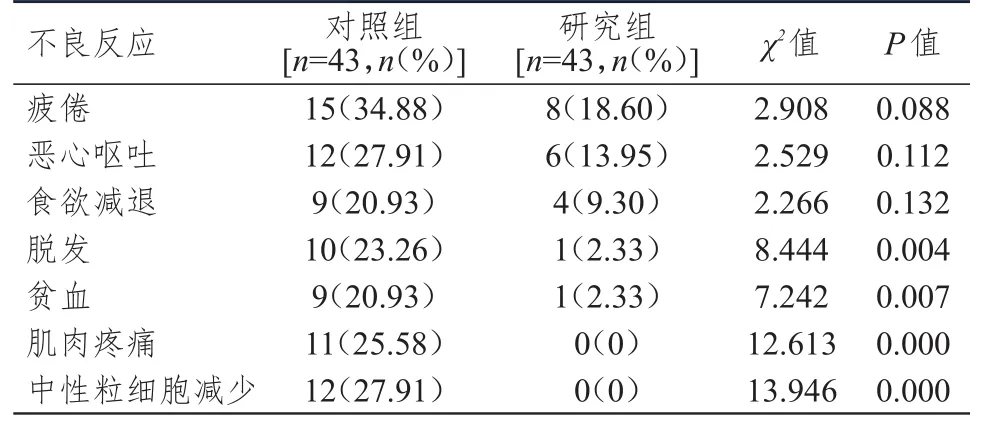
表2 两组患者不良反应发生情况的比较
2.3 生存分析
随访0.6~13.1个月后,失访0例。对照组患者中位生存时间为4.200个月(95%CI:2.787~5.613),1年累积生存率为6.98%;研究组患者中位生存时间为2.800个月(95%CI:2.029~3.571),1年累积生存率为18.60%。Log-rank检验显示,两组患者生存情况比较,差异无统计学意义(χ2=0.070,P=0.792)。(图1)

图1 研究组(n=43)与对照组(n=43)患者的生存曲线
3 讨论
多西他赛作为一线化疗失败或复发的晚期NSCLC患者的二线化疗药物,应用于临床已经有20年[9]。杨罡和李劲[10]的Meta分析报道患者中位生存时间为5.6个月,1年总生存率仅为3.6%,因此多西他赛对这类患者预后改善效果仍然较差。近年来,免疫治疗成为肿瘤研究的热点领域,新的机制及新的作用靶点不断被发现[11]。
免疫逃逸是肿瘤细胞难以被清除的重要原因[12]。Konishi等[13]研究发现,PD-L1广泛表达于NSCLC细胞表面,通过多种机制参与了肿瘤细胞的免疫逃逸。Chen等[14]研究发现,PD-L1表达上调增加了白细胞介素-10(interleukin-10,IL-10)的分泌,而后者可介导细胞毒性T淋巴细胞(cytotoxicity T lymphocyte,CTL)的凋亡。Cao等[15]研究指出,PD-L1表达上调会下调钙黏蛋白(calcium adhesion protein,CAP)的表达,对肿瘤细胞的上皮-间充质转化及免疫逃逸起到了促进作用。此外,PD-1/PD-L1还可以影响T细胞能量代谢,导致CTL能量耗竭而提前凋亡[16]。
本研究结果显示,对照组总有效率为9.30%,与以往文献报道[17]结果接近,研究组总有效率为20.93%,两组患者疗效比较,差异有统计学意义(P<0.01)。而对照组与研究组患者1年生存率比较,差异无统计学意义(χ2=0.070,P=0.792)。提示整体上纳武利尤单抗是能够使NSCLC患者获益的,但有效率仍然较低。因此,有学者指出,临床上可以通过免疫组化技术筛选PD-L1表达水平高的患者,以提高患者对纳武利尤单抗的有效率[18]。但是,由于肿瘤具有异质性,尤其是晚期NSCLC或经过化疗的患者,目前的方法仍难以反映患者肿瘤细胞整体的PD-L1表达水平,无法实现标准化检测,从而预测患者对纳武利尤单抗的反应性[19]。
由于本研究所选取患者均经过了铂类一线化疗方案的治疗,患者免疫功能可能低于常人,CTL对PD-L1表达下调肿瘤细胞的细胞毒作用可能较低[20]。生存分析结果显示,对照组中位生存时间(4.20个月)长于研究组(2.80个月),但差异无统计学意义(χ2=0.070,P=0.792)。因此,研究治疗NSCLC的纳武利尤单抗联合用药同样重要,对于免疫功能较差的患者,多西他赛等细胞毒性药物在短期内对控制肿瘤细胞增殖仍然是有效,甚至优于PD-L1抑制剂。Hellmann等[21]研究发现,纳武利尤单抗联合厄洛替尼治疗晚期NSCLC的客观有效率可达47.37%(18/38)。
纳武利尤单抗为人源化单克隆抗体,同其他治疗型单克隆抗体药物一样,毒性远小于普通化疗药物,更容易被患者接受。本研究结果显示,研究组脱发、贫血、肌肉疼痛及中性粒细胞减少不良反应发生率均明显低于对照组,差异均有统计学意义(P<0.01),提示纳武利尤单抗安全性较好。
综上所述,纳武利尤单抗安全性较好,可使一线化疗失败或复发的晚期NSCLC患者获益。

