去钙化脉络膜骨瘤伴脉络膜新生血管1例△
姚帮桃 刘刚 赵孝贵 王秀英 丁宇华
(1. 江苏省南京市溧水区人民医院眼科 南京 211200;2.南京医科大学第一附属医院眼科 南京 210029)
资料患者女性,52岁。因右眼视力下降1月余来我院眼科就诊,否认高血压、糖尿病、高脂血症、心脏病等病史,全身情况平稳。视力:右眼0.6,左眼:1.0;矫正视力:右眼 +0.50,无法提高。双眼前节未见异常。眼底:右眼视盘色淡红,边界清,视网膜、动静脉管径比约2∶3,颞侧黄斑区见大片不规则状且边界清楚的橘黄色病变,其间中心凹处见斑驳状黄白色病变,中心凹反光消失(图1A)。左眼底未见明显异常。眼压:右眼16.0 mmHg(1 mmHg=0.133 kPa),左眼15.0 mmHg。为明确诊断进一步行眼底自发荧光(fundus autofluorescence,FAF)、双眼底荧光血管造影(fundus fluorescein angiography,FFA)、吲哚菁绿血管造影(indocyanine green angiography,ICGA)、光学相干层析成像(optical coherence tomography, OCT)、CT检查。右眼底FAF示黄斑区自发弱荧光(图1B)。右眼FFA示造影早期病变区边缘的点片状强荧光,随造影过程轻度增强,后期强荧光逐渐变弱,未见明显渗漏(图1C、E、G);右眼ICGA示造影早期显示与病变相一致的弱荧光,其间夹杂斑驳状强荧光,黄斑区中心凹见一强荧光随造影过程逐渐增大,边界模糊,呈绒团状改变(图1D、F、H)。右眼OCT示黄斑区视网膜下方的高隆起信号、多发的色素上皮脱离和浆液性视网膜脱离,可见保存相对完整的椭圆体带(图2A、B)。CT示右眼后极部脉络膜层见与骨密度相似的小片状高密度影(图3)。诊断为右眼脉络膜骨瘤伴脉络膜新生血管(choroidal neovascularization, CNV)。患者因治疗费用问题,暂时拒绝接受抗血管内皮生长因子(anti-vascular endothelial growth factor,抗VEGF)治疗。
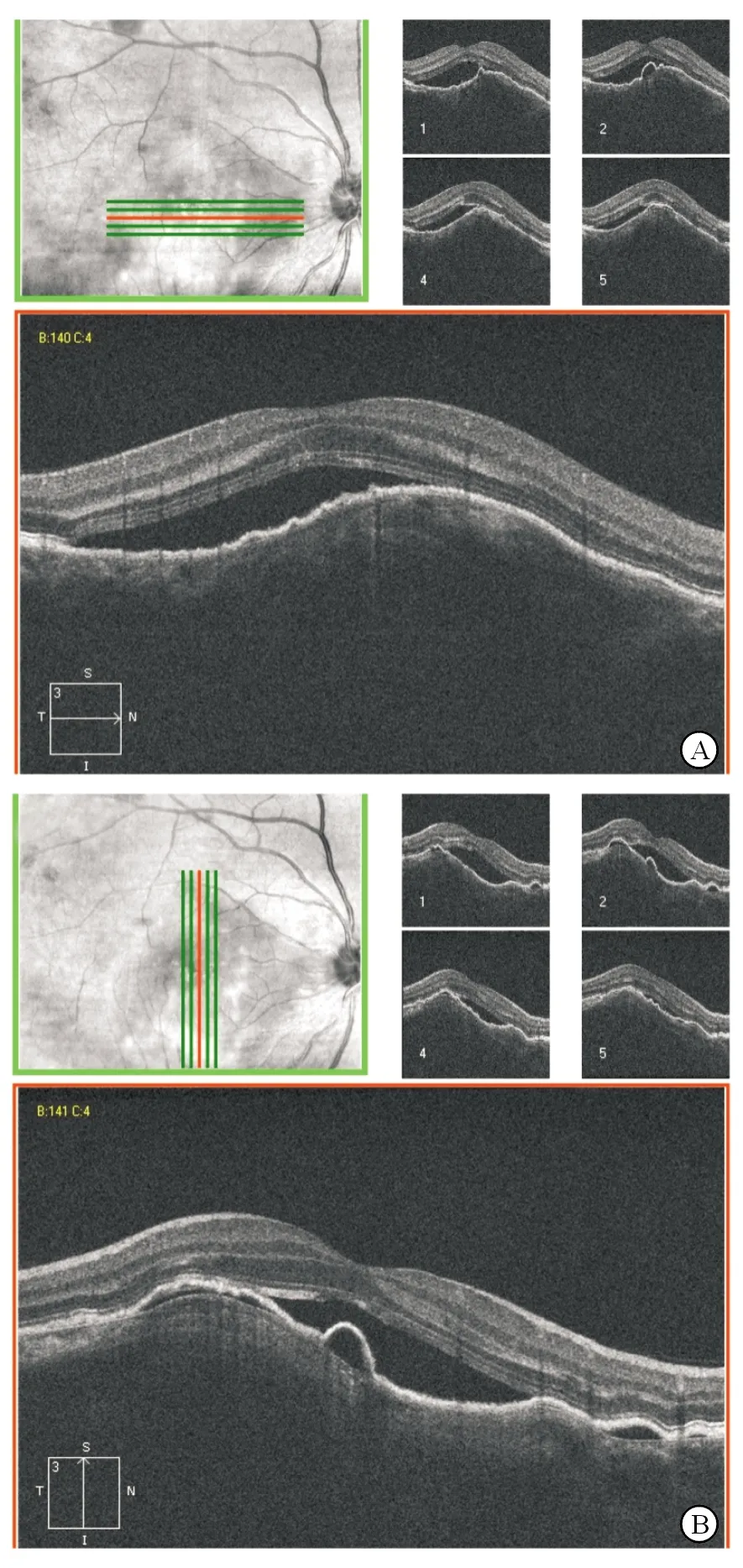
图2 患者右眼OCT 黄斑区视网膜下方高隆起信号、多发的色素上皮脱离和浆液性视网膜脱离,可见保存相对完整的椭圆体带。A.水平方向扫描;B.垂直方向扫描。
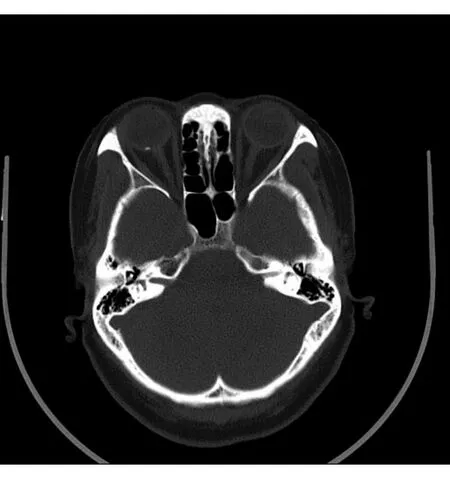
图3 患者CT 右眼后极部脉络膜层见与骨密度相似的小片状高密度影。
讨论脉络膜骨瘤是一种极为罕见的以脉络膜内骨化改变为特征的良性肿瘤,好发于年轻女性,一般单眼发病,偶见双眼发病。肿瘤边界清楚,一般位于视盘周围或黄斑区[1]。脉络膜骨瘤的发病机制尚不明确。根据其病变区域颜色可将脉络膜骨瘤区分为钙化区及去钙化区,钙化区域通常表现为橘黄色,而去钙化区表现为黄白色。去钙化区域色泽由视网膜色素上皮(retinal pigment epithelium,RPE)的厚薄及脱色素程度而决定,且因其病理改变不断向周围组织浸润扩展,故去钙化区域形态各异,可为斑驳状、片状、伪足状或不规则状[2]。
目前,脉络膜骨瘤继发CNV的原因尚不明确,普遍认为CNV的形成与脉络膜组织的缺血、缺氧或RPE-Brunch膜-脉络膜毛细血管复合体的损伤有关。最近的研究发现脉络膜骨瘤组织内去钙化的病理改变在CNV的形成中起着极为重要的作用。去钙化与RPE萎缩密切相关[3]。RPE的主要生理功能之一为将视网膜代谢产生的水等物质从神经视网膜层转运到脉络膜毛细血管层。去钙化可以损伤RPE、Bruch膜,乃至整个视网膜组织包括椭圆体带,导致RPE-Brunch膜-脉络膜毛细血管复合体的功能失调、视网膜色素上皮脱离,并引起脉络膜组织中VEGF浓度增高,继而诱发CNV。去钙化若累及黄斑部位,可以严重损伤黄斑功能,诱发黄斑下CNV形成, CNV可突破RPE及Brunch膜进入视网膜层,直接侵犯破坏椭圆体带,造成视网膜黄斑区椭圆体带的结构紊乱和断裂,引起继发性视网膜或视网膜下出血、积液及神经上皮层的脱离。上述病理性改变均会导致视功能缓慢性或突然性下降和丧失。另外,去钙化脉络膜骨瘤的瘤体也可突破Brunch膜,生长进入视网膜甚至玻璃体腔内[4]。有报道[5]称在脉络膜骨瘤的临床病程中,其钙化区可停止生长,但去钙化区则在不断进展。故由此可知,去钙化的脉络膜骨瘤具有很强的侵袭性。在此研究中,黄斑区CNV部位和去钙化的位置相吻合,考虑黄斑区去钙化的病理变化可能诱发了CNV,使上述学者的观点得到一定验证。
传统观点认为脉络膜骨瘤导致的视力下降与CNV、浆液性视网膜脱离关系密切;但近年来有学者[6]证实,其视力下降与CNV、浆液性视网膜脱离关系无明显相关性,而是更多取决于病变部位是否累及黄斑中心凹或视网膜椭圆体带是否完整。在此病例中,患者出现了CNV 和浆液性视网膜脱离,但其视力仍然可以达到0.6,考虑与患者视网膜的椭圆体带尚完整有关。
FFA曾被认为是检测CNV的首选,但如果视网膜RPE层完整,视网膜下CNV可能在FFA上无法显示,或者即使RPE层严重萎缩,下方CNV产生的渗漏很可能被脉络膜骨瘤本身在FFA中显示的强荧光遮挡,故明确判断脉络膜骨瘤有无继发CNV的存在,需要进一步行ICGA或光学相干断层扫描血管造影(optical coherence tomography angiography, OCTA)检查。ICGA不仅可在造影早期直接显示出瘤体的位置和形态,而且能在造影过程中明确CNV的位置和变化[7]。OCTA是一种无创性检查,可以在表层视网膜层、深层视网膜层、外层视网膜层和脉络膜毛细血管层不同的层面监测到新生血管,并可通过不同的模式观察新生血管的形态和血流面积,可作为FFA检查的补充,但目前尚不能完全代替FFA[8]。在此病例中,患者的FFA并未能检测出CNV的存在,但在ICGA中可明确显示患者的黄斑区有新生血管增生,证实ICGA在诊断脉络膜骨瘤继发CNV方面可展现出明显的优势。
针对脉络膜骨瘤的治疗目前尚无统一标准。无症状者可密切随诊观察,若继发CNV可选择光动力疗法、经瞳孔温热疗法、激光光凝等,但预后普遍不良。光动力疗法和激光光凝等可能加剧脉络膜骨瘤局灶性的去钙化或出血[9-11]。抗VEGF是治疗脉络膜骨瘤继发CNV的有效治疗措施。抗VEGF药物可降低脉络膜血管通透性,促进视网膜下积液吸收,在解剖功能和视力恢复上均可获得满意效果[12]。本例患者视力保持良好,但因抗VEGF药物价格昂贵而拒绝行抗VEGF治疗。
脉络膜骨瘤在诊断方面上需要与脉络膜血管瘤、脉络膜黑色素瘤等鉴别。现普遍认为CT或B超是脉络膜骨瘤诊断的金标准,其与其他脉络膜肿瘤的表现形式也各相迥异。
综上所述,我们报道了1例罕见的脉络膜骨瘤继发CNV和浆液性视网膜脱离。去钙化是脉络膜骨瘤重要的病理改变过程,它可破坏RPE-Brunch膜-脉络膜毛细血管复合体功能,诱发CNV。病例数量缺乏和无随诊资料是本研究的局限,希望今后能够收集到更多的病例,以便更好地了解脉络膜骨瘤的发病机制、去钙化的病理改变及其治疗。

