民族药水三七质量标准的提升研究
邓桃 杨昌贵 周涛


【摘 要】 目的:提升水三七的质量控制标准。方法:采用显微鉴别法对水三七药材粉末进行鉴别;参照2015年版《中国药典》测定水分、总灰分、酸不溶性灰分和醇浸出物的含量;采用紫外分光光度法,建立水三七总皂苷的定量方法。结果:淀粉粒、导管和草酸钙针晶为水三七粉末稳定性的显微特征;17批样品中,水分为7.38%~8.79%,总灰分为3.26%~7.06%,酸不溶性灰分为0.45%~3.12%,醇溶性浸出物含量为11.52%~22.32%,总皂苷含量为1.39%~4.56%。结论:该方法稳定可靠,可用于水三七的质量控制。
【关键词】 水三七;总皂苷;质量标准;提升研究
【中图分类号】R284.1 【文献标志码】 A 【文章编号】1007-8517(2020)12-0018-05
Abstract:Objective To improve the quality control standard of Rhizoma Schizocapsae. Methods The powder of Rhizoma Schizocapsae was identified by microscopic identification. The contents of water, total ash, acid insoluble ash and alcohol extract were determined with reference to the 2015 edition of Chinese pharmacopoeia. A quantitative method for the determination of total saponins of Rhizoma Schizocapsae was established by UV Spectrophotometer. Results starch granules, catheter and calcium oxalate needle crystals showed the microscopic characteristics of powder stability of Rhizoma Schizocapsae. Among the 17 samples, the water content was 7.38%~ 8.79%, the total ash content was 3.26%~ 7.06%, the acid insoluble ash content was 0.45%~ 3.12%, the alcohol soluble extract content was 11.52%~ 22.32%, and the total saponin content was 1.39%~4.56%. Conclusion the method is stable and reliable, and can be used for quality control of Rhizoma Schizocapsae.
Keywords:Rhizoma Schizocapsae; Total Saponins; Quality Standard;Upgrading Research
水三七又名水田七、屈頭鸡、水萝卜等,为蒟蒻薯科植物裂果薯 Schizocapsa plantaginea Hance.的块茎,水三七之名始载于《贵州卫生》[1],在《广西中药志》《湖南药物志》中均有记载,主要分布于贵州、湖南、广西等省区,为苗族、侗族、水族、瑶族等民族习用药物,用于百日咳、食积、胃痛、跌打损伤、咽喉肿痛的治疗[2]。现代药理和临床应用表明,水三七具有很好的抗肿瘤作用。2003年版《贵州省中药材、民族药材质量标准》和2014年版《广西瑶族习用药材质量标准》等标准中[3-5]均仅收载了水三七药材的来源、性状等简单的质控项目,缺少专属的鉴别方法和药效成分定量测定方法,这难以控制药材质量。因此,建立更为完善的水三七药材质量控制标准,显得非常有必要。
水三七主要化学成分为甾族皂苷、氨基酸、黄酮和花青色素[6]以及多种甾苦味物质[7],其中总皂苷为其抗肿瘤的主要活性成分,能明显抑制食管癌细胞、胃癌细胞和肝癌细胞的生长[8-11]。因此,本文以总皂苷作为水三七含量测定的指标成分。通过参考相关文献[5,12],对显微鉴别、水分、总灰分、酸不溶性灰分、浸出物和总皂苷含量测定进行研究,并对17批水三七药材进行测定,制定了合理的限度,为完善水三七质量控制标准提供了方法和依据。
1 材料与仪器
1.1 仪器与试剂 紫外可见分光光度计(苏州岛津仪器有限公司,型号UV-2700);型箱式电阻炉(天津市泰斯特仪器有限公司,型号SX-5-12);电子分析天平(梅特勒科学仪器公司,型号EL104,分度值0.1 mg)。
人参皂苷Re对照品(成都埃法生物科技有限公司,批号52286-59-6,纯度98 %);冰醋酸(上海申博化工有限公司,批号1803101)、香草醛(天津科密欧化学试剂有限公司,批号20180510)、高氯酸(国药集团化学试剂有限公司,批号20170113)、甲醇(天津市富宇精细化工有限公司,批号20180802)、无水乙醇(天津市富宇精细化工有限公司,批号20180228)均为分析纯。
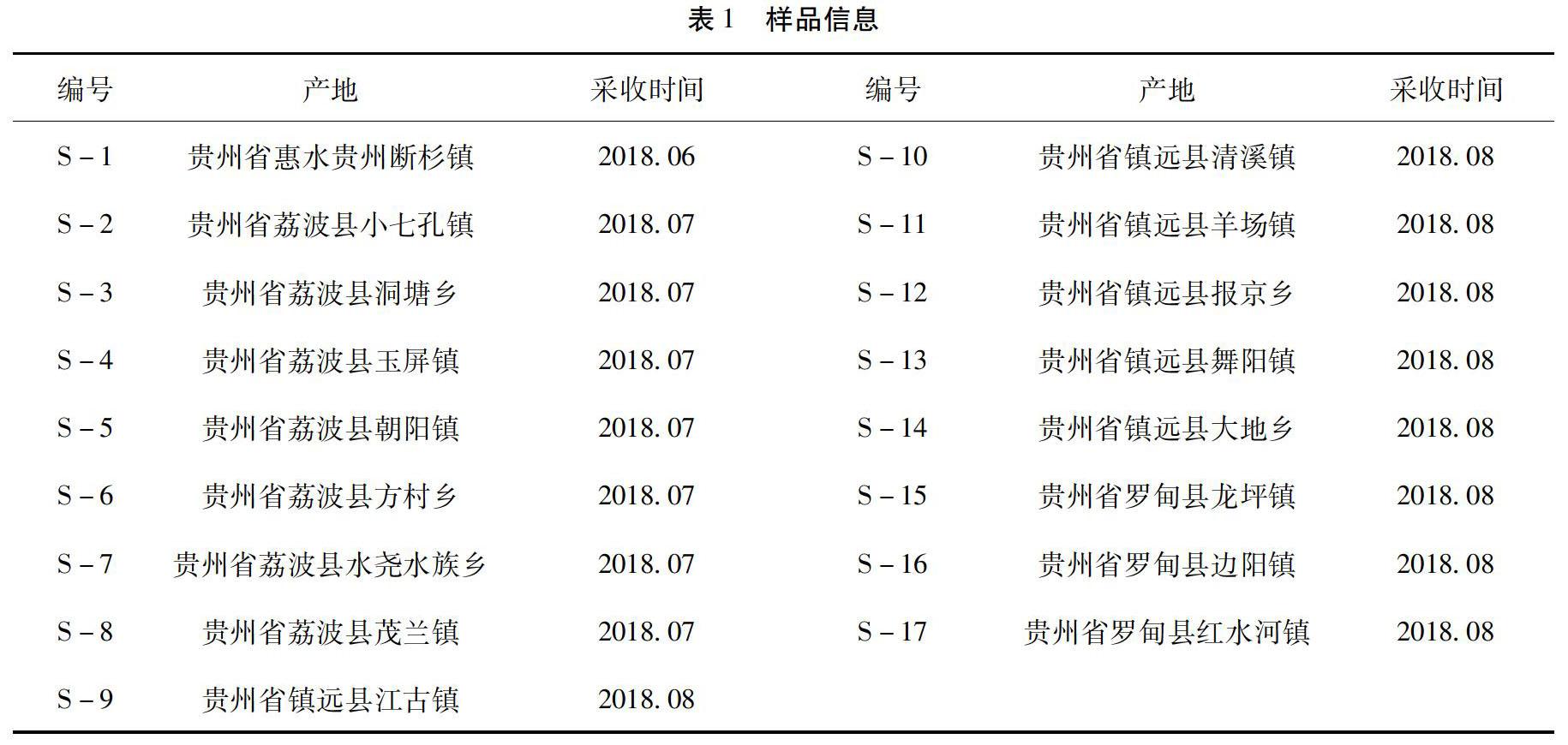
1.2 药材 水三七药材采自贵州省罗甸、惠水、荔波、镇远4县的不同乡镇,经贵州中医药大学生药学教研室江维克教授鉴定为蒟蒻薯科植物裂果薯 Schizocapsa plantaginea Hance 的块茎,样品信息见表1。
2 方法与结果
2.1 显微鉴别 粉末土黄色。淀粉粒类球形、半圆形、类三角形,直径5~25 μm,脐点点状、人字状,复粒由2~3分粒组成;草酸钙针晶散在或成束,长50~85 μm;螺纹导管可见,直径8~30 μm。见图1。
2.2 水分、总灰分、酸不溶性灰分的检查及醇浸出物的含量测定 参照2015年版《中国药典》第四部通则0832、2302测定水分、总灰分及酸不溶性灰分的含量;醇浸出物测定参照2015年版《中国药典》四部通则2201项下的热浸法测定,以55 %乙醇为溶剂。所测17批药材水分含量7.38%~8.79%,平均含量7.80%;总灰分含量3.26%~7.06%,平均含量3.89%;酸不溶性灰分含量0.45%~3.12%,平均含量0.72%;醇浸出物含量11.52%~22.32%,平均含量14.44%。结果见表3。
2.3 水三七总皂苷的含量测定
2.3.1 对照品溶液的制备 精密称取人参皂苷Re对照品18.6 mg,置25 mL容量瓶中,加甲醇稀释至刻度,摇匀,即得浓度为0.744 mg/mL的人参皂苷Re对照品溶液。
2.3.2 供试品溶液的制备 取水三七药材粉末约0.5 g,精密称定,置100 mL锥形瓶中,精密加入70 %的乙醇25 mL,超声处理90 min,滤过,滤液转移至50 mL的容量瓶中,用提取液稀释至刻度,即得。
2.3.3 显色条件及检测波长的选择 分别精密量取0.2 mL“2.3.1”和“2.3.2”项下的对照品、供试品溶液于10 mL比色管中,90℃水浴蒸干溶剂,依次精密加入新配置的10%香草醛-冰醋酸0.3 mL,高氯酸0.6 mL,摇匀,70℃水浴加热20 min,取出,立即用水迅速冷却至室温,加冰醋酸5 mL,以随行试剂为空白。在200 nm~800 nm范围扫描,供试品和对照品均在545 nm处有最大吸收波长。
2.3.4 线性关系考察 精密吸取“2.3.1”项下的对照品溶液50 μL、100 μL、150 μL、200 μL、250 μL、300 μL,于10 mL比色管中,按“2.3.3”项下显色,在545 nm测定各组吸光度。以浓度为横坐标(X),吸光度为纵坐标(Y)绘制标准曲线,得回归方程Y=0.027843X+0.127869(r=0.9994),表明人参皂苷Re在6.305 ~ 37.830 μg/mL范围线性关系良好。
2.3.5 精密度试验 精密吸取6份“2.3.1”项下对照品溶液1 mL于比色管在,按“2.3.3”项下显色,在545 nm测定各组吸光度,RSD值为0.19%,表明仪器精密度良好。
2.3.6 重复性试验 精密称取水三七药材粉末6份,按“2.3.2”项下方法制备供试品溶液,按“2.3.3”项下显色法测定吸光度,并代入标准曲线计算含量,平均含量为2.70%,RSD值为2.39%,表明方法的重复性良好。
2.3.7 稳定性试验 取“2.3.2”下供试品溶液,分别于室温0 h、0.5 h、1 h、2 h、14 h、18 h按“2.3.3”项下方法测定吸光度,RSD值为1.75%,表明供试品溶液在18 h内稳定性良好。
2.3.8 加样回收试验 称取已知含量的供试品6份,每份约0.25 g,精密称定,分别精密加入2.23 mg/mL的人参皂苷Re对照品溶液3 mL,按“2.3.2”项下供试品制备方法制备供试品溶液,按“2.3.3”项下显色法测定吸光度,计算回收率,回收率为95%~105%间,平均回收率为97.46%,RSD值为1.75%,结果见表2。
2.3.9 样品检测 取17批样品,按“2.3.2”项下方法制备供试品溶液,按“2.3.3”项下显色,在545 nm測定各组吸光度,计算各批次样品中总皂苷的含量,测定总皂苷含量1.39%~4.56%,平均含量为2.23%,RSD值为37.82%,结果见表3。
3 讨论
3.1 浸出物的测定 研究表明,水三七醇浸出物具有较好的抗肿瘤效果[8],控制醇浸出物的含量,对确保药材质量具有重要意义。本文考察了不同浓度的乙醇(55%、65%、75%、85%、95%)对浸出物含量的影响,发现55%乙醇作溶剂,浸出物的含量最高;比较了冷浸法和热浸法的提取效果,发现热浸法的提取效果较冷浸法好,且耗时短,故选择以55%乙醇为提取溶剂,热浸法测定含量。
3.2 总皂苷含量测定 水三七总皂苷为抗肿瘤的主要活性成分[9],参考相关文献[12],笔者对水三七总皂苷的提取工艺、显色条件进行了优选。提取溶剂考察发现70%甲醇和70%乙醇的提取率相对较高,且二者差异不显著,考虑到乙醇毒性较甲醇小,故选择70%乙醇作为提取溶剂。在此基础上,考察了提取方法(超声提取、回流提取),提取时间(15~105 min)以及溶剂用量(10~70 倍量)对总皂苷含量的影响,结果表明50倍量的70%乙醇超声提取90 min可将总皂苷提取完全,所建立的供试品制备方法相较文献报道的水浴回流4小时提取,不仅节约时间,而且提取率高、操作简便。显色条件考察了不同水浴挥干温度(70℃、80℃、90℃)对总皂苷含量的影响,发现挥干温度对总皂苷含量无显著性的影响,从节约时间的角度考虑,把水浴挥干温度定为90℃,相较于文献用70℃挥干溶剂,极大的节约了时间。接着对显色剂浓度和用量、显色温度及时间分别进行了优选,结果表明采用10%香草醛-冰醋酸0.3 mL,高氯酸0.6 mL,在70℃下水浴20 min显色,能充分反应,方法重复性良好。
3.3 限量标准制定 根据17批水三七药材的实验结果,水分、总灰分、酸不容性灰分按不高于平均值的120%制定标准限度,建议水分含量不得过9.0%,总灰分含量不得过5.0%,酸不溶性灰分含量不得过1.0%;浸出物、总皂苷按不低于平均值的80%制定标准限度,建议醇溶性浸出物含量不得少于12.0%,总皂苷含量以人参皂苷Re计,不得少于2.0%。
本文对水三七药材质量标准进行了系统的研究,相较于已有标准[3],增加了“显微鉴别”、“水分”、“总灰分及酸不溶性灰分”、“浸出物”和“含量测定”等项。且建立的质量控制方法简单易行,能够准确、科学地评价水三七质量,为水三七药材质量标准的提升提供了方法和依据。参考文献
[1]陈济中,蔡厚力.草药“水三七”临床疗效的初步观察[J].贵州卫生,1959(4):19-20.
[2]汪毅编著.黔本草[M].第1卷.贵阳:贵州科技出版社, 2015.3(1):277-278.
[3]贵州省药品监督管理局.贵州省中药材、民族药材质量标准(2003年版)[S].贵阳:贵州科学技术出版社,2003:105.
[4]湖南省食品药品监督管理局编.湖南省中药材标准[S]. 2009年版.长沙:湖南科技出版社,2010.02.266.
[5]广西壮族自治区食品药品监督管理局.广西壮族自治区瑶药材质量标准(第一卷)[S].南宁:广西科学技术出版社,2014:38-39.
[6]唐世蓉,庞自洁,吴余芳,等.南京中山植物园研究论文集[M].南京:江苏科学技术出版社,1980:122.
[7]欧明春,孙悦文,刘布鸣,等.裂果薯醇提取物对人肝癌裸鼠移植瘤生长与血管生成的影响[J].中国实验方剂学杂志,2015,21(4):106-110.
[8]邱汉琛,孙悦文,罗舜仁,等.裂果薯总皂苷对人肝癌细胞增殖、迁移、凋亡的影响及对正常肝细胞的毒性作用[J].山东医药,2017,57(15):1-4.
[9]孙悦文.广西特色中草药靶向抗肿瘤筛选及裂果薯皂苷的分离与抗肿瘤作用研究[D].南宁:广西医科大学,2013.
[10]YUE W, HAN C, MING C, et al. Saponins isolated from Schizocapsa plantaginea inhibit human hepatocellular carcinoma cell growth in vivo and in vitro via mitogen-activated protein kinase signaling[J]. Chin J Nat Med, 2018(1):29-40.
[11]罗舜仁,邱汉琛,陈燕燕,等.裂果薯皂苷的特征图谱及总皂苷中有效组分的抗肿瘤活性研究[J].天然产物研究与开发,2018(30):294-298.
[12]黄媛恒,黄晓亮,黄永运,等.正交实验优选水田七总皂苷的提取工藝研究[J].蛇志, 2018, 30(2):180-181.
(收稿日期:2020-03-15 编辑:刘 斌)

