基于UPLC-QTOF/MS技术鉴定雷公藤多苷片中的化学成分
章欣怡,辛贵忠,刘建群,刘丽芳*
(1.中国药科大学中药学院,天然药物活性组分与药效国家重点实验室,江苏 南京 210009;2.江西中医药大学 现代中药制剂教育部重点实验室,江西 南昌 330004)
雷公藤(TripterygiumwilfordiiHook.f)属于卫矛科雷公藤属植物,具有祛风除湿,活血通络,解毒杀虫,消肿止痛的功效。雷公藤多苷是从雷公藤药材去皮根部提取的总苷,主要有效成分包括二萜、三萜以及生物碱类[1]。以雷公藤多苷为主要成分的雷公藤多苷片目前在临床上广泛用于治疗类风湿性关节炎、自身免疫性肝炎、肾病综合症等,疗效已经得到普遍认可[2]。然而雷公藤中的主要活性成分雷公藤甲素、雷公藤红素等具有一定毒性,临床上有多例因服用雷公藤制剂引起的不良反应报道,限制了其进一步应用[3]。毒性反应的发生原因多样,可能由于药材品质欠佳、制剂工艺不足等多种因素导致。目前国内生产雷公藤多苷片的厂家众多,前期对多家企业生产的雷公藤多苷片的HPLC初步分析结果表明,不同来源的样品中所含化学成分的差异较大,可能为雷公藤多苷片不良反应产生的原因之一[4-5]。为了探究雷公藤多苷片的药效与毒性物质基础,规范制剂的生产标准,有必要对该类品的化学成分进行全面表征,为质量标准的制定提供分析依据。
超高效液相色谱(UPLC)与高分辨飞行时间质谱(Quadrupole Time-of-flight Mass Spectrometry, QTOF/MS)联用技术目前已被成功应用于中药化学成分的表征研究中[6]。本研究采用UPLC-QTOF/MS技术对雷公藤多苷片中所含的化学成分在电喷雾(electrospray ionization,ESI)质谱中的裂解特点进行了归纳总结,在此基础上,对雷公藤多苷片所含的化学成分进行了较全面的结构分析和鉴定,旨在为雷公藤多苷片的药效物质基础深入研究提供一定的思路和参考。
1 仪器与试药
Milli-Q纯水仪(Millipore公司,美国),Waters Acquity BEH C18(2.1 mm×100 mm,1.7 μm)色谱柱(Waters公司,美国),Shimadzu LC-30A Series UHPLC system (Shimadzu,德国),配备SIL-20AC自动进样器,LC-20AD 二元泵,CTO-20A柱温箱,SPD-M20A二极管阵列检测器等。AB SCIEX QTOFTM 5600+ system (AB SCIEX Technologies,美国),移液枪(eppendorf公司,德国),5424高速离心机(eppendorf公司,德国),Sartorius BT125D电子天平(赛多利斯科学仪器有限公司,中国),HH-2数显恒温水浴锅(国华电器有限公司,常州)。
乙腈(色谱纯,美国merck公司),甲醇(色谱纯,美国merck公司),超纯水(Milli-Q 纯水仪,美国Millipore公司),甲酸(质谱级,Sigma-Aldrich公司)。雷公藤多苷片(购自国内某药企,批号:180604)。雷公藤甲素(购自郑州丰耀农业科技有限公司,批号:140320)。雷公藤红素(购自郑州丰耀农业科技有限公司,批号:151208)。雷公藤次碱(购自成都普思生物科技股份有限公司,批号:PRF8042505),对照品纯度均大于98%。
2 方法
2.1 对照品溶液配制
取雷公藤甲素,雷公藤红素和雷公藤次碱,精密称定,置1 mL量瓶中,加甲醇溶解并定容至刻度,制成标准品储备溶液。将标准品储备溶液等量混合并稀释,制成浓度为100 μg/mL的混合标准工作溶液,置于4 ℃保存备用。
2.2 供试品溶液配制
取适量雷公藤多苷片,研细后精密称定750 mg粉末,加10 mL甲醇超声提取30 min。13 000 rpm/min离心取上清液,N2吹干,加1 mL甲醇复溶,得浓度为100 μg/mL(按雷公藤多苷含量计)的供试品溶液。置于4 ℃保存备用。
2.3 色谱和质谱条件
2.3.1 色谱条件
Shimadzu LC-30A Series UHPLC液相系统,柱温为35 ℃。流速为0.2 mL/min,流动相为0.1%甲酸-水(A)和0.1%甲酸-乙腈(B)。流动相梯度:0~2 min,5%~20% B;2~9 min,20%~40% B;9~14 min,40% B;14~24 min,40%~65% B;24~27 min,65%~90% B;27~29 min,90% B;29~33 min,5% B,进样体积为2 μL。
2.3.2 质谱条件
AB SCIEX TripleTOF TM 5600+质谱仪,ESI离子源,正离子模式下进行检测。雾化:N2,1.5 L/min;干燥器:N2,140 kPa,CID碰撞气:氩气,50 kPa;解簇电压:90 V;碰撞能:50 V;离子源温度:350 ℃;毛细管温度:300 ℃;扫描范围:m/z50~1 500;所有样品数据采集均采用全扫描模式,非靶向模式获得MS/MS二级碎片。
2.4 数据处理
使用Peak View 软件(AB公司,美国)进行数据分析,通过软件自带的分子式预测功能推测化合物的可能分子式,结合文献检索结果进行初步鉴定。
3 结果与讨论
通过2.3项下色谱条件对供试品溶液进行UPLC-QTOF-MS/MS分析,正离子模式下总离子流图(Total Ion Chromatogram, TIC)见图1。综合考虑保留时间,分子式,精确分子量,特征性离子碎片,参考文献,共鉴定了36个化合物,包括14种生物碱,10种二萜类及其内酯,11种三萜类及其内酯,1种烃类。
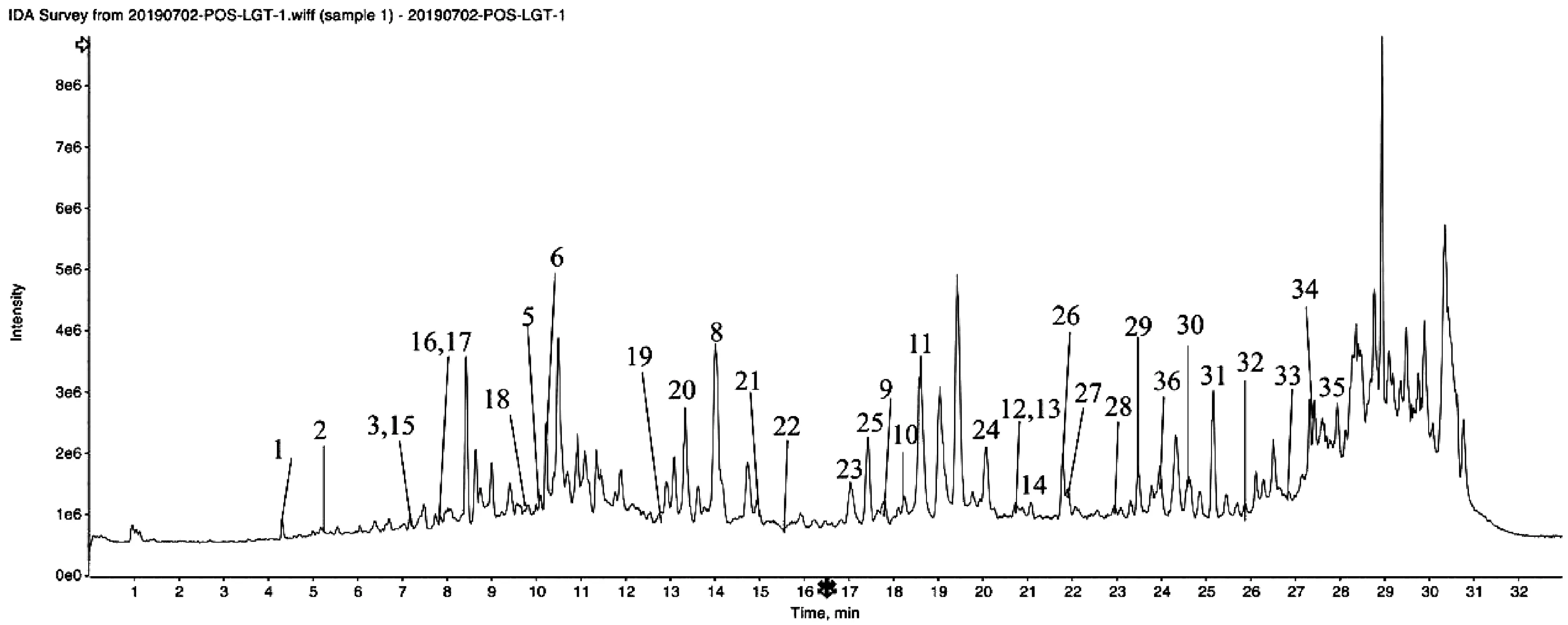
图1 雷公藤多苷片总提物UPLC-QTOF/MS总离子流图
3.1 生物碱类化合物
雷公藤多苷中的生物碱分为大环内酯型和非大环内酯型倍半萜类生物碱,以前者含量居多。本实验选取雷公藤次碱为对照品研究大环内酯型倍半萜类生物碱的质谱裂解路径,质谱图及裂解方式见图2。
由图2可知,雷公藤次碱在质谱中的分子离子峰以m/z868.3035 [M+H]+的加和形式存在,质谱碰撞裂解时首先丢失H2O,产生m/z850.292 7 [M+H-H2O]+的碎片。m/z850.292 7 [M+H-H2O]+的碎片离子易发生中性丢失,连续丢失一个C2H2O和H2O产生m/z808.282 8和m/z790.272 4的碎片。除丢失中性分子之外,雷公藤次碱中的苯甲酸基也会在碰撞中发生断裂,由母离子m/z868.303 5脱去一分子BzOH形成m/z746.266 2 [M+H-BzOH]+碎片离子。该离子会继续丢失C2H2O、H2O、CH3OH产生m/z704.256 7,m/z686.243 9,m/z644.236 0的碎片离子。此外,雷公藤次碱的大环断裂后会产生倍半萜部分和吡啶二羧酸部分,后者有一个响应较高的碎片离子m/z206.080 8。该碎片会继续丢失CO, H2O形成m/z178.086 1、160.075 1、132.080 8。对照标准品图谱,可推断化合物14为雷公藤次碱。结合其他倍半萜类生物碱的裂解方式,可以得到大环内酯型倍半萜生物碱质谱裂解的特点如下:1)分子离子峰以[M+H]+的加和形式存在。2)裂解方式有中性小分子丢失和开环,中性丢失过程中容易丢失H2O (18 Da)、CH3OH(32 Da)、C2H2O (42 Da)、CH3COOH(60 Da),开环裂解后吡啶二羧酸部分含有羟基的生物碱会形成m/z204的特征碎片离子,不含羟基则形成m/z206的特征碎片离子。
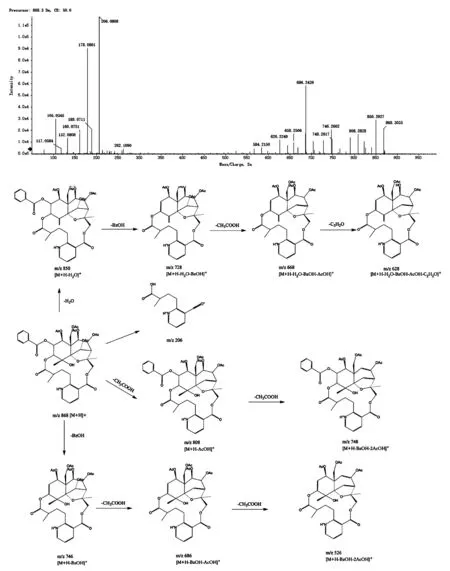
图2 雷公藤次碱质谱图及裂解规律
化合物1的准分子离子峰是m/z370.211 7,加和形式为[M+H]+。m/z353.188 4推断为准分子离子丢失一个NH3(17 Da)所获得的碎片。因此说明化合物1在N上没有甲基取代。化合物1 的二级质谱中有一明显的m/z160.1126 特征峰,为亚精胺类生物碱特征峰。根据另一特征峰m/z106.065 3,结合文献和精确分子量匹配[7],可知化合物1为Celafurine。化合物2的准分子离子峰为m/z380.234 5,加和形式为[M+H]+。准分子离子峰比化合物1多10 Da。化合物2的碎片裂解路径与化合物1相似,结合文献和精确分子量匹配[8],可知化合物2为Celabenzine。同理可推断化合物3为Celacinnine。
化合物4的准分子离子峰为m/z780.274 8,加和形式为[M+H]+。m/z752.278 0、734.264 7、674.252 5、632.234 8为准分子离子连续中性丢失CO(28 Da)、H2O(18 Da)、CH3COOH(60 Da)、C2H2O(42 Da)所获得的碎片,表明母核上有羟基和羧基取代基。同时还检测到较高的m/z204.065 0响应,表明吡啶二羧酸部分含有羟基。结合文献[9],可推断化合物4为Wilfordlongine。
化合物5的准分子离子峰为m/z764.278 7,在m/z大于500的区域有CO(28 Da)、H2O(18 Da)、CH3COOH(60 Da)、C2H2O(42 Da)的中性丢失,与化合物4的裂解规律相似。同时化合物5有一明显的m/z206.081 4响应,说明其吡啶二羧酸部分不含羟基。结合相关文献[10],推断化合物5为Aquifoliunine E-Ⅲ。
化合物6的准分子离子峰为822.289 4,加和形式为[M+H]+。化合物6与化合物5的准分子离子峰相差42 Da,推测二者之间相差一个OAc。结合文献[11]与特征峰m/z204.065 7,推测化合物6为Alatusinine。同理可推断准分子离子峰分别为m/z806.290 2、874.273 4、868.304 7的化合物8、9、11为Wilfordinine E,Wilfordine,Congorinine E-1[10,12]。
化合物7的准分子离子峰为m/z874.273 4,加和形式为[M+H]+。对照雷公藤次碱的标准图谱可知,m/z762.266 3为准分子离子峰丢失一分子呋喃甲酰基(FuOH,112 Da)所得,表明其含有呋喃甲酰基。结合文献推断化合物7为Wilfordconine[7]。化合物10的准分子离子峰m/z858.284 5,加和形式为[M+H]+,同样有112 Da的特征丢失,同理可推测化合物10为Wilforgine。
化合物12的准分子离子峰为m/z926.308 2,加和形式为[M+H]+。m/z804.273 9与准分子离子峰相差122 Da,推断其母核上可能有一苯甲酰基取代。化合物12有一明显特征峰m/z204.066 4,表明其含有羟基。结合相关文献[7],推断化合物12为Wilfornine A。
化合物13的准分子离子峰为m/z968.284 6,加和形式为[M+H]+。m/z856.269 4为准分子离子峰脱去一分子呋喃甲酰基(FuOH,112 Da)所得。化合物13在m/z500-840之间的碎片裂解方式与化合物10相似,且碎片离子质荷比均相差2 Da,推测可能是脱去一分子后形成了双键。结合相关文献[13],推测化合物13为Triptonine B。已推断出的生物碱类化合物化学结构式见图3。
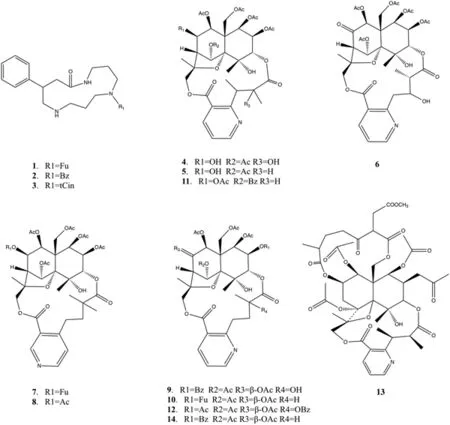
图3 生物碱类化合物化学结构式
3.2 二萜类化合物
雷公藤多苷中的二萜类化合物大部分属于松香烷型和贝壳杉烷型,松香烷型的雷公藤甲素为其代表性成分。本研究选择雷公藤甲素的对照品研究二萜类化合物质谱裂解规律。图4为雷公藤甲素可能的质谱裂解路径。
由图4可以看出,雷公藤甲素的准分子离子峰是m/z361.166 4,加和形式为[M+H]+。m/z343.154 8,m/z325.146 2推断为其连续丢失2分子H2O(18 Da)所得碎片,m/z287.128 7推断为丢失2分子CO(28 Da)所得碎片。首先参考对照品,确定化合物16为雷公藤甲素。雷公藤甲素的化学结构中因为具有醚键,酯键,羟基取代基,所以在质谱裂解路径中容易丢失H2O和CO从而产生18 Da和28 Da的中性丢失。另外文献报道,二萜内酯类化合物还有可能在质谱中发生C环均裂,从而生成互补碎片[14]。由于二萜类化合物的质谱裂解方式较为复杂多样,本研究主要通过准分子离子峰和二级碎片与已报道萜类化合物相匹配,对雷公藤多苷片中所含的二萜类化合物进行推断。化合物15、20、24裂解路径不明确,但是与雷公藤药材中已报道的萜类化合物质谱信息匹配度较高,分别推断为Tripterinin、Triptonoterpene methyl ether和Triptonoditerpenic acid[7]。
化合物17准分子离子是m/z319.226 9,二级碎片来自于H2O和CO的中性丢失。其中二级碎片m/z255与准分子离子峰之差为64 Da ,推测其可能为内酯环开裂丢失2分子H2O和1分子CO所得。结合相关文献报道[7],推断化合物17为Neotripterifordin。化合物21的准分子离子峰为m/z301.216 8,比化合物少18 Da。化合物21与化合物17的裂解方式十分相似,因此推断化合物21比化合物17少一个羟基,同理推断化合物21为Doianoterpene B[14]。
化合物18与化合物22的准分子离子峰分别为m/z303.231 9,m/z303.231 7,属于同分异构体。二者都有H2O和CO的中性丢失,区别在于化合物22有一m/z285.220 9碎片,可能为准分子离子峰丢失CO2所得。结合相关文献报道[15],推测化合物18为ent-19-hydroxykaur-16-ene,化合物22为Doianoterpene C。
化合物19的准分子离子峰为m/z329.175 2,二级碎片m/z269.114 8与准分子离子峰相差60 Da,推测其可能含有羧基取代。其余二级碎片有H2O中性丢失。化合物23与19的裂解方式相似。结合相关文献[10],推断化合物19为Triptoquinone A,化合物23为Triptoquinone B。已推断出二萜类化合物化学结构式见图5。
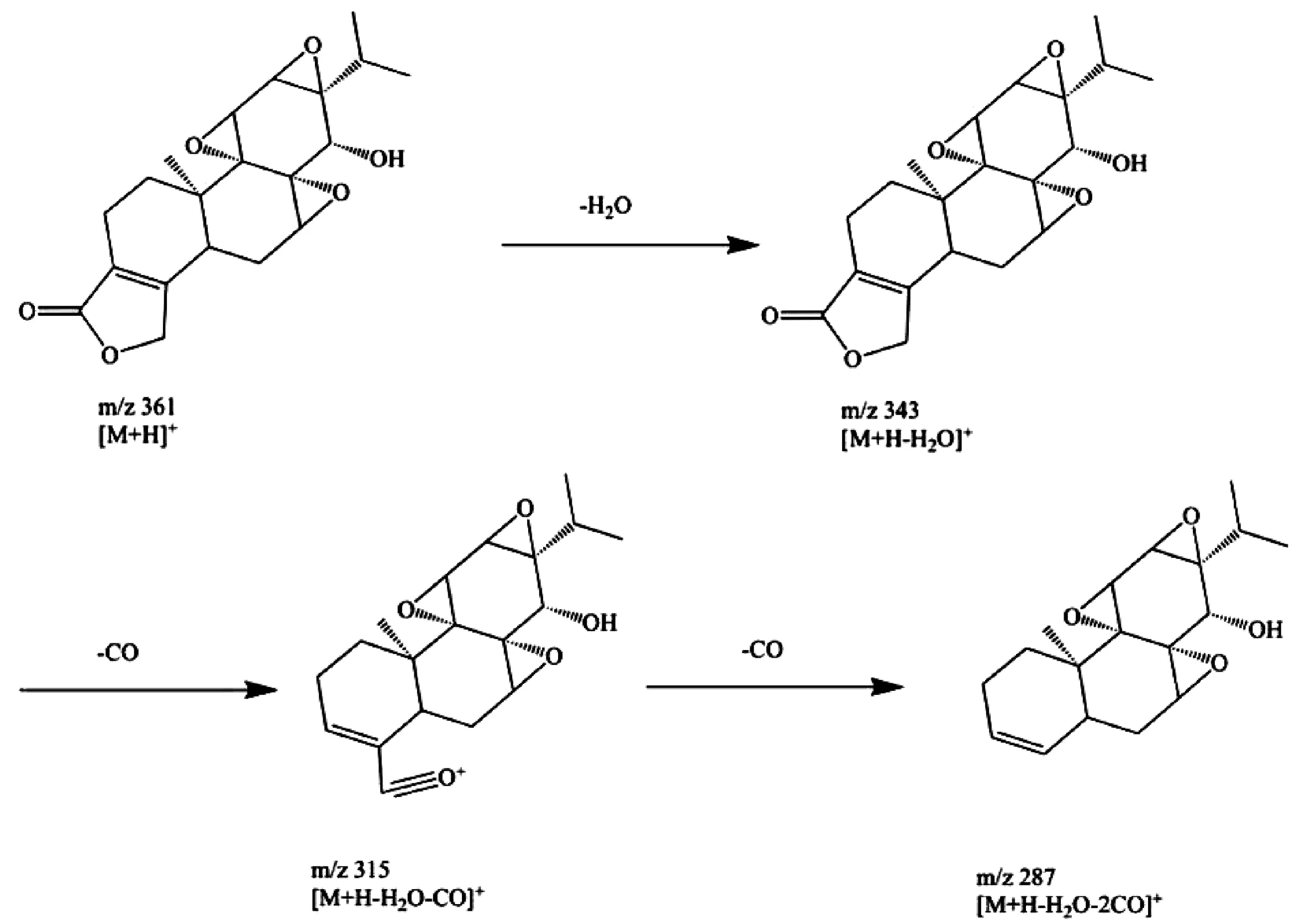
图4 雷公藤甲素裂解规律

图5 二萜类化合物化学结构式
3.3 三萜类化合物
雷公藤多苷中的三萜类化合物组成相对复杂,主要包括木栓烷,乌苏烷和齐墩果烷型等。木栓烷型的雷公藤红素为其代表性成分。本研究选择雷公藤红素的对照品研究三萜类化合物质谱裂解规律,图6为雷公藤红素的质谱裂解路径。
由图6可以看出,雷公藤红素的准分子离子峰是m/z451.285 0,加和形式为[M+H]+。m/z405.279 7为雷公藤红素脱去一个中性小分子甲酸HCOOH(46 Da)所得碎片。五环三萜中的角甲基易发生位移和脱去,雷公藤红素上的角甲基位于烯丙位,易脱去形成稳定的C+离子。m/z257.211 1为A环与B环共用键上的角甲基脱去后形成双键,接着发生Retro Diels-Alder(RDA)重排,最后脱去一个甲基后形成的离子。同理,碎片离子m/z249.185 1,m/z215.107 3分别为B环与C环,C环与D环共用键上的角甲基脱去重排后所得。参考对照品,确定化合物33为雷公藤红素。虽然相比二萜类,三萜类的质谱特征更加明显,特别是具有C12,C13双键的齐墩果烯和熊果烯,在质谱碰撞下能发生明显的C环裂解。但由于萜类化合物复杂的裂解路径,三萜化合物的鉴定依旧遵循结合裂解规律与文献报道的方式进行推断。其中化合物28,32无明显质谱裂解规律,根据精确相对分子质量和文献报道推断为30-hydroxyfriedelan-3-one与Orthosphenic acid[7,16]。

图6 雷公藤红素裂解规律
化合物25的准分子离子峰是m/z459.311 5,加和形式为[M+H]+。m/z441.297 9为其丢失一分子H2O(18 Da)所得碎片。m/z231.101 8,m/z228.230 0为互补碎片,推测其C环17位发生裂解。结合相关文献报道[7],推断化合物25为Triptotin H。化合物29的准分子离子峰是m/z485.329 1,加和形式为[M+H]+。准分子离子峰脱去一分子甲酸HCOOH(46 Da)形成碎片离子m/z439.329 1[M+H-HCOOH]+。化合物29的裂解路径与雷公藤红素相似,结合文献[7]可推断为Cangoronine。同理可推得化合31为Wilforol A。
化合物26的准分子离子峰是m/z455.353 6,加和形式为[M+H]+。准分子离子峰丢失一分子H2O后得碎片m/z437.342 8,提示该化合物上可能存在羟基取代。同时m/z317.210 9与准分子离子峰相差138 Da,该质量丢失为齐墩果-12-烯类的B环一般裂解方式,提示该化合物可能有齐墩果-12烯B环类似结构。同时m/z208.179 8与m/z247.170 2为互补碎片,因此推测该化合物可能属于齐墩果-12烯类。m/z219.138 1可能为m/z247.170 2中性丢失一分子CO(28 Da)所得,推测该化合物中可能有内酯结构。结合相关文献报道[7],推断化合物26为Wilforlide A。化合物27的准分子离子峰是m/z471.348 3,加和形式为[M+H]+。化合物27与化合物26的分子量之差为16 Da,二者之间可能有羟基取代的差异。化合物27的裂解方式与26相似,同样存在互补碎片,结合相关文献报道[7],推断化合物27为2α,3β,-dihydroxy-olean-12-ene-22,29-lactone。同理推测化合物30为Wilforlide B[12]。
化合物34的准分子离子峰为m/z473.363 8,加和形式为[M+H]+。m/z455.353 6,m/z437.342 4为准分子离子峰连续失去两分子H2O所得。m/z409.347 5为m/z437.342 4失去一分子CO(28 Da)所得。化合物34中同样有138 Da特征性B环碎裂所得碎片m/z335.234 2,推测该化合物34可能属于齐墩果-12-烯类。结合相关文献报道[12],推断化合物34为Triptotriterpenic acid C。同理可推得化合物35为3β,28-dihydroxy-3-oxo-olean-12-en-29-oic acid[7]。已推断出三萜类化合物化学结构式见图7。
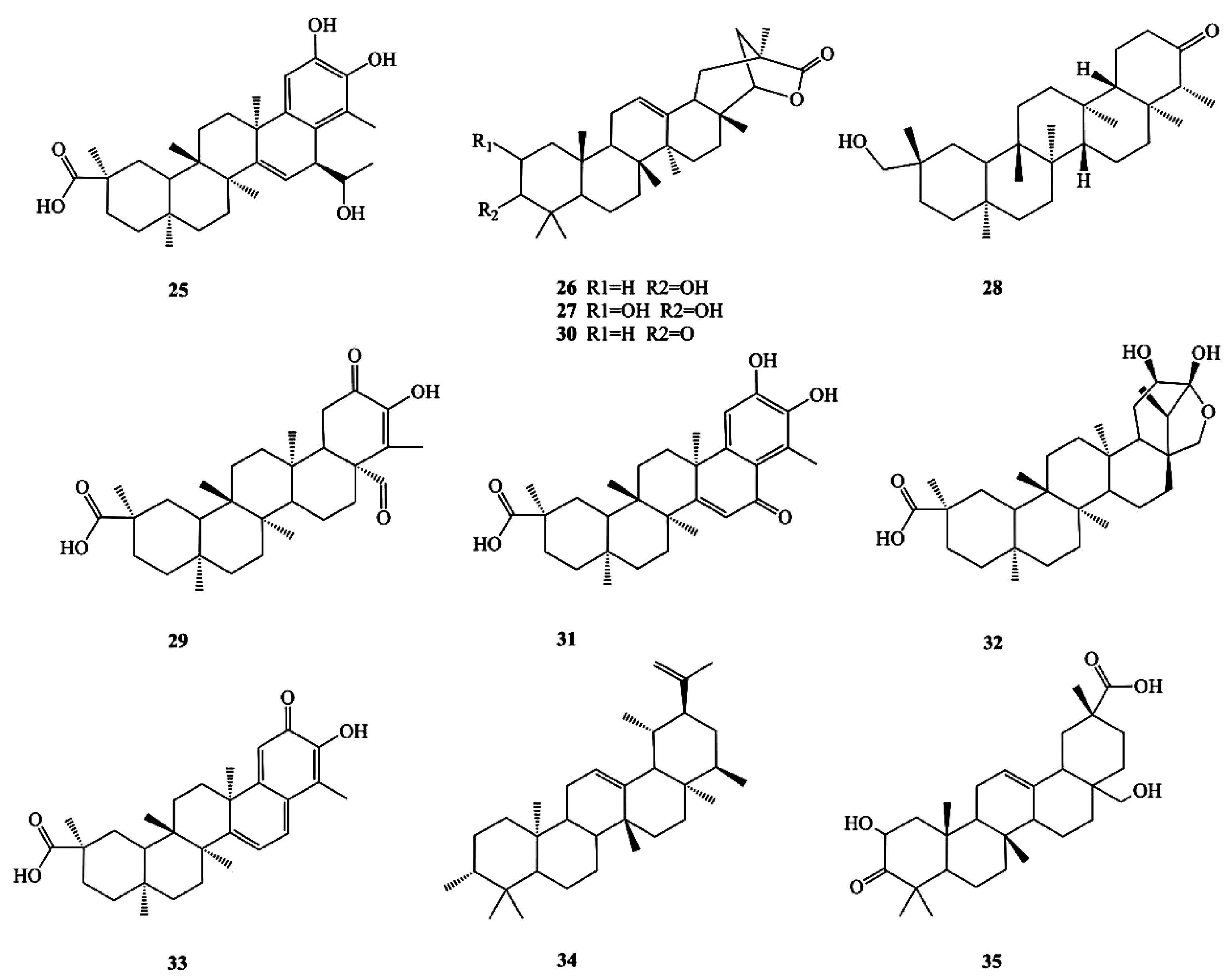
图7 三萜类化合物化学结构式
3.4 其他类化合物
化合物36的准分子离子峰为281.248 0,加和形式为[M+H]+。其二级质谱中有明显的一系列m/z相差14的碎片离子峰,推测其可能为链烃结构。结合精确相对分子质量和相关文献报道信息[1],推断化合物36为Linoleic acid。
已推断出的化合物结构见表1。
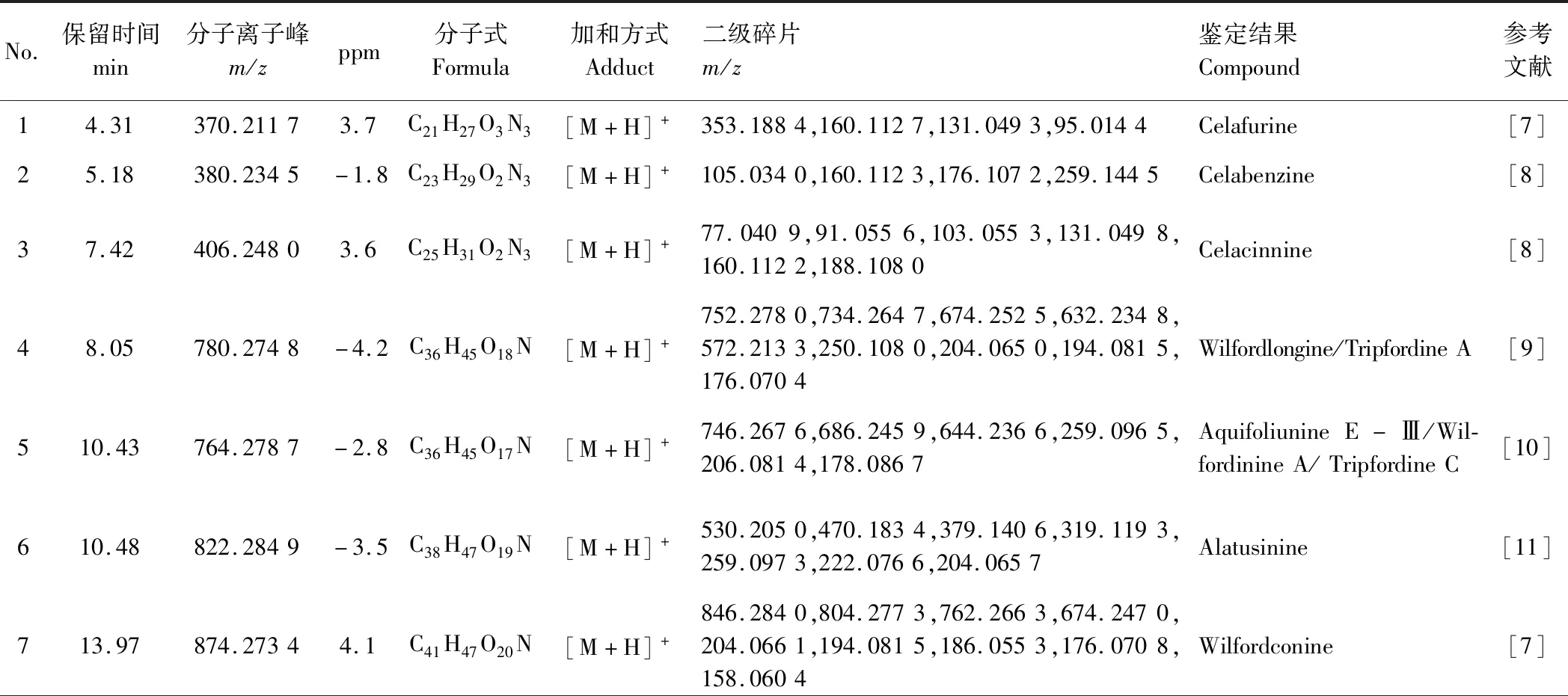
表1 雷公藤多苷片中36种化合物的定性分析结果
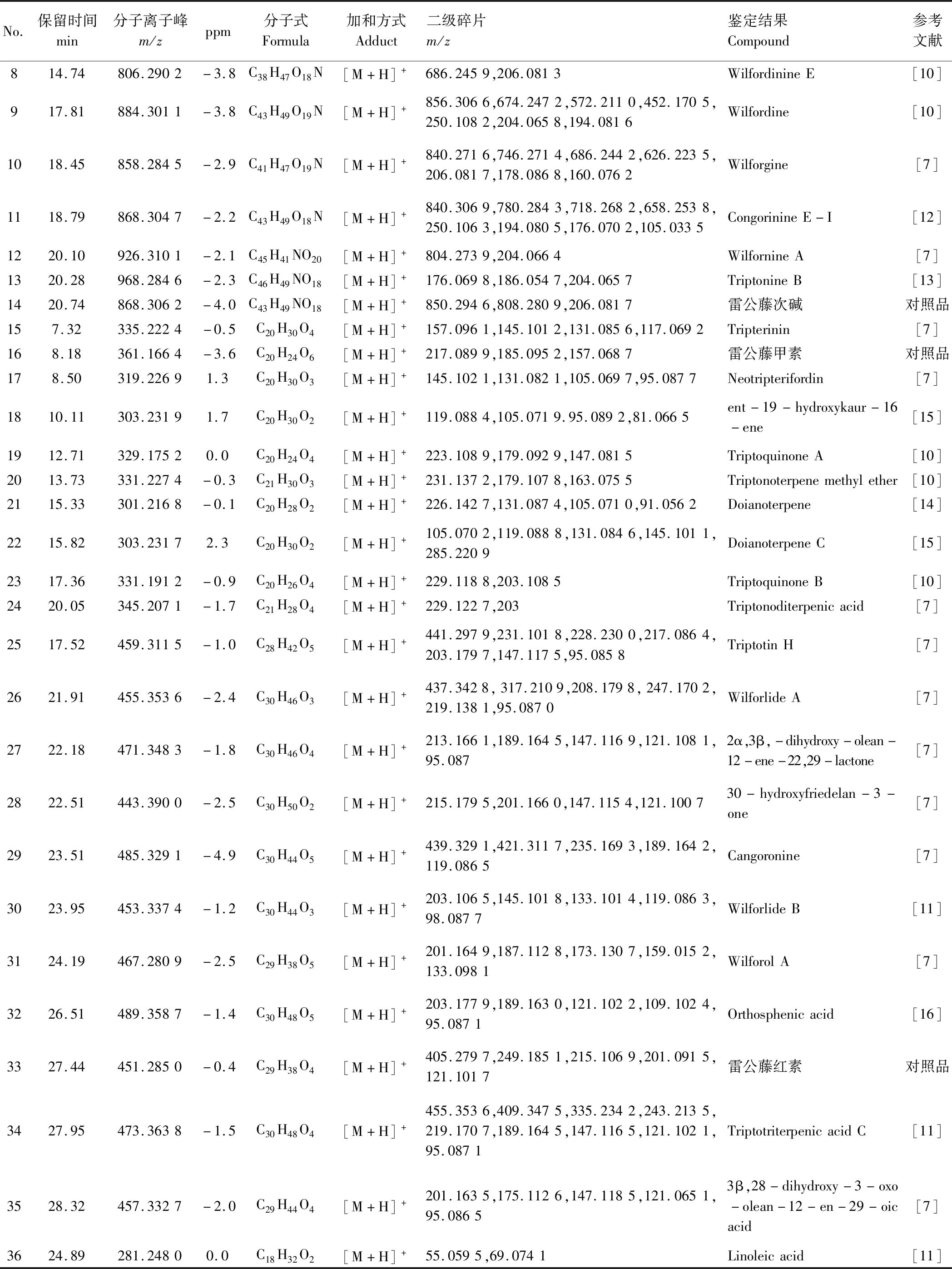
续表
4 结论
本研究基于目前已有的雷公藤化学成分研究报道和对照品裂解图谱,首先建立了雷公藤多苷成分的质谱信息数据库,根据化合物类型进行分类汇总后探讨了代表性成分的化学结构特点和质谱裂解规律,进而借助UPLC-QTOF/MS技术对雷公藤多苷片的主要化学成分进行了全面的表征,最终鉴定出该制剂中的36个化合物,为雷公藤多苷片质量标准的提及其药效物质基础深入研究提供了重要参考。

