八角水溶性膳食纤维对油脂乳液消化特性的影响
吴克刚,魏 浩,柴向华,段雪娟,,梁婉霞,廖经飞,沈雪荣
(1.广东工业大学轻工化工学院,广东 广州 510006;2.广州市香思馨情健康科技有限公司,广东 广州 511458;3.广州芬豪香精有限公司,广东 广州 510000;4.罗定市荣兴香料有限公司,广东 罗定 527200)
八角是我国的一种特色香料资源,重要产地为广西、广东。八角在两省的种植面积和产量约占全国85%、世界的70%以上[1]。目前绝大部分八角都是作为香料使用,以原料的方式直接销售,只有5%的八角被药用[2]。此外,工业上应用的八角提取物主要为八角油、莽草酸,而对于八角中丰富的膳食纤维(多糖)的应用则较少。随着经济的发展,人们对各种营养素的摄入量逐渐增加,但摄入过量脂质会导致肥胖、心脑血管疾病、动脉粥样硬化和II型糖尿病等营养代谢疾病[3]。大量的研究表明,摄入膳食纤维能够降低代谢疾病的致病风险及改善肠道菌群[4-6]。因此,对八角中的膳食纤维进行研究,既能开发新膳食纤维品种,又有利于提高八角的利用率和附加值。
研究表明,膳食纤维会通过不同方式对胃肠道中油脂的消化行为产生影响,从而改变机体对摄入脂肪的吸收和利用[7-11]。但另一方面,在食品和饲料工业上,常常使用乳液递送系统包被、保护和靶向递送敏感脂溶性生物活性成分。乳液递送系统会影响脂溶性生物活性物质的消化速率和消化程度,进而影响其生物有效性和生物利用度[12]。因此,研究膳食纤维对于乳液递送系统的影响,对于膳食纤维在食品和饲料工业中的应用具有重要的理论价值。
本研究采用微波辅助酶法制备八角水溶性膳食纤维(water soluble dietary fiber from star anise,SASDF),测定其常规营养成分、中性糖组成、半乳糖醛酸含量、酯化度和重均分子质量;检测消化前后其对蛋白包裹型乳液递送系统的理化性质和微观结构的影响;利用pH-stat法[13],即通过记录脂肪乳液在体外水解过程各反应时间点的用碱量,计算在体外小肠模型中被水解的三酰甘油在初始脂肪乳液样品中所占的比例,从而研究SASDF对纳米脂肪乳液消化速率和消化程度的影响,并探究SASDF对纳米脂肪乳液消化特性的影响机制,以期为SASDF在食品和饲料工业中的应用提供理论基础,以及为食用香料创新开发利用提供新的研究思路。
1 材料与方法
1.1 材料与试剂
八角(Illicium verumHook.f.)产地广西百色市;糖化酶 阿拉丁试剂(上海)有限公司;蛋白酶源叶生物科技有限公司;牛白蛋白,NaCl、CaCl2、NaOH、HCl(均为分析纯) 国药集团化学试剂有限公司;猪胆盐 上海麦克林生化科技有限公司;猪脂肪酶 东京化成工业株式会社。
1.2 仪器与设备
DS-1高速组织捣碎机 江阴市保利科研器械有限公司;AH-1500均质机 日本ATS株式会社上海代表处;DF-101S集热式恒温加热磁力搅拌器 巩义市予华仪器有限责任公司;PHS-3C pH计 上海仪电科学仪器股份有限公司;90plus PALS高灵敏度Zeta电位及粒度分析仪美国布鲁克海文仪器公司;MCR 301旋转流变仪 安东帕股份有限公司;LSM 800 with Airyscan超高分辨激光共聚焦显微镜 卡尔蔡司(上海)管理有限公司。
1.3 方法
1.3.1 SASDF的制备
称取一定量的脱脂八角粉,按料液比1∶45(g/mL)比例加入去离子水,浸泡均匀后调节pH值至6.0并以脱脂八角粉的添加量为100%,加入质量分数2%的蛋白酶,500 W微波提取3 次,每次20 s,间隔2 min,再调节pH值至5.0,加入质量分数4%的糖化酶,同样功率微波处理5 次,每次20 s,间隔2 min,沸水浴灭酶15 min,4 000 r/min离心15 min,取上清液,旋蒸至原液的1/4~1/5,加入3 倍体积的95%乙醇溶液醇沉,4 ℃静置24 h,4 000 r/min离心15 min,取沉淀物,用无水乙醇洗2 遍后4 000 r/min离心15 min,置于真空干燥箱中,在55 ℃条件下干燥,即得到SASDF。
1.3.2 组成和理化指标测定
常规营养成分:参照食品安全国家标准[14-18]测定;中性糖组成:采用高效阴离子交换色谱-脉冲安培检测法测定[19];半乳糖醛酸含量:采用紫外-可见光分光光度法测定[20];酯化度:采用高效液相色谱法测定[21];重均分子质量:采用尺寸排阻凝胶色谱法测定[20]。
1.3.3 SASDF储备液的配制
质量分数为2% SASDF储备液:将4 g SASDF溶于196 g去离子水中,于25 ℃持续搅拌12 h,将制得的SASDF储备液保存于4 ℃冰箱,每次使用前于室温条件下持续搅拌15 min。
1.3.4 脂肪乳液的制备
使用高速组织捣碎机,在6 000 r/min条件下将含质量分数5%橄榄油与质量分数95%的乳化溶液混合3 min,即可得到粗乳状液,其中乳化溶液为含有质量分数1%牛白蛋白的5 mmol/L磷酸缓冲溶液(pH 7)。将所得粗乳状液通过高压均质机,操作压强为100 MPa,重复5 次即可有效缩小乳液的粒径。所得乳液不添加SASDF即为“初级乳液”。
1.3.5 乳液-SASDF混合液的配制
将初级乳液、SASDF储备液、5 mmol/L磷酸缓冲溶液(pH 7)按比例混合。最终乳液-SASDF混合溶液中油脂质量分数0.5%、牛白蛋白质量分数0.1%,以及SASDF质量分数分别为0%、0.1%、0.2%、0.4%。所有样品均为新鲜制备,在体外小肠消化模型处理前置于磁力搅拌器上450 r/min搅拌30 min。
1.3.6 体外小肠消化模型的建立
体外消化模型的建立根据前人研究[12-13,22]所用的针对脂肪类物质体外消化的模型为基础略作改动:
1)量取30.0 mL乳液-SASDF混合液(含有0.5%的橄榄油和0%~0.4% SASDF),置于100 mL烧杯中,37 ℃恒温10 min,pH值调至7.0。
2)准确称取187.5 mg猪胆盐,溶解于3.5 mL磷酸缓冲溶液(5 mmol/L)中;配制1.5 mL矿物盐溶液(含0.25 mol/L Ca2+和3.75 mol/L Na+);准确称取60 mg胰脂肪酶,用2.5 mL磷酸缓冲溶液(5 mmol/L)配制成脂肪酶悬浊液。37 ℃恒温,pH值调至7.0。
3)在搅拌状态下,按照猪胆盐溶液、矿物盐溶液、脂肪酶悬浊液的顺序向1)中烧杯添加各活性成分后立即计时,并不断滴加0.1 mol/L NaOH溶液使反应体系的pH值维持在7.0。
1.3.7 粒径及Zeta电位分析
使用Zeta电位及粒度分析仪测定。为避免多重散射效应,在测定粒径之前,所有的乳液样品均被磷酸缓冲溶液(5 mmol/L,pH 7.0)稀释到约质量分数0.005%。测定Zeta电位则将待测样品用pH值相同的缓冲溶液以1∶100稀释后再进行测定[23]。
1.3.8 流变特性分析
使用旋转流变仪的同轴圆筒部件测定初始样和消化样的流变学特性。将样品注入旋转流变仪的外部圆筒腔中,正式测试前,仪器自动运行一个预热平衡过程(25 ℃、5 min)。随后开始测定样品的剪切应力随剪切速率(0.01~50 s-1)的变化情况,取剪切速率为20 s-1的黏度值为表观黏度[23]。
1.3.9 微观结构观察
将50 μL尼罗红染色液(1 mg/mL)滴入装有2 mL样品的玻璃试管中,充分吹打6~7 次混合均匀,然后从中取7 μL于显微镜载玻片上,盖上盖玻片后,利用超高分辨激光共聚焦显微镜于60×油镜下观察样品的共聚焦成像。尼罗红的激发光源为543 nm氩激光束,接收波长为555~620 nm,然后用仪器自带软件(ZEN 2.6)处理图像,使其呈现(512×512)像素,像素尺寸为414 nm,像素停留时间61.45 ms[23]。
1.3.10 脂肪消化率的计算
根据消化过程中消耗NaOH溶液的量,可以计算脂肪消化率:

式中:C0为NaOH溶液浓度(0.1 mol/L);Vt为当反应时间为tmin时,消耗的0.1 mol/L NaOH溶液总量/mL;m为加入的橄榄油总量/g;M为橄榄油的平均分子质量/(g/mol)。在相同实验条件下用NaOH溶液滴定未含橄榄油的样品,得到的曲线用于基线校正,以排除系统误差[24]。
1.3.11 一级反应速率常数
甘油三酯体外水解过程可以视为一个酶促分解过程,乳液中油脂的消化数据与以下一级反应方程拟合较好[12]:

式中:Ct为甘油三酯在脂肪酶作用下水解释放的脂肪酸在时间“t”时的浓度;Cmax为水解反应结束时甘油三酯水解所产生的脂肪酸浓度;k为一级反应速率常数。
由式(2)可得到如下公式:

由于本研究建立的是胰脂肪酶浓度固定的静态消化模型,Cmax在足够长的时间范围内可以确定,因此可对式(3)进行自然对数处理,得到式(4),完成一级反应速率常数k的线性转化,即对消化曲线进行LOS(logarithm of slope)处理。但在本研究中,消化模型中的脂肪酶及其他组分的浓度一定,因此此时的脂肪酶水解反应实际为伪一级反应。

以反应时间t为横坐标,以ln[(Cmax-Ct)/Cmax]为纵坐标作图,计算斜率则可得乳液中油脂消化反应的一级反应速率常数k。
1.4 数据分析
脂肪乳液消化的一级反应速率常数先经Origin Pro 2017进行回归分析,然后使用Excel拟合得到R2,比较后得到最佳线性回归方程。
2 结果与分析
2.1 SASDF的组成及理化指标
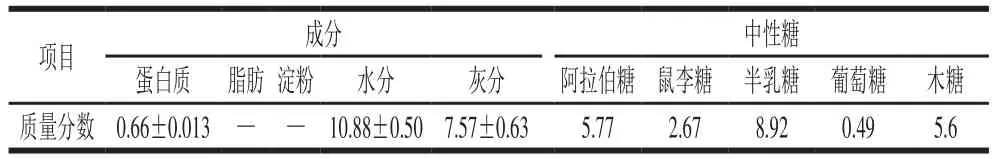
表1 SASDF常规营养成分和中性糖组成Table 1 Macronutrients and neutral sugar composition of SASDF
半乳糖醛酸含量测定结果表明,SASDF中半乳糖醛酸的质量分数约为52.02%。此外,还含有其他中性糖(表1)。由于半乳糖醛酸是果胶的主要成分,由此可推断SASDF中含有果胶。酯化度测试的结果表明,其酯化度为50.9%,因此SASDF中含有的果胶应为低酯果胶。与其他商品果胶相比,SASDF的重均分子质量相对较小,约为88 kDa(橘皮果胶为485 kDa,甜菜果胶为562 kDa,苹果果胶为963 kDa)。
2.2 SASDF对乳液消化前后有效粒径、粒度分布及微观结构的影响
2.2.1 消化前

图1 SASDF质量分数对消化前后乳液样品有效粒径的影响Fig.1 Impact of SASDF concentration on the effective particle diameter of emulsions before and after simulated intestinal digestion


图2 SASDF质量分数对消化前后粒度分布的影响Fig.2 Effect of SASDF concentration on the particle size distribution of emulsions before and after simulated intestinal digestion
由图1可以看出,在乳液中加入0.1% SASDF后,乳液的有效粒径并无显著增加(P>0.05),但当添加量为0.2%和0.4%时,乳液的有效粒径极显著增大(P<0.01)。前人研究发现,海藻酸钠对β-乳球蛋白包裹的乳液理化性质的影响表现为少量添加即能显著增大乳液的有效粒径[12]。Dickinson[25]研究表明,乳液体系中的高分子聚合物可以产生排空效应,进而诱发乳液液滴发生聚集现象。这种排空效应的产生是由于高聚物分子中心区域不能被脂肪液滴吸附于其表面,因此高聚物分子和脂肪液滴之间会产生一定的距离,且这一距离与高聚物分子的水合半径相当。在此空间内,脂肪液滴的有效浓度约等于零,但又与溶液体系中的脂肪液滴总体浓度存在差异。这种浓度差异就会产生渗透压,导致乳液液滴发生聚集,从而减小空位区间的相对体积。如果分散相中的高聚物分子浓度越大,则产生这种空位的相对体积越大,因此产生的渗透压力也会随之增大,乳液液滴也就越容易朝着聚集的方向发展。当高聚物分子浓度较低时,这种渗透压力不足以抵抗液滴表面电荷所产生的斥力;当高聚物分子浓度达到一定水平时,渗透压力足以克服脂肪液滴间的斥力时,就会产生聚集和絮凝现象。因此,当SASDF质量分数水平到0.2%时,便可能引发排空效应,乳液液滴则会发生聚集,从而导致样品的平均粒径增大。
而上述推测也可从图2得到验证:未加入SASDF时(图2A),粒度分布曲线呈现单峰分布;加入SASDF后(图2B~D),则粒度分布曲线开始出现双峰分布,尤其是当SASDF添加量达到0.4%时,双峰分布的情况显得更为明显。从激光共聚焦图像(图3A~D)也可以发现,乳液液滴颗粒中相对较大颗粒的比例随着SASDF添加量的增加相对变大,而且这种聚集的作用力较强,具有一定的不可逆性。

图3 激光共聚焦显微镜下SASDF质量分数对脂肪消化前后乳液微观结构的影响Fig.3 Impact of SASDF concentration on the microstructure of emulsions observed by confocal fluorescence microscopy before and after simulated intestinal digestion
2.2.2 消化后
如图1所示,向纳米脂肪乳液中加入较低水平(0.1%)的SASDF即可以使得消化后样品中的液滴有效粒径显著增加(P<0.05);然而,当乳液-SASDF混合溶液中SASDF的质量分数水平提高至0.4%,消化后样品中的乳液液滴有效粒径极显著增大(P<0.01)。从图3H也可以发现,此时的消化体系中存在大型聚集体。这可能是由于SASDF与海藻酸钠具有类似的性质,海藻酸钠可与钙离子结合形成蛋盒结构,进而形成凝胶体系[26-27]。本研究的人工小肠液中含有钙离子,SASDF质量分数为0.4%时,SASDF可与乳液消化体系中的钙离子形成凝胶;而在含有低质量分数水平的SASDF时(0.1%~0.2%),SASDF不易与钙离子形成凝胶。
尽管机械搅拌作用会加剧乳液液滴的聚集,但由于人工小肠液中胆盐的存在,可以使得食糜分子再次被乳化[12]。由于膳食纤维往往具有吸附胆酸钠的特性,因此也存在胆盐与SASDF结合,导致吸附在油水界面上的胆盐相对减少,即体系中的有效表面活性剂的量相对较少,导致体系抗絮凝能力相对较弱,因此在相同的机械搅拌作用下,乳液中含有SASDF的平均粒径较大。
2.3 SASDF对乳液消化前后Zeta电位的影响
Zeta电位常用于描述胶体颗粒之间的静电相互作用。一般情况下,Zeta电位绝对值小于30 mV时,体系不稳定,粒子容易发生聚集[28]。如图4所示,未添加SASDF的初始乳液表现出带有高强度的负电荷(Zeta电位=-(54.24±5.76)mV),这是由于牛白蛋白等电点约为4.7,乳液pH值(pH≈7)高于脂肪液滴油水界面的牛白蛋白等电点,因此此时脂肪液滴带负电荷。质量分数水平不同的SASDF均使乳液Zeta电位绝对值显著减小(P<0.05),且Zeta电位绝对值表现为0%添加量>0.1%添加量>0.2%添加量>0.4%添加量>30 mV,说明在一定添加量范围内,尽管SASDF不会导致乳液的体系由稳定状态转变为不稳定状态,但却能够使得体系朝着不稳定状态的趋势发展,进而导致颗粒与颗粒之间发生聚集行为变得相对容易。这可能是由于SASDF中含有半乳糖醛酸,使其具有阴离子多糖的性质,SASDF加入乳液后能够对体系的离子强度产生影响,进而对乳液的Zeta电位产生影响。

图4 SASDF质量分数对消化前后乳液样品Zeta电位的影响Fig.4 Impact of SASDF concentration on the zeta potential of emulsions before and after simulated intestinal digestion
经小肠消化模型处理后,各测试样品Zeta电位绝对值均显著减小(P<0.05),表明乳液的界面组成发生了改变。这是因为一方面,小肠模拟消化液中各种表面活性成分不断取代乳液液滴界面的牛白蛋白,另一方面,在120 min的小肠消化模型处理过程中,机械搅拌加快乳液液滴的聚集。由此也可以判断,消化后的体系变得不稳定,更容易发生聚集。含0.2%、0.4% SASDF的乳液在经小肠模拟消化后的Zeta电位的绝对值小于30 mV,而含有0.1% SASDF的乳液与不含SASDF的乳液在消化后的Zeta电位无显著性差异,且这两者的绝对值均大于30 mV,这可能是当SASDF添加量仅为0.1%时,SASDF与消化液中的活性物质如钙离子、胆盐形成的复合物浓度过低或无法形成复合物,对乳液的影响不大;而当SASDF添加量达到0.2%及以上时,此时SASDF与消化液中的活性物质(如钙离子)形成的复合物如水凝胶而产生的絮凝排斥效应影响了乳液的稳定性。
胆盐作为阴离子表面活性剂,在消化过程中,会不断替代油脂界面的牛白蛋白而吸附于油脂液滴表面,这也是消化后液滴颗粒剪切面的电位仍表现为负电荷的原因之一。因此,SASDF对于体系中胆盐的吸附也势必会导致吸附于油脂液滴界面胆盐的减少,因此导致界面携带的负电荷相对变少。含SASDF的乳液消化后粒径变大的另一原因是由于胆盐与SASDF结合导致吸附在油水界面上的胆盐量相对减少,相当于体系中有效表面活性剂的量相对变少,导致体系抗絮凝能力相对较弱。本实验在此处从液滴表面电荷情况证明了这一可能性。
2.4 SASDF对乳液消化前后流变学特性的影响

图5 不同质量分数水平SASDF对消化前后乳液的表观剪切黏度的影响(剪切速率20 s- 1)Fig.5 Effect of SASDF concentration on the apparent shear viscosity of emulsions before and after simulated intestinal digestion at 20 s-1 shear rate
已有研究发现一些天然多糖(如海藻酸钠、刺槐胶等)能够在不同程度上对乳液等流体的剪切黏度产生影响[12]。从图5可以发现,无论是否经过消化处理,SASDF的添加均能极显著提高乳液样品的表观剪切黏度(P<0.01),且不同添加量的乳液样品的表观剪切黏度差异极显著(P<0.01)。
乳液中油脂液滴聚集及SASDF形成的凝胶可能导致体系剪切黏度的增大。然而,尽管本研究发现消化后的乳液液滴粒径相较于消化前显著性增大,且消化后形成了絮凝和液滴聚集,从图5却发现除了含有高质量分数水平(0.4%)SASDF的乳液样品,其他乳液样品(即含有相同SASDF质量分数水平的乳液)经过小肠液消化处理前后无显著性差异(P>0.05),这是由于人工小肠液模型本身对乳液-多糖混合溶液存在明显的稀释作用。对于含有0.4% SASDF的乳液样品,尽管同样被消化液稀释,但稀释后SASDF浓度仍能够与Ca2+形成凝胶,从而提高了消化样体系中分散相的有效体积分数。
2.5 SASDF对乳液消化特性的影响

图6 在体外小肠消化模型中SASDF质量分数对乳液脂肪消化率的影响Fig.6 Influence of SASDF concentration on lipid digestion under simulated small intestinal conditions
有学者[29]研究了带正电荷的壳聚糖、带负电荷的海藻酸钠和不带电荷的刺槐胶对阴离子型表面活性剂包裹的纳米乳液的微观结构、理化性质和消化行为的影响,发现带负电荷的海藻酸钠能够通过结合钙离子形成水凝胶,抑制脂质消化;而带正电荷的壳聚糖则能够与阴离子胆盐结合,或与脂质颗粒表面的阴离子脂肪酸分子结合,形成保护层,阻碍脂肪酶与脂质颗粒的结合。而尽管刺槐胶能够引发乳液液滴发生聚集,且能够增大乳液体系的黏度,但刺槐胶却对脂质的消化速率及消化程度没有产生显著性的影响。此外,也有学者研究了对钙离子结合能力较差的高甲氧基果胶和对钙离子结合能力较强的海藻酸钠对油脂消化速度的影响,明确了高甲氧基果胶对油脂消化速度无显著影响,而少量的海藻酸钠就能对油脂消化速度产生显著性影响[30]。
SASDF中半乳糖醛酸质量分数约为50%,且酯化度较低(50.9%),因此SASDF具有类似低酯果胶的性质,即能与钙离子形成凝胶。因此从理论上,SASDF对脂肪乳液理化性质和消化行为的影响应该与海藻酸钠具有一定的相似性。
而这一推测从图6可以得到验证,即添加SASDF对于脂肪消化的速度和程度均表现出了抑制作用,且这种抑制作用随着SASDF添加量的增加表现为逐渐增强。结合SASDF本身的性质及其对消化前后乳液理化性质的影响,推测的抑制机理如下:
1)乳液体系剪切黏度的增加,会降低脂肪酶在乳液体系中的扩散速率,进而使得脂肪酶与乳液液滴表面的三酰甘油分子的结合效率降低。而导致乳液体系剪切黏度增加的原因可能有:SASDF的本身会增加体系剪切黏度;SASDF产生的排空效应,导致乳液液滴聚集,进而导致乳液颗粒变大;钙与SASDF形成的絮凝物质。2)SASDF对胆盐的吸附导致体系内的“有效”表面活性剂的减少、SASDF产生的排空絮凝效应导致乳液液滴聚集,均能导致的乳液粒径相对增大,也会导致乳液液滴的比表面积变小,从而使得脂肪酶与乳液液滴结合的概率变小。3)钙与SASDF形成的凝胶结构可能会将脂肪液滴包埋,阻碍了脂肪酶与脂肪液滴表面的三酰甘油分子的结合。4)脂肪消化过程中,水解出来的脂肪酸分子会附着在乳液液滴的表面,形成一层脂肪酸“分子壳”,这一脂肪酸分子层会阻碍脂肪酶与脂肪液滴表面的酶切位点结合。而小肠液中的钙离子则可以与这层“分子壳”结合并沉积,清除“障碍”,从而使得更多的脂肪酶酶切位点暴露出来,促使酶解反应高效、持续进行。但是当SASDF吸附消化液中的钙离子或者与消化液中的钙离子螯合时,则会导致与脂肪酸结合的钙离子量相应减少。
2.6 SASDF对乳液消化反应动力学的影响
对自由脂肪酸释放动态曲线更深入地分析,可能可以从中发现此过程中的潜在机理,这也能为SASDF的应用提供理论数据。
从图7可以看出,经过2 h的体外小肠模型模拟消化处理后,各个曲线均到达平台期;根据式(4),可求得伪一级反应速率常数k。不含SASDF时,油脂消化表现为二阶反应,即包含两个伪一级反应速率常数(k1和k2)。这说明了体系中部分甘油三酯分子相对较容易被与脂肪酶结合并水解,这部分的甘油三酯分子可能是附着在液滴或聚集体的表面。因此,在伪一级反应的第1反应阶段,人工小肠液中的脂肪酶能够以较高的扩散速率达到纳米油脂乳液液滴的界面,以较高的结合效率与甘油三酯分子的酶切位点结合。随着油脂消化过程的进行,体系的内部组成由于甘油三酯水解得到的游离脂肪酸附着于油脂液滴的表面而发生改变,脂肪酸分子层形成脂肪酶与内部甘油三酯脂肪酶酶切位点结合的阻碍。
含有SASDF的乳液样品,LOS回归曲线也表现为二阶性。对于第1阶段的反应速率常数的变化规律可以发现,k1与SASDF添加量相关,也就是随着SASDF添加量的增加,快速反应阶段的速率常数逐渐减小。而第2阶段(即慢速反应阶段)的反应速率常数k2则表现为与SASDF添加量无明显关系。

图7 SASDF质量分数对纳米脂肪乳液的消化LOS回归分析Fig.7 LOS plots obtained from the digestion data in the presence of different concentrations of SASDF
SASDF与钙离子形成凝胶,增大了体系的表观剪切黏度的同时也包埋了部分乳液液滴,SASDF的排空絮凝效应使得乳液液滴的有效粒径增大,这些都会对脂肪酶与油脂液滴的接触和结合效率产生显著影响;同时,SASDF本身对于钙离子的螯合也会加剧游离脂肪酸附着于油脂液滴表面的阻碍效应。而这些因素本身又与体系中SASDF质量分数相关,因此这些因素综合限制了脂肪酶对甘油三酯分子的酶解效率,同时导致k1表现为质量分数水平依赖型。
尽管k1表现为随着质量分数的增大而变小,但k2却无此规律,从表2可知,0.1% SASDF的乳液在反应第2阶段的水解比例C2(0.1%)却比不含SASDF在反应第2阶段的水解比例C2(0%)高。这是由于机械搅拌作用会破坏部分SASDF与消化液中的生物活性分子形成的聚集体,使得一部分被包埋的油脂液滴被释放出来,进入油脂消化反应的第2阶段。但当SASDF的质量分数继续增大时,这种被破坏的聚集体比例会下降,并在反应过程中不断形成新的凝胶结构。且SASDF质量分数越大,体系的表观剪切黏度也越大,因此最终的游离脂肪酸释放率也呈现出随着质量分数增大而减小的变化趋势。

表2 LOS回归分析所得反应动力学参数Table 2 Kinetic parameters calculated from the LOS model
3 结 论
SASDF对蛋白包裹型纳米乳液消化前后的有效粒径、粒径分布、Zeta电位、表观剪切黏度和微观结构均会产生显著性影响,且表现为质量分数水平依赖型。不管是否添加SASDF,纳米脂肪乳液的消化曲线都表现为二阶的伪一级反应,对于快速反应阶段的反应速率常数k1,呈现出随着SASDF质量分数的增大而变小的规律,但对于慢速反应阶段,其反应速率常数k2则与质量分数没有表现出相关性。但纳米脂肪乳液中脂肪的最终消化率却会随着体系中SASDF添加量的增加而降低。

