抗坏血酸和铁系还原剂修复铬污染土壤
张恩智,蹇 川,张 笑,谭绍林,高焕方
(1. 重庆理工大学 化学化工学院,重庆 400054;2. 重庆市生态环境监测中心,重庆 401147;3. 重庆市大渡口区生态环境局,重庆 400084)
Cr被广泛应用于电镀、制革、染色、防腐等工艺,使得铬酸盐合成、铬冶炼等工业生产活动大量涌现[1-2]。早期工厂对铬渣的不规范堆放,造成土壤的Cr(Ⅵ)含量和Cr(Ⅵ)浸出浓度严重超标[3-4]。饮用水和土壤灰尘的直接摄入及动植物体食物的间接摄入均会导致Cr(Ⅵ)中毒[5]。Cr(Ⅵ)的氧化性极强,除损伤人体器官外,还会损害DNA,造成癌症、畸形等危险疾病,毒性比Cr(Ⅲ)大百倍[6-7]。
减少土壤的Cr(Ⅵ)污染,一是从土壤中去除Cr;二是将Cr固定在土壤中,从而降低Cr(Ⅵ)的浸出浓度,提高土壤的生物可用性。从去除土壤中Cr的角度出发,发展出了两种主要方法:一种是利用化学药剂将Cr从土壤中淋洗出来,该方法成本过高,且可能造成二次污染;另一种则是利用植物吸收土壤中的Cr,该方法经济成本较低,但修复周期过长,时间成本过高[1,8]。从固定Cr于土壤的角度出发,则发展出了化学还原稳定技术,该技术因成本较低、修复效率高、修复速度快而成为目前Cr污染场地的主要修复技术[9-10]。
化学还原稳定技术的原理是基于Cr(Ⅲ)的迁移性远低于Cr(Ⅵ),Cr(Ⅲ)可与土壤中的胶粒和氧化物结合形成难迁移的沉淀物[11]。已应用于场地修复的Na2S2O3等硫系还原剂能显著还原和稳定土壤中的Cr(Ⅵ),但其浸出浓度会在修复数天后出现反弹[12-13]。而具有强还原性的抗坏血酸(C6H8O6)以及一些铁系还原剂还少见于该领域的研究报道。其中,C6H8O6不会对环境造成二次污染。
本研究通过投加还原剂(NH4)2Fe(SO4)2、FeCl2、FeS和C6H8O6修复Cr污染土壤,考察了土壤的Cr(Ⅵ)含量、Cr(Ⅵ)浸出浓度、Cr形态、pH及晶体结构的变化,以评价其修复效果和长期稳定性能,为今后Cr污染土壤的实验研究及场地修复提供科学依据。
1 实验部分
1.1 试剂和材料
实验所用还原剂FeCl2、FeS、(NH4)2Fe(SO4)2和C6H8O6均为采购自西陇科学股份有限公司的分析纯试剂。实验所用土壤取自重庆市某化工厂Cr污染场地的表层(0~50 cm)土壤,土壤质地为砂壤土,呈浅棕色,经风干研磨、过100目筛、混匀后待用,其基本理化性质见表1。

表1 供试土壤的基本理化性质
1.2 实验方法
分别取200 g待试土样,以溶液的方式投加40 mL去离子水溶解的FeCl2、(NH4)2Fe(SO4)2和C6H8O6,及固体方式投加碾碎后过100目筛的FeS。已有研究表明,亚铁还原剂的投加量为理论值的3倍和4倍时的修复效果较好[14],故以此作为还原剂投加量的依据,具体实验方案见表2。投加还原剂后手动搅拌,边搅拌边喷入去离子水,使土样含水率在30%左右,并保持蓬松状态。搅拌完成后用保鲜膜封住以减少水分蒸发,定期喷洒适量去离子水以保持30%左右的含水率,不定期取样分析。
理论值即理论价态水平上恰好完全还原土壤中Cr(Ⅵ)的还原剂投加量。每200 g待试土样的FeCl2,C6H8O6,(NH4)2Fe(SO4)2,FeS投加量的理论值分别为1.524,0.704,2.640,1.056 g。
1.3 分析方法
按照《土壤检测 第12部分:土壤总铬的测定》(NY/T 1121.12—2006)[15]测定土壤总Cr含量。
按照《固体废物 浸出毒性浸出方法 硫酸硝酸法》(HJ/T 299—2007)[16]对土壤重金属进行浸出,再按照《固体废物 六价铬的测定 二苯碳酰二肼分光光度法》(GB/T 15555.4—1995)[17]测定土壤Cr(Ⅵ)浸出质量浓度。根据处理前后的土壤Cr(Ⅵ)浸出质量浓度,计算还原剂对Cr(Ⅵ)的稳定效率[18]。
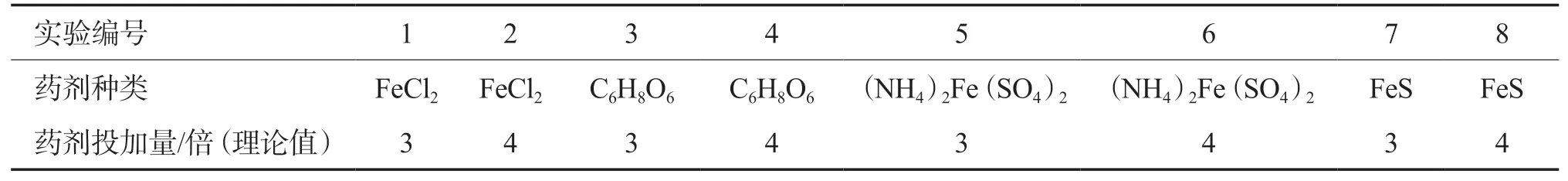
表2 Cr污染土壤修复实验方案
按照《危险废物鉴别标准 浸出毒性鉴别》(GB 5085.3—2007)[19]对土壤进行前处理,再按照GB/T 15555.4—1995测定土壤Cr(Ⅵ)含量。根据处理前后的土壤Cr(Ⅵ)含量,计算还原剂对Cr(Ⅵ)的还原率。
按照《土壤和沉积物 13个微量元素 形态顺序提取程序》(GB/T 25282—2010)[20]分析土壤Cr形态。
将去离子水和土壤按照2.5∶1的质量比混合均匀后,采用上海仪电科学仪器股份有限公司pHS-3E型pH计测定土壤pH。
采用日本津岛公司Shimadzu XRD-7000型X射线衍射仪分析土壤晶体结构:Cu靶,管电压40 kV,管电流40 mA,扫描范围10°~80°,扫描速率2 ( °)/min。
按照《土壤检测 第5部分:石灰性土壤阳离子交换量的测定》(NY/T 1121.5—2006)[21]测定土壤阳离子交换量。
2 结果与讨论
2.1 不同还原剂对土壤的修复效果对比
2.1.1 Cr(Ⅵ)浸出浓度
养护期间土壤Cr(Ⅵ)浸出质量浓度的变化见图1。由图1可知:C6H8O6对Cr污染土壤中的Cr(Ⅵ)稳定效果最好;4 d后,投加3倍和4倍理论值C6H8O6土壤的Cr(Ⅵ)浸出质量浓度快速降至1.32 mg/L和1.31 mg/L;4~30 d的Cr(Ⅵ)浸出质量浓度均低于《生活垃圾填埋场污染控制标准》(GB 16889—2008)[22]中Cr(Ⅵ)的浸出限值(1.5 mg/L);投加3倍理论值C6H8O6的土壤在32 d时Cr(Ⅵ)浸出质量浓度降至最低值0.83 mg/L,对Cr(Ⅵ)的稳定效率达98.3%;投加4倍理论值C6H8O6与3倍时相比,稳定效果无明显提升;养护期间,Cr(Ⅵ)的浸出浓度趋于平稳,相比于铁系还原剂在投加数天后出现浸出浓度增加,C6H8O6在修复过程中无反弹现象,这表明C6H8O6对Cr污染土壤的修复在长期稳定性方面更具优势。C6H8O6在水中具有一定的溶解性,适度的水分能保证药剂将土壤中的Cr(Ⅵ)快速还原为Cr(Ⅲ)。尽管C6H8O6在空气和水中极不稳定,但处于土壤中的有机分子可以与土壤胶粒螯合,这不仅增加了C6H8O6与吸附在土壤胶粒上的Cr(Ⅵ)的反应面积,同时也提高了C6H8O6的稳定性[23]。
FeCl2和(NH4)2Fe(SO4)2对Cr污染土壤具有一定的修复效果,以3倍和4倍理论值投加的FeCl2以及以3倍和4倍理论值投加的(NH4)2Fe(SO4)2在第4天时对土壤Cr(Ⅵ)的稳定效果最好,Cr(Ⅵ)浸出质量浓度分别快速降至4.09,2.64,4.31,1.62 mg/L,这可能与FeCl2和(NH4)2Fe(SO4)2投加后土壤pH快速下降有关(见后续图4)。已有研究表明,较低的土壤pH有利于Cr(Ⅵ)还原反应的发生[24]。在养护4 d后,土壤Cr(Ⅵ)浸出浓度持续上升,表明亚铁离子在第4天已基本耗尽。最终,两种还原剂对Cr(Ⅵ)的稳定效率均保持在73%以上。
即使添加了4倍理论值的药剂,FeS对Cr污染土壤的修复效果仍不明显。30 d时,土壤的Cr(Ⅵ)浸出质量浓度仍高达46.29 mg/L,与原土相差无几。这主要是因为FeS不溶于水,不能电离出还原性离子Fe2+和S2-;再加上FeS的粒径过大,导致与Cr(Ⅵ)的反应很难发生。尽管LI等[25]制备的纳米FeS能显著降低土壤的Cr(Ⅵ)浸出浓度至未检出的程度,但药剂成本的大幅升高将导致其很难应用于实际的工程修复。
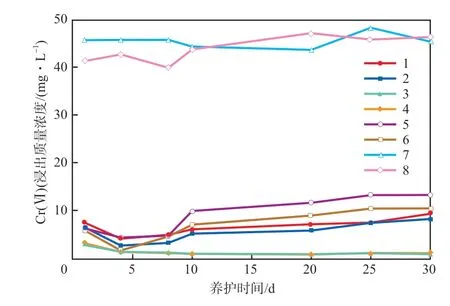
图1 养护期间土壤Cr(Ⅵ)浸出质量浓度的变化
2.1.2 Cr(Ⅵ)还原率
养护期间土壤Cr(Ⅵ)含量的变化见图2。4种还原剂对土壤中的Cr(Ⅵ)均有一定的还原性。30 d时,不溶的FeS还原效果最差,其3倍和4倍理论投加量对Cr(Ⅵ)的还原率仅为60%左右。尽管已有研究表明特制的纳米级FeS能显著修复土壤的Cr(Ⅵ)污染[25],但本实验使用的是工业生产的FeS,虽然对其进行了碾碎过筛处理,但相比于其他铁系还原剂,其粒径仍然较大,与Cr(Ⅵ)的接触率较低。其余还原剂对土壤中的Cr(Ⅵ)均有显著还原效果,而投加4倍理论值的(NH4)2Fe(SO4)2效果最好,其还原率可达86.88%,C6H8O6对Cr(Ⅵ)的还原率也可达86%以上。土壤颗粒的包裹导致还原剂无法接触到颗粒内部的Cr(Ⅵ),故无法完全还原土壤中的Cr(Ⅵ)[26]。相比于其他还原剂,C6H8O6在整个养护期间的Cr(Ⅵ)还原率更为稳定,未出现反弹现象。3种还原剂FeCl2、(NH4)2Fe(SO4)2和C6H8O6对土壤中Cr(Ⅵ)的还原率均达到了80%以上。
2.1.3 Cr形态变化
本实验按照GB/T 25282—2010对土壤中的Cr进行形态分级提取,共分为可交换态、碳酸盐结合态、铁锰氧化物结合态、有机物结合态和残渣态5个形态[27]。其中,残渣态Cr主要存在于矿物晶格和土壤胶粒中,其迁移性和生物有效性极低,不会危害到环境和生物[28]。在添加还原剂并养护30 d后,测定各个土壤样品的Cr形态数据并与原土进行对比,结果见图3。
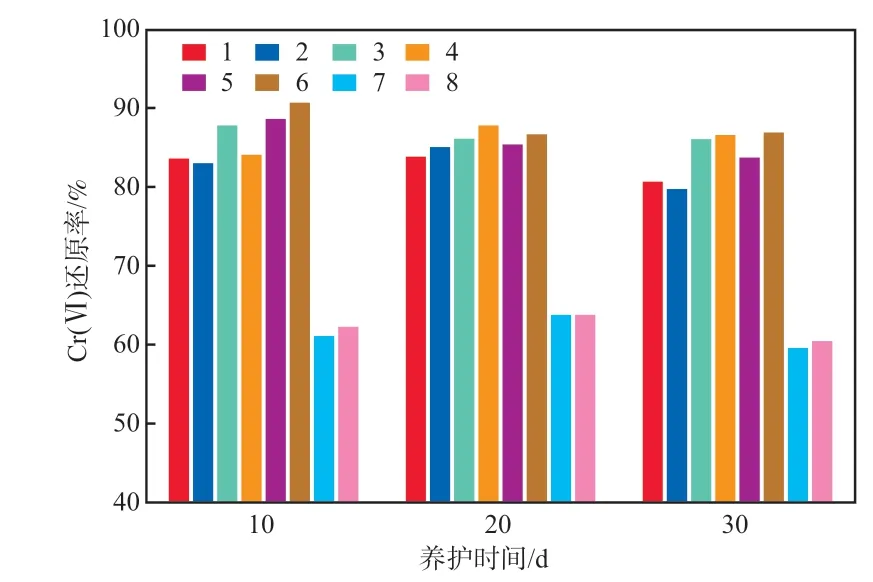
图2 养护期间土壤Cr(Ⅵ)含量的变化
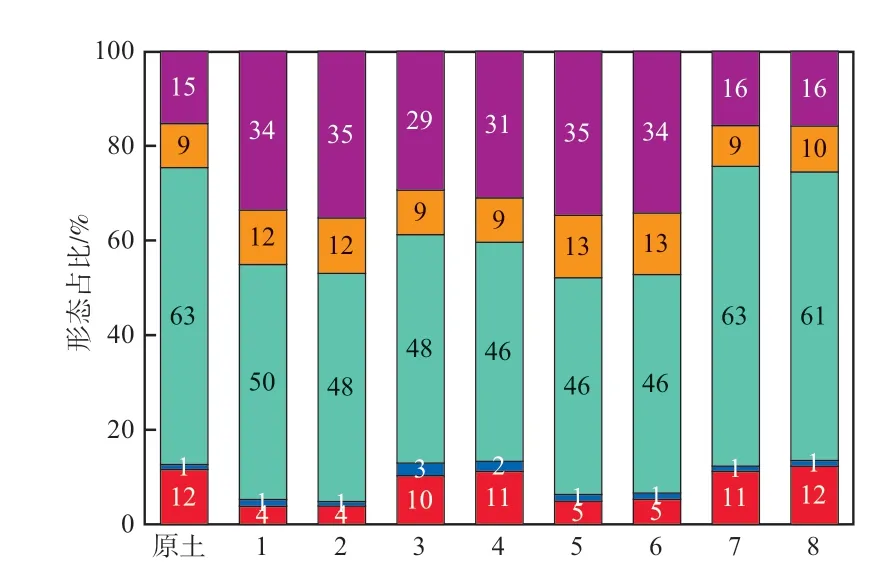
图3 修复后土壤与原土的Cr形态对比
由图3可以看出,投加了含Fe2+的FeCl2和(NH4)2Fe(SO4)2的土壤,其Cr的残渣态均为原土的2.3倍。有研究表明,Fe2+在还原Cr(Ⅵ)为Cr(Ⅲ)的同时,其自身的氧化产物Fe3+可与土壤中的OH-形成Fe(OH)3胶体,吸附重金属Cr和土壤胶粒,Fe(OH)3和Cr(OH)3共沉淀形成铬铁矿残渣态[29]。原土的pH为9.84,碱性较强,根据化学反应平衡有利于Fe(OH)3和Cr(OH)3的形成,促进了铬铁矿残渣态的产生[30]。而投加了FeS的两组样品相比于原土,其形态几乎没有改变,与前述原因一样,FeS颗粒较大,难以与土壤中的Cr(Ⅵ)反应并与之结合形成残渣态,这也是FeS处理后的土壤浸出浓度较大的根本原因。投加了C6H8O6的土壤样品相比于原土,其Cr的残渣态增加了1倍左右。这主要是由于:C6H8O6本身并不能与Cr形成矿物残渣态,被还原的Cr(Ⅲ)只能通过土壤本身所含的Al3+、Fe3+、Mn2+等阳离子形成的氧化物或氢氧化物,包裹或络合而形成矿物残渣态[31];另一方面,原土的阳离子交换量只有14.00 cmol/kg,土壤胶粒难以吸附大量的Cr3+,故其残渣态的增量略低[32]。
2.2 不同还原剂对土壤pH的影响
养护期间土壤pH的变化见图4。由图4可知,FeCl2和(NH4)2Fe(SO4)2的投加会导致土壤pH的降低,其中,投加了FeCl2和(NH4)2Fe(SO4)2的土壤样品pH出现不同程度的下降。这可能是由于FeCl2是以溶液的形式投加到土壤中,与土壤中的OH-有更多的接触面积,导致土壤pH快速下降[33]。而投加了C6H8O6的土壤样品的pH先迅速下降然后持续上升,最后稳定在9左右;与原土9.84的pH相比,土壤pH的变化较小。这主要是因为C6H8O6在土壤中会释放出H+,这会导致土壤pH先降低,随后在养护过程中C6H8O6逐渐与Cr(Ⅵ)反应而被消耗,土壤pH缓慢上升然后保持稳定[23]。由于FeS颗粒较大,与土壤中Cr(Ⅵ)的接触面积较小,反应较慢,土壤pH缓慢降低后趋于稳定,最后维持在9附近。
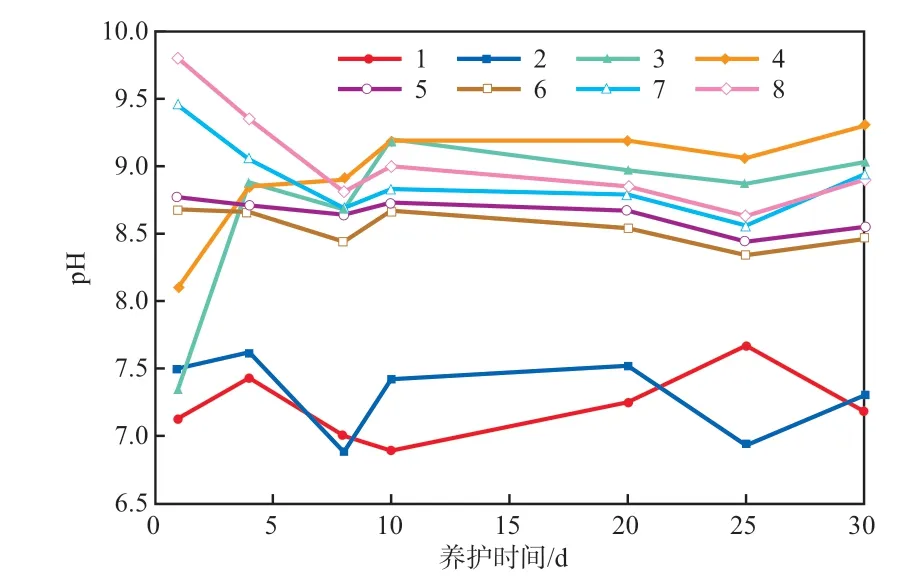
图4 养护期间土壤pH的变化
2.3 不同还原剂对土壤晶体结构的影响
以3倍理论值投加量还原剂修复土壤为例,不同还原剂修复后土壤与原土的XRD谱图见图5。由图5可见,与原土相比,投加还原剂修复后的土壤,其晶体结构未见明显改变,这主要是因为在还原剂修复过程中并没有生成新的晶体结构。FeCl2和(NH4)2Fe(SO4)2的投加尽管会导致土壤中铁含量的增加,但生成的晶体结构与土壤已存在的含Fe的晶体结构相同。C6H8O6的引入仅是利用土壤本身所存在的Al3+、Fe3+、Mn2+等金属离子,同样不会产生新的晶体结构。虽然FeS因其难溶、难分解的特性会在土壤中引入新的晶体结构,但由于含量较少,加上土壤结构的复杂性而难以被检测到。综上,4种还原剂的投加所引入或产生的新的结晶物质均未对土壤晶体结构产生明显影响。
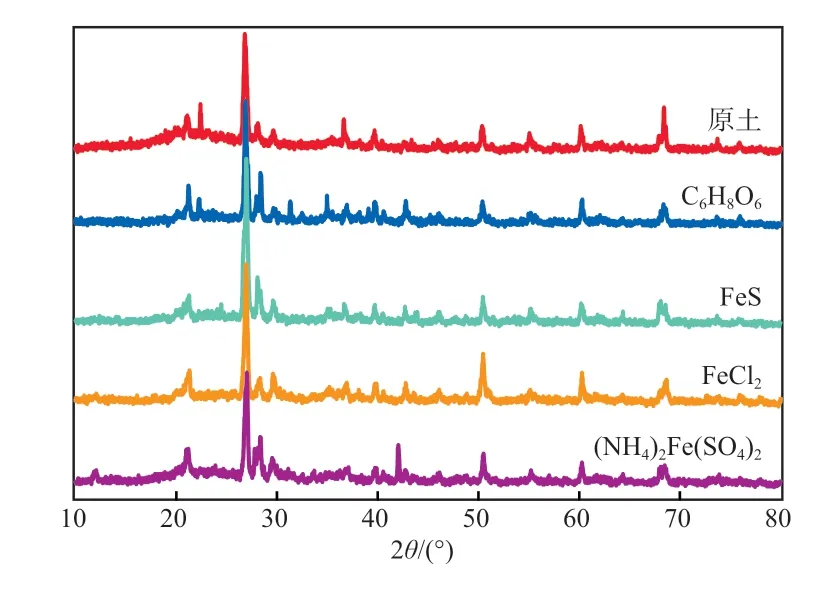
图5 不同还原剂修复后土壤与原土的XRD谱图
3 结论
a)还原剂FeS对土壤Cr(Ⅵ)的还原率仅为60%左右,且稳定效率极低。另外3种还原剂FeCl2、(NH4)2Fe(SO4)2和C6H8O6均能显著降低土壤的Cr(Ⅵ)含量和Cr(Ⅵ)浸出浓度,且投加量为理论值3倍和4倍时的效果相差不大,对土壤中Cr(Ⅵ)的还原率均达到了80%以上,稳定效率均超过了73%。
b)C6H8O6相比于铁系还原剂表现出更好的长期稳定性,4~30 d的Cr(Ⅵ)浸出质量浓度均低于《生活垃圾填埋场污染控制标准》(GB 16889—2008)中Cr(Ⅵ)的浸出限值(1.5 mg/L);投加3倍理论值C6H8O6的土壤在30 d时的Cr(Ⅵ)浸出质量浓度降至最低值0.83 mg/L,对Cr(Ⅵ)的稳定效率达98.3%。而亚铁还原剂FeCl2和(NH4)2Fe(SO4)2对Cr(Ⅵ)的稳定效率在养护数天后均出现反弹现象。
c)除FeS外,其余3种还原剂均显著增加了土壤中生物有效性极低的Cr残渣态占比;C6H8O6处理后的Cr污染土壤的残渣态是原土的约2倍,而FeCl2和(NH4)2Fe(SO4)2处理后的是原土的2.3倍。
d)C6H8O6还原剂的投加对土壤pH无明显影响;FeCl2和(NH4)2Fe(SO4)2还原剂的投加会导致土壤pH降低;FeS对土壤pH的影响较小。
f)4种还原剂的投加所引入或产生的新的结晶物质均未对土壤晶体结构产生明显影响。

